UHPLC-QTOF-MSMS比较两种不同基原火炭母的化学成分
吴尤娇,陈汀波,姬云青,程春松,,张子凌,周 华,,罗 培,,张志锋,*
1澳门科技大学中药质量研究国家重点实验室;2澳门科技大学中医药学院,澳门特别行政区 519020
火炭母PolygonumchinenseL.来源于蓼科Polygonaceae蓼属Polygonum,最早被记录在1977年版《中国药典》,其来源为植物火炭母原变种(PolygonumchinenseL.var.Chinense)及其变种硬毛火炭母(PolygonumchinenseL.var.Hispidum)的干燥全草[1]。火炭母别名老鼠蔗、火炭藤、乌炭子等,主要分布于广西、广东、福建、浙江、湖北及海南等地,是岭南习用的一味中草药,同时也是多种广东凉茶的主要成分之一[2]。其性寒、味微酸、涩,具有清热祛湿、凉血解毒、活血通络、平肝明目等功效,临床主要用于治疗痢疾、皮炎湿疹、角膜云翳等病症。现代药理研究表明,火炭母具有抗炎、镇痛、抗腹泻、抗肝癌、抗病毒、抗氧化、抑制中枢神经等作用[3]。火炭母主要含挥发油类、黄酮类、鞣质类、酚酸类等成分[2]。2004年版的《广东省药材标准》以及2017年出版的《香港中药材标准》中,均仅收载火炭母一种[4,5]。但据本项目调查,发现火炭母原变种与硬毛火炭母分布地区相同,有的甚至在同一地方两种混生,因而,在民间以及凉茶中,两种基原都不加区别的使用。但是目前尚未发现对二者的化学成分及品质进行比较研究。因此,本研究首次对火炭母的两个不同基原——火炭母原变种和硬毛火炭母变种,运用UHPLC-QTOF-MSMS对其化学成分进行比较研究,为二者是否可以等同入药提供科学依据,为药材标准的修订及品质评价提供参考资料。
1 仪器与试药
超高效液相色谱-四极杆飞行时间质谱联用仪(Agilent Technologies 6550 iFunnel Q-TOF LC/MS)、MassHunter 6.0工作站;色谱柱为Waters ACQUITY HSS-C18Column(1.8 μm,2.1×100 mm);AUY220电子天平(SHIMADZU,日本);CP500HT型超声波清洗器(Crest Ultrasonics,美国);高速离心机(Eppendorf,德国);乙腈、甲醇(Merck,德国,HPLC级);甲酸(Fluka,瑞典,HPLC级);Milli-Q超纯水系统(Millipore,美国)。
没食子酸对照品(批号110831-171010)、绿原酸对照品(批号 110753-201716)、鞣花酸对照品(批号 111959-201602)和槲皮苷对照品(批号111538-201606)均购自中国食品药品检定所。火炭母及硬毛火炭母样品分别于2017年6月采集于广西崇左、北海、钦州、柳州、广东茂名和清远等地,每个产地采集样品5份。经四川大学华西药学院生药教研室张浩教授鉴定:广西南宁、北海和钦州的样品为蓼科植物火炭母原变种P.chinensevar.chinense的干燥全草;广西柳州、广东茂名和清远的样品为其变种硬毛火炭母P.chinensevar.hispidum的干燥全草。
2 实验方法
2.1 超高效液相色谱条件
色谱柱为Waters Acquity HSS-C18(1.8 μm,2.1×100 mm),以0.2%甲酸水溶液为流动相(A),乙腈为流动相 (B),梯度洗脱为0~7 min,8%~27% B;7~10 min,27%~27% B;10~12 min,27%~65% B。流速0.30 mL/min,自动进样5 μL,柱温30 ℃。
2.2 质谱条件
电喷雾电离(ESI)离子源,负离子模式下采集数据,质量扫描范围m/z100~1 000,离子源参数毛细管电压为3 200 V,锥孔电压40 kV,离子源温度为100 ℃,脱溶剂气温度350 ℃,脱溶剂气(N2)体积流量700 L/h,碰撞能量(CE)30~45 V。实验数据采用MassHunter 6.0软件处理。
2.3 对照品溶液的制备
精密称取没食子酸、绿原酸、鞣花酸、槲皮苷对照品适量,置于10 mL容量瓶中,以60%乙醇溶液溶解,样品溶液经0.22 μm微孔滤膜过滤后制成混合对照品储备液。
2.4 供试品溶液的制备
分别精密称取各产地火炭母原变种、硬毛火炭母粗粉各0.25 g,置于25 mL容量瓶中,分别精密加入60%乙醇10 mL为提取溶剂,精密称定重量,超声提取30 min(100 W,40 kHz),温度60 ℃。放置至室温后,精密称定重量,以提取溶剂补足减失的重量,经微孔滤膜0.22 μm过滤,即得火炭母原变种、硬毛火炭母供试液。

图1 火炭母原变种(A)与硬毛火炭母(B)UHPLC-TOF-MSMS总离子流色谱图Fig.1 P.chinense var.chinense (A) and P.chinense var.hispidum (B) UHPLC-TOF-MSMS total ion chromatogram
3 实验结果
3.1 火炭母原变种和硬毛火炭母总离子流图比较
UHPLC-MS 中质谱检测有正、负离子两种扫描模式,火炭母原变种中以黄酮类、酚酸类为主要成分,其在负离子模式下的质谱响应较好[6],故本实验选择负离子扫描模式,质谱总离子流图(TIC)见图1。硬毛火炭母的离子流图中,在6~7 min出现了23号峰,而在火炭母原变种的离子流图中该保留时间并未出现化合物;火炭母原变种的离子流图中,在10~12 min出现了28、29号峰,而在硬毛火炭母的离子流图中该保留时间未出现化合物。
3.2 UHPLC-QTOF-MSMS成分分析
采用 MassHunter 6.0 软件进行数据处理,根据负离子模式下各化学成分的保留时间和质谱信息,并结合提取离子流图及与对照品、相关文献数据对比进行化学成分确认,鉴定或推断了25个化合物,包括17个酚酸类、8个黄酮类成分。结果见表1。
表1火炭母原变种与硬毛火炭母UHPLC-TOF-MSMS色谱图中指认的色谱峰
Table 1 UHPLC-TOF-MSMS identified in the chromatogram ofP.chinensevar.chinenseandP.chinensevar.hispidum
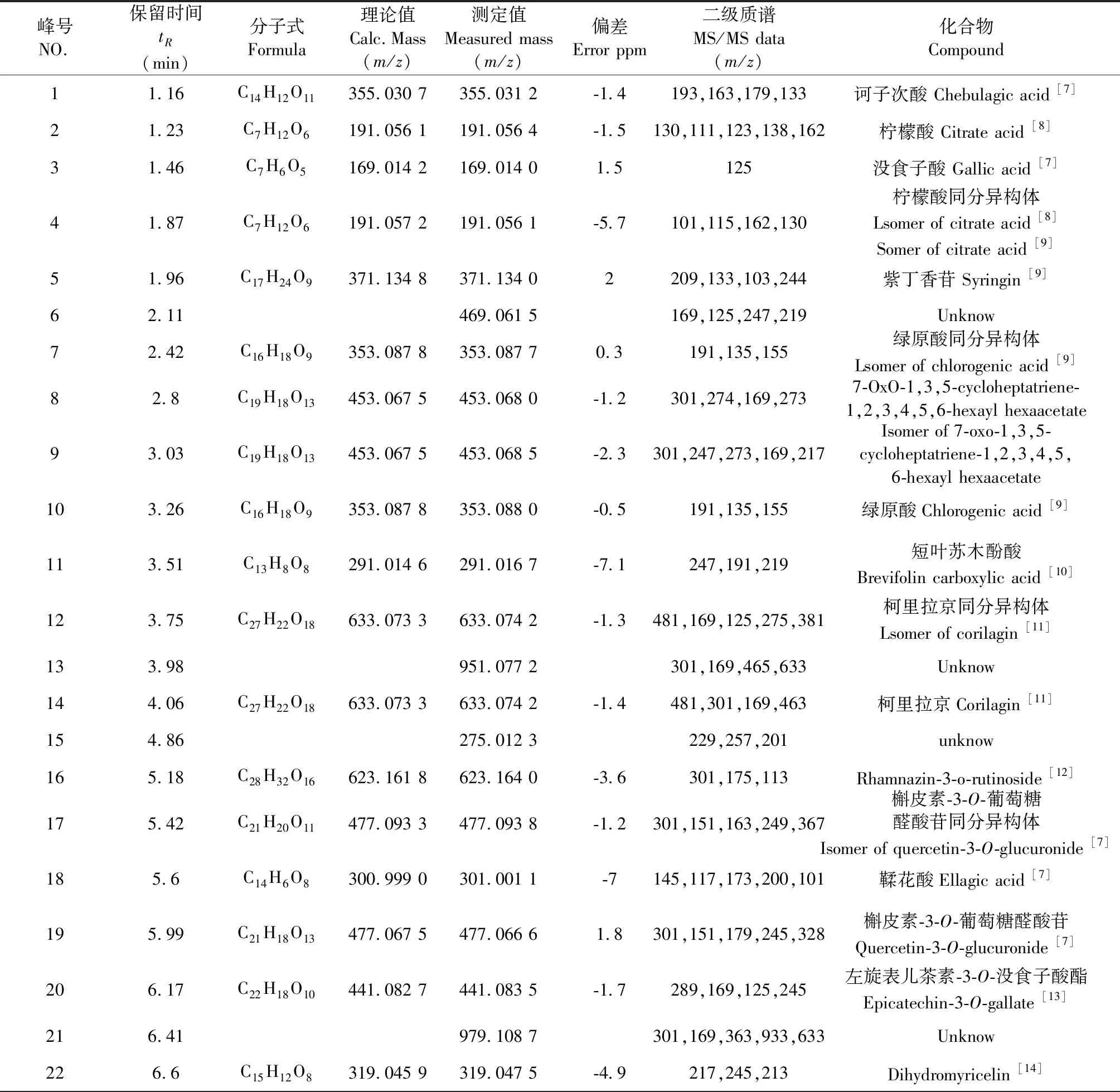
峰号NO.保留时间tR(min)分子式Formula理论值Calc.Mass (m/z)测定值 Measured mass (m/z)偏差Error ppm 二级质谱MS/MS data (m/z)化合物Compound11.16C14H12O11355.030 7355.031 2-1.4193,163,179,133诃子次酸 Chebulagic acid [7]21.23C7H12O6191.056 1191.056 4-1.5130,111,123,138,162柠檬酸 Citrate acid [8]31.46C7H6O5169.014 2169.014 01.5125没食子酸 Gallic acid [7]41.87C7H12O6191.057 2191.056 1-5.7101,115,162,130柠檬酸同分异构体Lsomer of citrate acid [8]Somer of citrate acid [9]51.96C17H24O9371.134 8371.134 02209,133,103,244紫丁香苷 Syringin [9]62.11469.061 5169,125,247,219Unknow72.42C16H18O9353.087 8353.087 70.3191,135,155绿原酸同分异构体 Lsomer of chlorogenic acid [9]82.8C19H18O13453.067 5453.068 0-1.2301,274,169,2737-OxO-1,3,5-cycloheptatriene-1,2,3,4,5,6-hexayl hexaacetate93.03C19H18O13453.067 5453.068 5-2.3301,247,273,169,217Isomer of 7-oxo-1,3,5-cycloheptatriene-1,2,3,4,5,6-hexayl hexaacetate103.26C16H18O9353.087 8353.088 0-0.5191,135,155绿原酸Chlorogenic acid [9]113.51C13H8O8291.014 6291.016 7-7.1247,191,219短叶苏木酚酸Brevifolin carboxylic acid [10]123.75C27H22O18633.073 3633.074 2-1.3481,169,125,275,381柯里拉京同分异构体 Lsomer of corilagin [11]133.98951.077 2301,169,465,633Unknow144.06C27H22O18633.073 3633.074 2-1.4481,301,169,463柯里拉京Corilagin [11]154.86275.012 3229,257,201unknow165.18C28H32O16623.161 8623.164 0-3.6301,175,113 Rhamnazin-3-o-rutinoside [12]175.42C21H20O11477.093 3477.093 8-1.2301,151,163,249,367槲皮素-3-O-葡萄糖醛酸苷同分异构体Isomer of quercetin-3-O-glucuronide [7]185.6C14H6O8300.999 0301.001 1-7145,117,173,200,101鞣花酸Ellagic acid [7]195.99C21H18O13477.067 5477.066 61.8301,151,179,245,328槲皮素-3-O-葡萄糖醛酸苷 Quercetin-3-O-glucuronide [7]206.17C22H18O10441.082 7441.083 5-1.7289,169,125,245左旋表儿茶素-3-O-没食子酸酯 Epicatechin-3-O-gallate [13]216.41979.108 7301,169,363,933,633Unknow226.6C15H12O8319.045 9319.047 5-4.9217,245,213Dihydromyricelin [14]
续表1 (Continued Tab.1)
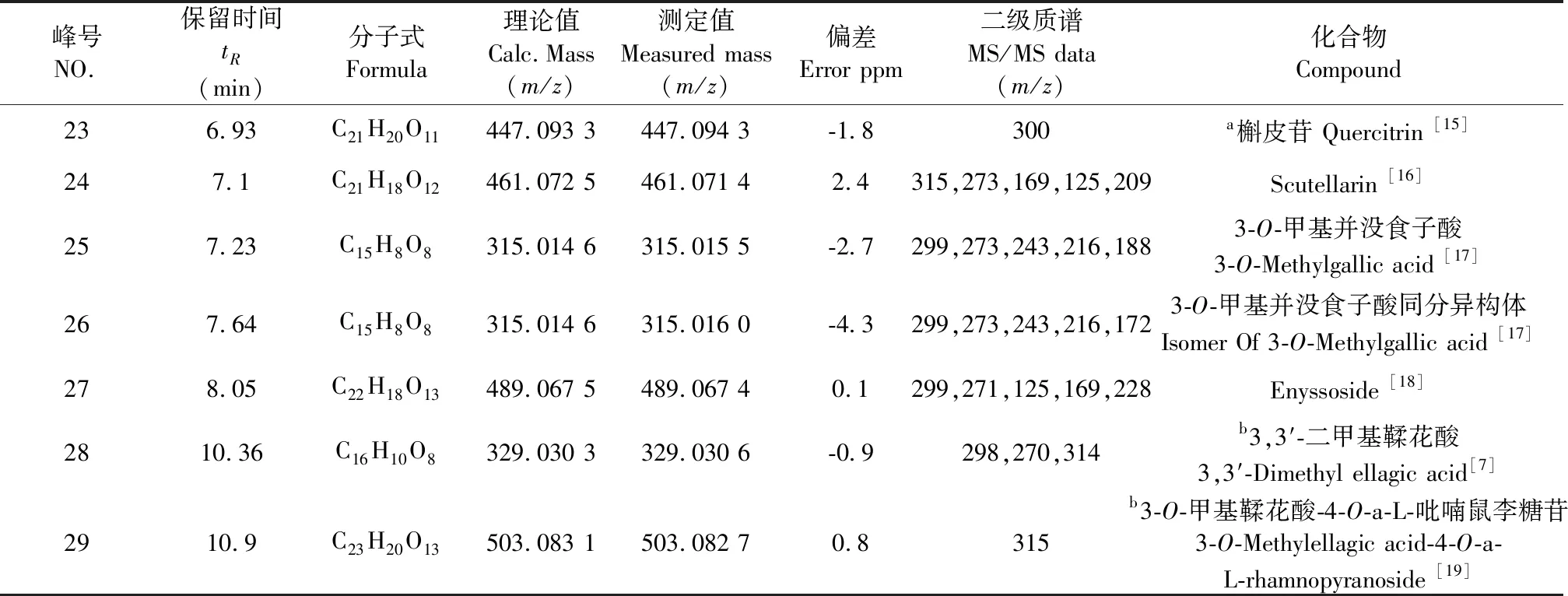
峰号NO.保留时间tR(min)分子式Formula理论值Calc.Mass (m/z)测定值 Measured mass (m/z)偏差Error ppm 二级质谱MS/MS data (m/z)化合物Compound236.93C21H20O11447.093 3447.094 3-1.8300a槲皮苷 Quercitrin [15]247.1C21H18O12461.072 5461.071 42.4315,273,169,125,209Scutellarin [16]257.23C15H8O8315.014 6315.015 5-2.7299,273,243,216,1883-O-甲基并没食子酸 3-O-Methylgallic acid [17]267.64C15H8O8315.014 6315.016 0-4.3299,273,243,216,172 3-O-甲基并没食子酸同分异构体 Isomer Of 3-O-Methylgallic acid [17]278.05C22H18O13489.067 5489.067 40.1299,271,125,169,228Enyssoside [18]2810.36C16H10O8329.030 3329.030 6-0.9298,270,314b3,3′-二甲基鞣花酸 3,3′-Dimethyl ellagic acid[7]2910.9C23H20O13503.083 1503.082 70.8315b3-O-甲基鞣花酸-4-O-a-L-吡喃鼠李糖苷3-O-Methylellagic acid-4-O-a-L-rhamnopyranoside [19]
注:化合物3、10、18、23同时由对照品进行确认;a表示在火炭母原变种中未检测到;b表示在硬毛火炭母中未检测到。
NOte:The compounds 3,10,18 and 23 were confirmed by chemical reference substances,aIndicates undetected inP.chinensevar.chinens,bIndicates undetected inP.chinensevar.hispidum.
3.3 酚酸类化合物的鉴定[8-19]
酚酸类成分通过准分子离子峰丢失没食子酰基m/z152是其典型的质谱裂解规律,特征碎片离子m/z169可以作为推测酚酸类成分的依据。通过一级质谱发现,表1中含有较多m/z633、m/z453、m/z441、m/z191等分子离子峰,且部分大于m/z300的分子离子峰存在丢失没食子酰基m/z152的规律。以化合物20为例,Q-TOF/MSm/z441[M-H]-,在MS/MS图谱中存在m/z289[M-H]-的碎片离子峰,两者之间相差152,主要通过丢失没食子酰基基团形成,根据碎片离子m/z289、m/z169、m/z125、m/z245推测该化合物为酚酸类成分左旋表儿茶素-3-O-没食子酸酯。结合参考文献,共鉴定出诃子次酸、柠檬酸、没食子酸、柠檬酸同分异构体、绿原酸同分异构体、7-oxo-1,3,5-cycloheptatriene-1,2,3,4,5,6-hexayl hexaacetate、7-oxo-1,3,5-cycloheptatriene-1,2,3,4,5,6-hexayl hexaacetate同分异构体、绿原酸、短叶苏木酚酸、柯里拉京同分异构体、柯里拉京、鞣花酸、左旋表儿茶素-3-O-没食子酸酯、3-O-甲基并没食子酸、 3-O-甲基并没食子酸同分异构体、3,3′-二甲基鞣花酸和3-O-甲基鞣花酸4-O-a-L-吡喃鼠李糖苷等17种酚酸类成分。
3.4 黄酮类化合物的鉴定
黄酮类成分中黄酮苷主要发生糖苷键的断裂,形成失去一个或多个糖的次级苷和苷元的碎片离子。黄酮苷含有的糖基主要是鼠李糖、半乳糖、葡萄糖和芸香糖,ESI负离子模式下主要产生丢失该糖基的[M-H-146]-、[M-H-162]-、[M-H-162]-、[M-H-308]-碎片离子。黄酮苷元特征碎片离子m/z301、m/z151,也可以作为黄酮类化合物鉴定的有利证据。以化合物24为例,Q-TOF/MSm/z461.071 4 [M-H]-,产生脱去鼠李糖糖基的碎片离子[M-H-146]-,得到二级碎片离子m/z315,推测其为scutellarin。化合物19的Q-TOF/MSm/z477.066 6 [M-H]-,丢失1个葡萄糖醛酸[M-H-176]-,得到二级碎片离子m/z301[M-H-C6H12O5]-,根据碎片离子m/z179、m/z151推测m/z301为槲皮素母核,推测该化合物为槲皮素-3-O-葡萄糖醛酸苷。结合文献,共鉴定出紫丁香苷、rhamnazin-3-O-rutinoside、槲皮素-3-O-葡萄糖醛酸苷、槲皮素-3-O-葡萄糖醛酸苷同分异构体、dihydromyricelin、槲皮苷、scutellarin和enyssoside等8种黄酮类成分。
3.5 通过对照品验证化合物
根据文献报道的酚酸类和黄酮类成分的裂解规律,对本实验的化学成分质谱裂解规律进行分析,提高鉴定的可信度,并根据对照品的保留时间、分子量和裂解碎片比对,鉴定出4个化合物,分别是化合物3(没食子酸)、10(绿原酸)、18(鞣花酸)和23(槲皮苷)。
3.6 化学成分的相对含量变化
本实验通过提取各主要成分对应的峰面积代表其相对含量,以18号化合物为参照,得到各样品中同一化合物的相对峰面积的平均值,比较各化学成分在火炭母原变种与硬毛火炭母的相对含量变化,见图2。由图2可知,火炭母原变种和硬毛火炭母样品中有26个共有化学成分,其共有成分在量上存在明显的差异。
酚酸类化合物是两种火炭母中含量较高的成分,其中化合物18、3和11的相对峰面积较高,说明其是火炭母中重要的酚酸类物质。化合物11、2和4在硬毛火炭母中的含量明显高于火炭母原变种,而化合物20在火炭母原变种中的含量明显高于硬毛火炭母。
黄酮类成分含量较高的化合物16、17、19、22和23,在硬毛火炭母中的含量明显高于火炭母原变种。
差异化学成分有3个,分别是化合物23、28和29。其中化合物23只在硬毛火炭母中存在、且含量较大;火炭母原变种中含有在硬毛火炭母中未检测到的酚酸类成分化合物28、29。

图2 火炭母原变种与硬毛火炭母化学成分相对峰面积比较Fig.2 The comparison of relative area of chromatography peaks of P.chinense var.chinense and P.chinense var.hispidum注:A:火炭母原变种;B:硬毛火炭母。Note:A:P. chinense var. Chinense;B: P. chinense var. hispidum.
4 讨论
根据负离子模式一级质谱相对分子质量,二级质谱的裂解信息,结合数据库搜索及已报道文献,对25个化合物进行分析,推断出其可能的成分。结果显示,火炭母原变种及硬毛火炭母主要含酚酸类、黄酮类等成分,具有多羟基结构、成分较复杂的特点。利用与对照品比对鉴定出没食子酸、绿原酸、鞣花酸和槲皮苷等4个化合物,实验表明,UHPLC-QTOF-MSMS技术具有快速、精确、灵敏度高等优点,能有效地分析火炭母的成分及主要色谱峰的化学结构,为控制火炭母药材的质量提供依据。
火炭母原变种和硬毛火炭母中各化学成分的含量存在明显差异,其中酚酸类成分在两种火炭母中的含量均较高、硬毛火炭母中黄酮类成分的含量明显高于火炭母原变种。两种火炭母最显著的差异性物质槲皮苷只存在于硬毛火炭母中,且含量较高,因此槲皮苷可作为区别火炭母原变种及硬毛火炭母药材的重要参考标准。槲皮苷是一种黄酮类化合物,具有一定的抗炎、抗动脉粥样硬化、清除多种活性氧自由基、抗病毒、止血等药理活性[20]。因而,槲皮苷的有无是否会导致药理活性的差异尚不得之。本实验可为深入研究两种不同基原火炭母药理活性及临床疗效提供基础资料,为扩大药源、更加全面研究火炭母药材的质量标准和品质评价提供科学依据。

