利拉鲁肽对2型糖尿病合并非酒精性脂肪肝疗效的荟萃分析
张盈盈,金建军
(河南科技大学临床医学院 河南科技大学第一附属医院消化内科,河南 洛阳 471003)
糖尿病是临床常见的一种以糖代谢异常为主要表现的代谢性疾病,且以2型糖尿病(type 2 diabetes,T2DM)常见。非酒精性脂肪肝(non-alcoholic fatty liver disease,NAFLD)是指除外酒精和其他明确的损肝因素所致的肝细胞内脂肪过度沉积为主要特征的临床病理综合征。随着人们生活水平的不断提高,糖尿病发病率和患病率逐年上升,截止到2015年全球糖尿病患者人数已达4.15亿,估计到2040年全球糖尿病患者人数将会上升至6.42亿,其中以T2DM为主[1]。糖尿病易引发各种肝脏损伤,常见的有NAFLD、肝硬化以及肝脏肿瘤等。有文献报道T2DM合并NAFLD的患病率达28%~55%[2-3],显著高于性别、年龄、体重相匹配的非糖尿病患者[4]。利拉鲁肽是人胰高血糖素样肽1类似物,可以促进葡萄糖浓度依赖性的胰岛素合成、分泌及抑制胰高血糖素的释放,激活胃肠道及大脑的人胰高血糖素样肽1受体后,可以减弱胃肠蠕动,延缓胃排空,抑制食欲和食物摄入等。有研究表明[5],利拉鲁肽作为一种新型降糖药物在降糖的同时可以减轻体重、降低血脂,但针对降低肝脏内脂肪含量、肝酶学的疗效报道不一,且目前临床上常用的降糖药物在降糖的同时对NAFLD并没有确切疗效。本研究系统评价利拉鲁肽治疗T2DM合并NAFLD的临床疗效。
1 资料与方法
1.1文献检索 文献检索按照PRISMA(Preferred Reporting Items for Systematic Reviews and Meta-Analyses)流程进行处理[6]。文献的筛选由两位研究者进行中英文检索。英文数据库:PubMed、The Cochrane Library、Embase、Web of Science;中文数据库:中国知网、中国生物医学文献数据、万方数据库,各数据库检索时限均从建库至2018年6月,语言限定为中文和英文,并手工检索相关资料和各论文参考文献目录。采用自由词与主题词相结合的方式,英文检索词:("liraglutide"[MeSH Terms] OR "liraglutide"[All Fields]) AND T2DM[All Fields] AND ("non-alcoholic fatty liver disease"[MeSH Terms] OR ("non-alcoholic"[All Fields] AND "fatty"[All Fields] AND "liver"[All Fields] AND "disease"[All Fields]) OR "non-alcoholic fatty liver disease"[All Fields] OR "nafld"[All Fields];中文检索词为“利拉鲁肽”“非酒精性脂肪肝”“2型糖尿病”“GLP-1受体激动剂”,并以题名、摘要和关键词进行检索。
1.2纳入与排除标准
1.2.1纳入标准 ①研究类型:临床随机对照试验(randomized controlled trial,RCT);②研究对象:诊断为T2DM合并NAFLD的患者,诊断标准符合1999年WHO制订的T2DM标准[7]、2010年版T2DM诊疗指南[8]及2010年中华医学会肝病学会制订的NAFLD的诊断标准[9]。③干预措施:对照组给予常规治疗(生活方式干预、二甲双胍控制血糖),利拉鲁肽组在常规治疗基础上给予利拉鲁肽治疗。④结局指标:主要结局指标为肝脏脂肪含量(liver fat content,LFC)(通过磁共振成像及超声评估分别记为LFC、B超分数)[10-11]。次要结局指标包括三酰甘油(triglyceride,TG)、总胆固醇(total cholesterol,TC)、丙氨酸转氨酶(alanine aminotransferase,ALT)、天冬氨酸转氨酶(aspartate aminotransferase,AST)、糖化血红蛋白(glycated hemoglobin,HbA1c)。
1.2.2排除标准 ①非RCT;②动物实验等基础研究;③分子机制类研究;④由饮酒、病毒或其他不确定因素引起的脂肪肝患者。
1.3文献质量评价 根据Cochrane系统评价手册5.3版中的评估工具对筛选文献进行质量评估,并多人评价,对结果不一致性进行讨论。
1.4资料提取 由两位作者分别独立筛选文献,并对筛选后的文献经仔细阅读全文后进行资料提取。①纳入文献的基本信息(文献作者,发表时间,样本量);②研究对象的特征(性别、年龄、诊断标准、实施国家);③干预措施的特征(利拉鲁肽组和对照组例数,利拉鲁肽剂量、用药频次、用药方法、疗程);④结局指标(研究中的B超分数、LFC、TG、TC、ALT、AST、HbA1c)。使用标准数据提取表对各文献进行数据提取,由第三人核对,若有分歧,需经3人讨论后确定共识意见。
1.5统计学方法 采用Cochrane协作网提供的RevMan 5.3软件进行Meta分析,计量资料以均数及标准差表示。通过加权均差(weight mean difference,WMD)进行结局变量比较。各效应量均采用95%置信区间(95% confidence interval,95%CI)表示,RevMan绘制的森林图系统默认为不利事件,即某研究95%CI横线不与森林图无效线相交并落在无效线左侧时,可认为利拉鲁肽组某指标的均数小于对照组,即利拉鲁肽组的试验因素会减少不利事件的发生,说明试验因素为有益因素并有效。当研究有利事件并应用RevMan绘制森林图需改变系统默认值(即将无效竖线左右结局指标调换),检验水准α=0.05。对纳入研究进行异质性检验,异质性检验以I2表示,I2<25%,表明异质性较小,25%≤I2<50%为中度异质,I2≥50%为高度异质。若研究结果的效应量无明显统计学异质性,采用固定效应模型进行Meta分析。若I2≥50%,存在高度异质性,需进行敏感性及亚组分析讨论异质性来源,并采用随机效应模型进行分析。
2 结 果
2.1文献检索结果 最初筛选文献共139篇,其中英文127篇,中文12篇,通过排除重复文献、初筛并阅读全文后,最终筛选出符合标准的RCT文献10篇(英文3篇,中文7篇)。筛选文献流程见图1,纳入文献的基本特征见表1。文献总体质量为中等,评价结果见图2。
2.2Meta分析结果
2.2.1利拉鲁肽组与对照组LFC水平、B超分数分析 共有2篇[13-14]RCT报道了LFC水平,共170例,其中利拉鲁肽组85例,对照组85例。各研究间异质性较小(P=0.77,I2=0%),采用固定效应模型合并分析,Meta分析结果显示利拉鲁肽组LFC水平低于对照组(WMD=-5.84,95%CI-7.58~-4.10,P<0.000 01),见图3。共有2篇[7-8]RCT报道了B超分数水平,共188例,其中利拉鲁肽组100例,对照组88例。各研究间异质性较小(P=0.40,I2=0%),采用固定效应模型合并分析,Meta分析结果显示利拉鲁肽组B超分数低于对照组(WMD=-0.98,95%CI-1.13~-0.83,P<0.000 01),见图4。
2.2.2利拉鲁肽组与对照组TG水平分析 共有9篇[10-12,14-19]RCT报道了TG水平,共665例,其中利拉鲁肽组347例,对照组318例。各研究间存在中度异质性(P=0.17,I2=31%),采用固定效应模型合并分析,Meta分析结果显示利拉鲁肽组TG水平低于对照组(WMD=-0.50,95%CI-0.56~-0.43,P<0.000 01),见图5。
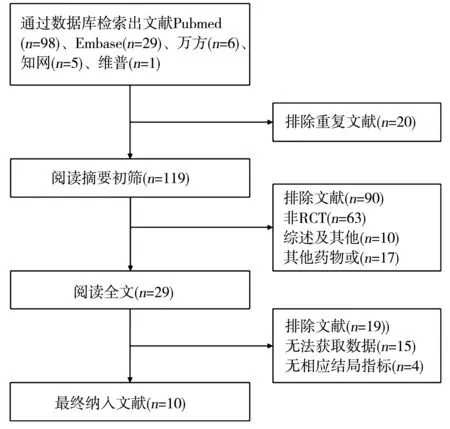
RCT:随机对照试验

表1 纳入文献的基本特征
TG:三酰甘油;TC:总胆固醇;ALT:丙氨酸转氨酶;AST:天冬氨酸转氨酶;HbA1c:糖化血红蛋白;HDL:高密度脂蛋白;LDL:低密度脂蛋白;LFC:肝脏脂肪含量;BMI:体质指数;FBG:空腹血糖
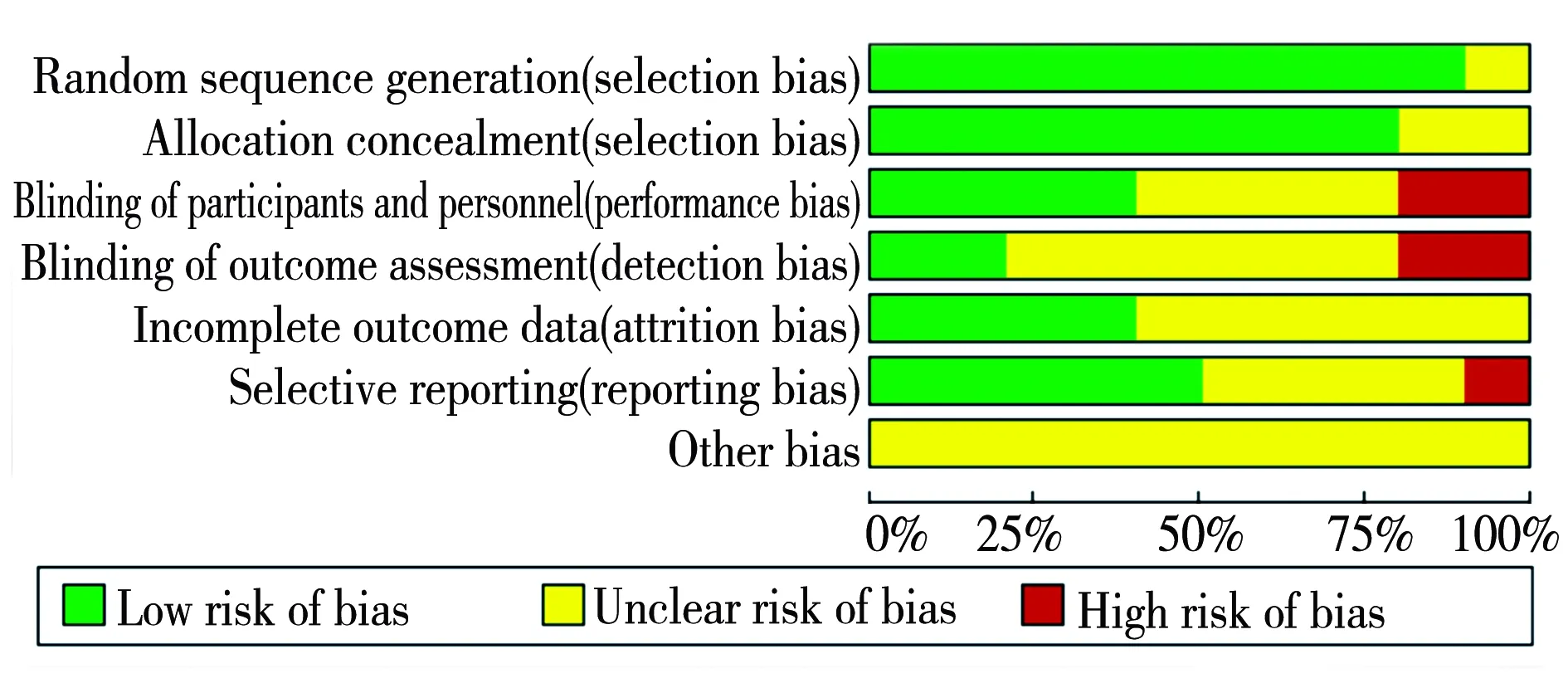
图2 质量评价图
2.2.3利拉鲁肽组与对照组TC水平分析 共有8篇[10-12,15-19]RCT报道了TC水平,共546例,其中利拉鲁肽组279例,对照组267例。各研究间存在中度异质性(P=0.14,I2=37%),采用固定效应模型合并分析,Meta分析结果显示利拉鲁肽组TC水平低于对照组(WMD=-1.28,95%CI-1.38~-1.19,P<0.000 01),见图6。
2.2.4利拉鲁肽组与对照组ALT水平分析 共有9篇[10-16,18-19]RCT报道了ALT水平,共674例,其中利拉鲁肽组343例,对照组331例。各研究间存在高度异质性(P<0.000 01,I2=99%),采用随机效应模型合并分析,Meta分析结果显示利拉鲁肽组与对照组ALT水平比较差异无统计学意义(P>0.05),见图7。
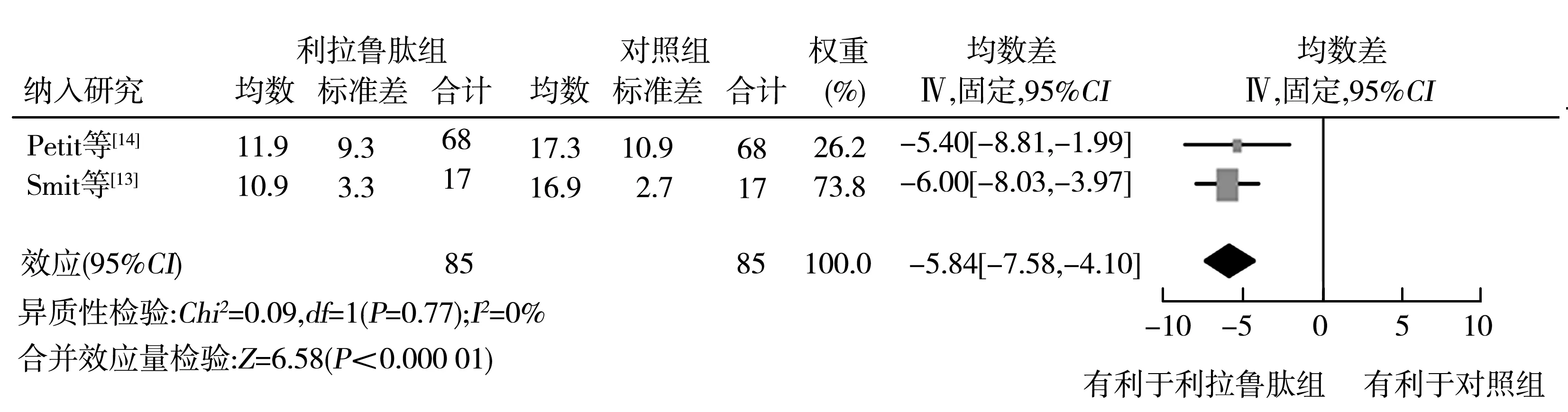
T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝;LFC:肝脏脂肪含量

T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝
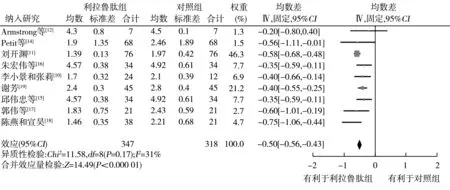
T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝;TG:三酰甘油
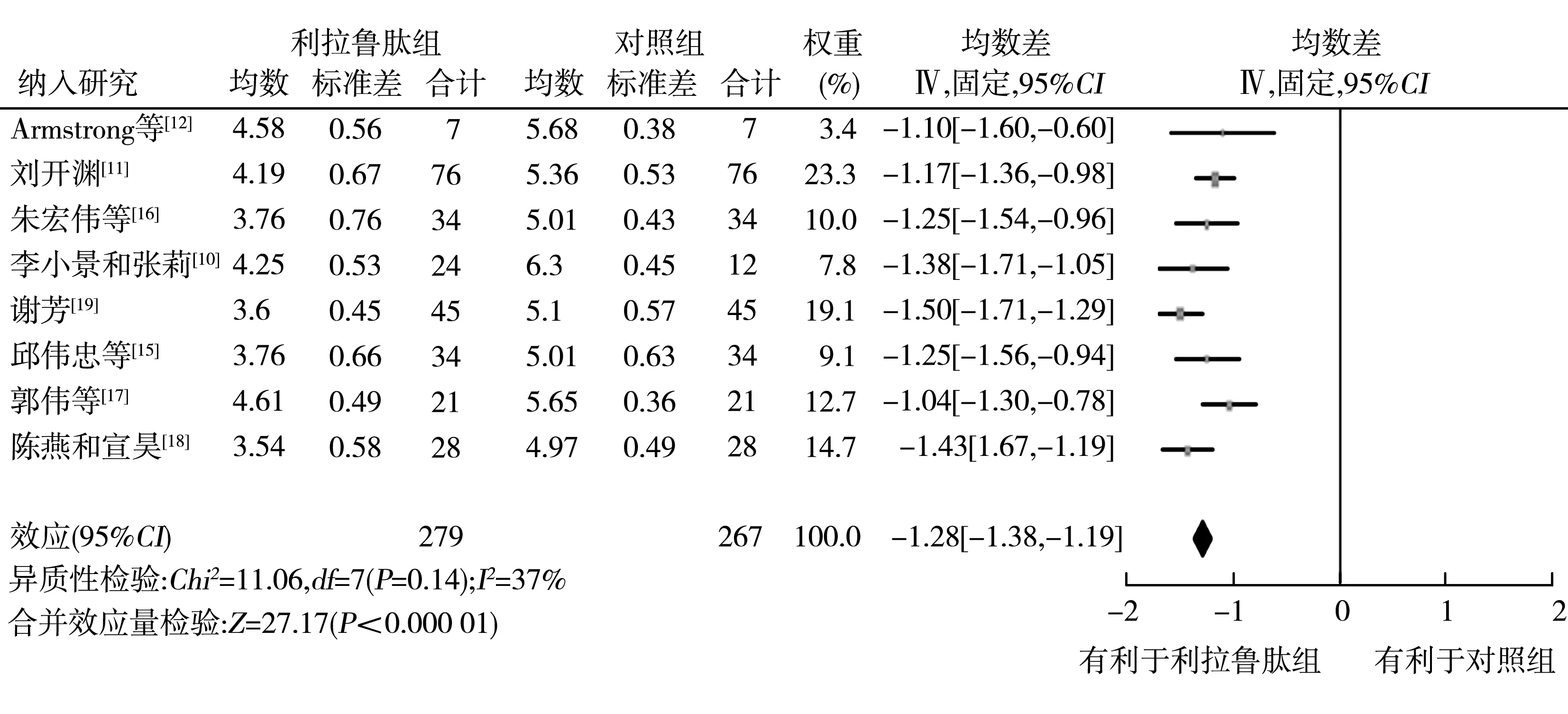
T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝;TC:总胆固醇
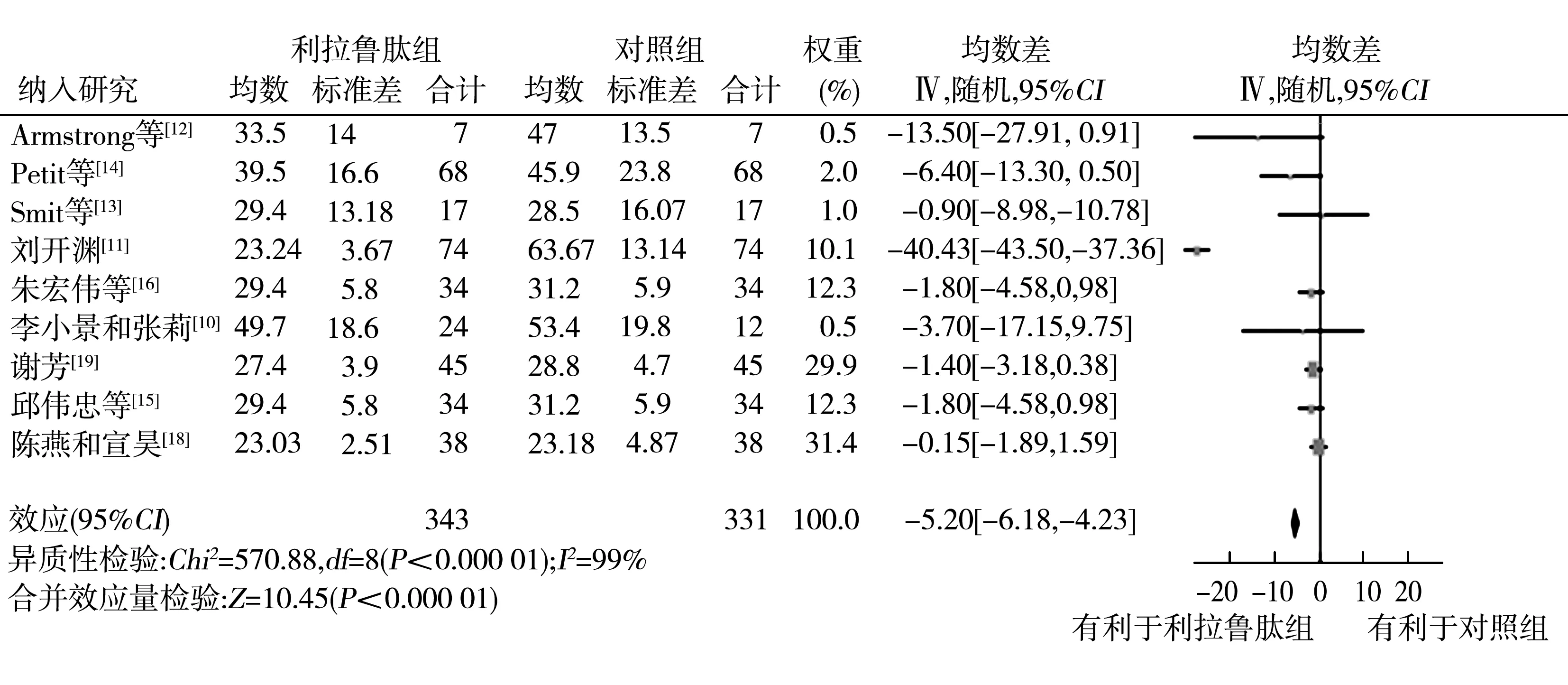
T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝;ALT:丙氨酸转氨酶
2.2.5利拉鲁肽组与对照组AST水平分析 共有9篇[10-16,18-19]RCT报道了AST水平,共674例,其中利拉鲁肽组343例,对照组331例。各研究间存在中度异质性(P=0.05,I2=49% ),采用固定效应模型合并分析,Meta分析结果显示利拉鲁肽组AST水平低于对照组(WMD=-3.95,95%CI-4.94~-2.96,P<0.000 01),见图8。
2.2.6利拉鲁肽组与对照组HbA1c水平分析 共有7篇[12-17,19]RCT报道了HbA1c水平,共452例,其中利拉鲁肽组226例,对照组226例。各研究间存在高度异质性(P<0.000 01,I2=93%),见图9。通过逐一剔除文献进行灵敏性分析及按照用药剂量及用药时间进行亚组分析,异质性仍较大,考虑异质性可能与纳入样本量过小、血红蛋白基线值、检测方法等有关,采用随机效应模型进行合并,Meta分析结果显示利拉鲁肽组HbA1c水平低于对照组(WMD=-0.92,95%CI-1.09~-0.75,P<0.000 01),见图10。
2.3异质性分析及发表偏倚分析 TG水平的漏斗图中效应点基本位于顶部且基本对称,说明无明显发表偏倚,本研究将每项研究按所占权重逐一剔除进行敏感性分析,并未影响Meta分析结果,说明纳入文献的稳定性良好,本研究结果真实可靠。见图11。

T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝;AST:天冬氨酸转氨酶

T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝;HbA1c:糖化血红蛋白

T2DM:2型糖尿病;NAFLD:非酒精性脂肪肝;HbA1c:糖化血红蛋白
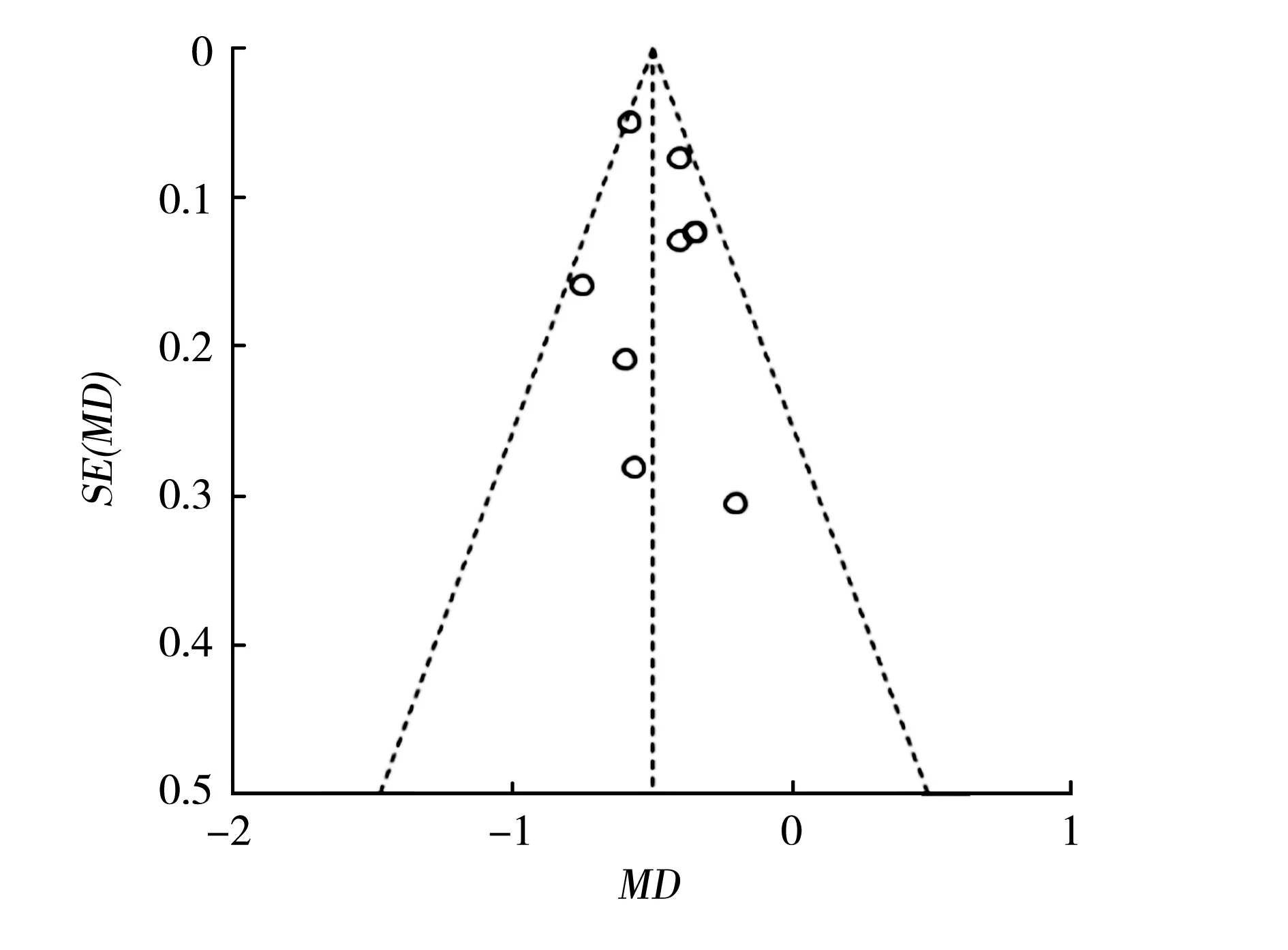
TG:三酰甘油
3 讨 论
NAFLD作为一种慢性病,在T2DM患者中的发生率高达62%,可能因女性体内雌激素有一定保护的作用,所以女性发生率略低于男性[20]。临床NAFLD最常见的因素有血脂紊乱、肥胖及T2DM,且与冠心病、高血压以及动脉粥样硬化等均被称为代谢综合征,其共同的作用机制为胰岛素抵抗[20]。有研究提示,NAFLD患者有与胰岛素抵抗相关的较高血浆抵抗素,并与胰岛素抵抗呈正相关[21]。胰岛素抵抗可使脂代谢出现紊乱,空腹胰岛素水平升高可使血浆高密度脂蛋白水平降低,TG水平升高[22]。健康人群的机体存在胰岛素敏感酯酶抑制作用,使脂肪酸被有效存储,并不释放入血,相反在糖尿病患者中由于肝脏存在胰岛素抵抗现象会造成血浆中非酯化脂肪酸与胆固醇水平升高,高密度脂蛋白水平降低,导致脂代谢紊乱,此时肝细胞遭到大量脂肪入侵,造成肝内脂肪沉着、肝细胞变性、坏死等,进一步形成脂肪肝,肝源性胰岛素抵抗是NAFLD发生的关键[23]。NAFLD的发病机制目前尚不十分清楚,认为它是一种获得性代谢应激性肝损伤,并且与胰岛素抵抗和遗传易感性密切相关。而T2DM合并NAFLD会进一步恶化糖代谢,增加非酒精性脂肪性肝炎发生率,高糖毒性、高脂毒性的并存明显增加了糖尿病大血管事件的发生率,并且加速了脂肪肝向肝硬化甚至肝癌转化的进程[23-24]。近年来,Day和James[25]提出的“二次打击”学说占主导地位,其核心仍为胰岛素抵抗。胰岛素抵抗同时也是T2DM的主要发病机制之一。由此可知,T2DM与 NAFLD之间有共同的作用机制,即胰岛素抵抗。
本研究Meta分析结果显示,利拉鲁肽组LFC、B超分数、TG、TC、AST、HbA1c水平低于对照组(P<0.05)。由此可得出,利拉鲁肽在有效降低T2DM合并NAFLD患者血糖的同时,可有效降低LFC,改善血脂,有效治疗T2DM合并NAFLD。但目前对于利拉鲁肽治疗NAFLD的作用机制尚不明确,其作用机制可能是通过提高脂联素水平、阻断c-Jun氨基端激酶信号通路、AMP活化的蛋白激酶-哺乳动物雷帕霉素靶蛋信号通路增强自噬、降低肝组织中的胰岛素样生长因子2-mRNA结合蛋白3来改善胰岛素抵抗,从而发挥治疗T2DM合并NAFLD的作用[26-27]。本研究数据显示,利拉鲁肽可以明显改善T2DM合并NAFLD患者的血糖、血脂、肝酶及LFC,其治疗机制可能与利拉鲁肽具有改善胰岛素抵抗的作用有关[28]。
总之,利拉鲁肽可有效治疗T2DM合并NAFLD,但仍需进一步研究为临床提供充分的循证医学证据。

