地西他滨联合改良CAG方案在急性髓系白血病中的应用价值
胡 萌,程英英,杨海平
(河南科技大学第一附属医院血液科,洛阳 471000)
急性髓细胞性白血病(acute myelocytic leukemia,AML)是一种血液科较为常见的髓系造血干细胞恶性增殖性疾病,包括所有源自非淋巴细胞的急性白血病,是一种高度异质的疾病群,由正常髓系细胞在分化过程中的造血祖细胞恶性变转化[1-2]。AML的临床表现主要有脏器浸润、出血、感染、代谢异常、贫血等。自1995年国外首次报道CAG(阿克拉霉素+阿糖胞苷+粒细胞集落刺激因子)方案治疗AML以来,临床上广泛使用CAG方案治疗复发性、难治性、低增生以及老年AML,并取得一定疗效,但是缓解率仍不理想。如何提高AML的治疗效果目前仍是临床上的一个棘手问题[3]。地西他滨属于一种DNA甲基化转移酶抑制剂,通过将DNA过度甲基化使基因重新激活,最终诱导肿瘤细胞分化和凋亡[4]。目前已有研究证实地西他滨与其他治疗方法的联合治疗方案在AML治疗中取得了一定成效,但各研究结果存在一定差异[5-6]。因此,本研究选取2016年8月~2019年2月我院收治的AML患者80例作为研究对象,旨在探讨地西他滨联合改良CAG方案在AML治疗中的临床价值,为提高AML的临床疗效提供参考依据,现报道如下。
1 资料与方法
1.1 一般资料
选取2016年8月~2019年2月我院收治的AML患者作为研究对象。纳入标准:① 符合WHO造血与淋巴组织肿瘤分类(2016)[7]中关于AML的相关诊断标准,且经骨髓细胞形态学、细胞遗传学以及分子生物学等明确分型诊断;② 年龄≥18岁;③ 临床资料完整;④ 患者自愿参与本研究,并签署知情同意书。排除标准:① 合并严重心、肝、肾等其他脏器疾病;② 合并精神性疾病或者认知功能障碍;③ 近期曾接受过其他治疗;④合并其他恶性肿瘤。本研究经我院伦理委员会批准实施。最终纳入研究的患者共80例,按照就诊顺序单双号分为对照组(n=40)与观察组(n=40)。
1.2 给药方法
对照组患者予改良CAG方案治疗:注射用盐酸阿克拉霉素(扬州奥赛康药业有限公司,国药准字H20060196,规格:20 mg),于治疗周期d 1、d 3、d 5、d 7 静脉滴注;注射用阿糖胞苷[赛德萨,阿特维斯(佛山)制药有限公司,进口药品注册标准JX20040073,规格:0.5 g]10~15 mg/m2在治疗周期d 1~14静脉滴注,q12h;重组人粒细胞集落刺激因子注射液(协和发酵麒麟株式会社,国药准字S200100631,规格:300 μg),于治疗周期d 1~14静脉滴注,qd。治疗过程密切监测患者各项相关指标,当白细胞升高至20×109/L时,先中止给予重组人粒细胞集落刺激因子注射液。观察组在对照组的基础上联用注射用地西他滨(江苏豪森药业集团有限公司,国药准字H20130067,规格:50 mg)15 mg/m2,于治疗周期的d 2、d 4、d 6静脉滴注。治疗过程中,详细记录所有患者的临床症状及体征变化,定期复查血常规及肝肾功能,同时予保心、保肝及护胃等对症处理,在必要时予输血小板、抗感染等支持治疗。所有患者均连续治疗2个疗程,14天为1个疗程。
1.3 观察指标
治疗结束后比较两组的完全缓解率和总缓解率[(完全缓解例数+部分缓解例数)/组例数×100%],并记录治疗期间患者的不良反应发生情况。疗效评价标准依据患者的临床表现、外周血及骨髓象进行评定。完全缓解:患者白血病症状和体征完全消失,患者生活基本恢复正常;女性患者或者儿童血红蛋白>90 g/L,男性>100 g/L,血小板计数>100×109/L,中性粒细胞>1.5×109/L,外周血细胞中无白血病细胞;骨髓象原始单核细胞、幼稚单核细胞及幼稚淋巴细胞或者原始淋巴细胞的比例小于5%,巨核细胞和红细胞均恢复正常。部分缓解:患者临床症状或者血常规有一项未满足上述标准,骨髓象原始单核、幼稚单核细胞及幼稚淋巴细胞或者原始淋巴细胞的比例为5%~20%。无缓解:患者的临床症状、血常规以及骨髓象均未满足完全缓解和部分缓解的标准。不良反应参照WHO关于抗癌药物不良反应以及分级标准[8]。
1.4 统计学方法

2 结果
2.1 两组患者基线资料比较
两组患者一般资料无统计学差异,具有可比性,见表1。
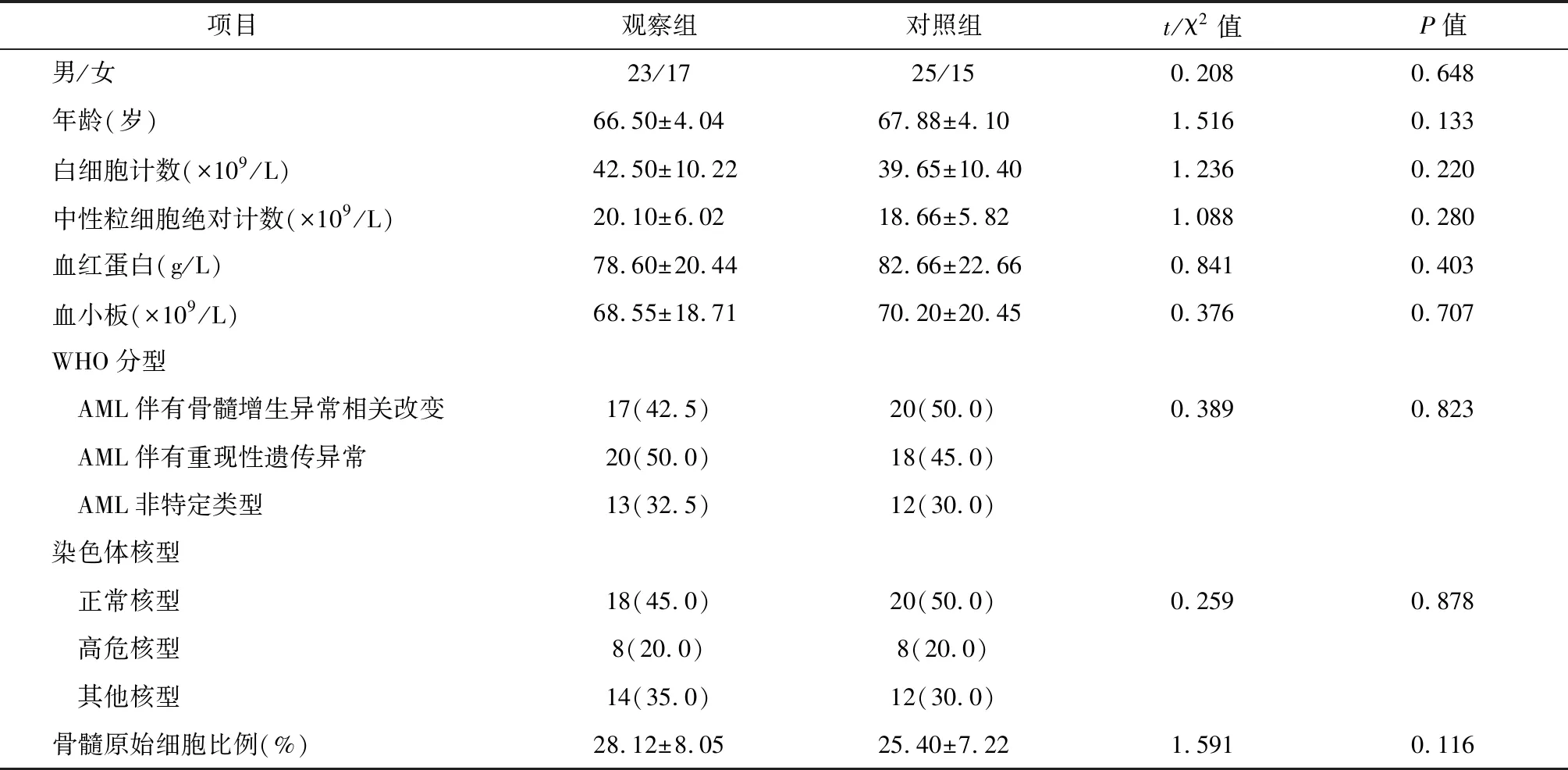
表1 两组患者基线资料比较 n=40
2.2 两组患者完全缓解率和总缓解率比较
观察组完全缓解率(60.0%)显著高于对照组(30.0%),观察组总缓解率(77.5%)显著高于对照组(50.0%),差异有统计学意义(P<0.05)。见表2。

表2 两组患者完全缓解率和总缓解率比较 n=40,n(%)
2.3 两组患者的不良反应情况比较
两组患者各项不良反应比较无统计学差异,见表3。
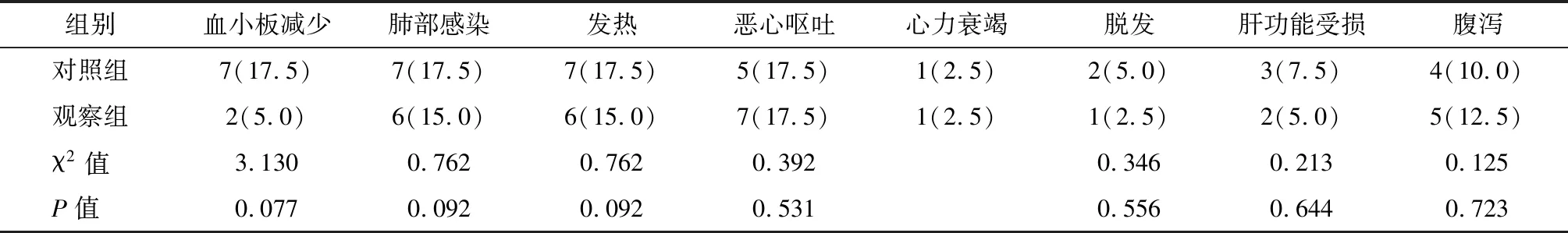
表3 两组患者的不良反应情况比较 n=40,n(%)
3 讨论
CAG方案是现阶段临床治疗AML的常用方案。粒细胞集落刺激因子与幼稚细胞表达的粒细胞集落刺激因子受体结合,促进生成粒细胞集落,加强药物对白血病细胞的杀伤力,同时还可提高幼稚细胞对药物的敏感度,促使粒细胞成熟并向外周血释放,使骨髓抑制作用周期明显缩短,减少不良反应[9]。阿糖胞苷可与肿瘤细胞的DNA结合,进而破坏肿瘤细胞的DNA结构,抑制DNA转录与复制,加速肿瘤细胞凋亡,最终阻止肿瘤恶性增殖[10]。此外,粒细胞集落刺激因子可有效增强较小剂量的阿糖胞苷对髓系白血病细胞的诱导凋亡和分化作用,在CAG治疗患者的外周血中检出的凋亡细胞数量与疗效有关。高亲脂性蒽环类抗恶性肿瘤药物阿克拉霉素,属于细胞周期非特异性药物,在生物体内能够迅速穿过磷脂双分子层,最后进入细胞核,嵌入DNA双螺旋结构并中断DNA转录及复制,从而使癌细胞的有丝分裂停滞于G1晚期以及S晚期,最终控制癌灶扩张[11]。CAG方案是3种药物联合使用,可通过不同的药理作用直接杀灭癌细胞,并加强自身免疫对肿瘤细胞的攻击,发挥强效抗癌作用。但是,目前报道CAG方案治疗AML的总缓解率约为50%~60%[12-13],同时本研究中对照组患者单独使用CAG方案治疗的总缓解率为50.0%,与上述报道相符。可见单独使用CAG方案治疗效果不理想,仍需进一步优化。
普遍认为,肿瘤的发展涉及某些癌基因的活化以及抑癌基因的失活。DNA异常甲基化可造成抑癌基因表达丢失、功能失效,进而导致细胞恶性转化,而这些基因涉及细胞生长与分化、周期调控、DNA修复、血管生成及侵袭等多种生物学过程[14]。近几年来,DNA甲基化相关研究进展迅速,使用去甲基化药物治疗AML的方案备受关注。地西他滨属于一种2-脱氧胞苷类似物,具有显著的去甲基化作用。同时,该药具有与5-氮杂胞苷类似的结构,因此可发挥与5-氮杂胞苷相似的药理作用,抑制肿瘤DNA甲基转移酶的活性,迅速改善抑癌基因的过度甲基化,从而重新启动细胞的正常衰老凋亡系统。地西他滨对DNA甲基化的抑制作用是传统5-氮杂胞苷的30倍[15]。此外,地西他滨还可提高白血病细胞对阿糖胞苷的敏感度,激活TRAIL通路,诱导AML细胞凋亡;同时可诱导T淋巴细胞协同刺激分子,克服免疫耐受,促使CTL细胞发挥抗肿瘤作用。地西他滨自2006年经美国FDA批准用于治疗骨髓增生异常综合征以来,至今已被广泛应用于西方发达国家临床之中,并且已有较多地西他滨成功治疗慢性、急性髓细胞性白血病的相关报道。张婧玲等[16]Meta分析发现地西他滨联合CAG治疗中、高危骨髓增生异常综合征及AML具有确切且显著的疗效,优于地西他滨和CAG方案的单药方案。周冰等[17]表示,地西他滨联合CAG的治疗方案应用于复发难治性AML患者,可显著提高治疗效果,降低死亡率,且不会增加不良反应的发生风险。在孟景晔等[18]的研究中,接受地西他滨联合CAG方案治疗的AML患者总有效率(72.22%)显著高于单独接受CAG方案治疗(50.0%)的患者。同时,本研究结果显示:观察组完全缓解率(60.0%)显著高于对照组(30.0%),观察组总缓解率(77.5%)显著高于对照组(50.0%),提示地西他滨联合CAG方案治疗AML,能有效抑制癌细胞增殖,促进癌灶凋亡,从而有效提高完全缓解率和总缓解率,与上述报道相符。在吴国才等[19]的研究中,采用地西他滨联合CAG方案治疗的AML患者肺部感染和发热的发生率较高。而本研究结果显示两组不良反应发生情况比较无统计学差异,与报道结果差异较大,可能是纳入研究的患者年龄差异较大所致。李志慧[20]的研究结果显示,CAG联合地西他滨治疗与单独使用CAG方案后成人AML出现的不良反应比较无统计学差异,与本研究结果一致,说明地西他滨联合CAG方案治疗AML具有安全性和可行性。由于样本量较小,或患者就医偏倚(医院选择),本研究结果可能存在一定偏倚,因此仍需更深入的研究予以进一步证实。
综上所述,地西他滨联合改良CAG方案治疗AML可有效提高完全缓解率和总缓解率,且没有增加不良反应发生的风险,具有安全性和可行性,有较高的临床价值。

