海底电缆铜铠装层在舟山海水模拟溶液中的腐蚀行为
胡家元1,钱洲亥1,张 娣,王 竹,张 雷
(1. 国网浙江省电力有限公司 电力科学研究院,杭州 310014; 2. 北京科技大学,北京 100083)
随着全球石化能源的枯竭和人类对电力需求的不断增加,世界各国都大力发展新能源产业,特别是海洋领域的新能源开发,例如海上风机发电、海洋潮汐能、海洋天然气与石油开采等,而海上新能源至陆地使用的通道只有一个,那就是海底电缆[1-3]。舟山500 kV联网输变电工程旨在满足“一带一路”战略新形势下浙江舟山群岛新区经济增长用电需求,进一步提高宁波舟山电网抵御自然灾害的能力。海底电缆敷设在海水中,其最外层的铠装铜丝直接接触海水,由于海水中存在腐蚀性离子、细菌等腐蚀因素[4],容易造成铠装铜丝的腐蚀损坏,影响海缆寿命[5-8]。
电缆铠装层可以增加电缆的机械强度,提高防侵蚀能力,还可以增强抗拉强度、抗压强度等,延长电缆的使用寿命。因此研究如何提高海缆铠装层寿命对海缆的长期安全运行尤为重要。但是要想研究提高海缆铠装层寿命的方法,首先就要研究海缆铠装层材料无氧铜的腐蚀规律,从而得出无氧铜材料的防腐蚀方法,进而得出延长海缆寿命的方法。
本工作选择交流500 kV海底电缆铠装无氧铜丝,通过在舟山海水模拟溶液中的全浸试验,结合极化曲线对比分析海水中不同的腐蚀性离子,即Cl-、SO42-、HCO3-对海底电缆铠装铜丝的影响规律,建立海底电缆铜铠装层在舟山海水模拟溶液中的腐蚀主控因素,以期为海底电缆的腐蚀防护提供一定的理论支撑。
1 试验
试验用无氧铜取自交流500 kV交联聚乙烯海底电缆铜铠装层,其化学成分见表1。

表1 试验材料的化学成分Tab. 1 Chemical composition of test material %
模拟腐蚀试验采用棒状试样,尺寸为φ7 mm×5 cm,每个试验条件下取3个平行试样,用于腐蚀形貌观察及腐蚀速率测量。试验前,用水砂纸(200~1 200 号)逐级打磨试样表面,丙酮超声清洗10 min后,用蒸馏水和无水乙醇清洗,干燥后备用。
对舟山海水成分进行取样检测分析,结果显示,舟山海水中主要含有Cl-、SO42-和HCO3-等阴离子,其余阴离子的含量可忽略不计,因此,为了研究这三种离子对无氧铜的腐蚀影响,根据检测结果配置4种试验溶液,分别为只含1.33×104mg/L Cl-的1号溶液,只含2.48×103mg/L SO42-的2号溶液,只含143.8 mg/L HCO3-的3号溶液和模拟舟山海水溶液(4号溶液,含1.33×104mg/L Cl-+2.48×103mg/L SO42-+143.8 mg/L HCO3-)。每组设置3个平行试样,浸泡周期分别为30,60,90 d;试验温度为常温(25 ℃)和38 ℃[9]。
模拟腐蚀试验结束后,用除锈液(100 mL浓硫酸稀释成1 000 mL稀硫酸)去除试样表面腐蚀产物,然后依次用蒸馏水、无水酒精清洗后烘干。根据试验前后试样腐蚀质量损失计算腐蚀速率,见式(1)。

(1)
式中:v为腐蚀速率,mm/a;K=8.76×104;D为密度,g/cm3,铜的密度为8.94 g/cm3;A为试样表面积,mm2;T为试验时间,d。
采用Quanta 250型环境扫描电镜(SEM)及其附带能谱仪(EDS)对试验后试样的表面腐蚀形貌和腐蚀产物进行观察和分析。
电化学试验用试样为工作面积10 mm×10 mm的海缆铜铠装试样,将导线焊接在试样的一端,非工作面用环氧树脂(100 g环氧树脂+7 g邻苯二甲酸二丁酯+10 g乙二胺)封装。电化学试验在CHI660D电化学工作站上完成,采用标准三电极体系,辅助电极(CE)为铂(Pt)电极,参比电极(RE)为饱和甘汞电极(SCE),工作电极(WE)为海缆铜铠装试样。文中电位若无特指,均相对于SCE。首先测量试样的开路电位(OCP),待开路电位的波动范围稳定在±0.005 V之内时,进行动电位极化曲线测量。
2 结果与讨论
2.1 开路电位与极化曲线
由图1(a)可见:在常温条件下,在4种溶液中,海缆铜铠装试样的开路电位在初期略有下降,后趋于稳定,其在1~4号溶液中的稳定开路电位分别为-0.16,0.006,-0.07,-0.20 V。试样在4号溶液(模拟海水溶液)中的开路电位最负,在2号溶液(只含2.48×103mg/L SO42-的溶液)中的最正,即无氧铜在模拟海水溶液中最易发生腐蚀,在SO42-作用下最不易发生腐蚀。这是因为模拟海水溶液中不仅含有单一的腐蚀离子,还会发生腐蚀离子间的相互促进作用,因此腐蚀比较严重。由图1(b)可见:与在常温中的情况一致,试样在38 ℃、4种溶液中的开路电位初期也略有下降,后趋于稳定,其在1~4号溶液中的开路电位分别-0.19,-0.05,-0.08,-0.32 V,即无氧铜在38 ℃的模拟海水溶液中最易发生腐蚀,在SO42-作用下最不易发生腐蚀,这与常温条件下的腐蚀规律一致,说明铜腐蚀的主要影响因素为离子因素,温度对腐蚀的影响较小。

(a) 25 ℃
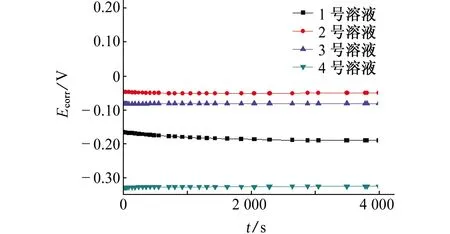
(b) 38 ℃图1 不同温度条件下,试样在4种溶液中的开路电位Fig. 1 Open circuit potentials of samples in 4 solutions at 25 ℃ (a) and 38 ℃ (b)
对图2所示极化曲线进行拟合可知:在25 ℃条件下,试样在1~4号溶液中的腐蚀电流密度分别为12.15,0.59,0.62,12.15 μA·cm-2,即试样在4号溶液中的腐蚀最严重;在38 ℃条件下,试样在1~4号溶液中的腐蚀电流密度分别为0.89,1.28,1.44,12.55 μA·cm-2。综上,在两种温度条件下,试样均在4号溶液(模拟海水溶液)中发生最严重的腐蚀。

(a) 25 ℃

(b) 38 ℃图2 不同温度下,试样在4种溶液中的极化曲线Fig. 2 Polarization curves of the samples in 4 solutions at 25 ℃ (a) and 38 ℃ (b)
2.2 平均腐蚀速率
铜及铜合金在海洋环境中以均匀腐蚀为主,且其在全浸区的腐蚀最重。赵月红等通过铜及其合金的长期暴露试验发现:随着暴露时间的延长,铜及铜合金的平均腐蚀速率降低;随着海水温度的升高,多数铜及其合金在全浸区的平均腐蚀速率增加[7-8]。
由图3可见:在2种温度条件下,试样在4种溶液中的腐蚀速率基本均随着腐蚀时间的延长而减小,这和电化学测试所显示的规律是一致的。这是因为随着腐蚀时间的延长,腐蚀产物膜增厚且变得稳定,从而降低腐蚀速率。综合浸泡试验结果可知:在不同腐蚀环境中,无氧铜的腐蚀速率均随着温度的升高而略有增加。

(a) 25 ℃

(b) 38 ℃图3 不同温度条件下,浸泡时间对试样在不同溶液中腐蚀速率的影响Fig. 3 Effect of immersion time on corrosion rate of samples in different solutions at 25 ℃ (a) and 38 ℃ (b)
2.3 腐蚀产物的微观形貌
由图4~7可见:无氧铜在4种溶液中的腐蚀具有一定的差异。与未腐蚀试样相比,无氧铜在1号和4号溶液中的腐蚀产物膜最厚,而且在不同的腐蚀环境中,腐蚀产物的形貌也不相同。
由图4可见:在1号溶液中,腐蚀初期,试样表面腐蚀产物膜较薄,且并没有完全覆盖基体;随着腐蚀时间的延长,腐蚀产物膜完全覆盖基体,产物层较厚,且有部分脱落,较厚的产物层阻挡了无氧铜与溶液直接接触,腐蚀速率降低。
由图5和6可见:在2号和3号溶液中,腐蚀初期,试样表面腐蚀产物膜都较薄,不能阻挡无氧铜与溶液直接接触,腐蚀继续进行;腐蚀后期,腐蚀产物膜增厚,基本完全覆盖基体,且没有出现产物膜脱落现象,腐蚀被抑制,腐蚀速率降低。
由图7可见:在4号溶液中,腐蚀初期,试样表面腐蚀产物膜较薄,且已有部分脱落;腐蚀后期,腐蚀产物增多,但腐蚀产物呈疏松状,对基体的保护性较差,因此,虽然试样在腐蚀后期的腐蚀速率有所降低,但仍比在其他环境中的大。

(a) 30 d (b) 60 d (c) 90 d图4 试样在1号溶液中腐蚀不同时间后的表面SEM形貌 Fig. 4 Surface SEM morphology of samples corroded in solution No. 1 for different times

(a) 30 d (b) 60 d (c) 90 d图5 试样在2号溶液中腐蚀不同时间后的表面SEM形貌Fig. 5 Surface SEM morphology of samples corroded in solution No. 2 for different times

(a) 30 d (b) 60 d (c) 90 d图6 试样在3号溶液中腐蚀不同时间后的表面SEM形貌 Fig. 6 Surface SEM morphology of samples corroded in solution No. 3 for different times

(a) 30 d (b) 60 d (c) 90 d图7 试样在4号溶液中腐蚀不同时间后的表面SEM形貌Fig. 7 Surface SEM morphology of samples corroded in solution No. 4 for different times
研究发现[8-18],在SO42-存在的环境中,铜表面会形成2层铜绿,内层是Cu2O,外层是Cu4SO4(OH)6。Cu4SO4(OH)6层很可能是由Cu2O层外部的水表层发生沉淀反应形成的。
腐蚀形貌观察结果表明,无氧铜以均匀腐蚀为主,且其在3号溶液中的腐蚀程度最低,在4号溶液中的腐蚀程度最大,这与电化学试验结果一致。
2.4 腐蚀产物成分
由图8可见:试样在4种溶液中腐蚀后,表面腐蚀产物存在差异,在1号溶液中形成的腐蚀产物主要含有CuO;在2号溶液中形成的腐蚀产物主要含有Cu2O,没有生成Cu4SO4(OH)6,这可能是由于溶液中SO42-含量较低或腐蚀时间较短;在3号溶液中形成的腐蚀产物主要含有CuO;在4号溶液中形成的腐蚀产物主要含有Cu2O、CuS和Cu2Cl(OH)3。
铜及铜合金在含氧海水中的腐蚀是吸氧腐蚀,在一定条件下,阳极反应产生的Cu2O可在铜表面形成完整的保护膜,其表层的Cu2O在水中溶解氧的作用下被部分氧化成CuO。因此,铜表面的氧化物保护膜具有双层结构,其内层为Cu2O,外层则由Cu2O和CuO组成。铜表面这种保护膜的形成防止了铜在水中的进一步腐蚀,其完整性和稳定性也决定了铜在水中的腐蚀速率。
综合各种离子对铜腐蚀的影响,腐蚀产物最外层为绿色的碱式氯化铜Cu2Cl(OH)3,在碱式氯化铜下为暗红色的氧化亚铜(Cu2O)中间层,最底层为白色的氯化亚铜(CuCl)[19]。
由于铜锈最外层结构疏松并存在薄弱区域,环境中的水和氧气很容易进入到铜锈内部与 CuCl直接接触而反应生成蓬松的CuCl2·3Cu(OH)2和HCl,见式(2)。当生成的HCl与基底铜直接接触时会生成CuCl,见式(3);当HCl分别与Cu2O和Cu2(OH)2CO3接触时都会发生反应从而生成CuCl2·3Cu(OH)2,见式(4)~(5)[20]。CuCl2·3Cu(OH)2在局部区域不断累积,形成了腐蚀瘤。由于CuCl2·3Cu(OH)2为蓬松的结构,更易于周围环境中水分和氧气的进入,加速腐蚀,使腐蚀不断扩展和深入。

2HCl
(2)
(3)

(a) 1号溶液

(b) 2号溶液

(c) 3号溶液

(d) 4号溶液图8 在不同溶液中腐蚀后试样表面腐蚀产物的XRD图谱Fig. 8 XRD patterns of corrosion products on the surface of samples corroded in different solutions
(4)

(5)
综上所述,当环境中同时存在Cl-、SO42-和HCO3-等3种离子时,会对腐蚀产生协同效应,使腐蚀速率增加,腐蚀产物种类也会不同,腐蚀加剧。
3 结论
(1) 在阴离子Cl-、SO42-、HCO3-中,Cl-对铜的腐蚀起主要作用。
(2) 常温条件下,铜在单一HCO3-模拟溶液中的腐蚀倾向最低,在模拟海水溶液中的腐蚀倾向最高;38 ℃条件下,铜在单一SO42-模拟溶液中的腐蚀倾向最低,在模拟海水溶液中的腐蚀倾向最高。
(3) 铜铠装在含有单一HCO3-的模拟溶液中的腐蚀程度最低,在模拟舟山海水溶液中的腐蚀程度最大,这与电化学结果相一致。
(4) 铜在模拟海水溶液中的腐蚀产物主要为铜的氧化物Cu2O和CuO。

