嘧啶苯磺酰脲衍生物除草活性的CoMFA模型
冯 惠,石春玲,李 靖,冯长君
(徐州工程学院材料与化学工程学院,中国 徐州 221018)
上世纪70年代,杜邦公司以乙酰乳酸合成酶(ALS)为靶标开发的磺酰脲(SU)类除草剂,因低毒、广谱、高效、高选择性等特点而被广泛应用。李正名团队合成了多类磺酰脲(SU)化合物[1-3],其中N-[2-(4-甲基)嘧啶基]-N′-2-甲氧羰基-苯磺酰脲衍生物(N-[2-(4-methyl)pyrimidinyl]-N′-2-methoxycarbonyl-benzene sulfon-ylurea derivatives)具有良好的除草活性(以“pIC50”表示)[4],简称为“嘧啶苯磺酰脲衍生物”(Pyrimidinyl benzene sulfonylurea derivatives)。同时,针对磺酰脲(SU)类化合物除草活性的定量结构-活性相关(quantitative structure-activity relationship,QSAR)[5-10]也引起人们普遍关注。李吉来等[11]在B3LYP/6-31G(d)水平下, 计算了23种磺酰类化合物的分子极化率及分子骨架中各原子的Milliken电荷,训练集18个化合物的最佳四元回归方程的交叉验证系数Q2值为0.71,R2=0.92。班树荣等[12]采用比较分子力场(CoMFA)方法研究85个磺酰脲类化合物对除草靶标-乙酰羟基酸合成酶(Acetohydroxyacid synthase,AHAS)抑制常数Kiapp,训练集的Q2=0.811,R2=0.934。郭万成等[13]基于比较分子相似性指数分析(CoMSIA)对27个新型4,5,6-三取代嘧啶苯磺酰脲类化合物的除草活性进行三维-定量构效关系(3D-QSAR)研究,其交叉验证系数Q2值为0.520,R2=0.739。王美怡等[14]采用比较分子力场方法,研究9个新型苯环5位取代的磺酰脲类化合物水解半衰期3D-QSAR,其R2=0.887。上述学者都是基于药物小分子单体结构的QSAR研究。Xia等[4]基于小分子聚集态结构,提出了定量聚集-活性关系(quantitative aggregation-activity relationship,QAAR)方法,并被用来分析24种嘧啶苯磺酰脲衍生物的除草活性(pIC50)。他们计算这些小分子的二聚体回转半径(rgyr)2、水溶性对数(lgS)2、辛醇/水分配系数对数(lgP(o/w))2、表面球度(vsurf_G)2,建立训练集(20个化合物)。其最佳三元回归方程含(rgyr)2,lgP(o/w))2和(vsurf_G)2,其Q2=0.825,R2=0.913,呈现良好的稳定性、相关性及预测能力(对测试集的平均预测误差仅为0.320),但未能引入分子的空间构象建模。他们的研究对进一步设计新颖高效、环境友好的磺酰脲类除草剂具有一定的指导意义。
为了进一步探讨影响嘧啶苯磺酰脲衍生物除草活性的结构因素,揭示可能的除草作用机理,本文基于CoMFA方法[6,15-18],建立这些化合物除草活性(pIC50)[4]的3D-QSAR模型,以揭示嘧啶苯磺酰脲衍生物分子周围立体场、静电场分布,即分子的构象对pIC50的影响,探讨其发挥除草作用的分子机理。
1 材料与方法
1.1 数据来源
24种嘧啶苯磺酰脲衍生物分子的基本结构见图1。它们的除草活性(pIC50)来自文献[4],具体数值见表1。

图1 嘧啶苯磺酰脲衍生物分子的基本结构
1.2 建模方法
本文使用Tripos公司Sybylx 2.1.1药物设计软件建立嘧啶苯磺酰脲衍生物除草活性的CoMFA模型,并进行3D-QSAR分析。
1.2.1 化合物药效活性构象的确定及分子叠合 以Sketch molecule模块构建24个嘧啶苯磺酰脲衍生物分子[4]及新设计分子的初始三维结构;采用Minimize模块,对上述分子的三维构象进行分子力学优化,获取相应最低能量构象。以此最低能量构象代替其药效活性构象用于分子叠合。
按照一般5∶1原则,将26个嘧啶苯磺酰脲衍生物分子分为训练集(Training set)和测试集(Test set)。其中训练集20个分子;测试集7个分子(为表1中带“*”的分子和4号模板分子,所谓模板分子是指样本中生物活性最强的分子)。在Sybylx 2.1.1药物设计软件中,Align database模块采用公共骨架的原子契合的叠合方式,以保证所有分子取向相同及均方根偏差最小。以除草活性最强的4号分子(pIC50=6.502)中的公共骨架为叠合模板,对训练集、测试集中分子运用Align database模块予以叠合。训练集与测试集的叠合图见图2,所有分子中公共骨架的原子都契合密切。

表1 嘧啶苯磺酰脲衍生物的除草活性(pIC50)
注:25和26号为新设计的分子。

图2 训练集(a)、测试集(b)的叠合图
1.2.2 CoMFA模型的建立 对训练集中叠合分子周围每个网格点上的立体场(Steric,St)及静电场(Electrostatic,El),采用Tripos标准力场计算它们的场能值。在偏最小二乘法(Partial least squares,PLS)模块中,第一步用逐一剔除法(Leave-one-out,LOO)予以交叉验证,即以pIC50为因变量,场能值为自变量建模,得交叉验证系数Q2和最佳主成分数N。要求Q2>0.5,模型才具有95%的可信度[19]以及良好的稳健性与预测能力。模型中的最佳主成分数(N)比其化合物数(m),以“Sv”表示。Sv≥5的模型才具有统计意义及较低随机性[20]。第二步非交叉验证,以判定系数R2(又称为削减误差比例)、统计方差比F为评价指标。最后采用View CoMFA模块,显示立体场和静电场的三维等势图对化合物pIC50的贡献。
2 结果与讨论
2.1 CoMFA模型
训练集的CoMFA模型见表2,其中SD为估计标准误差,St./%和El./%分别为立体场、静电场对pIC50的贡献。

表2 CoMFA模型与文献[4]模型的比较
模型质量检验:
(1)交叉验证:Q2>0.5,Sv=5,表明模型具有很好的稳健性与预测能力。
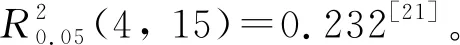
(3)外部预测能力:以训练集的CoMFA模型对测试集中分子的pIC50予以预测,以检验其外部预测能力。测试集的pIC50预测值见表1中“pIC50,cal”。与相应实验值比较接近,平均绝对误差仅为0.359,显示模型较佳的外部预测能力。
本文训练集CoMFA模型质量明显优于文献[4],但其外部预测水平稍低于文献[4],后者预测的平均绝对误差仅为0.320。
2.2 CoMFA等势图
CoMFA的立体作用分布图中的绿色区域表示增大取代基体积有利于提高化合物的生物活性,黄色区域表示减小立体位阻对生物活性有利。图3(a)(彩图见封三)为训练集中pIC50最高的4号分子为模板的CoMFA模型的三维立体作用分布图,其中绿色区域处于苯环2-位和嘧啶环的3-位,表示在这些区域大体积的取代基有利于提高化合物的除草能力。如1号分子与4号分子比较,是后者R1=—CO2CH3的体积大于前者R1=—NO2,故1号分子的pIC50小于4号分子。此因—CO2CH3的疏水性强于—NO2,易透过细胞膜,与靶标结合而显示很好的除草活性。图3(a)中没有黄色区域,说明靶标生物大分子提供的空穴容积足够大,对这些分子不存在空间位阻。
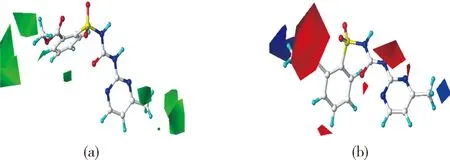
图3 CoMFA模型的立体场(a)与静电场(b)等势图
图3(b)为4号分子周围的静电场分布,红色区域主要处于苯环2-位,表示在这些位上引入带负电荷的基团对pIC50有利;一个蓝色区域处于较远离苯环的2-位,另一个蓝色区域处于嘧啶环的3-位,表示能增大该区域正电性的基团有利于化合物pIC50的提高。如4号分子R1=—CO2CH3中2个负电氧原子均处于红色区域,R2=—CH3中3个正电氢原子处于蓝色区域,因此,其除草活性最强。
CoMFA模型的立体场和静电场对pIC50的贡献分别为79.1%和20.9%,显示立体作用远强于静电作用。由于立体场主要为疏水作用。R1=—CO2CH3中含酯氧及醚氧原子,有良好的疏水性,与靶标ALS形成良好的疏水作用,相应pIC50升高。静电场主要为酯氧及醚氧原子上部分负电荷(δ-)与靶标蛋白质大分子中部分正电荷(δ+)间的库伦力及孤对电子与蛋白质中正电性氢形成氢键。可见,影响嘧啶苯磺酰脲衍生物除草活性pIC50的主要因素是疏水作用、库仑力及氢键。
2.3 分子设计
根据所建模型中隐含的影响生物活性的结构信息进行分子设计是QSAR研究的目的之一。由2.2可知,对于R1以“—CO2CH3”为宜,因为比其体积大的“—CO2C2H5”或者比其体积小的“—NO2”,在R2相同条件下,其pIC50都低。对于R2以“—CH3”为宜,因为比其体积大的“—OCH3”及“—SCH3”等,或者比其体积小的“—Cl”,在R1相同条件下,其pIC50都低。因此,对于R1应保持—CO2CH3,不宜换为其它基团。据此,可对R2予以修饰,即替换为与—CH3体积相近的负电性基团,以提高嘧啶苯磺酰脲衍生物除草活性。据此设计2个化合物(见表1中第25和26号化合物),3D-QSAR模型给出较大的pIC50预测值分别为5.939和6.223,与4号分子预测值6.228非常接近。这些化合物的除草活性,有待生物医学实验确认。
3 结论
(1) 基于比较分子力场方法(CoMFA)建立的嘧啶苯磺酰脲衍生物除草活性pIC50的训练集构效关系:N=4,Sv=5,Q2=0.703,R2=0.968,F=114.614,显示良好的相关性、稳定性和预测能力。
(2)CoMFA模型的立体场和静电场对pIC50的贡献分别为79.1%和20.9%,显示立体作用近4倍于静电作用。
(3)所建CoMFA模型的三维等势图较好地解释了嘧啶苯磺酰脲衍生物除草活性pIC50的主要影响因素是疏水作用、库仑力及氢键。据此设计的2个化合物,预测有较强的除草活性,有待生物医学实验确认。

