铁酸锌配碳选择性还原的热力学分析和试验研究
汪鑫,邓寅祥,许继芳,鲁菊
(苏州大学沙钢钢铁学院,江苏 苏州 215021)
电炉炼钢粉尘中含有大量的有价元素,如铁,锌等[1]。我国电炉粉尘中锌含量约10% ~ 15%,主要以铁酸锌和氧化锌的形式存在。大量的电炉粉尘堆积不仅造成金属资源的浪费,还造成环境污染[2-3]。因此,电炉粉尘中铁和锌的回收利用的研究具有重要意义。
电炉粉尘处理工艺中,填埋处理法工艺简单,但无法利用有价金属资源[4];循环利用进入钢铁生产流程,可回收其中的铁资源,但铅锌的富集对后续高炉炼铁以及炼钢生产造成影响;火法工艺则受设备投资大,能耗大等问题限制[5];湿法工艺处理过程中,氧化锌中的锌较易浸出,不易浸取铁酸锌中的锌,导致锌浸出率低[6-7]。此外还有真空冶金法[8]、铝浴熔融法[9]、焙烧转化-分离[10]等方法。其中焙烧转化-分离方法是通过焙烧把它变成易溶解的化学相(如氧化锌以及锌的氯化物或硫酸盐等),再浸出回收锌,关键是提高电炉粉尘铁酸锌的转化率[11-12]。
铁酸锌的焙烧转化的关键在于铁酸锌的高效分解和焙烧产物的有效调控。本文为研究铁酸锌配碳选择性还原分解过程,通过Factsage计算和试验研究相结合,分析铁酸锌配碳还原分解的热力学,讨论反应温度和配碳量对铁酸锌分解行为的影响,获得铁酸锌选择性还原和抑制还原产物过还原的条件,为铁酸锌选择性还原、铁和锌等资源的综合利用提供依据。
1 试验原料
将ZnO粉末试剂(AR)和Fe2O3粉末试剂(AR)按摩尔比1:1球磨混匀,高温马弗炉内在1200℃下固相反应2 h,期间发生的主要反应为ZnO+Fe2O3→ZnFe2O4,随后采取自然冷却至室温,随后进行研磨(小于74 μm)、筛分和干燥保存,用于后续配碳还原试验。X射线衍射仪物相分析结果见图1。由图1可知,衍射峰峰型尖锐,晶型完好,与铁酸锌标准衍射峰一一对应,表明固相反应产物为铁酸锌(JCPD #22-1012),且产物结晶度好、纯度较高[13]。

图1 固相合成铁酸锌的XRD图谱Fig. 1 XRD pattern of synthetic zinc ferrite by solid-state synthesis
将固相反应合成的铁酸锌和活性炭粉(AR)按10:1质量比(C/O摩尔比为0.50)称量后,球磨混匀。然后压块、干燥后装入刚玉坩埚,高温马弗炉内进行不同温度下2 h的还原反应,随后自然冷却至室温,研磨、筛分和干燥保存。
2 研究方法
为研究铁酸锌配碳选择性还原分解过程,采用Factsage计算和分析铁酸锌配碳还原分解的热力学,主要计算的各反应的标准吉布斯自由能变化(ΔGθ)随温度的变化关系,分析配碳还原铁酸锌在不同反应温度和气体组成条件下的物质平衡关系,讨论反应温度和配碳量对铁酸锌分解行为的影响。通过固相反应法制备铁酸锌,进行铁酸锌配碳还原试验,验证计算结果,获得铁酸锌选择性还原和抑制还原产物过还原的条件。
3 铁酸锌配碳还原的热力学研究
3.1 铁酸锌配碳还原过程ΔGθ的变化
铁酸锌配碳还原过程中固体碳是主要还原剂,可能发生的主要反应如式(1)~(5)所示。计算的各反应的标准吉布斯自由能变化(ΔGθ)随温度的变化关系见图2。
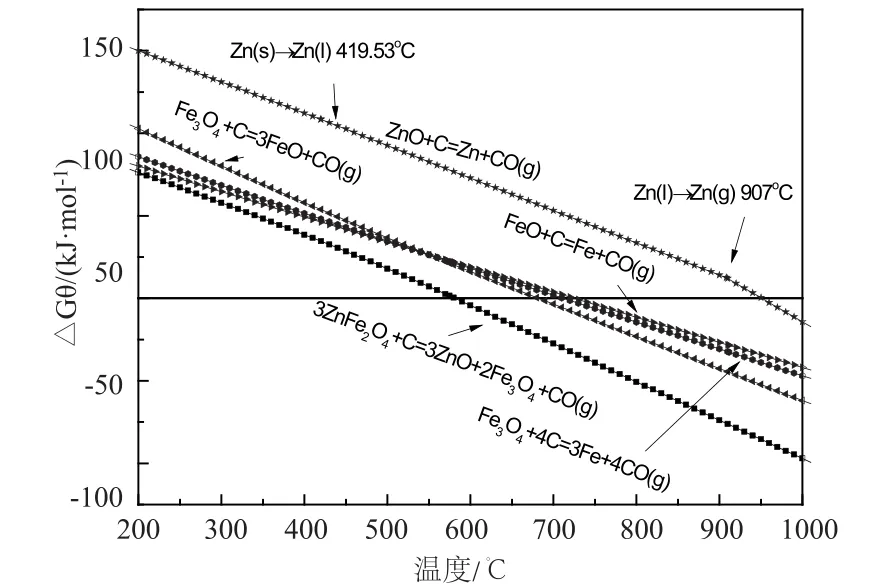
图2 铁酸锌配碳还原过程的ΔGΘ随温度的变化关系Fig. 2 ΔGΘ changes with temperature for reduction of zinc ferrite by carbon
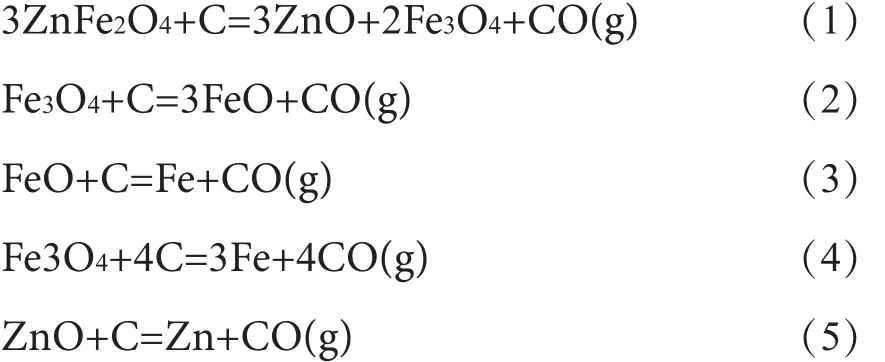
结果显示,上述反应的ΔGθ随着温度的增加,呈下降趋势,在计算温度范围内由正转为负,说明固体碳可将铁酸锌进行还原,提高温度可以促进反应的发生。铁酸锌配碳还原过程,铁酸锌和铁氧化物较易被还原,还原过程遵循逐级还原规律;铁酸锌在582℃时被还原为Fe3O4和ZnO。随着温度的升高,铁氧化物被过还原,在682℃时Fe3O4可被还原为FeO,在712℃时就可还原出金属铁;ZnO虽然比Fe2O3难以还原,但由于Zn的沸点较低,在标准状态下约907℃形成锌蒸气[14],ZnO在941℃时被还原为锌蒸气。由此可见,铁酸锌配碳择性还原为ZnO而抑制氧化锌的过还原在热力学上是可行的,合适的温度范围为582 ~941℃之间,温度过低不利于铁酸锌的分解,温度过高则存在氧化锌的过还原。
3.2 铁酸锌配碳还原条件下的物质平衡关系
采用Factsage分析配碳还原铁酸锌在不同反应温度和气体组成条件下的物质平衡关系。计算初始条件为1 mol 铁酸锌,配碳量按照不同的C/O摩尔比(O为铁酸锌中所有的氧)添加,假定反应体系总压为1 atm(约为101 kPa)。铁酸锌配碳还原过程中不同条件的计算结果见图3、4。
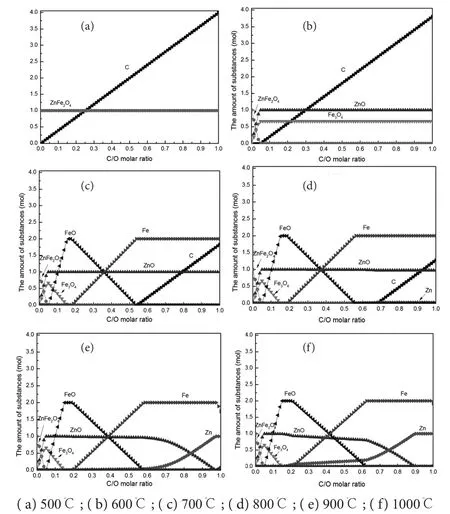
图3 不同恒温条件下各物质的量与配碳量的关系Fig. 3 Relationships between substances and the C/O molar ratio at different temperatures
由图可见,当温度为500℃时,铁酸锌质量保持不变,未发生还原分解,调节C/O摩尔比均不能还原铁酸锌。当温度高于600℃时,铁酸锌能够被还原为Fe3O4和ZnO,当C/O摩尔比超过0.04时,铁酸锌完全分解转化为Fe3O4和ZnO,且提高C/O摩尔比也不会发生铁氧化物的过还原。随着温度的升高,铁酸锌完全分解的C/O摩尔比略有降低。随着温度的升高,还原产物为Fe3O4、FeO和Fe,即发生铁氧化物的过还原。在700℃时,当C/O摩尔比为0.06时,铁酸锌分解的Fe3O4开始被还原为FeO,当C/O摩尔比为0.18时,完全分解转化为FeO和ZnO,同时部分的FeO被还原为Fe,当C/O摩尔比为0.54时,FeO完全转化为Fe。随着温度的增加,铁氧化过还原的C/O摩尔比也略有降低。
当温度低于800℃时,铁酸锌分解的锌以氧化锌形式存在,生成的氧化锌并未明显被进一步还原为金属锌;800℃时,在高C/O摩尔比的情况下(C/O摩尔比>0.6),才会有少量的金属锌(0.01 mol~0.02 mol)产生;随着温度继续升高,锌完全还原所需要的C/O摩尔比逐渐减少;当温度为900℃时,在低C/O比例的情况下就会产生金属锌,随着C/O摩尔比的增加,更多的氧化锌转化为金属锌,当C/O摩尔比超过0.97时,体系中的锌将完全转化为金属锌;1000℃时,当C/O摩尔比超过0.89时,体系中的锌将完全转化为锌蒸气。
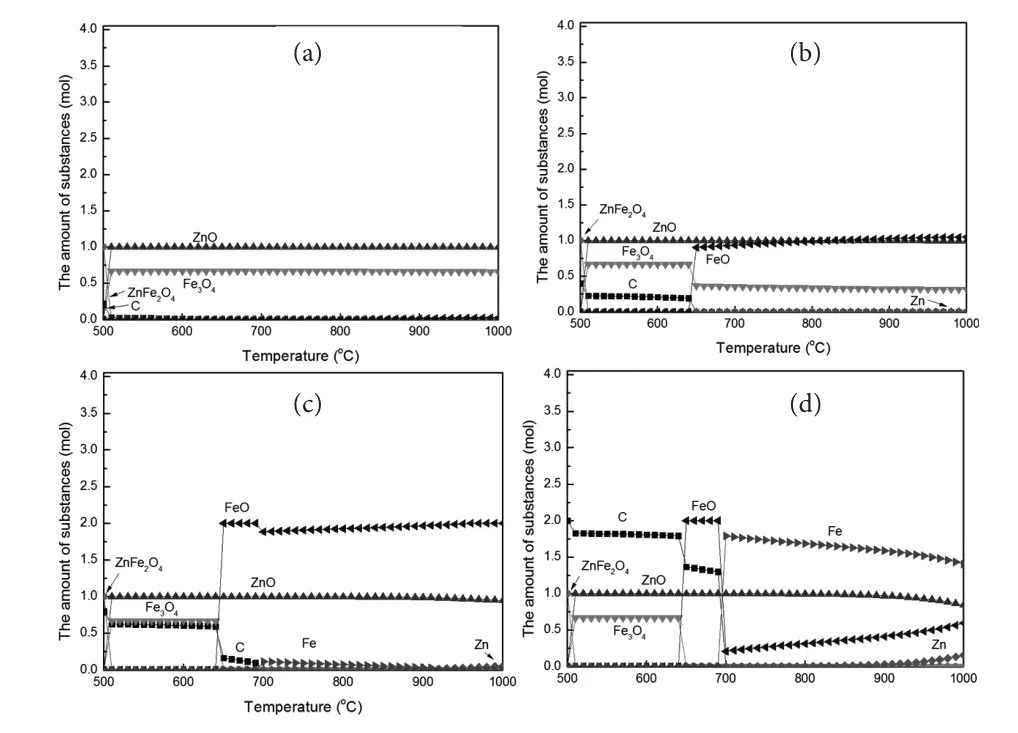
图4为恒定C/O摩尔比条件下各物质的量与反应温度的关系(C/O摩尔比分别为0.05、0.10、0.20、0.50、0.80和1.00)。结果表明,当C/O摩尔比为0.05时,铁酸锌在温度超过500℃时被碳还原为Fe3O4和ZnO,随着温度的增加,还原产物并未发生改变;当C/O摩尔比为0.10时,铁酸锌首先被还原为Fe3O4和ZnO,过量的碳在650℃左右将部分Fe3O4进一步还原为FeO。随着C/O摩尔比的增加,过量的碳将Fe3O4还原为FeO,同时部分的FeO在700℃左右被进一步还原为Fe。当C/O摩尔比为0.80时,过量的碳将FeO还原为Fe。
当C/O摩尔比小于0.50时,铁酸锌中分解的锌以ZnO形式存在,生成的ZnO并未明显被还原为金属锌,只发生了铁氧化物的逐级还原;当C/O摩尔比超过0.50时,随着温度的增加,部分铁酸锌分解的ZnO在高温条件下还原为金属锌,当温度为850℃时,还原产物中会有少量的金属锌(0.02 mol),当温度超过850℃时,还原产物中出现明显的金属锌(0.15 mol);当C/O摩尔比为1.00时,体系中的锌在900℃左右将完全转化为金属锌。
计算结果中碳含量的变化体现碳还原的历程,如C/O摩尔比为1.00时,随着温度的升高,体现中碳含量逐渐减少,出现4个明显的降低阶段,分别对应着铁酸锌还原为Fe3O4和ZnO、Fe3O4还原为FeO、FeO还原为Fe、以及ZnO还原为Zn,每个阶段反映出各个还原过程中消耗的碳含量,即控制反应历程所需要的配碳量。
综上所述,为了抑制氧化锌的过还原,必须保持适宜的C/O摩尔比和温度条件,控制C/O摩尔比0.6以下,温度低于900℃时,还原产物中会有少量的金属锌(0.04 mol)出现,铁酸锌分解的锌主要以氧化锌的形式存在,生成的氧化锌并未明显被进一步还原为金属锌,满足后续处理过程对锌存在形式的要求,从而实现铁酸锌的有效分解、ZnO过还原的抑制。
4 铁酸锌配碳选择性还原试验
4.1 铁酸锌配碳选择性还原
结果显示,在650℃时,产物中出现Fe3O4和ZnO衍射峰,铁酸锌还原分解为Fe3O4和ZnO,由于铁酸锌和Fe3O4均为尖晶石结构,故图谱中有衍射峰的重叠。在800℃时,产物中出现明显的FeO和ZnO衍射峰,还存在少量的Fe衍射峰,铁酸锌和Fe3O4衍射峰不明显,铁酸锌分解出的Fe3O4进一步还原为FeO,少量的FeO被还原为Fe。在950℃时,产物中存在较为明显的中FeO和ZnO衍射峰,但ZnO衍射峰明显被800℃产物中ZnO衍射峰弱,还存在Zn和Fe衍射峰,铁酸锌分解出的Fe3O4进一步还原为FeO,同时FeO部分被还原分解Fe,ZnO部分被还原为Zn。虽然Zn的沸点为907℃,部分ZnO被还原为锌蒸气而挥发,但仍有少量的锌残留在粉末颗粒中;不同温度下的产物中均存在碳的衍射峰,产物中还有过量的碳存在。由此可见,XRD分析的试验结果与上述热力学计算结果基本一致。
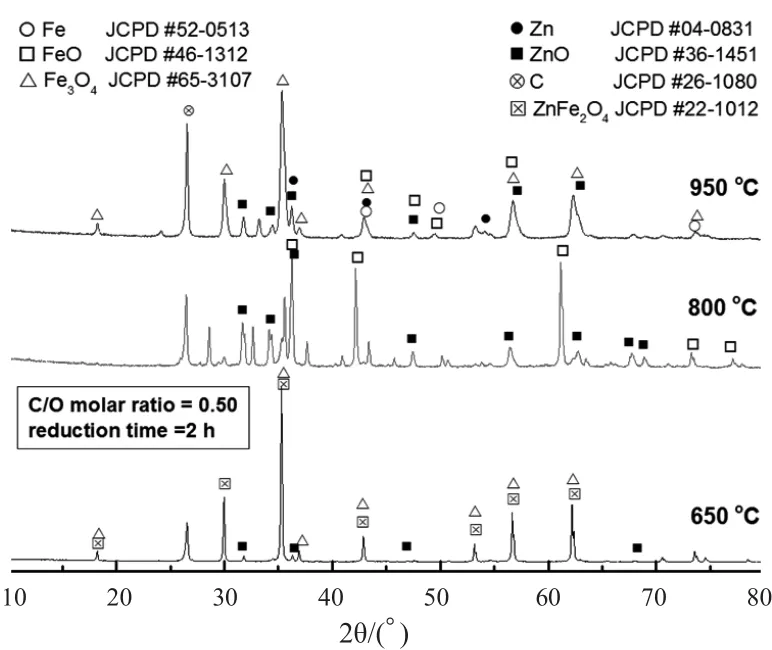
图5 不同温度下铁酸锌配碳还原的XRDFig. 5 XRD pattern of reduction of zinc ferrite with carbon at different temperatures
4.2 还原过程中锌的挥发
Zn的沸点为907℃,部分ZnO被还原为锌蒸气而挥发,将导致产物中锌含量降低,为研究反应产物中锌含量随反应温度的变化,对还原产物中锌含量进行了测量,结果见图6。

图6 铁酸锌配碳还原过程中锌含量变化Fig .6 The Zn content of reduction of zinc ferrite with carbon
结果表明,当温度为650℃和800℃时,随着反应温度的增加,产物中的锌含量略有下降;在950℃时,由于ZnO被还原为锌蒸气而挥发,产物中锌含量明显降低。
5 结 论
(1)铁酸锌配碳选择性还原热力学计算结果表明,铁酸锌配碳择性还原为ZnO而抑制氧化锌的过还原在热力学上是可行的。
(2)铁酸锌配碳还原过程遵循逐级还原规律,控制C/O摩尔比0.6以下,温度低于900℃时,可实现铁酸锌的有效分解、ZnO过还原的抑制,有利于后续铁锌资源的有效分离。
(3)采用固相反应法合成了结晶度好、纯度较高的铁酸锌;650℃时,铁酸锌配碳还原分解为Fe3O4和ZnO,随着温度的升高,铁氧化物的逐级还原为Fe3O4、FeO和Fe,ZnO被还原为Zn。试验结果与热力学计算结果基本一致。

