紫杉醇-介孔氧化铜纳米球给药体系的制备及对肝癌细胞SMMC-7721作用
李家辉,崔海悦,马晓茜,高宇
(1.锦州医科大学药学院;2.锦州医科大学附属第一医院肿瘤学教研室,辽宁 锦州 121000)
近年来,恶性肿瘤的发病率和死亡率逐年升高,恶性肿瘤已成为世界范围内人口死亡的主要原因之一[1]。根据2019年国家癌症中心发布的数据,肝癌是我国常见恶性肿瘤之一,发病率居于第四位,死亡率均位于第二位[2]。大部分晚期恶性肿瘤患者已无手术机会,首选化疗治疗,但很多抗癌药物是不溶于水,其水溶性严重限制了化疗药物的吸收。紫杉醇(paclitaxel,PTX)是一种已发现的最优秀的天然广谱抗癌药物之一,通过抑制微管蛋白的解聚,进而抑制细胞有丝分裂达到抗肿瘤作用,在临床上已经广泛用于乳腺癌、卵巢癌、肝癌、部分头颈癌和肺癌的治疗[3-4],并且效果很好,但是其水溶性较差,水中溶解度仅6 ng/mL[5],因此如何改善紫杉醇溶解性是目前晚期恶性肿瘤治疗中亟需解决的问题,对于扩大其临床应用更具重要意义。
纳米材料是指材料的基本单元在纳米级的范围内,尺度约为 100 个原子紧密贴合,排列整齐。根据Ostwld-Freundilich 方程和Noyes-Whitney 方程[6],纳米粒子尺寸小比表面积大,不但增加难溶药物溶解度或溶出速率,还能增加纳米粒与细胞膜或生物膜的接触。这些优点都有利于增加难溶药物吸收,这都为解决难溶性药物的水溶性和吸收问题提供了良好的机遇。纳米药物载体,是指粒径大小为10~500 nm的纳米粒子应用纳米技术包裹或吸附治疗药物,药物载体被细胞摄取后在胞内释放药物,从而实现安全有效的药物输送。目前用于改善紫杉醇溶解性的方法包括制备胶束[7-9]、脂质体[10]、纳米粒[11]等。已有的紫杉醇纳米药物,包括脂质体紫杉醇和白蛋白结合型紫杉醇。如Paclitaxel liposome(脂质体紫杉醇)的缺点包括稳定性差、载药量低、不易保存等。白蛋白结合型紫杉醇(albumin-boundpaclitaxel,Abraxane)中,紫杉醇和白蛋白为直接结合,不存在过敏反应,但是无法调节药物释放,并且成本高,工艺复杂,价格昂贵[12]。
随着纳米技术的发展,介孔材料用于改善难溶性药物水溶性的应用引起了广泛的关注[13-14],比如介孔硅材料[15-16],介孔碳材料[17-19]等。根据国际联合会(IUPAC)的定义,孔径在2~50 nm之间的纳米材料称之为介孔纳米材料(mesopore),介孔纳米材料作为药物载体时,药物以无定形态存在于载体内部。药物存在状态与药物溶解度有关:当药物以无定型态存在时,溶解度最好。这类材料具有高的比表面积、大的孔容积、易改性等优势。本实验采用介孔氧化铜纳米球作为载体材料,在既往研究中,介孔氧化铜给药体系显示出了低毒、靶向肿瘤细胞、诱导细胞凋亡的作用[20]。本实验用介孔氧化铜纳米球给药体系的纳米效应,改善紫杉醇的水溶性,并考察了该给药体系对SMMC-7721肝癌细胞的作用。
1 仪器与材料
KQ-250B型超声波清洗仪(昆山市超声仪器有限公司)、AL204电子天平(梅特勒-托利多仪器有限公司)、DF-101S恒温磁力搅拌器(郑州市亚荣仪器有限公司)、JEM-1010透射电镜(日本电子株式会社)、LC-2030 高效液相色谱仪(日本岛津公司)、TG22-WS台式高速离心机(上海赵迪生物科技有限公司)、HS-DSC-101差示扫描量热仪(上海和晟仪器科技有限公司)、ZEISS LSM 700激光共聚焦显微镜(上海莱瑟光谱仪器分析技术有限公司)HBS-1096酶标分析仪(深圳良谊仪器有限公司)。
紫杉醇PTX(纯度≥98%,西安天丰生物科技有限公司,批号:20151015),间苯二酚(阿拉丁),正硅酸乙酯(TEOS),谷胱甘肽(GSH)(国药集团化学试剂有限公司),3-巯基丙基-三甲氧基硅烷(MPTMS)(阿拉丁),甲醇(色谱醇,天津光复精细化工有限公司),噻唑兰(MTT),Hoechst 33342,罗丹明鬼笔环肽,异硫氰酸荧光素(FITC),RPMI-1640培养基(北京鼎国昌盛生物科技有限公司),其余试剂为市售分析纯。
2 方法与结果
2.1 载体制备及载药研究
2.1.1 MCON的制备[19]
70 mL乙醇、3 mL氨水、10 mL水置于磨口锥形瓶中混合均匀,然后3.46 mL正硅酸乙酯滴加到上述溶液中,搅拌下反应15 min,接下来加入0.4 g间苯二酚和0.56 mL的甲醛,反应24 h后,得到的白色沉淀经干燥后,于700 ℃氮气氛围下煅烧7 h,5%的氢氟酸除去二氧化硅,得到介孔中空碳纳米球。取100 mg介孔中空碳纳米球分散在10 mL 1.5 M的硝酸铜溶液中,搅拌24 h后,离心得到的样品经干燥于500 ℃空气中煅烧3 h,得到MCON。
2.1.2 载药研究
吸附法被用于载药研究。取200 mg MCON分散于2 mL的PTX二氯甲烷溶液(2 mg/mL)中,经超声进一步分散后继续搅拌6 h,离心得到的沉淀经真空干燥后,得到MCON-PTX。精密称量5.0 mg CS-SS-MSN-PTX /MSN-PTX置于10 mL容量瓶,加甲醇溶解并稀释至刻度。静置1 h,离心,取上清液为供试品,HPLC法测定PTX浓度并计算载药量,按如下公式计算得到:载药量 (DLC) %=包裹在APMSN载药体系中的紫杉醇重量/载药体系重量×100%。
2.2 表征
2.2.1 透射电子显微镜(transmission electron microscopy,TEM)表征
采用透射电子显微镜(Tecnai G2F30,FEI,USA) 观察MCON的形态结构特征。
2.2.2 DSC表征
差示扫描量热扫描仪检测PTX在MCON孔道中的存在状态,实验条件为氮气氛围下从50~120 ℃ 以 10 ℃/min的加热速率进行扫描,绘制DSC曲线。
2.3 体外溶出实验
根据2015版《中华人民共和国药典》溶出度测定第二法,考察MCON-PTX和PTX的溶出行为。取相当于3.0 mg PTX 的原料药PTX和MCON-PTX分散于400 mL pH=7.4 PBS中,在温度为37.0 ℃和转速为100 rpm条件下,分别于5、10、20、30、45、60 min 取样2 mL,取样后补充等量空白释放介质。通过HPLC法对PTX进行定量分析,计算PTX的累积溶出度。色谱条件:使用的流动相比例为甲醇-水(65∶35),色谱柱为Agilent TC-C18(250 mm×4.6 mm,5 μm),柱温为30 ℃,检测波长为227 nm,流速为1 mL/min,进样量为20 μL。
2.4 体外细胞实验
2.4.1 细胞毒性实验
SMMC-7721细胞培养条件:培养基为含10%血清的DMEM,温度为37 ℃,5%二氧化碳。试验中所用细胞均经过细胞计数。MCON-PTX的细胞活力用MTT法检测。5×104浓度的细胞被种到96孔板中,贴壁后,系列浓度的MCON,PTX、MCON-PTX被加入孔中,孵育48 h每孔加入MTT试剂20 μL,孵育4 h后,去除介质,每孔加入150 μLDMSO。酶标仪在492 nm测定光密度值。
2.4.2 细胞摄取实验
500 mg MCON置于 100 mL锥形瓶中,在100 ℃下干燥 30 min,降至室温后在氮气保护下加入 50 mL无水乙醇和2 mL的 3-氨丙基三乙氧基硅烷,77 ℃下搅拌加热回流10 h,经离心得到的样品用无水乙醇洗涤3次,真空干燥后置于1 mg/mL的 FITC无水乙醇溶液中,静置吸附3 h,离心得到含有 FITC 标记的MCON(FITC-MCON)。将细胞密度为5×104的对数期SMMC-7721细胞接种于共聚焦皿中,贴壁后,50 μg/mL MCON-PTX分散液填加入共聚焦皿中,37 ℃下分别孵育1、2 h,弃去培养基后用PBS洗3次,4%多聚甲醛溶液固定10 min,1 mg/mL 的Hoechst 33342和1 mg/mL的罗丹明鬼笔环肽分别进行染色,最后激光共聚焦显微镜(Leica DM-6000 CS microscope,Germany)下观察SMMC-7721细胞对FITC-MCON的摄取情况。
3 结果与讨论
3.1 载体形态结构及载药研究
通过TEM对制备的介孔碳纳米球和MCON的形貌进行表征。介孔碳纳米球呈单分散的球形颗粒,具有介孔中空结构,粒径分布约为230 nm,见图1A。MCON为核壳结构,是介孔碳纳米球结构的复制,其介孔壳结构能够提供足够的空间存贮药物并限制药物粒径大小,短的孔道距离具有相对低的扩散阻力,在改善PTX的水溶性的同时有利于药物的快速释放。通过HPLC测定载药量,得到PTX-MCON载药量为(13.65±0.725)%,见图1B。
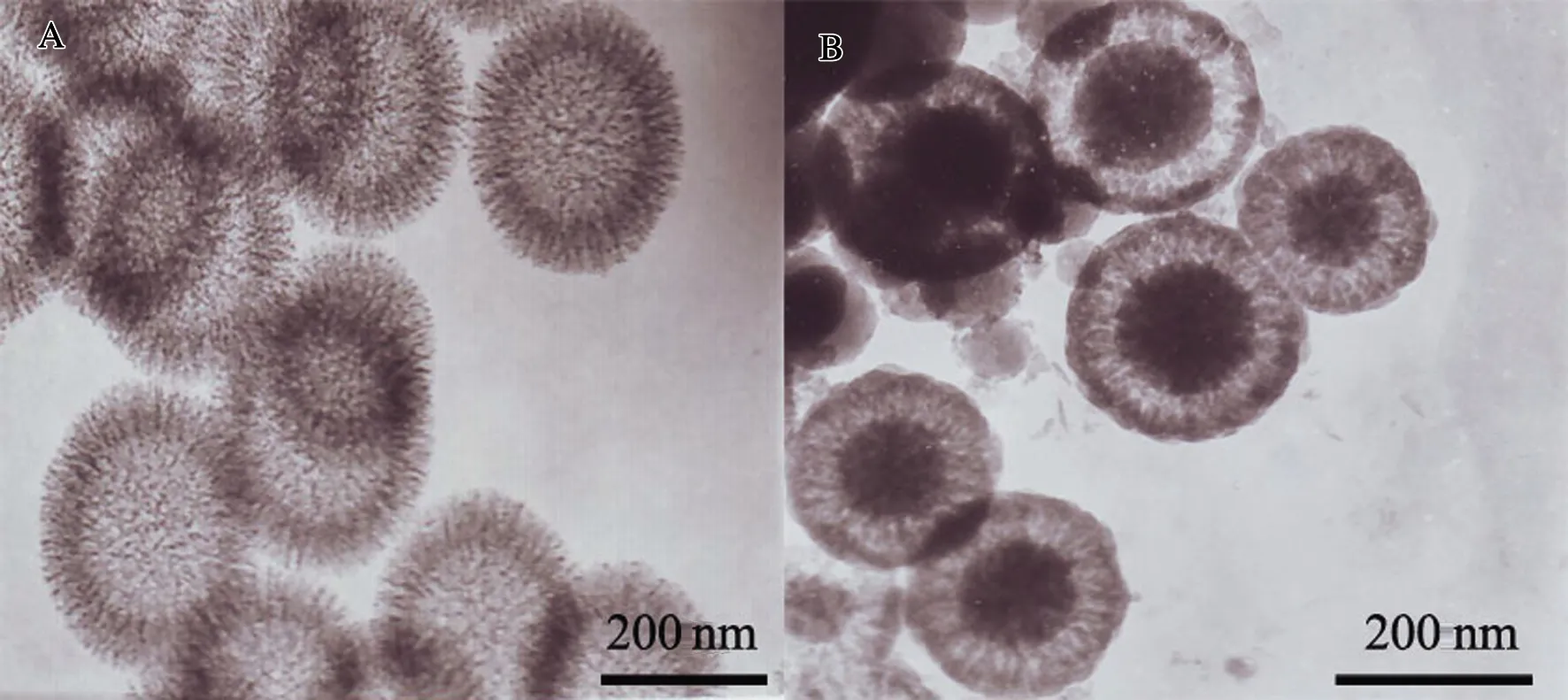
A:介孔碳纳米球;B:MCON
3.2 DSC
采用差式扫描量热法对MCON、PTX、PTX-MCON、PM(PTX和MCON物理混合)和进行检测,PTX在223 ℃显示吸热峰,PM也在此温度出现吸热峰,表明将PTX和PM中药物是晶体状态,MCON呈现一条平滑曲线,无相转变发生,表明载体是无定形的,见图2。PTX-MCON未见PTX的吸热峰,说明PTX以无定型状态存在于MCON的介孔结构中,无定型状态的药物具有更大的溶解度和溶出速率,这是PTX溶出改善的原因。
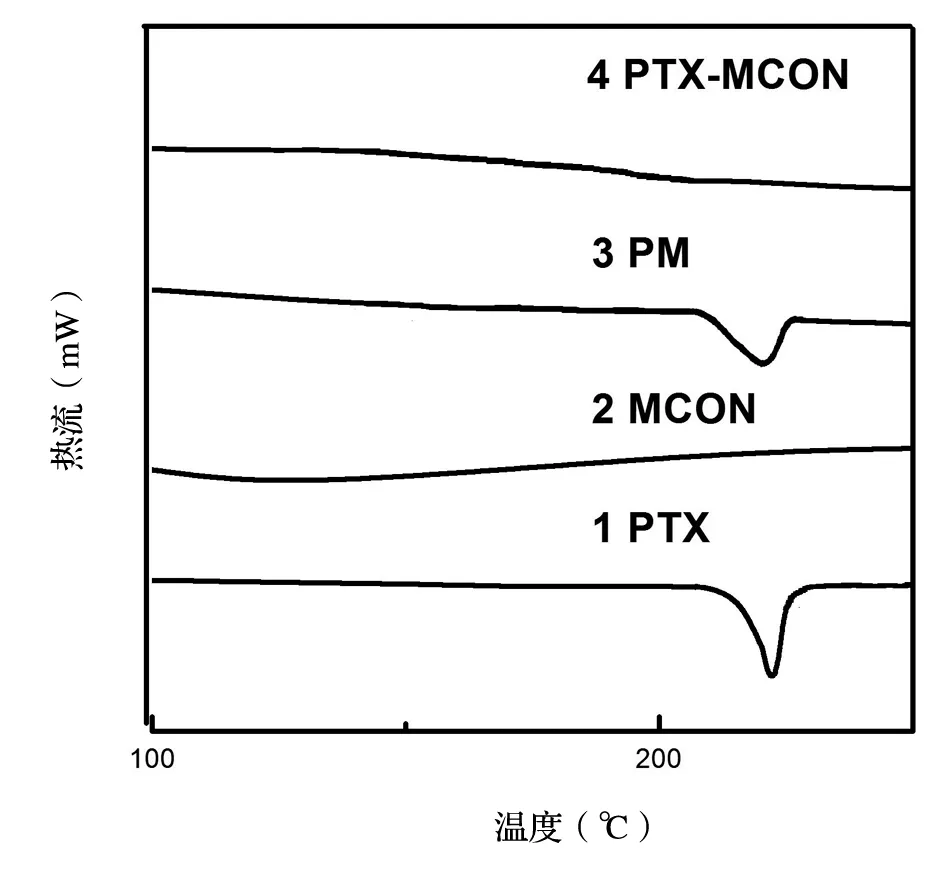
图2 DSC曲线图
3.3 体外溶出实验
采用pH=7.4的PBS作为溶出介质,考察PTX-MCON的溶出情况,PTX原料药在5 min时,药物溶出(5.633±0.45)%,在1 h时药物累积溶出量仅为(20.198±1.48)%,相比之下,PTX-MCON中PTX释放较快,5 min 药物释放(10.536±2.15)%,1 h累积溶出量为(86.347±3.06)%,表明MCON包载后的PTX溶出速率得到显著的提高,见图3。
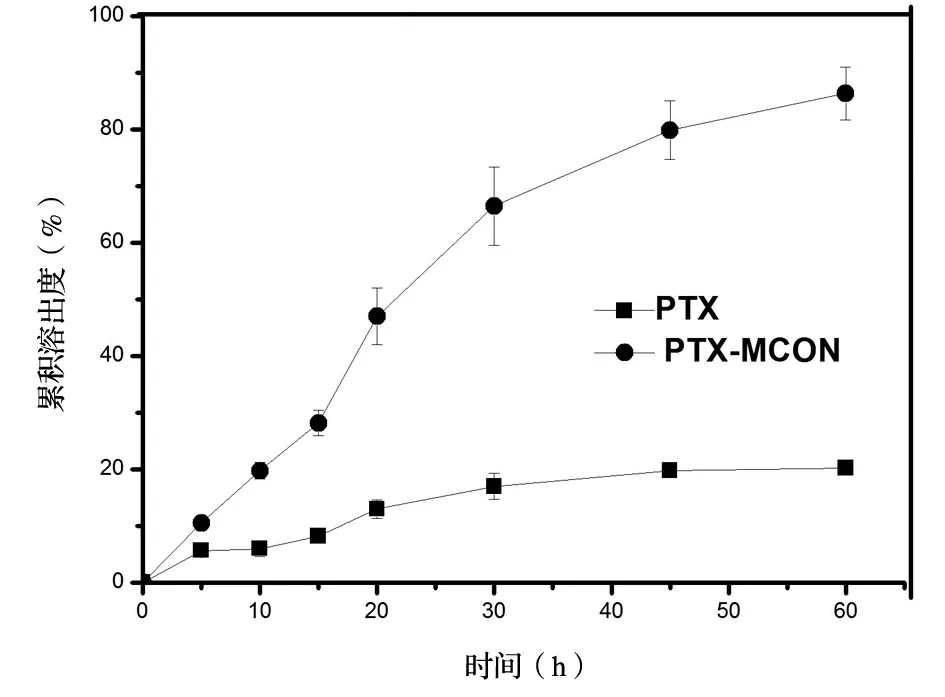
图3 PTX-MCON的累积溶出度
3.4 细胞实验
3.4.1 细胞毒性实验
通过MTT法考察系列浓度的MCON对SMMC-7721细胞的作用效果,评估MCON的生物相容性。SMMC-7721细胞在浓度10~500 μg/mL的MCON孵育48 h后细胞活力均高于80%,这表明MCON对SMMC-7721细胞具有良好的生物相容性,见图4 A。通过系列浓度的PTX和PTX-MCON对SMMC-7721细胞的抑制率评价载药样品的细胞毒性,PTX和PTX-MCON孵育的SMMC-7721细胞在10~500 ng/mL浓度范围内细胞毒性呈现浓度依赖性,并且PTX-MCON具有更强的细胞毒性,见图4B。
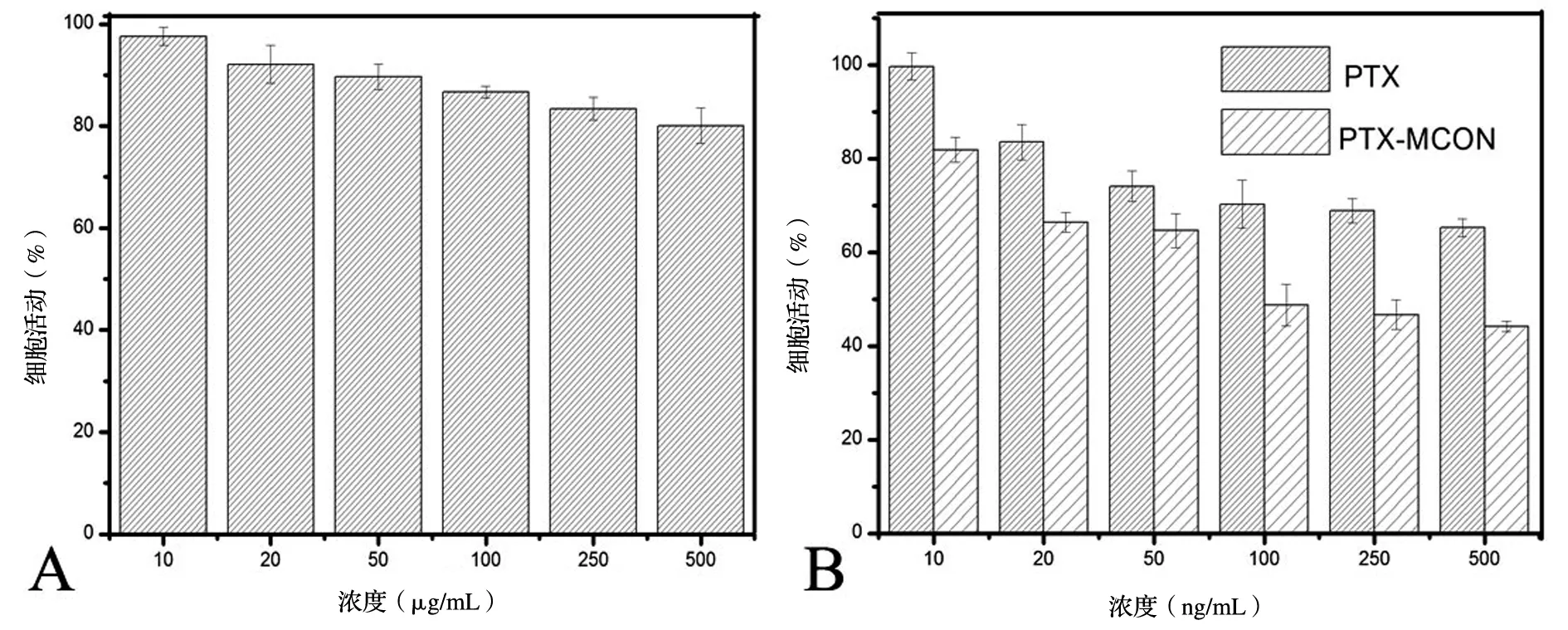
图4 MCON(A)、PTX和PTX-MCON(B)对SMMC-7721的细胞毒性作用
3.4.2 细胞摄取实验
通过激光共聚焦显微镜观察SMMC-7721细胞在0.5、1 h对FITC-MCON的摄取情况。根据荧光强度变化说明FITC-MCON能够被细胞摄取跨膜进入细胞质,并呈时间依赖性实验,见图5。
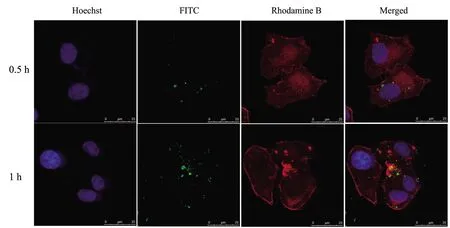
图5 FITC-MCON被细胞摄取的激光共聚焦图像
4 结 论
本研究制备了MCON,并以其为载体改善难溶性药物PTX的水溶性,载药样品中PTX以无动态存在,体外溶出结果说明PTX-MCON明显改善了PTX的溶出速率。细胞实验结果进一步表明PTX-MCON对SMMC-7721细胞的显著抑制作用。综上,MCON是一种具有改善难溶性药物水溶性的潜力载体,为改善难溶性抗肿瘤药物疗效提供参考。

