2016—2019年常州地区无偿献血者酶免和核酸平行检测结果分析
杨爱龙,濮云峰,董珀,贺晨峰
江苏省常州市中心血站检测中心,江苏常州 213004
输血治疗是救治病人的一种重要手段,但存在患者因输血感染传染性病原体的风险,目前公认的病原体主要包括HBV、HCV、HIV 和TP 等。 为了保证临床用血安全, 国家对血液制品实行强制性检测, 酶免检测即ELISA 包括HBsAg、抗HCV、抗HIV 和抗TP,核酸检测即NAT 包括HBV DNA、HCV RNA 和HIV RNA。 从病毒进入人体开始直至可以检测出病毒抗原或抗体之前的时期为病毒感染的“窗口期”。 HBV、HCV 和HIV 的ELISA 检测“窗口期”分别为56 d、72 d 和22 d[1]。 目前,广泛应用的ELISA 技术已非常成熟,检测对象为抗原或抗体,对血液传染性病毒HBV、HCV 和HIV 的检出能力强,但检测“窗口期”相对较长,经输血传播病毒的风险依然存在。 核酸扩增检测(nucleic acid amplification testing,NAT)是通过扩增病原体核酸进行检测的一系列技术总称,技术灵敏度高,检测“窗口期”较短[2]。 为了进一步保证输血安全,该血站自2012年开始采用ELISA 和NAT 平行检测策略。 现回顾性分析2016—2019年度该血站的酶免和核酸检测情况,了解无偿献血人群中血液传染病的流行状态,为降低输血风险提供依据。 现报道如下。
1 资料与方法
1.1 标本来源与处理方法
270215例血液标本来自2016年1月—2019年12月常州地区无偿献血者。使用含惰性分离胶的真空采血管留取标本5~8 mL,第1 管不含抗凝剂用于酶免检测,第2 管含EDTA-K2 抗凝剂用于核酸检测。 标本采集后8 h 内4℃离心,酶免管4000 rpm 离心10 min,核酸管1600 g 离心20 min, 离心结束后即保存于2~8℃冰箱待检。
1.2 仪器与试剂
TECAN 全自动加样仪(长沙泰肯生物技术有限公司),FAME 全自动酶联免疫分析仪(瑞士HAMILTON),Cobass 201 核酸检测系统[罗氏诊断(上海)产品有限公司],DL5M低速冷冻离心机(长沙迈佳森仪器设备有限公司),恒温保存箱(日本松下健康医疗器械株式会社)。ELISA 试剂盒,一检:HBs Ag(上海科华生物工程股份有限公司)、抗HCV(珠海丽珠试剂股份有限公司)、抗HIV(北京万泰生物药业股份有限公司)和抗TP(上海科华生物工程股份有限公司),二检:HB sAg、抗HCV、抗HIV 和抗TP均为英科新创(厦门)科技股份有限公司。 HBV DNA、HCV RNA、HIV RNA 三联检核酸试剂盒为罗氏诊断(上海)产品有限公司。室内质控品(北京康彻思坦生物技术有限公司)。 以上所有试剂均在有效期内使用。
1.3 方法
酶免检测[3]:按照ELISA 试剂盒说明书、仪器操作规程进行HBs Ag、抗HCV、抗HIV 和抗TP 的检测,主要步骤为加样仪加样、酶免仪检测、数据接收及分析。一检和二检项目分别由不同的检验人员执行,对于一检或二检的单项阳性结果进行双孔复检。对于同一个检测项目,一检和/或二检结果为阳性就判定为阳性结果,一检和二检结果均为阴性时才判定为阴性结果。 抗HIV 阳性标本送常州市疾病预防控制中心实验室用蛋白印迹法进行确认。 核酸检测:按罗氏诊断Cobass201 核酸检测系统操作说明书对ELISA 阴性标本进行HBV DNA、HCV RNA 和HIVRNA 的检测,主要步骤为样品混合(6人份为1 个pool)、核酸提取、核酸扩增及检测、数据接收及分析,结果阳性的pool 进行拆分单检,最终确定阳性单个标本及项目。 抗HIV 跟踪检测:HIVRNA 阳性者进行抗HIV 单项跟踪检测,间隔期为4 d。
1.4 统计方法
采用SPSS 19.0 统计学软件进行数据处理,计数资料比较采取率表示,进行χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 酶免结果
270215例无偿献血者HBs Ag、抗HCV、抗HIV 和抗TP 的阳性率分别为2.58‰(697 例)、1.49‰(402例)、0.23‰(61 例)和3.06‰(827 例),酶免阴性者为268264例,见表1。 2017年与2019年间的HBsAg 阳性率对比差异有统计学意义(P<0.05),2016年与2018年间的抗HCV 阳性率对比差异有统计学意义(P<0.05),2018年与其他年度间的抗HIV 阳性率差异有统计学意义(P<0.05),而2019年与2016、2017年间的抗TP 阳性率差异有统计学意义(P<0.05)。
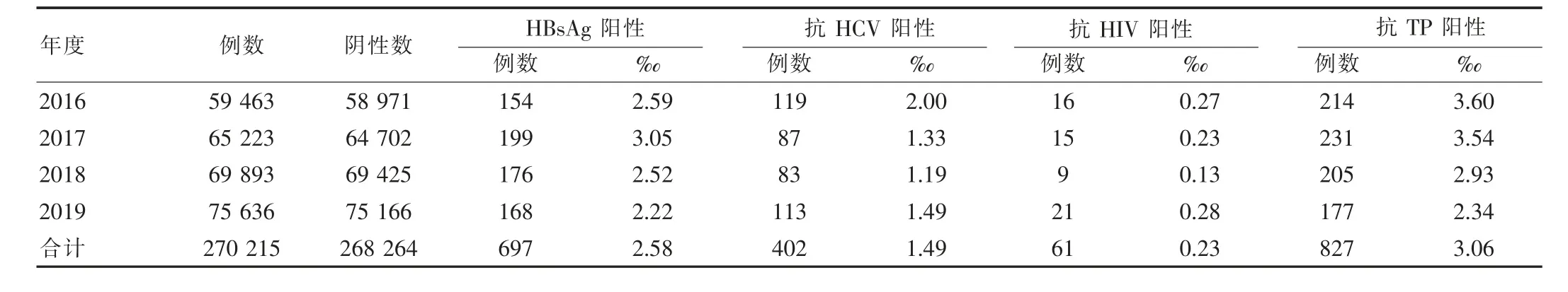
表1 2016—2019年度270215 例无偿献血者HBsAg、抗HCV、抗HIV 和抗TP 检测结果
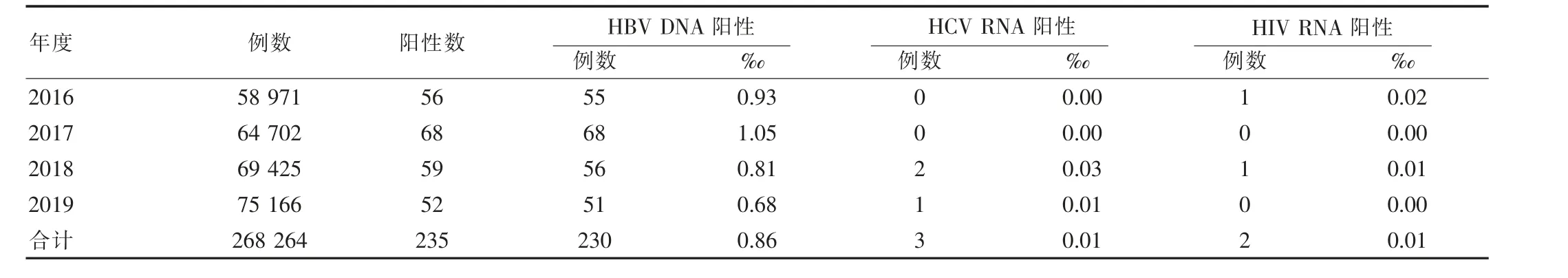
表2 268264 例酶免阴性者HBV DNA、HCV RNA 和HIV RNA 检测结果
2.2 核酸结果
268264例酶免阴性无偿献血者HBV DNA、HCV RNA 和HIVRNA 阳性率分别为0.86‰(230 例)、0.01‰(3 例)和0.01‰(2 例),总阳性率为0.88‰(235 例),结果见表2。
2.3 抗HIV 跟踪检测
第1 例HIV RNA 阳性者在献血后第12 天抗HIV为阳性,S/CO 值为0.469。 第2 例HIVRNA 阳性者在献血后第16 天抗HIV 为阳性,S/CO 值为0.372。
3 讨论
“窗口期”的血液病毒抗原及抗体的检测结果为阴性,但实际上血液中含有病毒,具有复制能力和传染性[4]。另外,病毒抗原、抗体蛋白结构会发生变异,以及免疫沉默,容易造成ELISA 的非“窗口期”漏检[5]。 因此,现有的两次ELISA 检测由于技术局限性完全可能造成病毒漏检。 NAT 敏感性相对于ELISA 更高,在病毒感染后数天即能检出标本中的极微量的病毒核酸,可大大缩短病毒检测“窗口期”[6]。 Busch 等利用数学模型研究证实,NAT能将HBV、HCV 和HIV 血清学ELISA 检测的“窗口期”分别缩短约20 d、50 d 和10 d[7]。 目前NAT 被视为降低ELISA 漏检风险的最佳解决方法[8]。因此,ELISA 和NAT平行检测能形成很好的互补作用,极大降低血液病毒的漏检风险,对保证血液安全和降低输血感染风险具有十分重要的作用。
该血站自2012年采用ELISA 和NAT 平行检测策略以来,取得了很好的检测效果。 2016—2019年常州地区无偿献血者的ELISA 检测结果表明,HBsAg、抗HCV、抗HIV 和抗TP 的总阳性率分别为2.58‰、1.49‰、0.23‰和3.06‰,HBsAg、抗HCV 和抗TP 的年阳性率总体呈逐年下降趋势,抗HIV年阳性率有明显波动但总体呈上升趋势。 NAT 检测结果表明,268264 例酶免阴性者HBV DNA、HCVRNA 和HIVRNA 阳性率分别为0.86‰(230例)、0.01‰(3 例)和0.01‰(2 例),显然,HBV DNA 阳性率远大于HCV RNA、HIV RNA 阳性率,HCV RNA 阳性率和HIV RNA 阳性率基本相等。 HBV DNA 阳性率有波动但总体呈下降趋势,HCV RNA 阳性率和HIV RNA 阳性率呈散发状态。以上这些结果表明,ELISA 检测“窗口期”的病毒漏检现象的确存在,且证明实施NAT 检测的必要性。
隐匿性乙型肝炎病毒感染(Occult Hepatitis B Virus Infection, OBI)定义:在现有检测条件下血清HBsAg 阴性,但血清和(或)肝脏组织中HBV DNA 阳性的一种特殊HBV 感染状态,此时病毒载量常<200 IU/mL[9]。 在HBV 高流行的中国,献血者中OBI 流行率约为0.094%[10],显然常州地区献血者中OBI 流行率略低于全国平均水平。 OBI 献血者潜在威胁着输血安全,已成为一个不容忽视的公共卫生问题,应不断加强和改进NAT 检测。
综上所述,ELISA 检测与NAT 检测能够组成有效互补的血液筛查模式,可以充分反映献血者病毒感染状况,大大降低输血感染病毒风险,应积极推广会和应用。NAT 检测对标本处理、实验室环境、实验操作和试剂灵敏度等都有非常严格的要求,其检测结果也会存在一些假阳性和假阴性,这对实验室今后工作提出了更高的要求。

