100例肝病重症患者管饲给药情况分析Δ
杜春辉,孙金丹,曲 阳,张丽冰,蒋翠云,赵艳玲,牟劲松#
(1.解放军总医院第五医学中心药学部,北京 100039; 2.解放军总医院第五医学中心重症医学中心,北京 100039; 3.廊坊爱德堡医院药学部,河北 廊坊 065000; 4.海南医学院第一附属医院药学部,海南 海口 570102)
重症患者因吞咽困难或意识障碍等常需经饲管输入肠内营养或口服药物。但药物碾碎后管饲给药,可能破坏药物稳定性、改变药物吸收部位或速度、增加堵管发生风险,导致不良治疗结局[1]。终末期肝病患者常存在胃静脉曲张、肠黏膜水肿和肠蠕动减弱等病理变化,胃肠道吸收功能和屏障保护功能降低,在该类患者中药物形态改变对药动学、药效学的影响更大。临床药师在肝病重症监护室(intensive care unit,ICU)工作期间了解到,护士往往将多种药在药袋里一起研碎后经鼻胃管注入。本研究拟通过分析肝病重症患者的管饲给药情况,评估肝病专科常用口服药物管饲给药的适宜性,作为其他研究[2-5]的补充,进一步规范管饲给药操作。
1 资料与方法
采用信息化手段回顾性抽取2020年某医疗机构肝病重症监护室全部出院病例392例,筛选其中包含管饲给药的病例100例,收集患者的基本资料和管饲给药情况,根据药品说明书及相关文献资料分析管饲给药的适宜性。
2 结果
2.1 患者基本情况
100例肝病重症患者均留置鼻胃管,其中男性患者75例,女性患者25例;年龄19~87岁,中位年龄57岁;ICU滞留时间1~165 d,中位ICU滞留时间9 d;终末期肝病者91例;置管原因:意识障碍48例,胃肠道减压37例,呼吸机辅助通气15例。
2.2 管饲给药方式
片剂在药袋内研碎、胶囊去壳,药粉或颗粒在水中分散后注入胃管;液体制剂原液或经稀释后注入胃管。管饲给药前后用适量水冲管,给药后胃管夹闭3~4 h;若有持续肠内营养输注,仅在给药时暂停输注,与药物无明显时间间隔。
2.3 管饲给药整体情况
100例肝病重症患者管饲给药共4 917例次,涉及99种药物,药物剂型分布见表1。给药例次数最多的药物类别为消化系统用药(2 540例次),其次为抗感染药(1 002例次);给药例次数排序居前3名的药品为乳果糖口服溶液(984例次)、利福昔明片(522例次)和地衣芽孢杆菌活菌胶囊(366例次)。
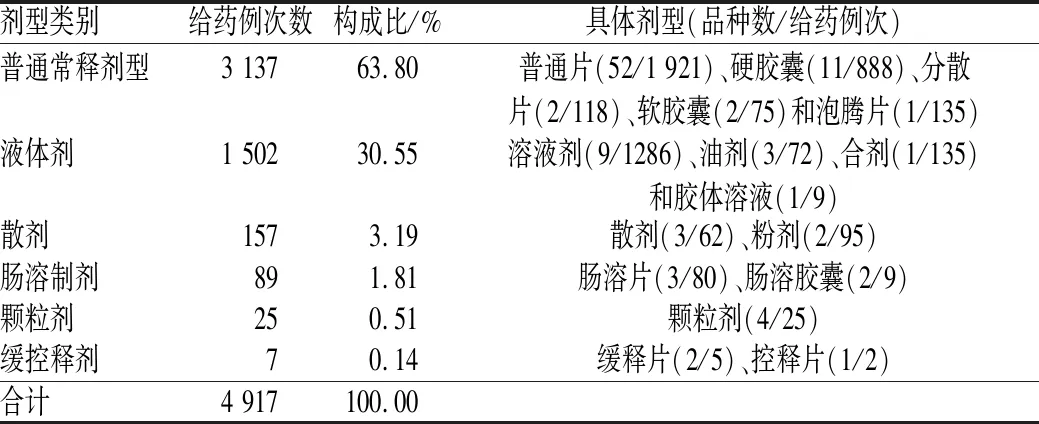
表1 管饲给药的药物剂型分布Tab 1 Distribution of drug dosage form for tube feeding
2.4 管饲给药的联合用药情况
定义不同药物胃管注入的医嘱执行时间间隔<10 min为联合用药。100例患者中有47例存在联合用药情况,合用药物种类2~14种,共计77种联合应用组合,其中2~3种药物联合的有49组,占63.64%(49/77);4~5种药物联合的有21组,占27.27%(21/77);5种以上药物联合的有7组,占9.09%(7/77)。有17例患者存在肠内营养液与药物联合应用的情况,肠内营养品种包括肠内营养混悬液(TP-MCT)、肠内营养混悬液(TPF-FOS)、肠内营养粉(TP)、肠内营养混悬液(TPF)和肠内营养混悬液(TPF-D),涉及药物品种为45种。
2.5 不合理用药情况
在统计范围内,管饲给药不合理用药合计544例次,不合理用药率为11.06%。其中,剂型选择不适宜424例次,涉及13种药物,见表2;联合用药不适宜120例次,见表3。

表2 管饲给药中药物剂型选择不适宜的情况Tab 2 Inappropriate dosage form selection for tube feeding

表3 管饲给药中联合用药不适宜的情况Tab 3 Inappropriate drug combination for tube feeding
3 讨论
3.1 管饲给药存在的问题
3.1.1 药物剂型选择:药物剂型是决定给药途径的主要因素之一[6]。本研究结果显示,剂型选择不当是最常见的管饲给药问题,占不合理用药的77.94%(424/544)。患者管饲给药的剂型多为普通片剂、硬胶囊和溶液剂。普通片剂和硬胶囊一般可经研碎,去壳后分散于水中。但分散片和泡腾片可快速分散于水中,无需研磨以避免减少药物损失或受热变性;且安罗替尼、吗替麦考酚酯和恩替卡韦等药物有细胞毒性或致癌性,药粉接触皮肤和呼吸道存在安全隐患,不宜在无防护下研磨。
肠溶制剂和缓控释制剂是利用特殊包衣材料或制剂工艺制成,可保护药物成分不被胃酸破坏,避免药物对胃的损伤,达到缓慢或恒速释放目的,研磨或胶囊去壳会使药物吸收部位、释放速度改变,影响生物利用度及疗效,也可能增加不良反应发生风险,如麦考酚钠和阿司匹林制成肠溶制剂分别是为保护疗效和避免不良反应。此外,由不溶性骨架、渗透泵制成的缓控释制剂在遇水后药物成分即开始释放,除禁止研碎外,给药前应避免与水接触,代表药品有硝苯地平缓释片(Ⅱ)、硝苯地平控释片和盐酸曲马多缓释片等[7-8]。经工艺改进,某些药物成分被制成特效微丸,只要不破坏其微丸结构,便能保留肠溶或缓控释效果,该类药物可将药片或胶囊内颗粒分散于水中(勿研碎)管饲给药,代表药品有琥珀酸美托洛尔缓释片、文拉法辛缓释胶囊以及部分质子泵抑制剂肠溶制剂[9];但缺少了包衣层或胶囊壳的保护,单元颗粒的药物释放仍可能受到一定影响,如Hoover等[10]发现艾司奥美拉唑肠溶胶囊的内容颗粒在胃酸下暴露15 min之后会出现突释现象。因各药品生产企业的生产工艺不同,除药品说明书有相应说明外,肠溶制剂和缓控释制剂应禁止研碎、避免管饲给药。
油性制剂易吸附于注射器及饲管的管壁,且水不易冲刷,导致药量损失较多;同时,挂壁的油性成分会吸附其他药物成分及辅料,影响疗效且容易堵管。基于存在操作不便、剂量不准的缺陷,内容物为油性成分的软胶囊不宜管饲给药。液状石蜡和橄榄油等油性制剂往往需要给予更大的处方量方能达到预期的治疗效果。
3.1.2 药物相互作用:本研究中联合用药现象较为普遍,药物-药物、药物-食物均可存在潜在相互作用,是不合理用药的另一主要原因。肠道菌群调节剂和肝性脑病治疗药物是肝病重症患者主要的管饲药物,均为1日多次给药,联合给药的概率较大[11-12]。现有的微生态药物多为活菌制剂,与抗菌药物接触可被灭活,上述2类药物应错开给药时间。活菌制剂与其他药物的相互作用及影响机制尚未完全明确,但是联合用药可能会使菌体被吸附在管壁或包裹在其他药物辅料中而影响疗效,因此,微生态药物宜单独给药。
肠内营养制剂对药物的影响主要体现在:(1)减慢胃排空速率,延缓药物吸收,如可降低恩替卡韦和他克莫司的吸收速度和程度;(2)营养成分尤其是脂肪对药物吸收利用度的影响,如可降低伏立康唑的血药峰浓度和药时曲线下面积;(3)吸附药物辅料增加堵管风险[13-14]。因此,尤其对于联合应用口服药较多、且需长期管饲肠内营养制剂的患者,应重视肠内营养液和药物的相互作用以及饲管的通畅性。
3.2 管饲给药优化建议
为模拟临床给药,将药片放入10 ml温水中,轻微搅拌下,恩替卡韦分散片和乙酰半胱氨酸泡腾片均可在30 s内完全分散,吗替麦考酚酯分散片约需60 s;奥美拉唑镁肠溶片、利福昔明片等常释片剂至少需2 min,包衣片较未包衣片所需时间更长。固体药物分散并静置后可见大量辅料沉淀,奥美拉唑镁肠溶片分散后可见粒径<1 mm的完整肠溶微球。这与Beserra等[15]的实验结果吻合。
基于上述理论和实验数据,临床药师建议:(1)分散片、泡腾片放入水中自然分散;(2)肠溶制剂和缓控释制剂用普通制剂或胃肠外制剂代替;(3)质子泵抑制剂口服制剂用静脉制剂代替,必要时可选用药品说明书中明确标示可管饲给药的制剂,如某些药品生产企业的艾司奥美拉唑镁肠溶片、奥美拉唑镁肠溶片可分散于水或果汁中再给药;(4)软胶囊换为硬胶囊或其他替代治疗药物;(5)微生态药物与抗菌药物至少间隔2 h以上给药,肠内营养液在给药前后充分冲管,需要空腹给药的药物在给药前和给药后分别将肠内营养夹闭至少1和2 h。
综上所述,肝病重症患者管饲药物种类相对集中,不合理用药率相对较低,但仍需引起临床重视并进一步优化[16-17]。在临床药师反馈后,医护人员普遍认可上述建议并依照执行。临床药师利用药学专业知识,与临床医师和护士协作互补,有利于促进管饲给药的合理用药,提高患者药物治疗的有效性和安全性。

