基于适配体调控碳点催化反应的SERS法检测农残啶虫脒
黎小椿,吴凤莲,庞永丰,聂 辉,黄双全,罗杨合
(贺州学院食品科学与工程技术研究院, 广西贺州 542899)
啶虫脒(Acetamiprid,AC)是一种氯化烟碱类新型高效广谱杀虫剂。其能作用于蔬菜、果树、水稻及茶叶上的同翅目、鳞翅目及鞘翅目害虫神经系统突触部位烟碱乙酰胆碱受体,干扰害虫神经系统的刺激传导,引起神经系统通路阻塞,导致害虫麻痹,从而达到杀虫的效果[1-2]。啶虫脒在植物和环境中难以降解,频繁和广泛地施用啶虫脒会导致环境污染,且残留在蔬菜中的啶虫脒还会对人类有轻微的急性和慢性毒性[3-4],它通过干扰人的中枢神经系统,引起如阿尔茨海默病、帕金森病、精神分裂症和抑郁症疾病。
目前,啶虫脒的检测方法包括色谱法[5-6]、电化学法[7-8]、荧光法[9-11]和Surface-enhanced Raman scattering(SERS)[12-13]法。这些方法中,色谱法成本高、操作复杂、耗时长,不能满足现场检测的要求;电化学法和荧光法选择性低、线性范围窄,限制其在实际检测中的应用。而SERS法是一种选择性好、敏感性高的检测方法,在农残检测应用中具有操作简便、灵敏度高和对样品无损等其它常规农残检测方法无法比拟的优势[14-15]。
核酸适配体(Aptamer,Apt),又称核酸适体或适体,是通过指数富集系统(SELEX)技术从体外随机单链脱氧核糖核酸(DNA)或核糖核酸(RNA)序列库中筛选出来的能与靶物质产生类似于抗原-抗体高特异性结合的寡核苷酸链[16]。随着生物技术的发展,核酸适配体基于高亲和力及与目标小分子(配体或靶分子)结合的特异性,被作为新型分子识别元件,在食品安全、环境分析、生物医学等领域中的应用十分普遍。此外,适配体还具有体积小、易于人工合成和修饰等多种优势[17-18],成为SERS分析和农残检测中识别目标分子的理想选择。
碳点由于具有优异的表面效应、良好的电子传导性能、特殊的尺寸效应,使其在SERS分析中得以广泛应用。碳点和异原子掺杂碳点的催化反应可用于制备高稳定性高SERS活性基底,提高SERS分析重现性,大大拓宽了SERS分析应用领域。Luo等[19]利用碳点(CD)还原HAuCl4制备平均粒径8~44 nm的Au@CD纳米基底,并比较其与AuNP基底对罗丹明6G(rhodamine 6G,Rh6G)的吸附能力,结果显示:Au@CD纳米基底对Rh6G表现出的SERS效应高于相同纳米尺寸的AuNP基底。Wang等[20]利用N掺杂碳量子点催化HAuCl4与H2O2反应可制备高稳定性纳米金基底,建立重现性好的SERS检测SO42-的新方法。Zhao等[21]将碳点(CD)与AgNP反应制备高的AgNPs/CD作为SERS基底,该基底能检测浓度低至10-8mol/L的PATP(paminothiophenol)。迄今为止,关于碳点运用于农药残留检测的研究大多局限于荧光探针的制备,啶虫脒的检测未见碳点和掺杂碳点结合SERS检测啶虫脒的报道[22-28]。碳点具有比表面积大、生物相容性等优势,将其SERS技术相结合,可以大大提高在农残检测中的速度、灵敏度和选择性。
本文将高灵敏度简便快速的SERS分析方法与具有较高亲和力的适配体和具有优异催化活性的碳点有机结合,通过适配体和啶虫脒农药靶标分子调节碳点催化反应,构建重现性好、灵敏度高、简便快速的蔬菜中啶虫脒、农药残留检测方法,这既是提高SERS分析方法重现性和农药残留快速检测方法灵敏度低的新探索,又是适配体化学、纳米酶化学、催化反应理论及应用的新拓展,符合公众对蔬菜质量安全越来越高的要求,对保障人类健康和促进社会经济发展具有重要意义,同时可为果蔬汁加工企业解决在生产过程中检测痕量农残的难题提供参考依据。
1 材料与方法
1.1 材料与仪器
3500 Da透析袋;核酸适配体(Aptamer,Apt)序列[27]:5’-CTCTCTCTCTCTGACACCATATTATGAA GATCTCTCTCTC-3’ 上海生工生物有限公司;啶虫脒、吡虫啉(纯度98.5%),阿特拉津(98%)纯度,多菌灵、毒死蜱(纯度99%) 上海阿拉丁生化科技股份有限公司;1 mol/L AgNO3分析纯,广东光华科技股份有限公司,使用时稀释至所需浓度;0.1 mol/L柠檬酸三钠 分析纯,广东汕头西陇化工厂;1 mol/L NaCl 分析纯,西陇化工股份有限公司;1.0×10-5mol/L维多利亚蓝B(VBB)溶液 上海阿拉丁生化科技股份有限公司;果糖纯度99% 上海阿拉丁生化科技股份有限公司;尿素 分析纯,广东省化学试剂工程技术研发中心;小白菜500 g、黄瓜500 g、西红柿500 g 购置于农贸市场;啶虫脒标准溶液的配制:准确称取0.0050 g啶虫脒粉末,加2 mL丙酮超声完全溶解后转移至50 mL容量瓶,加水定容至刻度线,得到100 mg/L啶虫脒标准溶液,稀释至100倍得到1 mg/L,稀释两倍得到0.5 mg/L,备用;实验用水 为亚沸水。
DXR smart拉曼光谱仪 美国Thermo公司;日立F-7000荧光分光光度计 日立高新技术公司;TU-1901型双光束紫外可见分光光度计 北京普析通用仪器有限责任公司;HH-S2电热恒温水浴锅 金坛市大地自动化仪器厂;S-4800场发射扫描电子显微镜 日立高新技术公司英国牛津公司;SYZ-550型石英亚沸蒸馏水器 江苏晶玻仪器厂;EG 823 LA6-NR3美的微波炉 广东美的厨房电器制造有限公司。
1.2 实验方法
1.2.1 掺氮及掺氮银碳量子点(CDN、CDN/Ag)的制备将0.5 g果糖、0.8 g尿素和0、0.5、1、1.5 mL 0.01 mol/L AgNO3于烧杯中超声溶解完全,用亚沸水定容至15 mL,用保鲜膜封口,在薄膜上扎几个小孔后置于微波炉(700 W)中加热5 min。加热结束后,自然冷却至室温即得到棕黑色固体,用适量去离子水将其溶解并定容至15 mL,将溶液于10000 r/min离心5 min,取上清液,用截留分子量为3500 Da的透析袋透析12 h,用50 mmol/L NaOH调至中性,再用亚沸水定容至15 mL,得到CDN、CDN/Ag0.5、CDN/Ag1、CDN/Ag1.5碳量子点浓度为0.021 g/mL(以果糖计),使用时稀释至所需浓度。
1.2.2 SERS法测定啶虫脒 在5 mL具塞试管中依次加入适量浓度的啶虫脒、60 μL 0.60 μmol/L的啶虫脒适配体溶液,混匀静置反应8 min;加入125 μL 2.13 mg/L CDN或CDN/Ag溶液,充分混匀后再静置大约5 min;然后加入120 μL 0.01 mol/L AgNO3、80 μL 0.1 mol/L柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加20 μL 1 mol/L NaCl、50 μL 1.0×10-5mol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度,不加啶虫脒溶液做空白,测定其空白值,计算值。数据采集时,拉曼光谱仪的参数设置为:激光波长633 nm,激光功率为3.5 mW, 狭缝为50 μm,采集时 间为5 s。
1.2.3 电镜样品的制备 取1.5 mL反应液:AC+22.93 nmol/L Apt+169.35 μg/L CDN/Ag1+0.90 mmol/L AgNO3+6.45 mmol/L trisodium citrate+80 ℃+20 min(其中啶虫脒浓度分别为0、286.04、429.05 nmol/L)放入2 mL离心管中于7000 r/min下离心10 min,取上清液,加水定容至1.5 mL,超声15 min。重复上述离心步骤两次,加水1.5 mL进行扫描电镜检测。
1.2.4 碳点催化反应的SERS光谱采集 分别在5 mL具塞试管中依次加入不同浓度的CDN或CDN/Ag溶液、0.90 mmol/L AgNO3溶液和6.45 mmol/L柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min,冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB,测定1617 cm-1拉曼位移处的表面 增强拉曼散射峰强度。
1.2.5 啶虫脒-Apt-碳点(CDN/Ag1)催化反应的猝灭与增强光谱采集
1.2.5.1 猝灭光谱采集 在5 mL具塞试管中依次加入适量浓度的啶虫脒适配体溶液、169.35 μg/L CDN/Ag1溶液,充分混匀后静置大约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散 射峰强度。
1.2.5.2 增强光谱采集 在5 mL具塞试管中依次加入适量浓度的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置大约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散 射峰强度。
1.2.6 检测条件的优化
1.2.6.1 CDN/Ag1浓度的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入不同浓度的CDN/Ag1溶液,充分混匀后再静置约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.6.2 柠檬酸三钠浓度的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置大约5 min;然后加入0.90 mmol/L AgNO3、不同浓度的柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.6.3 AgNO3浓度的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置约5 min;然后加入不同浓度的AgNO3溶液、6.45 mmol/L的柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.6.4 Apt浓度的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、不同浓度的啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L的柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.6.5 NaCl浓度的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置大约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L的柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加不同浓度的NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.6.6 水浴温度的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L的柠檬酸三钠溶液,用亚沸水定容到1.5 mL,置于不同温度下水浴反应20 min;冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.6.7 水浴时间的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置大约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L的柠檬酸三钠溶液,用亚沸水定容到1.5 mL,设置不同的水浴时间于80 ℃下进行反应;冰水终止反应,加12.90 mmol/L NaCl和0.33 μmol/L VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.6.8 VBB浓度的优化 在5 mL具塞试管中依次加入457.67 nmol/L的啶虫脒溶液、22.93 nmol/L啶虫脒适配体溶液,混匀静置反应8 min;加入169.35 μg/L CDN/Ag1溶液,充分混匀后再静置大约5 min;然后加入0.90 mmol/L AgNO3、6.45 mmol/L的柠檬酸三钠溶液,用亚沸水定容到1.5 mL,80 ℃水浴反应20 min;冰水终止反应,加12.90 mmol/L NaCl和不同浓度的VBB。测定1617 cm-1拉曼位移处的表面增强拉曼散射峰强度。不加啶虫脒溶液做空白,测定其空白值,计算值。
1.2.7 蔬菜样品检测及加标回收实验 准确称量白菜、黄瓜、西红柿各50 g,充分研磨后加1 mL 99.5%丙酮静置5 min,取滤液1000 r/min离心5 min,取无色上清液,用亚沸水定容至15 mL存放于4 ℃冰箱中。采用啶虫脒-适配体-CDN/Ag1-柠檬酸三钠-AgNO3-NaCl-VBB体系SERS法,分别平行5次对3种蔬菜样品进行加标回收实验。
2 结果与讨论
2.1 方法原理
在80 ℃的条件下,CDN、CDN/Ag对AgNO3-柠檬酸三钠生成银纳米粒子的反应具有很强的催化作用。在一定浓度范围内,随着CDN、CDN/Ag浓度的增大,其催化作用增强,生成高稳定性高SERS活性的银纳米粒子增多,加入VBB后体系的SERS强度随之增强。当体系中存在一定浓度啶虫脒核酸适配体时,CDN、CDN/Ag与适配体由于静电作用相结合,其催化活性被抑制,体系的SERS强度减弱。加入靶分子啶虫脒后,它与适配体发生特异性结合,形成啶虫脒-适配体复合物而脱离CDN、CDN/Ag的表面,此时CDN、CDN/Ag得到释放,催化作用活化,体系的SERS强度增强。随着啶虫脒浓度的增加,体系中游离的啶虫脒-适配体减少,CDN、CDN/Ag浓度相对增大,催化作用增强,体系的SERS信号线性增强(图1)。据此建立了一种简便、快速、灵敏高、选择性和重现性好的测定啶虫脒的SERS新方法。

图1 SERS测定啶虫脒的分析原理图Fig.1 The principle of determination of acetamiprid by SERS
2.2 扫描电镜结果
用扫描电镜对生成的银纳米颗粒的粒度和表面形态进行观察。在啶虫脒-Apt-CDN/Ag1-柠檬酸三钠-AgNO3体系中,当溶液中没有啶虫脒时,Apt包裹碳点,抑制了CDN/Ag1催化柠檬酸三钠-AgNO3反应,反应生成的银纳米粒子较少(平均粒径约为30 nm,图2A)且较分散。加入啶虫脒后,CDN/Ag1被释放,体系的催化作用恢复,生成了更多粒径较大(平均粒径约为60 nm,图2B)且有一定聚集度的纳米银,导致体系SERS强度增强。随着啶虫脒浓度的增加,被释放的CDN/Ag1增多,体系的催化作用增强,生成了更多粒径更大(平均粒径约为150 nm,图2C)聚集度更强的纳米银。

图2 AC-Apt-CDN/Ag1-柠檬酸三钠-AgNO3体系SEM图Fig.2 SEM of AC-Apt-CDN/Ag1-trisodium citrate-AgNO3 system
2.3 表面增强拉曼散射(SERS)光谱
2.3.1 碳点催化反应的SERS光谱 在80 ℃水浴条件下,AgNO3-柠檬酸三钠体系很难发生反应。当CDN、CDN/Ag催化剂存在的情况下,能很快催化柠檬酸三钠还原AgNO3生成有SERS活性的黄色纳米银,加入VBB后,体系在1617 cm-1处出现较强的特征拉曼峰,并随着CDN、CDN/Ag浓度的增加,CDN、CDN/Ag催化性能增强,体系的SERS信号增强(图3)。其中,CDN/Ag1的催化作用最强(图4,当CDN、CDN/Ag0.5、CDN/Ag1、CDN/Ag1.5的 浓 度 均 为270.96 μg/L时,其在1617 cm-1处的SERS强度分别为2748、1980、4273、3330 cps,因此以CDN/Ag1作为催化剂。

图3 CDN/CDN/Ag-AgNO3-柠檬酸三钠-NaCl-VBB SERS光谱Fig.3 SERS spectra of CDN/CDN/Ag-AgNO3-trisodium citrate- NaCl-VBB

图4 CDN/CDN/Ag-AgNO3-柠檬酸三钠-NaCl-VBB SERS光谱Fig.4 SERS spectra of CDN/CDN/Ag-AgNO3-trisodium citrate-NaCl-VBB
2.3.2 啶虫脒-Apt-碳点(CDN/Ag1)催化反应的猝灭与增强机制 由图5可知,随着适配体浓度的增加,体系的SERS强度降低。这是由于CDN/Ag1具有良好的生物相容性,在CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB催化体系中加入啶虫脒适配体,CDN/Ag1表面很快被适配体包裹,使其与AgNO3-柠檬酸三钠的接触面积大大减小,致使其催化活性受到抑制,反应生成的纳米银减少,SERS强度降低。其中,在3.82~45.86 nmol/L浓度范围内,啶虫脒适配体对CDN/Ag1催化活性的抑制作用逐渐增强。当体系中加入啶虫脒时,啶虫脒与适配体发生特异性结合,逐渐释放出CDN/Ag1,体系催化作用恢复,体系的SERS强度增强(图6)。啶虫脒在14.30~457.67 nmol/L浓度范围内,CDN/Ag1催化的SERS强度逐渐增强。

图5 Apt- CDN/Ag1- AgNO3-柠檬酸三钠-NaCl-VBB体系SERS光谱Fig.5 SERS spectra of Apt- CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system

图6 AC-Apt- CDN/Ag1- AgNO3-柠檬酸三钠-NaCl-VBB体系SERS光谱Fig.6 SERS spectra of AC-Apt- CDN/Ag1- AgNO3- trisodium citrate-NaCl-VBB system
2.4 检测条件的优化
在水浴温度为80 ℃,反应时间为20 min条件下对AC-Apt-碳点-AgNO3-柠檬酸三钠-NaCl-VBB体系中CDN/Ag1、柠檬酸三钠、AgNO3、Apt、NaCl浓度进行优化。当其浓度分别为169.35 μg/L、6.45 mmol/L、0.90 mmol/L、22.93 nmol/L、12.9 mmol/L时,体系达到最大值(图7、图8、图9、图10、图11的分别为2228、2096、2588、1671、1129 cps)。故实验最后选取CDN/Ag1浓度为169.35 μg/L,AgNO3浓度为0.90 mmol/L,柠檬酸三钠浓度为6.45 mmol/L,Apt浓度为22.93 nmol/L,NaCl浓度为12.9 mmol/L。在优化完以上条件的情况下,对水浴温度和时间进行优化。当水浴温度为80 ℃、反应时间为20 min时,体系达到最大值(图12、图13的分别为1960、1775 cps),故选反应温度为80 ℃,反应时间为20 min。最后对探针分子进行优化。当VBB浓度在0.323 μmol/L时,体系达到最大值(图14的为1682 cps),故选取VBB浓度为0.323 μmol/L。

图7 CDN/Ag1浓度对AC-Apt- CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.7 Effect of CDN/Ag1 concentration on AC- Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system
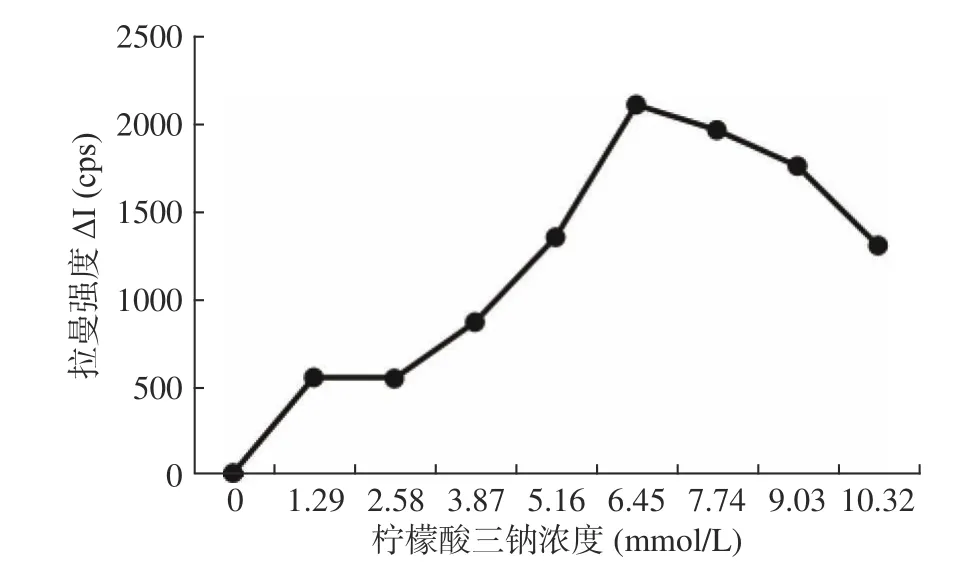
图8 柠檬酸三钠浓度对AC-Apt-CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.8 Effect of trisodium citrate concentration on AC-Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system

图9 AgNO3浓度对AC-Apt-CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.9 Effect of AgNO3 concentration on AC-Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system

图10 Apt浓度对AC-Apt-CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.10 Effect of Apt concentration on AC-Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system

图11 NaCl浓度对AC-Apt-CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.11 Effect of NaCl concentration on AC-Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system

图12 温度对AC-Apt-CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.12 Effect of temperature on AC-Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system

图13 时间对AC-Apt- CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.13 Effect of time on AC- Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system

图14 VBB浓度对AC-Apt-CDN/Ag1-AgNO3-柠檬酸三钠-NaCl-VBB体系的影响Fig.14 Effect of VBB concentration on AC- Apt-CDN/Ag1-AgNO3-trisodium citrate-NaCl-VBB system
2.5 工作曲线
根据试验方法,对适配体-CDN/Ag1-柠檬酸三钠-AgNO3-NaCl-VBB体系,以啶虫脒(nmol/L)对绘制工作曲线。结果表明,啶虫脒在14.30~457.67 nmol/L范围内与呈线性关系,其回归线性方程为6.9714x+21.094,决定系数R2=0.9967,检出限为10.03 nmol/L。
2.6 干扰离子的影响
按实验方法考察了常见离子、啶虫脒共施农药和结构相似农药对啶虫脒-适配体-CDN/Ag1-柠檬酸三钠-AgNO3-NaCl-VBB体系SERS法测定85.80 nmol/L啶虫脒的干扰情况。从表1中可以看出,8.580 μmol/L Mg2+、Na+、Cu2+、Zn2+、Al3+、Ba2+、Fe3+、K+、NH4+、CO32-、NO3-、SO42-、Cl-、HCO32-不干扰测定,6.864 μmol/L Ca2+不干扰测定,8.580 μmol/L多菌灵、吡虫啉、特拉津、毒死蜱不干扰测定;丙酮作为啶虫脒的溶剂,在浓度为8.580 μmol/L时也不干扰测定。以上说明,该方法具有较好的选择性。
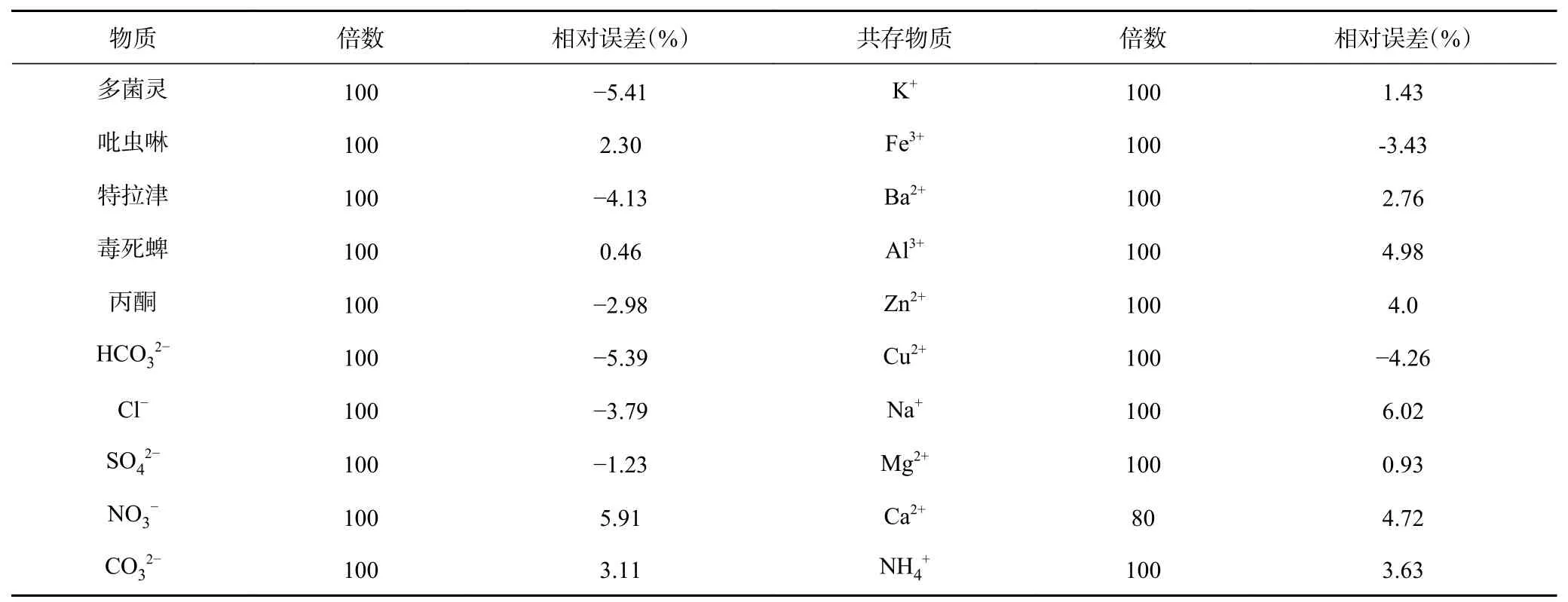
表1 常见干扰物质的影响Table 1 Effect of common interfering substances
2.7 样品分析
蔬菜样品检测及加标回收实验结果如表2所示,小白菜、西红柿、黄瓜不同样品回收为98.27%~101.78%,相对标准偏差分别为2.31%、0.83%和1.69%,说明建立的方法检测结果精密度高,重复性好。

表2 样品测定结果Table 2 Results of sample determination
2.8 啶虫脒检测方法的比较
啶虫脒检测方法的比较结果如表3所示。相比其他方法,本方法具有操作方便、灵敏度较高、选择性好的优点,线性范围为14.30~457.67 nmol/L,检出限低至10.03 nmol/L。

表3 啶虫脒检测方法的比较Table 3 The comparison of detection methods of acetamiprid
3 结论
在80 ℃水浴条件下,AgNO3-柠檬酸三钠很难发生反应。该体系在CDN/Ag1纳米酶的催化作用下,反应迅速发生,生成了高稳定性、高SERS活性的黄色银纳米粒子(AgNP)。在体系中加入VBB探针分子后,有较强的SERS峰。适配体通过物理静电等作用吸附在CDN/Ag1纳米酶表面,阻断了其与反应物的结合,抑制了其催化作用。当加入啶虫脒之后,啶虫脒可与适配体特异性结合,形成非常稳定的啶虫脒-适配体复合物而脱离CDN/Ag1表面,CDN/Ag1催化作用恢复,导致体系的SERS强度线性增强。据此,建立了适配体调控CDN/Ag1催化柠檬酸三钠-AgNO3反应检测范围为14.30~457.67 nmol/L啶虫脒的SERS新方法。该方法用于检测小白菜、黄瓜和西红柿中的痕量啶虫脒,回收率在98.27%~101.78%,相对标准偏差分别为2.31%、0.83%和1.69%。

