ICIs单用或联合常规化疗药物用于NSCLC患者致非免疫相关不良事件的Meta分析
张清树 陈瑞祥 温瑾 夏从龙 何姣 赵倩


摘 要 目的:系統评价免疫检查点抑制剂(ICIs)单用或联合常规化疗药物用于非小细胞肺癌(NSCLC)患者致非免疫相关不良事件(irAEs)的发生情况,为临床用药提供循证参考。方法:计算机检索PubMed、Cochrane 图书馆、Embase、中国知网、中国生物医学文献数据库、维普网和万方数据等,检索时限均为建库至2020年10月。收集ICIs单用或联合常规化疗药物(试验组)对比常规化疗药物或安慰剂联合常规化疗药物(对照组)的随机对照试验(RCT)。筛选文献、提取数据后,采用Cochrane系统评价员手册5.1.0推荐的偏倚风险评估工具对纳入文献质量进行评价,采用Rev Man 5.3和Stata 15.0软件进行Meta分析;采用Stata 15.0软件进行敏感性分析;采用倒漏斗图和Eggers检验进行发表偏倚分析。结果:共纳入20项RCT,共计12 283例患者。Meta分析结果显示,试验组患者总体所有级别和总体重度AEs发生率、贫血发生率、中性粒细胞减少症、呕吐、脱发发生率以及所有级别血小板减少症、恶心、周围神经病变发生率均显著低于对照组(P<0.05);而两组患者终止治疗、死亡、重度血小板减少症、重度恶心和重度周围神经病变发生率以及所有级别和重度腹泻发生率比较,差异均无统计学意义(P>0.05)。亚组分析结果显示,试验组单用ICIs患者的总体所有级别和总体重度AEs发生率、贫血发生率、中性粒细胞减少症发生率、血小板减少症发生率、临床相关症状发生率(除重度腹泻外)以及终止治疗发生率、死亡发生率均显著低于对照组(P<0.05);而试验组使用ICIs+化疗患者的终止治疗发生率、死亡发生率以及所有级别恶心、呕吐、腹泻、脱发和重度腹泻发生率均显著高于对照组(P<0.05)。敏感性分析支持上述结果;发表偏倚分析结果显示,本研究存在发表偏倚的可能性较小。结论:对于NSCLC患者,ICIs在治疗相关AEs、血液系统毒性和临床相关症状方面的安全性优于常规化疗药物或安慰剂联合常规化疗药物;但当其联合常规化疗药物时,因AEs终止治疗和死亡的风险以及所有级别恶心、呕吐、腹泻、脱发及重度腹泻的风险将有所增加。
关键词 非小细胞肺癌;免疫检查点抑制剂;非免疫相关不良事件;安全性;Meta分析
ABSTRACT OBJECTIVE: To systematically evaluate the occurrence of non-immune related adverse events (AEs) caused by immune checkpoint inhibitors (ICIs) alone or combined with routine chemotherapy in the treatment of non-small cell lung cancer (NSCLC), and to provide evidence-based reference for clinical medication. METHODS: Retrieved from PubMed, Cochrane Library, Embase, CNKI, CBM, VIP and Wanfang database during the inception to Oct. 2020, randomized controlled trials (RCT) about ICIs alone or combined with routine chemotherapy (trial group) versus routine chemotherapy or placebo combined with routine chemotherapy (control group) were collected. After literature screening and data extraction, the quality of included literatures were evaluated with bias risk evaluation tool recommended by Cochrane systematic evaluator manual 5.1.0. Meta-analysis was performed by using Rev Man 5.3 software and Stata 15.0 software. Sensitivity analysis was conducted with Stata 15.0 software. Inverted funnel plot and Eggers test were used to analyze publication bias. RESULTS: A total of 20 RCTs were included, involving 12 283 patients. Results of Meta-analysis showed that the incidence of all grades and severe AEs, anemia, neutropenia, vomiting and alopecia as well as the incidence of thrombocytopenia, nausea and peripheral neuropathy in all grades of trial group were all significantly lower than control group (P<0.05). There was no statistical significance in the incidence of termination of treatment, death, severe thrombocytopenia, severe nausea and severe peripheral neuropathy or all grades and severe diarrhea between 2 groups (P>0.05). Subgroup analysis showed that the incidence of all grade and total severe AEs, the incidence of anemia, neutropenia, thrombocytopenia, clinically relevant symptoms (except for severe diarrhea), termination of treatment and death of patients receiving ICIs alone in trial group were significantly lower than control group (P<0.05). The incidence of ermination of treatment and death, the incidence of nausea, vomiting, diarrhea and alopecia in all grade, severe diarrhea of patients receiving ICIs and chemotherapy in trial group were all significantly higher than control group (P<0.05). Sensitivity analysis supported the above results. Analyze publication bias results showed that the possibility of publication bias in this study was small. CONCLUSIONS: For NSCLC patients, the safety of ICIs is better than that of routine chemotherapy or placebo combined with routine chemotherapy in the treatment-related AEs, hematologic toxicity and clinically relevant symptoms; however, the risks of treatment discontinuation, AEs-induced deaths, and all-grade nausea, vomiting, diarrhea, alopecia and severe diarrhea will be increased in the ICIs combined with routine chemotherapy.
KEYWORDS Non-small cell lung cancer; Immune checkpoint inhibitors; Non-immune related adverse events; Safety; Meta-analysis
肺癌是常见的恶性肿瘤之一,也是全球发病率和病死率最高的肿瘤[1]。非小细胞肺癌(NSCLC)是肺癌的一种类型,属于一种异质性肿瘤,包括腺癌、鳞癌和大细胞癌。NSCLC约占所有新诊断肺癌患者的85%,由于筛查计划不足和临床症状出现较晚,患者确诊时大多已为晚期,失去了手术治疗的机会,以致其预后较差[2-3]。NSCLC的常规治疗主要为手术切除和以铂类药物为主的化疗、放疗和靶向治疗[4-5]。虽然,NSCLC的临床治疗已取得了巨大的进展,但获得性耐药的发生导致了患者复发率高、总生存率低,最终预后不良[6]。
随着免疫疗法的迅速发展,免疫检查点抑制剂(ICIs)在NSCLC患者免疫系统调节和免疫治疗中取得了较大突破,包括程序性死亡蛋白1(PD-1)、程序性死亡蛋白配体1(PD-L1)和细胞毒性T淋巴细胞相关抗原4(CTLA-4)在内的ICIs已在临床实践中被证实可通过调节T细胞介导的免疫反应来清除晚期/难治性和转移性NSCLC患者体内的肿瘤细胞,延长了NSCLC患者的无进展生存期和总生存期,极大地改善了患者预后,显示出显著的抗肿瘤效果,甚至有望在一线治疗中成为有效的治疗选择[5,7]。但在临床试验中发现,与化疗或分子靶向治疗不同,ICIs可引发严重的不良事件(AEs)——免疫相关不良事件(irAEs),其临床表现为涉及多个器官和组织的自身免疫样反应和炎症反应,包括皮肤、胃肠道、肝脏、胰腺、內分泌系统、肺脏、肾脏、眼睛、神经系统、心血管系统、肌肉骨骼等[5,7-8]。然而,常见的化疗毒性,如恶心、呕吐、腹泻、脱发和血液系统不良反应等传统化疗相关的AEs(即非irAEs)也在使用ICIs的患者中被发现,严重影响了患者的生存质量,临床应予以重视[9]。既往研究和Meta分析大多集中在ICIs引起的irAEs[10-11],而非irAEs的发生以及ICIs是否会增加非irAEs发生风险的研究较少。虽然,既往有研究分析了ICIs引起的非irAEs,但研究样本量较小,结论存在争议[9],且缺乏相关的系统评价。基于此,本研究采用Meta分析的方法比较了ICIs单用或联合常规化疗药物用于NSCLC患者致非irAEs的发生情况,旨在为临床使用ICIs的安全性提供循证参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 国内外公开发表的Ⅱ或Ⅲ期双臂随机对照试验(RCT)。语种限定为中文和英文。
1.1.2 研究对象 经病理证实为NSCLC,肿瘤分期不限;年龄大于18岁;地区、种族和性别不限。
1.1.3 干预措施 对照组患者给予常规化疗药物或安慰剂联合常规化疗药物;试验组患者单用ICIs或ICIs联合常规化疗药物。两组患者的用药剂量、疗程均不限。
1.1.4 结局指标 ①治疗相关AEs发生率,包括总体所有级别和总体重度AEs、终止治疗、死亡发生率(该项所有指标均包含了因治疗产生的AEs,即irAEs和非irAEs);②血液系统AEs发生率,包括所有级别和重度贫血、中性粒细胞减少症、血小板减少症发生率;③临床相关症状发生率,包括所有级别和重度恶心、呕吐、腹泻、脱发、周围神经病变发生率(②③均为非irAEs)。AEs严重程度按美国国家癌症研究所AEs通用术语标准(CTCAE4.0版)进行分级,≥3级为重度AEs [12]。
1.1.5 排除标准 ①综述、评论、会议论文和生存质量研究;②无本研究纳入的任何一项结局指标的研究或无法获取全文的文献。
1.2 文献检索策略
计算机检索PubMed、Cochrane图书馆、Embase、中国知网、中国生物医学文献数据库、维普网和万方数据等。英文检索词为“NSCLC”“immunotherapy”“PD-1”“PD-l1”“CTLA-4”“immune checkpoint blockade”“pembrolizumab”“nivolumab”“atezolizumab”“durvalu- mab”“ipilimumab”“toripalimab”“camrelizumab”“cemiplimab”“sintilimab”“avelumab”“tremlimumab”;中文检索词为“非小细胞肺癌”“免疫疗法”“免疫检查点抑制剂”“帕博利珠单抗”“纳武单抗” “阿特珠单抗”“阿维单抗”“度伐利尤单抗”“伊匹木单抗”“特瑞普利单抗”“卡瑞利珠单抗”“西米普利单抗”“信迪利单抗”“西木单抗”。采用主题词与检索词相结合的方式检索,检索时限均为各数据库建库起至2020年10月。
1.3 文献筛选与数据提取
由2名研究者独立筛选文献并交叉核对,如遇分歧,双方进行协商并请求第3位研究者裁定。提取信息包括第一作者、发表年份、临床试验分期、患者例数、干预措施、ICIs类型、临床治疗线数和结局指标等。
1.4 文献质量评价
采用Cochrane系统评价员手册5.1.0推荐的偏倚风险评估工具对纳入文献质量进行评价。具体包括随机序列生成、分配隐藏、盲法、结果数据的完整性和其他偏倚来源。每项内容均分为高风险、不清楚和低风险[13]。
1.5 统计学方法
采用Rev Man 5.3和Stata 15.0软件进行Meta分析。计数资料以相对危险度(RR)及其95%置信区间(CI)表示。采用Q检验和I 2检验分析异质性。若各研究间无统计学异质性(I 2<50%,P>0.10),采用固定效应模型进行分析;反之,则采用随机效应模型进行分析。同一结局指标根据试验组是否联合常规化疗药物进行亚组分析。采用Stata 15.0软件进行敏感性分析;采用倒漏斗图和Eggers检验进行发表偏倚分析。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果与纳入研究基本信息
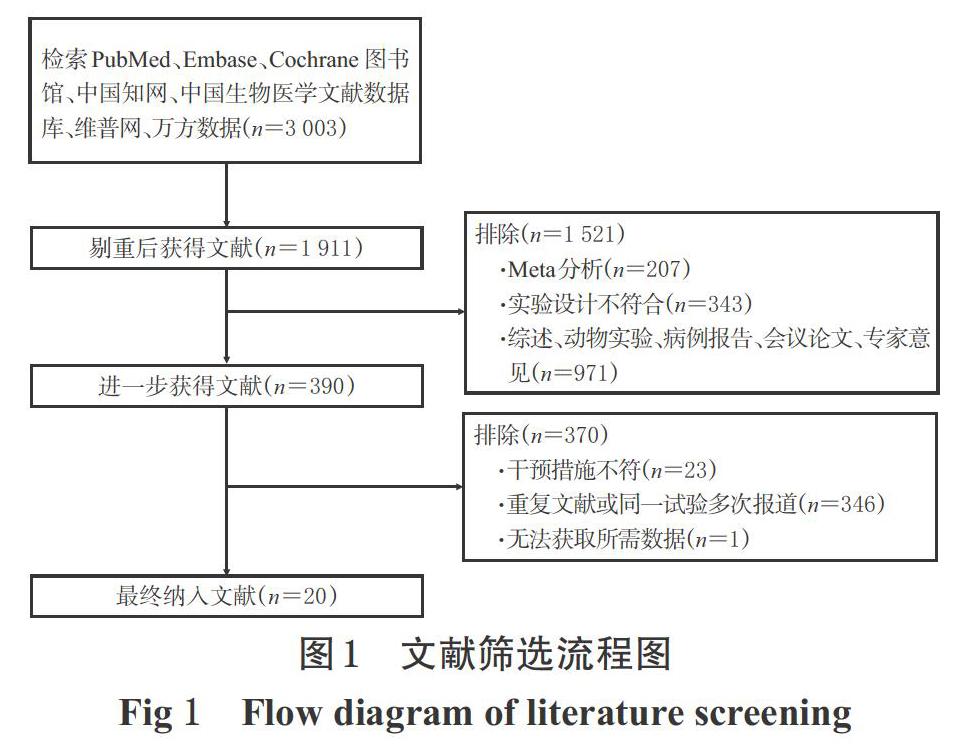
初检共获得相关文献3 003篇,按纳入与排除标准阅读题目、摘要和全文后,最终纳入20项研究[14-33],共计12 283例患者,其中对照组5 638例、试验组6 645例;文献筛选流程见图1,纳入研究基本信息见表1。
2.2 纳入研究质量评价结果
所有研究均为RCT[14-33]。19项研究描述了随机序列产生的方法和分配隐藏[14-27,29-33];14项研究结局数据完整[15-17,20-26,28-30,32];1项研究选择性报告结果[29];4项研究对研究者和受试者采用盲法[25-26,28,31];5项研究在结局评估时使用盲法[21,24-25,28,31];所有研究均不存在其他偏倚来源,详见图2、图3。
2.3 Meta分析结果
2.3.1 治疗相关AEs发生率 总体所有级别AEs发生率——20项研究报道了总体所有级别AEs发生率[14-33]。Meta分析结果显示,试验组患者的总体所有级别AEs发生率[RR=0.87,95%CI(0.80,0.94),P<0.001]显著低于对照组。总体重度AEs发生率——20项研究报道了总体重度AEs发生率[14-33]。Meta分析结果显示,试验组患者的总体重度AEs发生率[RR=0.60,95%CI(0.47,0.76),P<0.001]显著低于对照组。终止治疗发生率——17项研究报道了终止治疗发生率[14-29,31]。Meta分析结果显示,两组患者的终止治疗发生率比较,差异无统计学意义[RR=0.80,95%CI(0.55,1.17),P=0.25]。死亡發生率——20项研究报道了死亡发生率[14-33]。Meta分析结果显示,两组患者的死亡发生率比较,差异无统计学意义[RR=1.04,95%CI(0.80,1.35),P=0.78],详见表2。
亚组分析结果显示,试验组单用ICIs患者的总体所有级别和总体重度AEs发生率、终止治疗发生率、死亡发生率均显著低于对照组(P<0.001);而试验组使用ICIs+化疗患者的终止治疗发生率、死亡发生率均显著高于对照组(P<0.05),详见表3。
2.3.2 血液系统AEs发生率 贫血发生率——19项研究报道了所有级别和重度贫血发生率[14-18,20-33]。Meta分析结果显示,试验组患者的所有级别贫血发生率[RR=0.40,95%CI(0.29,0.56),P<0.001]、重度贫血发生率[RR=0.47,95%CI(0.31,0.74),P<0.001]均显著低于对照组。中性粒细胞减少症发生率——19项研究报道了所有级别和重度中性粒细胞减少症发生率[14-18,20-33]。Meta分析结果显示,试验组患者的所有级别中性粒细胞减少症发生率[RR=0.28,95%CI(0.18,0.44),P<0.001]、重度中性粒细胞减少症发生率[RR=0.50,95%CI(0.45,0.56),P<0.001]均显著低于对照组。血小板减少症发生率——12项研究报道了所有级别和重度血小板减少症发生率[18,20-21,24-28,30-33]。Meta分析结果显示,试验组患者的所有级别血小板减少症发生率[RR=0.83,95%CI(0.75,0.93),P<0.001]显著低于对照组,而两组患者的重度血小板减少症发生率比较差异无统计学意义[RR=0.91,95%CI(0.73,1.13),P=0.39],详见表4。
亚组分析结果显示,试验组单用ICIs患者的所有级别和重度贫血、中性粒细胞减少症、血小板减少症发生率均显著低于对照组(P<0.001),而试验组使用ICIs+化疗患者的上述指标与对照组比较差异均无统计学意义(P>0.05),详见表5。
2.3.3 临床相关症状发生率 恶心发生率——18项研究报道了所有级别和重度恶心发生率[14-18,20-21,23-33]。Meta分析结果显示,试验组患者的所有级别恶心发生率[RR=0.60,95%CI(0.44,0.82),P=0.001]显著低于对照组,而两组患者的重度恶心发生率比较差异无统计学意义[RR=0.85,95%CI(0.61,1.18),P=0.34]。呕吐发生率——17项研究报道了所有级别和重度呕吐发生率[14-16,18,20-21,23-33]。Meta分析结果显示,试验组患者的所有级别呕吐发生率[RR=0.64,95%CI(0.44,0.93),P=0.02]、重度呕吐发生率[RR=0.63,95%CI(0.43,0.94),P=0.02]均显著低于对照组。腹泻发生率——19项研究报道了所有级别和重度腹泻发生率[14-18,20-33]。Meta分析结果显示,两组患者的所有级别腹泻发生率[RR=0.99,95%CI(0.78,1.25),P=0.94]、重度腹泻发生率[RR=1.24,95%CI(0.82,1.89),P=0.31]比较差异均无统计学意义。脱发发生率——分别有15项[14-17,20-22,24-25,27-28,30-33]和14项[14-17,20-22,24-25,27-28,30,32-33]研究报道了所有级别和重度脱发发生率。Meta分析结果显示,试验组患者的所有级别脱发发生率[RR=0.50,95%CI(0.46,0.54),P<0.001]、重度脱发发生率[RR=0.16,95%CI(0.05,0.55),P=0.004]均显著低于对照组。周围神经病变发生率——10项研究报道了所有级别和重度周围神经病变发生率[14-16,20-21,25,28,30-31,33]。Meta分析结果显示,试验组患者的所有级别周围神经病变发生率[RR=0.48,95%CI(0.29,0.80),P=0.005]显著低于对照组,而两组患者的重度周围神经病变发生率比较差异无统计学意义[RR=0.68,95%CI(0.41,1.12),P=0.13],详见表6。
亚组分析结果显示,除重度腹泻外,试验组单用ICIs患者的所有级别和重度临床相关症状发生率均显著低于对照组(P<0.05);试验组使用ICIs+化疗患者的所有级别恶心、呕吐、腹泻、脱发和重度腹泻发生率均显著高于对照组(P<0.05),而该组其余临床相关症状发生率与对照组比较差异均无统计学意义(P>0.05),详见表7(表中,“-”表示报道重度脱发的6项研究中仅1项研究[25]详细记录了患者重度脱发的发生情况,故无异质性检验数据)。
2.4 敏感性分析
经亚组分析后,异质性检验结果显示,在单用ICIs亚组和使用ICIs+化疗亚组患者的总体所有级别AEs发生率方面,各研究间仍存在明显的异质性,故采用Stata 15.0软件中的“Metainf”命令,以总体所有级别AEs发生率为指标进行敏感性分析。结果发现,在单用ICIs亚组中,Mok等[20]和Rizvi等[24]的研究对异质性影响较大,去掉这两项研究后,各研究间的异质性改变较明显(P=0.45,I 2=0),试验组患者的总体所有级别AEs发生率与对照组比较仍有显著性差异[RR=0.78,95%CI(0.75,0.80),P<0.001];在使用ICIs+化疗亚组中,Govindan等[28]和Hellmann等[29] 的研究对异质性影响较大,去掉这两项研究后,各研究间的异质性改变较明显(P=0.35,I 2=10%),试验组患者的总体所有级别AEs发生率与对照组比较无显著性差异[RR=1.01,95%CI(0.99,1.03),P=0.32],详见图4。
2.5 发表偏倚分析
以总体所有级别AEs发生率为指标绘制倒漏斗图。结果显示,单用ICIs亚组和使用ICIs+化疗亚组vs.对照组的倒漏斗图两侧基本对称;Eggers检验结果显示,PICIs=0.808,PICIs+化疗=0.343,提示本研究存在发表偏倚的可能性较小,详见图5、图6。以其余指标进行的发表偏倚分析所得结果相似(图略)。
3 讨论
ICIs在用于治疗各种肿瘤的临床研究中表现出显著疗效,其主要通过阻断PD-1/PD-L1、CTLA-4信号通路来解除肿瘤细胞的免疫耐受状态,从而产生抗肿瘤活性[5]。随着PD-1(如纳武单抗和帕博利珠单抗)和PD-L1(如阿特珠单抗、度伐利尤单抗和阿维单抗)等多种ICIs被批准用于恶性肿瘤的治疗,使得患者的总生存期和无进展生存期得到极大改善[34]。其中,纳武单抗、帕博利珠单抗因用于NSCLC患者的疗效显著而被美国FDA批准用于以铂类为基础的一线化疗后效果不佳的晚期NSCLC患者[25-26,29]。虽然,ICIs的疗效显着,但其临床表现出的与治疗相关的AEs的风险仍不能忽视[35]。研究者在ICIs用于治疗NSCLC患者的临床研究中发现,除特殊的irAEs外,包括血液系统AEs(贫血、中性粒细胞减少症、血小板减少症)和临床相关症状(恶心、呕吐、腹泻、脱发、周围神经病变)在内的非irAEs也时有发生,且不同程度地影响患者预后[9,14,30]。有研究发现,单用ICIs患者的呕吐、腹泻等非irAEs发生率与常规化疗相当[14,21];但也有研究认为,非irAEs虽有发生,但其发生率低于常规化疗[15];当ICIs与常规化疗药物联合使用时,腹泻、周围神经病变等非irAEs发生率有所增加[25,32]。目前,现有研究对ICIs致非irAEs的结果不一致,而这些非irAEs与患者预后紧密相关,临床须予以重视。
本研究结果显示,试验组患者的总体所有级别和总体重度AEs发生率均显著低于对照组,而两组患者的终止治疗、死亡发生率比较差异均无统计学意义。亚组分析结果显示,试验组单用ICIs患者的总体所有级别和总体重度AEs、终止治疗、死亡发生率均显著低于对照组;试验组使用ICIs+化疗患者的总体所有级别和总体重度AEs发生率与对照组比较差异均无统计学意义,但终止治疗发生率、死亡发生率均显著高于对照组。这提示ICIs在单一疗法中的毒性较低,且联合化疗会增加终止治疗和死亡的发生风险。试验组患者所有级别和重度贫血、中性粒细胞减少症以及所有级别血小板减少症发生率均显著低于对照组。亚组分析结果显示,试验组单用ICIs患者的所有级别和重度贫血、中性粒细胞减少症、血小板减少症发生率均顯著低于对照组,而试验组使用ICIs+化疗患者的上述指标与对照组比较差异均无统计学意义。这提示ICIs对血液系统的毒性较低,且联合化疗不会增加血液系统AEs的发生风险。另外,试验组患者所有级别恶心和周围神经病变以及所有级别和重度呕吐、脱发发生率均显著低于对照组;而两组患者所有级别和重度腹泻发生率以及重度恶心、周围神经病发生率比较差异均无统计学意义。亚组分析结果显示,除重度腹泻外,试验组单用ICIs患者的所有级别和重度临床相关症状发生率均显著低于对照组;而试验组使用ICIs+化疗患者的所有级别恶心、呕吐、腹泻、脱发及重度腹泻的发生率显著高于对照组。这提示ICIs致所有级别和重度临床相关症状的风险较低,但联合化疗可增加所有级别恶心、呕吐、腹泻、脱发及重度腹泻的发生风险。既往研究发现,ICIs可增加患者结肠炎的发生风险,这可能是造成其使用ICIs联合化疗药物时腹泻发生率增加的原因[36]。虽然ICIs与各种自身免疫性神经毒性有关[37],但当前研究并没有证据表明接受ICIs联合化疗的患者的周围神经病变发生率会升高。敏感性分析支持上述结果;发表偏倚分析结果显示,本研究存在发表偏倚的可能性较小。
综上所述,对于NSCLC患者,ICIs在治疗相关AEs、血液系统毒性和临床相关症状方面的安全性优于常规化疗药物或安慰剂联合常规化疗药物,但当其联合常规化疗药物时,因AEs终止治疗和死亡的风险以及所有级别恶心、呕吐、腹泻、脱发及重度腹泻的风险将有所增加。本研究的局限性为:(1)仅检索了中英文数据库,一些相关的研究可能由于语言的限制而未被纳入;(2)为计算相关AEs发生率的RR值,本研究仅纳入了双臂RCT,部分单臂试验被排除,导致纳入研究有限、总体样本量相对较小;(3)由于部分研究的化疗方案、ICIs种类和治疗剂量不尽相同,以致部分指标在研究间的异质性较大,研究结果具有不确定性;(4)纳入研究未提供患者关于免疫治疗的详细信息,因此无法分析不同种族、民族或不同地区总体AEs和非irAEs的发生情况和风险是否相似;(5)一项涉及ICIs相关AEs的报告表明,与PD-1/PD-L1抑制剂相比,CTLA-4单药或联合化疗可能更易引发相关AEs[38]。由于CTLA-4的相关研究较少,本研究未对不同类别ICIs进行亚组分析。因此,本文结论尚有待更多大样本、多中心、高质量的RCT进一步证实。
参考文献
[ 1 ] BRAY F,FERLAY J,SOERJOMATARAM I,et al. Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2018,68(6):394-424.
[ 2 ] GRIDELLI C,ROSSI A,CARBONE D P,et al. Non-small- cell lung cancer[J]. Nat Rev Dis Primers,2015,1:15009- 15025.
[ 3 ] TRAVIS W D,BRAMBILLA E,RIELY G J. New pathologic classification of lung cancer:relevance for clinical practice and clinical trials[J]. J Clin Oncol,2013,31(8):992-1001.
[ 4 ] NG T L,LIU Y,DIMOU A,et al. Predictive value of oncogenic driver subtype,programmed death-1 ligand(PD-L1)score,and smoking status on the efficacy of PD-1/PD-L1 inhibitors in patients with oncogene-driven non-small cell lung cancer[J]. Cancer,2019,125(7):1038-1049.
[ 5 ] WU Z,MAN S,SUN R,et al. Recent advances and challenges of immune checkpoint inhibitors in immunotherapy of non-small cell lung cancer[J]. Int Immunopharmacol,2020,85:106613-106623.
[ 6 ] MA J,LI J,QIAN M,et al. PD-L1 expression and the prognostic significance in gastric cancer:a retrospective comparison of three PD-L1 antibody clones:SP142,28-8 and E1L3N[J]. Diagn Pathol,2018,13(1):91-101.
[ 7 ] LIM S M,HONG M H,KIM H R. Immunotherapy for non-small cell lung cancer:current landscape and future perspectives[J]. Immune Netw,2020,20(1):e10-e24.
[ 8 ] LUO W,WANG Z,TIAN P,et al. Safety and tolerability of PD-1/PD-L1 inhibitors in the treatment of non-small cell lung cancer:a meta-analysis of randomized controlled trials[J]. J Cancer Res Clin Oncol,2018,144(10):1851- 1859.
[ 9 ] ABDEL-RAHMAN O. Toxicity patterns associated with chemotherapy/immune checkpoint inhibitor combinations:a meta-analysis[J]. Immunotherapy,2019,11(6):543- 554.
[10] SUN X,ROUDI R,DAI T,et al. Immune-related adverse events associated with programmed cell death protein-1 and programmed cell death ligand 1 inhibitors for non- small cell lung cancer:a PRISMA systematic review and meta-analysis[J]. BMC Cancer,2019,19(1):558-571.
[11] 秦僑西,王稼劲,王红. ICIs治疗晚期非小细胞肺癌免疫相关不良事件的系统综述及Meta分析[J].中国肺癌杂志,2020,23(9):772-791.
[12] 皋文君,刘砚燕,袁长蓉.国际肿瘤化疗药物不良反应评价系统:通用不良反应术语标准4.0版[J].肿瘤,2012,32(2):142-144.
[13] 谷鸿秋,王杨,李卫. Cochrane偏倚风险评估工具在随机对照研究Meta分析中的应用[J].中国循环杂志,2014,29(2):147-148.
[14] RITTMEYER A,BARLESI F,WATERKAMP D,et al. Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer(OAK):a phase 3,open-label,multicentre randomised controlled trial[J]. Lancet,2017,389(10066):255-265.
[15] BRAHMER J,RECKAMP K L,BAAS P,et al. Nivolu- mab versus docetaxel in advanced squamous-cell non- small-cell lung cancer[J]. N Engl J Med,2015,373(2):123-135.
[16] BORGHAEI H,PAZ-ARES L,HORN L,et al. Nivolu- mab versus docetaxel in advanced nonsquamous non- small-cell lung cancer[J]. N Engl J Med,2015,373(17):1627- 1639.
[17] HERBST R S,GARON E B,KIM D W,et al. Long-term outcomes and retreatment among patients with previously treated,programmed death-ligand 1-positive,advanced non-small-cell lung cancer in the keynote-010 study[J]. J Clin Oncol,2020,38(14):1580-1590.
[18] RECK M,RODRIGUEZ-ABREU D,ROBINSON A G,et al. Pembrolizumab versus chemotherapy for PD-L1-po- sitive non-small-cell lung cancer[J]. N Engl J Med,2016,375(19):1823-1833.
[19] FEHRENBACHER L,SPIRA A,BALLINGER M,et al. Atezolizumab versus docetaxel for patients with previously treated non-small-cell lung cancer(POPLAR):a multicentre,open-label,phase 2 randomised controlled trial[J]. Lancet(London,England),2016,387(10030):1837- 1846.
[20] MOK T S K,WU Y L,KUDABA I,et al. Pembrolizumab versus chemotherapy for previously untreated,PD-L1-expressing,locally advanced or metastatic non-small-cell lung cancer(KEYNOTE-042):a randomised,open-label,controlled,phase 3 trial[J]. Lancet(London,England),2019,393(10183):1819-1830.
[21] CARBONE D P,RECK M,PAZ-ARES L,et al. First-line nivolumab in stage Ⅳ or recurrent non-small-cell lung cancer[J]. N Engl J Med,2017,376(25):2415-2426.
[22] WU Y L,LU S,CHENG Y,et al. Nivolumab versus docetaxel in a predominantly chinese patient population with previously treated advanced nsclc:checkmate 078 randomized phase Ⅲ clinical trial[J]. J Thorac Oncol,2019,14(5):867-875.
[23] HELLMANN M D,CIULEANU T E,PLUZANSKI A,et al. Nivolumab plus ipilimumab in lung cancer with a high tumor mutational burden[J]. N Engl J Med,2018,378(22):2093-2104.
[24] RIZVI N A,CHO B C,REINMUTH N,et al. Durvalumab with or without tremelimumab vs standard chemotherapy in first-line treatment of metastatic non-small cell lung cancer:the mystic phase 3 randomized clinical trial[J]. JAMA Oncology,2020,6(5):661-674.
[25] PAZ-ARES L,VICENTE D,TAFRESHI A,et al. A randomized,placebo-controlled trial of pembrolizumab plus chemotherapy in patients with metastatic squamous non- small-cell lung cancer:protocol-specified final analysis of keynote-407[J]. J Thorac Oncol,2020,15(10):1657- 1669.
[26] GANDHI L,RODR?GUEZ-ABREU D,GADGEEL S,et al. Pembrolizumab plus chemotherapy in metastatic non- small-cell lung cancer[J]. N Engl J Med,2018,378(22):2078-2092.
[27] LANGER C J,GADGEEL S M,BORGHAEI H,et al. Carboplatin and pemetrexed with or without pembrolizu- mab for advanced,non-squamous non-small-cell lung cancer:a randomised,phase 2 cohort of the open-label keynote-021 study[J]. Lancet Oncol,2016,17(11):1497- 1508.
[28] GOVINDAN R,SZCZESNA A,AHN M J,et al. Phase Ⅲtrial of ipilimumab combined with paclitaxel and carboplatin in advanced squamous non-small-cell lung cancer[J]. J Clin Oncol,2017,35(30):3449-3457.
[29] HELLMANN M D,PAZ-ARES L,BERNABE CARO R,et al. Nivolumab plus ipilimumab in advanced non-small- cell lung cancer[J]. N Engl J Med,2019,381(21):2020- 2031.
[30] SOCINSKI M A,JOTTE R M,CAPPUZZO F,et al. Atezolizumab for first-line treatment of metastatic nonsquamous NSCLC[J]. N Engl J Med,2018,378(24):2288-2301.
[31] LYNCH T J,BONDARENKO I,LUFT A,et al. Ipilimu- mab in combination with paclitaxel and carboplatin as first-line treatment in stage ⅢB/Ⅳ non-small-cell lung cancer:results from a randomized,double-blind,multicenter phase Ⅱ study[J]. J Clin Oncol,2012,30(17):2046-2054.
[32] WEST H,MCCLEOD M,HUSSEIN M,et al. Atezolizu- mab in combination with carboplatin plus nab-paclitaxel chemotherapy compared with chemotherapy alone as first-line treatment for metastatic non-squamous non- small-cell lung cancer(IMpower130):a multicentre,randomised,open-label,phase 3 trial[J]. Lancet Oncol,2019,20(7):924-937.
[33] JOTTE R,CAPPUZZO F,VYNNYCHENKO I,et al. Atezolizumab in combination with carboplatin and nab-paclitaxel in advanced squamous NSCLC(IMpower131):results from a randomized phase Ⅲ trial[J]. J Thorac Oncol,2020,15(8):1351-1360.
[34] GONG J,CHEHRAZI-RAFFLE A,REDDI S,et al. Development of PD-1 and PD-L1 inhibitors as a form of cancer immunotherapy:a comprehensive review of registration trials and future considerations[J]. J Immunother Cancer,2018,6(1):8-26.
[35] SAIGI M,ALBURQUERQUE-BEJAR J J,SANCHEZ- CESPEDES M. Determinants of immunological evasion and immunocheckpoint inhibition response in non-small cell lung cancer:the genetic front[J]. Oncogene,2019,38(31):5921-5932.
[36] LIN L L,LIN G F,LUO Q,et al. The incidence and relative risk of PD-1/PD-L1 inhibitors-related colitis in non- small cell lung cancer:a meta-analysis of randomized controlled trials[J]. Int Immunopharmacol,2019,77:105975.
[37] ELTOBGY M,OWEIRA H,PETRAUSCH U,et al. Immune-related neurological toxicities among solid tumor patients treated with immune checkpoint inhibitors:a systematic review[J]. Expert Rev Neurother,2017,17(7):725-736.
[38] WANG D Y,SALEM J E,COHEN J V,et al. Fatal toxic effects associated with immune checkpoint inhibitors:a systematic review and meta-analysis[J]. JAMA Oncol,2018,4(12):1721-1728.
(收稿日期:2021-01-27 修回日期:2021-05-05)
(編辑:陈 宏)

