止痒搽剂质量控制标准的方法研究
叶吉明,杨景然,刘 宇,陈米林,冉忠梅*,周培德,柏永强
(1.云南省第一人民医院 药学部 ,云南 昆明650032;2.宁波工程学院 理学院,浙江 宁波315211;3.昆明赛诺制药股份有限公司 质量部,云南 昆明650051)
止痒搽剂是某医院皮肤科的外用经验方,临床上已使用多年.其主要由薄荷脑、麝香草酚、甘油,溶于75%乙醇制成.该搽剂具有清凉止痒作用,主要用于治疗蚊虫叮咬及瘙痒性皮肤病患者.作为医院的传统制剂,其具有疗效确切、价廉物美的优势.但对其质量标准的鉴定仍停留在对薄荷脑、麝香草酚等使用化学显色法所做的定性鉴别上,导致质量控制环节相对单一,不能对制剂质量进行全面有效管理和控制.目前,对薄荷脑、麝香草酚和乙醇等的相关测定报道[1-6]很多,但作为复方制剂协同处方,应该从止痒搽剂制剂自身入手,对制剂中的关键药物成分进行分析和评价,而非仅对单一成分进行监测.为此,采用毛细管气相色谱法对止痒搽剂进行系统稳定性考察,以期为止痒搽剂的质量控制、安全性和有效性提供科学依据.
1 仪器与方法
1.1 仪器与试剂
GC-2010气相色谱仪、FID检测器、氢气发生器、AO-20i自动进样器(均为日本岛津有限公司);CA-2空气发生器(武汉科林普丰仪器有限公司);CPA225D型电子天平(赛多利斯);高纯氮气(昆明广瑞达特种气体有限责任公司,9.999%).
薄荷脑对照品(中国食品药品检定研究院,批号:100508-201603);麝香草酚对照品(中国食品药品检定研究院,批号:110728-201707);止痒搽剂(云南省第一人民医院制剂,批号:20181217;20181218;20181219.规格:100 mL/瓶,含麝香草酚、薄荷脑各 1 g).
萘、乙醇、无水乙醇(均为分析纯,天津市风船化学试剂有限公司);正丙醇(分析纯,汕头市西陇化工厂有限公司,批号:0805312);甘油(药用辅料,江西益普生药业有限公司,批号:20181201);其他试剂为分析纯;水为纯化水.
1.2 方法
1.2.1 制剂样品的色谱条件
色谱柱:6%氰丙基苯基-94%二甲基聚硅氧烷为固定液的毛细管柱,以聚乙二醇2000(或极性相近)为固定液.起始温度为 130 ℃,维持 8 min,再以 50 ℃/min 的速率升温至 200 ℃,维持 6 min.进样口温度 250 ℃,检测器温度 250 ℃,不分流进样,载气为氮气,流速 3.0 mL/min,进样体积 1 μL,按内标法以峰面积计算.
1.2.2 溶液的制备
1)内标溶液制备:取萘适量,精密称定,加无水乙醇溶解并定量稀释制成每 1 mL 中含 0.4 mg 的溶液,作为内标溶液.
2)对照品溶液制备:精密称定薄荷脑对照品 20 mg ,置于 50 mL 容量瓶中,然后加无水乙醇稀释至刻度,制成每 1 mL 含 0.4 mg 的溶液;精密称定麝香草酚对照品 20 mg,置于 50 mL 容量瓶中,加无水乙醇稀释至刻度,制成每 1 mL 含 0.4 mg 的溶液;取甘油 25 mg,精密量取,置 50 mL 量瓶中,然后用无水乙醇稀释至刻度,制成每 1 mL 中含甘油 0.5 mg 的溶液;精密吸取薄荷脑对照品溶液、麝香草酚对照品溶液、甘油溶液和内标溶液各 5 mL ,置于 25 mL 容量瓶中,加无水乙醇稀释至刻度,作为混合对照品溶液.
3)供试品溶液制备:精密吸取止痒搽剂(规格:100 mL/瓶,批号:20181217;20181218;20181219)2 mL,置于 50 mL 容量瓶中,再用无水乙醇稀释至刻度,摇匀.精密量取上述溶液 5 mL,置于 25 mL 容量瓶中,再加入内标溶液 5 mL 后,加无水乙醇稀释至刻度,摇匀作为供试品溶液.
4)阴性样品溶液制备:麝香草酚阴性样品溶液制备.取薄荷脑 1 g、甘油 6 g,加75%乙醇溶解并稀释至刻度,摇匀,制成 100 mL 溶液.精密吸取上述溶液 2 mL 置 50 mL 容量瓶中,加无水乙醇稀释至刻度,摇匀,制成麝香草酚阴性样品溶液.
薄荷脑阴性样品溶液制备:取麝香草酚 1 g、甘油 6 g,加75%乙醇溶解并稀释至刻度,摇匀,制成 100 mL 溶液.精密吸取上述溶液 2 mL 置 50 mL 容量瓶中,加无水乙醇稀释至刻度,摇匀,制成薄荷脑阴性样品溶液.
甘油样品溶液制备:取甘油 6 g ,加75%乙醇溶解并稀释至刻度,摇匀,制成 100 mL 甘油样品溶液.
1.2.3 测定乙醇的色谱条件
6%氰丙基苯基-94%二甲基聚硅氧烷为固定液的毛细管柱.起始温度为40 ℃,维持 2 min,以 3 ℃/min 的速率升至 65 ℃,再以 25 ℃/min 的速率升温至 200 ℃ ,维持 10 min;进样口温度 200 ℃,分流比为1∶1;检测器(FID)温度 220 ℃;载气为氮气,流速 3.0 mL/min;顶空进样,进样体积 1 μL,平衡温度 85 ℃,平衡时间 20 min.
2 试验结果
2.1 系统适用性试验
按1.2.2项下方法配制各溶液,按1.2.1项下色谱条件进样分析,记录色谱图,见图1~图9.结果表明,麝香草酚对照品溶液、薄荷脑对照品溶液、甘油样品溶液、内标溶液、供试品溶液(无内标)、供试品溶液(有内标)、麝香草酚阴性样品溶液和薄荷脑阴性样品溶液各峰形良好,分离度大于1.5,理论塔板数按薄荷脑、麝香草酚峰计算不低于 1 500.
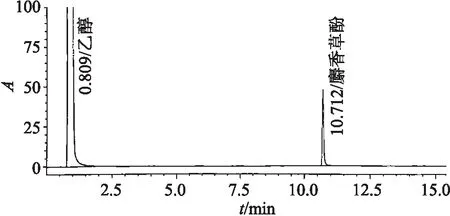
图1 麝香草酚对照品溶液色谱图

图2 薄荷脑对照品溶液色谱图
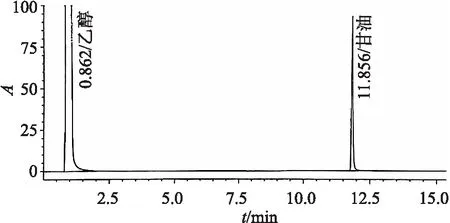
图3 甘油样品溶液色谱图

图4 内标溶液色谱图

图5 供试品溶液(无内标)色谱图
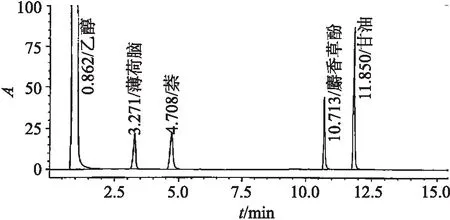
图6 供试品溶液(有内标)色谱图
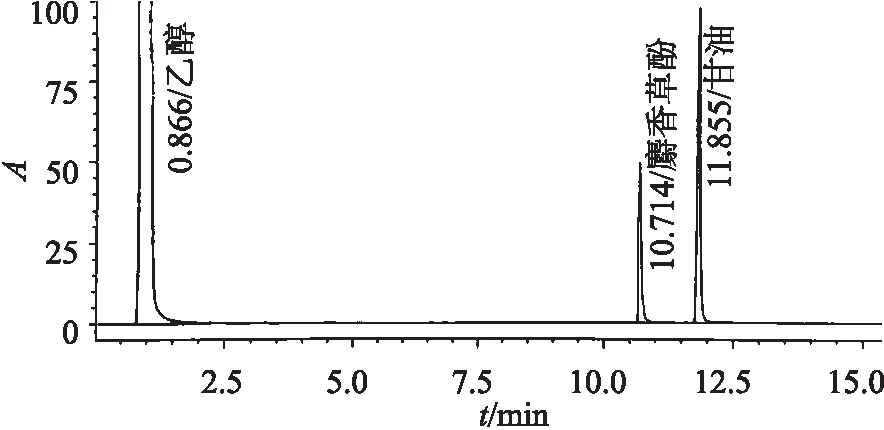
图7 麝香草酚阴性样品溶液色谱图

图8 薄荷脑阴性样品溶液色谱图

图9 混合对照品溶液色谱图
2.2 标准曲线的绘制
分别精密吸取薄荷脑、麝香草酚对照品溶液(0.4 mg/mL)1,2,5,8,10 mL 置 25 mL 量瓶中,加内标溶液 5 mL,加无水乙醇定容至每 1 mL 含薄荷脑、麝香草酚0.016,0.032,0.080,0.129,0.162 mg 的溶液.精密吸取上述溶液各 1 μL,按1.2.1项下色谱条件进样分析,以峰面积(Y)为纵坐标,质量浓度(X)为横坐标,进行线性回归计算,得到薄荷脑和麝香草酚回归方程分别为:Y=10.855X-0.021 4,R2=0.999 5;Y=12.304X-0.032 4,R2=0.999 4.
结果表明,薄荷脑、麝香草酚质量浓度在0.016~0.161 mg/mL 内与峰面积呈良好线性关系.
2.3 精密度试验
取对照品溶液1 μL,在上述色谱条件下,重复进样5次,记录峰面积,计算得到麝香草酚、薄荷脑峰面积的RSD分别为0.33%和0.16%.
2.4 重复性考察
取批号为20181217制剂样品,重复进样6次,记录峰面积,计算得到麝香草酚、薄荷脑峰面积的RSD分别为0.80%和0.21%.
2.5 稳定性考察
取供试品溶液(批号:20181217)于室温下存放,分别于0,2,4,6,24 h 进行测定,得到麝香草酚、薄荷脑峰面积的RSD分别1.14%和0.40%.
2.6 加样回收试验
2.6.1 麝香草酚加样回收试验
精密吸取按1.2.2项下方法制备的麝香草酚阴性样品溶液 5 mL,置 25 mL 量瓶中,共6份,分别精密加入4,5,6 mL 麝香草酚对照品溶液和 5 mL 内标溶液,用无水乙醇稀释至刻度,摇匀.精密吸取上述溶液各 1 μL,按1.2.1项下色谱条件进样分析,结果见表1.
2.6.2 薄荷脑加样回收试验
精密吸取按1.2.2项下方法制备的薄荷脑阴性样品溶液 5 mL,置 25 mL 量瓶中,共6份,分别精密加入4,5,6 mL 薄荷脑对照品溶液和 5 mL 内标溶液,用无水乙醇稀释至刻度.精密吸取上述溶液各 1 μL,按1.2.1项下色谱条件进样分析,结果见表2.

表1 麝香草酚加样回收试验结果

表2 薄荷脑加样回收试验结果
2.7 样品质量分数测定及限度确定
取止痒搽剂(规格:100 mL/瓶,批号:20181217;20181218;20181219),按1.2.2项下方法配制溶液,按1.2.1项下色谱条件进样分析,其质量分数测定结果见表3、表4.
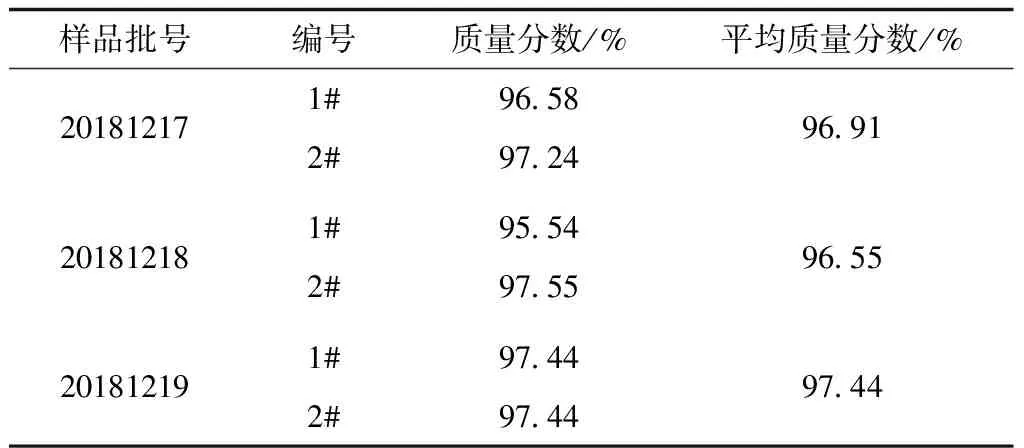
表3 3批止痒搽剂中薄荷脑的质量分数测定
2.8 校正因子测定
准确量取恒温至 20 ℃ 的无水乙醇 5 mL ,2份平行.置于 100 mL 量瓶中,准确加入恒温至 20 ℃ 的正丙醇(内标物质)5 mL,加水稀释至刻度,摇匀,精密吸取该溶液 1 mL,并置于 100 mL 量瓶中,用水稀释至刻度,摇匀,作为对照品溶液.准确吸取上述溶液 3 mL,置于 10 mL 顶空进样瓶中,密封,按1.2.3项下测定乙醇的色谱条件,进样分析,每份对照品溶液各进样3次,测定其峰面积,并计算平均校正因子.由计算结果可知,校正因子相对标准偏差为1.3%.
2.9 乙醇体积分数测定
精密吸取恒温至 20 ℃ 的供试品适量(相当于乙醇 5 mL),置于 100 mL 量瓶中,准确加入恒温至 20 ℃ 的正丙醇 5 mL,加水稀释至刻度,摇匀,准确吸取该溶液 1 mL,置于 100 mL 量瓶中,加水稀释至刻度,摇匀,作为供试品溶液.精密吸取上述溶液 3 mL,置 10 mL 顶空进样瓶中,密封,按1.2.3项下测定乙醇的色谱条件,进样分析,测定峰面积,按内标法以峰面积计算,结果见表5.
3 小结
本研究表明,采用毛细管气相色谱法能够同时测定薄荷脑、麝香草酚、甘油和乙醇的含量,且方法简便、准确,精密度好、准确度高,具有专属性和耐用性.此外,无论是理论塔板数还是分离度对薄荷脑、麝香草酚的分离能力都较为适合,且分析时间短,能够快速准确地进行定性和定量分析,有利于制剂质量的控制.
医院制剂有着强烈的“地方特色”,其作为医院使用多年的协定处方,具有临床疗效确定、价格便宜等优势.目前,由于医院制剂大多为品种多、数量少、周期短,为避免在制剂制备过程中出现“短板”,应该对制剂质量标准、工艺、生产和使用等过程进行严格管控,以保证其临床疗效和安全[7].而在现行制剂质量标准中,对质量的控制方法简单、粗糙,长久以往,将大大影响临床疗效和制剂的发展.因此,对制剂质量标准进行提升,进一步保障患者安全用药[8]是当务之急和必然趋势.

