2型糖尿病合并桥本甲状腺炎患者血清25(OH)D浓度变化及与临床指标的相关性研究
任 旋 武宏霞 张 涛
维生素D(vitamin D,Vit D)是一种脂溶性类固醇的衍生物,主要生理作用是调节钙磷平衡和骨骼代谢,此外,在自身免疫性疾病、代谢综合征、癌症、感染以及全因死亡等方面也发挥着重要作用[1]。25-羟维生素D [25 (OH) D]是其主要的循环形式,在血液中稳定存在。Vit D缺乏已经成为一个全球性的公共卫生问题,目前全球Vit D缺乏或不足的发生率已超过十亿[2]。桥本甲状腺炎(HT)是内分泌最常见的器官特异性自身免疫性疾病,Vit D作为一种免疫调节剂,被广泛证明参与了疾病的发生和发展[3]。2型糖尿病(T2DM)作为我国内分泌第一大疾病,研究表明,T2DM患者具有更高的自身免疫性甲状腺疾病的罹患率,以桥本甲状腺炎导致的甲状腺功能减退症为主要表现,进而增加了心脑血管并发症的风险[4]。血清低Vit D水平已成为2型糖尿病可能的危险因素。在T2DM的背景下,Vit D和甲状腺自身免疫的相互作用及因果关系仍存在争议。本研究旨在探讨T2DM合并TH患者中血清25(OH)D浓度变化及其与甲状腺功能、临床指标的相关性,为Vit D补充剂作为一种潜在的降低T2DM患者自身免疫性甲状腺疾病的干预措施提供理论依据。
资料与方法
1.研究对象:按照WHO(1999年)制定的糖尿病诊断标准及分类,选择2019年1月~2020年12月于兰州大学第二医院内分泌科住院的T2DM患者142例。依据甲状腺功能检测结果,分为甲状腺功能正常的2型糖尿病组80例,简称T2DM组,2型糖尿病合并桥本甲状腺炎组62例,简称T2DM+HT组。HT诊断符合2008年《中国甲状腺疾病诊治指南》。排除标准:①酮症酸中毒、高渗性昏迷等糖尿病急性并发症;②既往甲状腺手术史;③甲状旁腺疾病史;④糖皮质激素、磷酸盐、雌激素等影响血钙、磷代谢、Vit D水平的药物史;⑤全身性自身免疫性疾病及严重感染;⑥严重肝、肾功能不全。
2.临床资料:收集142例患者的性别、年龄、糖尿病病程、体重指数(BMI)、空腹血糖(FPG)、糖化血红蛋白(HbA1c)、血钙(Ca)、血磷(P)、血清碱性磷酸酶(ALP)、甲状旁腺激素(PTH)、25(OH)D、促甲状腺激素(TSH)、游离三碘甲状腺原氨酸(FT3)、游离甲状腺素(FT4)、甲状腺球蛋白抗体(ATG-Ab)和甲状腺过氧化物酶抗体(TPO-Ab)。维生素D状态评定标准:25(OH)D≥30ng/ml为充足;20ng/ml≤25(OH)D<30ng/ml为不足;25(OH)D<20ng/ml为缺乏。
结 果
1.临床指标比较:与T2DM组比较,T2DM+TH组患者的病程、TSH、ATG-Ab、TPO-Ab均升高,25(OH)D、FT3、FT4水平下降,差异有统计学意义(P<0.05)。两组年龄、性别、BMI、HbA1c、Ca、P、PTH、ALP比较,差异无统计学意义(P>0.05,表1)。
表1 两组研究对象一般临床指标比较
2.两组患者维生素25(OH)D营养状态比较:T2DM组Vit D不足的发生率为35.0%,缺乏的发生率为60.0%,Vit D充足的发生率仅为5.0%。T2DM+TH组,Vit D不足的发生率19.4%,缺乏的发生率高达77.4%,Vit D充足的发生率仅占3.2%。与T2DM组比较,T2DM+TH组的Vit D不足发生率下降,缺乏发生率明显上升,差异均有统计学意义(P<0.05)。两组Vit D充足发生率比较,差异无统计学意义(P>0.05,表2)。

表2 两组研究对象25(OH)D营养状态比较[n(%)]
3.T2DM+TH组不同25(OH)D代谢状态下甲状腺功能的比较:根据25(OH)D 浓度,将T2DM+TH组患者分为Vit D缺乏组和Vit D不足组,分析不同25(OH)D代谢状态下甲状腺功能的差异。与Vit D不足组比较,Vit D缺乏组患者的TSH、TPO-Ab水平明显升高,差异均有统计学意义(P<0.05,表3)。
表3 T2DM+TH组不同25(OH)D水平甲状腺指标的比较
4.T2DM+TH组25(OH)D水平与临床指标相关性分析:T2DM+TH组的血清25(OH)D水平与病程、TSH、TPO-Ab之间呈负相关(P<0.05)。25(OH)D与HbA1c、FT3、FT4、ATG-Ab之间无相关性(P>0.05,表4)。
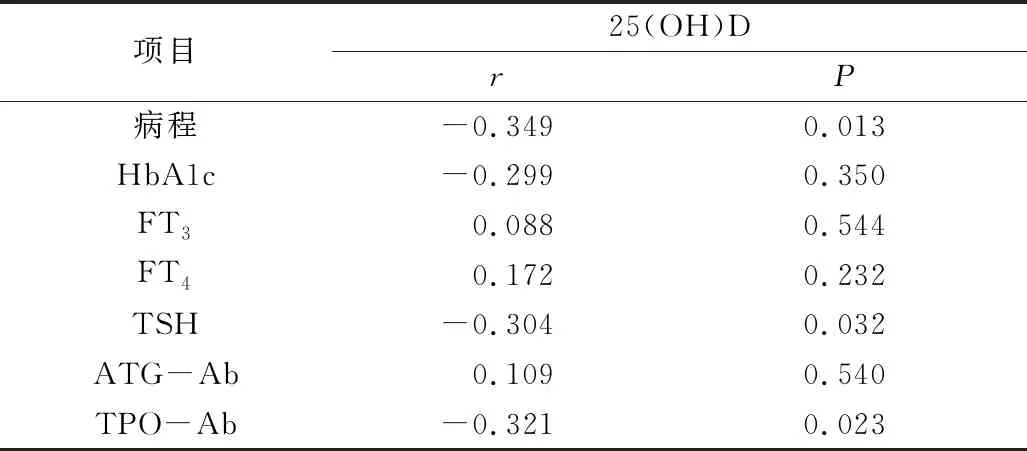
表4 T2DM+TH组25(OH)D与临床指标相关性分析
讨 论
T2DM和自身免疫性甲状腺疾病(AITD)是两种最常见的慢性内分泌疾病,研究已证实甲状腺功能异常与糖尿病密切相关,糖尿病患者甲状腺疾病发生率明显增加,并且相互影响,对心脑血管及并发症的发生、发展产生了有害影响[5]。继发于2型糖尿病的Vit D缺乏和糖尿病背景下甲状腺自身免疫的相互作用被认为是甲状腺功能异常发生率增加的重要因素。我国人群普遍存在25(OH)D不足或缺乏,整体发生率高达90%以上[6]。这种现象在T2DM患者中更加突出,认为与胰岛素抵抗、血糖控制不佳、血脂代谢紊乱等相关。同时口服降糖药和饮食限制也会影响糖尿病患者的Vit D水平。合并出现的甲状腺功能障碍将进一步影响Vit D的摄入和代谢。25(OH)D在2型糖尿病患者自身免疫性甲状腺疾病中是因、是果,还是恶性循环,机制仍然不明确。特别对T2DM合并TH患者的血清Vit D水平变化及与甲状腺功能指标的相关性少有研究。
本研究中单纯T2DM患者25(OH)D不足或缺乏的比例达到了95.0%,而合并TH的T2DM患者该比例更是高达96.8%,两组患者25(OH)D充足的比例仅为5.0%和3.2%。与此同时,比较两组患者25(OH)D营养状态发现,T2DM+TH组患者的 25(OH)D缺乏更加显著,达77.4%,而不足比例仅为19.4%,差异有统计学意义。结合两组患者血清25(OH)D浓度水平(分别为15.75±5.850和13.49±4.318),提示合并TH的T2DM患者25(OH)D水平明显下降,缺乏症的发生率更高,这与Wang等[7]的研究结果一致,Vit D的缺乏可能参与了自身免疫性甲状腺炎的发病。
Vit D与AITD自身免疫发病的相关研究已得到越来越多横断面研究的支持。25(OH)D缺乏被认为与更高的AITD发生率(主要是HT)相关[1]。25(OH)D的水平每升高4ng/ml,总体上观察到的AITD风险将降低[8]。有研究显示HT组患者的25(OH)D水平明显下降,甲状腺功能减退症患者的Vit D缺乏症发生率高于正常人群[9]。根据25(OH)D水平,笔者将T2DM+TH组分为不足和缺乏组,比较两组之间的甲状腺功能,结果显示,25(OH)D缺乏组的TSH和TPO-Ab的水平明显高于不足组,差异有统计学意义。T2DM+TH组的相关性分析结果也表现出25(OH)D水平与血清TSH值及TPO-Ab浓度呈负相关。这与Giovinazzo等[10]的研究结果一致。不同的研究者在不同人群中的研究也证实了较低水平的25(OH)D与HT风险之间的相关性,认为HT组患者的25(OH)D水平随着TSH的升高而下降,甲状腺功能减退患者的缺乏症发生率显著升高,但与抗体效价的关系存在更多不一致的数据[11,12]。Ke等[13]研究发现HT组25(OH)D水平与抗体效价无相关性。一项基于我国人群的研究数据也支持25(OH)D水平与TPO-Ab和ATG-Ab水平之间无相关性[14]。
Vit D参与AITD自身免疫发病的机制目前尚不明确。无论是垂体水平还是甲状腺水平,Vit D对下丘脑-垂体-甲状腺轴的调节作用已经被提出[15]。25(OH)D是Vit D在体内最主要的循环形式,由维生素D在肝脏中羟基化而产生,在肾脏中进一步羟基化为1,25-二羟基维生素D [1,25(OH)2D],成为具有生物活性的Vit D激素,通过与其受体(VDR)结合发挥生物学效应。VDR和甲状腺激素之间具有强分子同源性,几乎存在于机体的任何组织,VDR基因多态性与AITD的发病相关[2]。另外,维生素D作为一种新的免疫调节剂,促进了Th1向Th2的转化,限制了细胞免疫反应引起的损伤。同时抑制Th17细胞的增殖,减少CD8+T细胞产生的细胞因子,进而抑制了免疫细胞的分化和免疫球蛋白的产生[16]。总之,Vit D的水平、VDR的多态性以及控制其代谢的酶可能都会影响其调节能力,这种贡献的大小取决于多种其他因素,如年龄、性别、性激素等。而AITD的遗传易感性以及其他内源性和环境因素也可能影响两者的相关性,从而解释了在不同人群中获得的结果存在不一致之处。因此,Vit D在AITD,尤其是TH的发病中可能起很重要的作用[17]。
T2DM患者作为25(OH)D不足或缺乏的高危人群,有着高于正常人的AITD的发生率,Vit D水平影响着甲状腺功能的改变,甲状腺功能障碍进一步加剧了Vit D水平的下降,这种恶性循环加重了这一缺陷。笔者的相关性分析发现,25(OH)D水平与糖尿病病程呈现弱的负相关,与HbA1c无相关性,这与Alaidarous等[18]的结论相同。T2DM的持续时间为Vit D缺乏的独立预测因子,而与血糖控制之间无相关性。研究表明,当25(OH)D≥50ng/ml时,可使甲状腺功能减退症的风险降低30%,升高的抗体效价降低32%[19]。T2DM的持续时间无法干预,基于更低的25(OH)D水平,补充Vit D在AITD的预防和治疗中具有更直接的影响。Wang等[20]研究发现≥6个月的Vit D补充治疗,显著降低了TPO-Ab的水平,甲状腺功能得到改善。但是,目前仍缺乏足够的数据来确定获得超生理水平的25(OH)D水平带来的益处和损害,甚至可能与骨折和死亡风险的增加相关。
综上所述,T2DM合并TH患者的25(OH)D水平明显低于T2DM组,主要表现为缺乏,并且高浓度的TSH及TPO-Ab,具有更低的25(OH)D水平。25(OH)D与T2DM持续时间,TSH、TPO-Ab浓度呈现弱的负相关。更低水平的25(OH)D是导致T2DM患者发生TH的病因,还是合并TH导致的后果,在学术界仍存在争议。Vit D补充治疗仍需要开展更多个体、更大范围的研究,提供Vit D作为AITD预防、治疗工具功效和安全性的见解。

