早产儿呼吸窘迫综合征围产期危险因素分析
王 敏,李管明,孙 倩,姜春明,房晓祎
(1.中山大学附属第七医院新生儿科,广东 深圳 518107;2.哈尔滨医科大学附属第一医院新生儿科,黑龙江 哈尔滨 150070)
随着新生儿重症监护病房医护质量、救治水平的不断提高、医疗环境的逐步优化,我国早产儿的发生率早已由过去的约5%上升至10%左右[1]。早产儿呼吸窘迫综合征(respiratory distress syndrome,RDS)的发病率15%~16%[2],主要是由于肺表面活性物质合成不足或结构不成熟,以出生后数小时内出现的进行性呼吸困难为主要临床特征,是引起早产儿死亡及各种并发症的最常见原因之一[3]。随着人工合成及天然制剂的肺表面活性物质的广泛使用,RDS的救治成功率明显提高,但肺表面活性物质制剂价格昂贵,插管又带来感染、气压伤等并发症,故预防早产儿RDS仍旧是国内外新生儿学者的关注焦点。本研究收集新生儿重症监护病房的RDS早产儿的相关临床资料进行回顾性分析,探讨早产儿发生RDS的主要危险因素,以便早期干预,改善预后。
1 资料与方法
1.1 一般资料
收集2012年1月—2015年12月哈尔滨医科大学附属第一医院新生儿重症监护病房871例早产儿的临床资料,其中符合RDS诊断标准[4]511例,为RDS组,均为本院分娩、出生后6 h内入住新生儿重症监护病房,其中男性305例,女性206例,平均胎龄(31.36±2.44)周,平均体重(1 731.36±592.76)g,剖宫产271例,自然分娩240例,产前使用糖皮质激素共393例;同期住院的早产非RDS患儿360例,为非RDS组,男性214例,女性146例,平均胎龄(34.25±1.69)周,平均体重(2 289.46±552.40)g,剖宫产249例,自然分娩111例。
1.2 方法
1.2.1 观察指标(1)一般情况:性别、胎龄、出生体重等。(2)围产期因素:胎产次、是否多胎妊娠、分娩方式、父亲年龄、母亲年龄、胎膜早破、妊娠期糖尿病、妊娠期高血压、羊水异常、窒息、宫内窘迫、1 min Apgar评分、产前糖皮质激素的应用情况等。(3)并发症:气胸、新生儿肺炎、颅内出血、肺动脉高压、肺出血、败血症、支气管肺发育不良和真菌感染。(4)出生头围、身长等体格发育及5 min经皮动脉血氧饱和度情况。
1.2.2 分组情况根据患儿是否存在RDS分为RDS组(511例)和非RDS组(360例);根据胎龄分为超早产儿(胎龄<28周)27例,极早产儿(胎龄28~31+6周)[5]234例,中期早产儿(胎龄32~33+6周)145例,晚期早产儿(胎龄34~36+6周)[6]105例。根据患儿母亲产前是否应用糖皮质激素分为产前应用激素组(74例)和产前无应用激素组(22例)。
1.3 统计学方法
应用SPSS 17.0统计软件进行分析。正态分布的计量资料以xˉ±s表示,两组间比较采用独立样本t检验;多组间比较采用单因素方差分析。计数资料以百分率表示,组间比较用χ2检验或Fisher确切概率法检验。采用多因素Logistic回归分析筛选早产儿发生RDS的危险因素。以P<0.05为差异有统计学意义。
2 结果
2.1 早产儿RDS危险因素分析
2.1.1 早产儿发生RDS单因素分析RDS早产儿较非RDS早产儿的胎龄小、母亲年龄大,窒息、宫内窘迫、产前未应用糖皮质激素、顺产、羊水污染的发生率高,见表1。
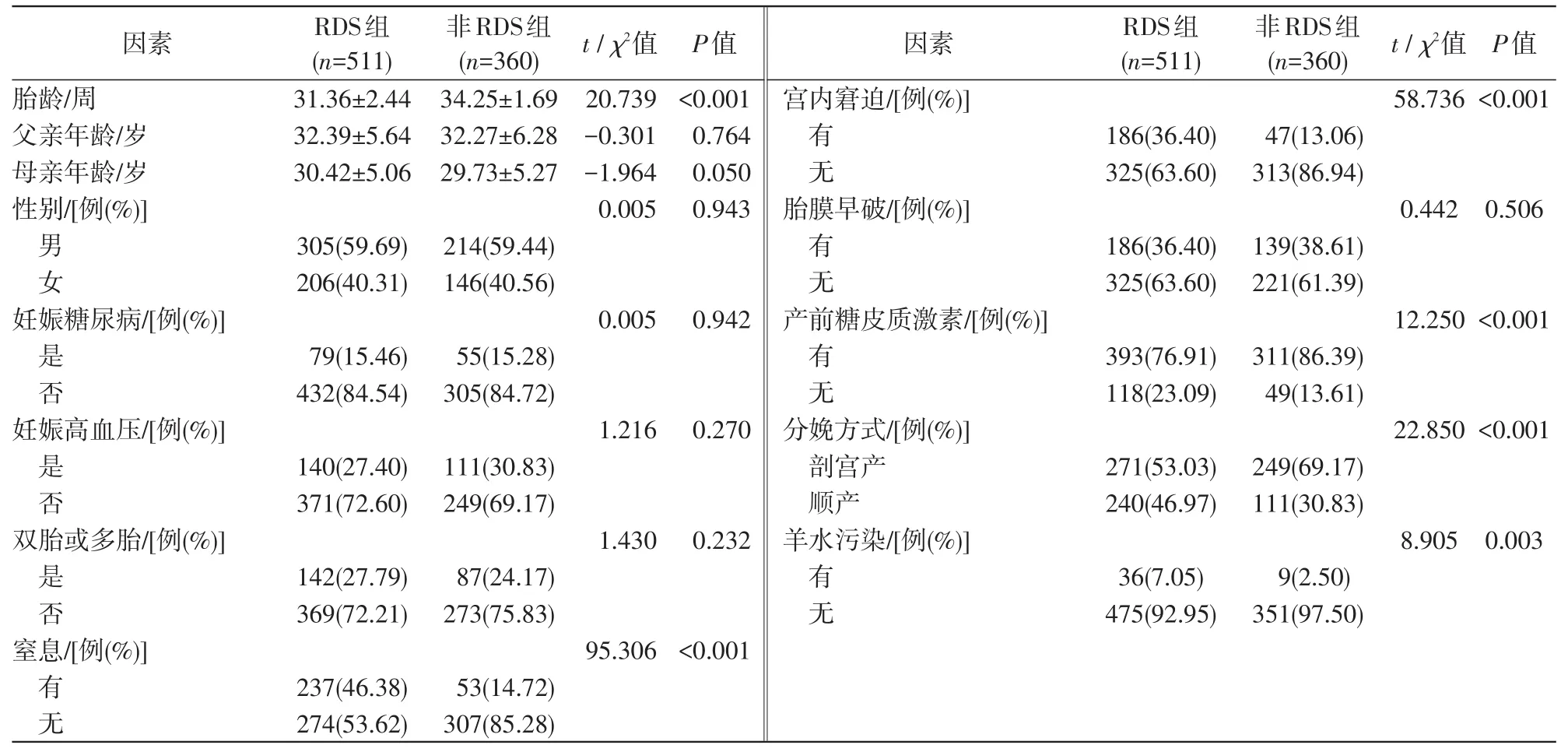
表1 早产儿发生RDS单因素分析
2.1.2 早产儿发生RDS多因素Logistic回归分析多因素Logistic回归分析表明胎龄大(OR=0.521,95%CI:0.470~0.577,P<0.001)及产前预防性应用糖皮质激素(OR=0.529,95%CI:0.329~0.850,P=0.008)是早产儿RDS的保护因素,窒息(OR=2.266,95%CI:1.479~3.469,P<0.001)和宫内窘迫(OR=3.667,95%CI:2.344~5.736,P<0.001)是早产儿RDS的危险因素,见表2。
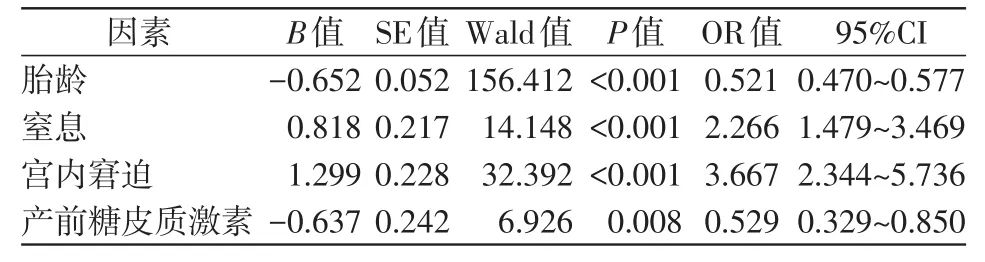
表2 早产儿发生RDS的多因素Logistic回归分析
2.2 不同胎龄RDS早产儿的并发症情况
511例RDS早产儿中有323例(63.21%)存在并发症,其中超早产儿、极早产儿、中期早产儿和晚期早产儿组的并发症发生率分别为85.19%、67.10%、57.24%和57.14%。肺出血、败血症、支气管肺发育不良的发生率在不同胎龄RDS早产儿中差异有统计学意义(P<0.05),胎龄越小并发症发生率越高,见表3。

表3 不同胎龄早产儿RDS的并发症情况 [例(%)]
2.3 产前应用糖皮质激素对RDS早产儿的影响
产前应用糖皮质激素组患儿的5 min氧饱和度高于未应用激素组(P<0.05);两组体重、身长、头围、1 min Apgar评分以及并发症情况差异无统计学意义(P>0.05),见表4。

表4 产前应用糖皮质激素对RDS早产儿的影响
3 讨论
本研究对早产儿RDS的多因素Logistic回归分析显示,存在窒息和宫内窘迫早产儿的RDS发生率是未发生窒息及宫内窘迫早产儿的2~3倍,产前应用糖皮质激素和胎龄越大的早产儿RDS的发生率越低。窒息和宫内窘迫是早产儿RDS的危险因素,产前预防性应用糖皮质激素及胎龄大是早产儿RDS的保护因素。窒息和宫内窘迫引发RDS发生的机制在于,窒息所产生的低氧会导致肺泡Ⅱ型上皮细胞损伤,减少肺表面活性物质分泌并降低其活性,而宫内窘迫所致的急性低氧会引发肺表面活性物质的合成和利用障碍[7],二者导致低灌注和缺氧酸中毒的发生,致使肺急性损伤,引发大量炎症因子及氧自由基释放,肺泡Ⅱ型上皮细胞的肺表面活性物质合成和分泌受到抑制[8],引发肺部通气功能障碍,诱导早产儿RDS的发生。
一项对我国13家医院早产儿RDS的并发症情况的前瞻性研究结果发现,2014年视网膜病变、支气管肺发育不良、坏死性小肠结肠炎、动脉导管未闭、肺出血、败血症等并发症的发病率较2013年增高,并且均高于非RDS早产儿,RDS是造成早产儿预后不良的重要因素[2]。本研究中RDS早产儿并发症发生率随着胎龄的增大而降低,其中支气管肺发育不良发生率最低,考虑这与支气管肺发育不良确诊所需的时间较长、家属依从性差、提前出院等原因有关;不同胎龄早产儿并发症的比较发现,超早产儿肺出血和颅内出血的发生率最高,考虑与超早产儿肺发育的极不成熟有关;胎龄影响新生儿成熟情况,Sweet等[9]研究显示,胎龄24~25周的早产儿RDS发生率为92%,26~27周的为88%,28~29周的为76%,30~31周的为57%。胎龄愈小,早产儿RDS的患病率越高[10-11]。故在RDS的诊治中需充分考虑胎龄因素,必要时采取相应手段,预防自发性早产[12]。
肺泡Ⅱ型上皮细胞合成和分泌肺表面活性物质,稳定肺泡内压,减少肺泡萎陷是防止RDS发生的根本机制。糖皮质激素结合肺泡表面受体并表达相关蛋白,促进肺泡肺表面活性物质生成[13]。孕母产前应用糖皮质激素后可能会对母婴产生不同程度的影响。Meneguel等[14]研究显示,单疗程产前应用糖皮质激素可有效降低早产儿脑室出血、动脉导管未闭、坏死性小肠结肠炎等并发症的发生率,缩短住院天数,对神经、生长发育未产生副作用,也未增加败血症等感染的发生。Carson等[15]研究显示,多疗程糖皮质激素使用可能使生长受到抑制,出生体重及脑重量减轻,头围相对减少,生长发育迟滞,神经系统发育落后表现,甚至出现远期心血管以及母亲感染及糖尿病等疾病。本研究排除了妊娠高血压、妊娠糖尿病、窒息、宫内窘迫等因素,发现产前应用糖皮质激素可提高早产儿出生5 min经皮动脉血氧饱和度,同时并未造成对胎儿生长发育(如头围缩小、出生体重减轻等)的不良影响,但未能证实糖皮质激素是否可降低颅内出血、肺动脉高压等并发症的发生率,对患儿的远期影响也有待进一步探讨。产前激素使用的安全性尚存争议,是单疗程还是多疗程,如何规范地使用,减少不良后果仍是未来研究关注的热点。
综上所述,发生宫内窘迫、出生时窒息、产前未用糖皮质激素、胎龄小是早产儿RDS发病的主要危险因素。做好妊娠随访、定期产前超声检查,评估胎龄、正确判断分娩时机与方式,预防胎儿窘迫及新生儿缺氧窒息的发生,产前糖皮质激素的规范使用,有利于预防早产儿RDS的发生。

