间质性肺疾病合并肺癌患者的临床特征及预后分析
任雁宏 李全国 刘敏 张欣然 赵玲 代华平
1中日友好医院呼吸与危重症医学科 国家呼吸医学中心 国家呼吸临床研究中心中国医学科学院呼吸病学研究院,北京 100029;2中日友好医院放射诊断科 国家呼吸医学中心 国家呼吸临床研究中心 中国医学科学院呼吸病学研究院,北京 100029;3中日友好医院病理科 国家呼吸医学中心 国家呼吸临床研究中心 中国医学科学院呼吸病学研究院,北京 100029
间质性肺疾病 (interstitial lung disease,ILD)是以肺组织炎症反应和纤维化改变为特征的一组良性的异质性疾病。肺癌起源于支气管肺泡上皮细胞,是发病率和病死率高的恶性肿瘤之一。两者病变性质不同,但是都与不同刺激因素作用下,肺组织细胞的异常分化和增殖有关[1]。与普通人群相比,ILD 患者肺癌发病率呈现显著增高趋势[2]。尽管手术、化疗、放疗及分子靶向等治疗在肺癌中取得了明显进展,但是这些治疗方法在ILD 合并肺癌患者中并未获得良好效果,需要提高对ILD合并肺癌的临床特点、病理特点和治疗风险评估认识。本研究回顾性分析了50例ILD 合并肺癌患者的临床特征和预后,旨在为早期识别ILD 合并肺癌病例,并合理选择治疗方法提供依据。
1 对象与方法
1.1 研究对象 回顾性分析2015年1月至2018年12月中日友好医院呼吸与危重症医学科收治的记录完整临床、病理和影像资料的ILD 合并肺癌患者50例。纳入标准:在中日友好医院完成胸部CT 检查,经放射诊断科医师阅片,符合ILD 影像特点,且肺组织病理证实肺癌诊断的患者。排除标准:记录资料不完整的患者。
1.2 方法 收集50例ILD 合并肺癌患者的影像资料,由2名放射诊断科医师独立阅片,描述ILD合并肺癌的影像特点,若出现分歧经双方讨论后共同判定。汇总肺癌病理类型、分子病理特点,参照肺癌TNM 分期标准 (第八版)[3]进行肿瘤分期。分析ILD 合并肺癌患者临床特征及预后。
1.3 统计学分析 采用SPSS 20.0统计学软件,计量资料以±s表示,计数资料以百分比表示。生存期分析采用Kaplan-Merier曲线法和log-rank检验。对患者预后产生影响的临床及病理因素采用Cox比例风险模型进行多因素分析。P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 通过病例检索系统共检出ILD 合并肺癌患者102例,其中临床、病理和影像资料均完整的患者50例。男40例,女10例,平均年龄(66±7)岁,平均吸烟指数(537±413)年支,体质量指数 (23.3±3.2)kg/m2。咳嗽、呼吸困难加重是最常见的临床症状 (18例,36.0%),其次为 咯 血 (16 例,32.0%) 和 胸 痛 (12 例,24.0%)。
2.2 ILD 合并肺癌影像特点 在50例ILD 合并肺癌患者中,39 例 (78.0%)ILD 影像特点符合寻常型间质性肺炎 (usual interstitial pneumonia,UIP),8例 (16.0%)符合非特异性间质性肺炎,1例(2.0%)符合机化性肺炎,1例 (2.0%)符合呼吸性细支气管炎伴间质性肺炎,1例 (2.0%)符合脱屑性间质性肺炎。
在50例中39例(78.0%)为周围型肺癌,11例(22.0%)为中央型肺癌。肿瘤位于上肺21例(42.0%), 中 下 肺 29 例 (58.0%)。41 例(82.0%)肿瘤位于间质病变区域内,9 例(18.0%)肿瘤分布于间质病变外。肿瘤影像表现为团块23例(46.0%),结节18例(36.0%),实变8 例 (16.0%),胸 腔 积 液1 例 (2.0%)。见图1。

图1 间质性肺疾病合并肺癌患者肿瘤影像可表现为团块、实性结节、实变和胸腔积液 A:UIP合并小细胞肺癌,可见左上肺临近细网格区域的实性结节,边界清晰,经EBUS-TBNA 取4区淋巴结明确病理诊断;B:UIP合并小细胞肺癌,可见右上肺肿块,位于细网格内,与纵隔淋巴结融合,边缘呈分叶状,经气管镜行右上叶支气管黏膜活检明确病理诊断;C:UIP合并肺腺癌,肺野内未见明确占位性病变,右侧胸腔积液,胸膜活检病理诊断腺癌;D:UIP合并肺鳞癌,左下肺蜂窝、网格内可见肿块,伴厚壁空洞形成,洞腔内呈虫噬样改变,CT 引导下经皮肺穿刺获取组织标本明确病理诊断;E:UIP合并肺腺癌,右下肺蜂窝、网格区域内大片实变,实变内可见串珠样支气管扩张影,CT 引导下经皮肺穿刺获取组织标本明确病理诊断
2.3 ILD 合并肺癌病理特点 在50例患者中,34例(68.0%)通过经皮肺穿刺获取肺组织,明确病理诊断(13例经超声引导穿刺,21例经CT 引导穿刺),10例 (20.0%)经气管镜检查诊断,5例(10.0%)经外科胸腔镜诊断,1例 (2.0%)经浅表淋巴结活检诊断 (表1)。获取肺组织操作过程顺利,除3 例 (6.0%)发生小量气胸外 (CT 引导1例,超声引导1例,气管镜1例),余患者均无并发症发生 (表1)。50 例ILD 合并肺癌患者中,腺癌21例 (42.0%),鳞癌12 例 (24.0%),小细胞癌15 例 (30.0%),大细胞癌1 例(2.0%),腺鳞癌1例(2.0%)(图2),腺癌、鳞癌和小细胞癌均以外周型生长方式为主 (表1)。21例腺癌和1例腺鳞癌患者中,分子病理检测出1例表皮生长因子受体 (epidermal growth factor receptor,EGFR)21 外 显 子 L858R 突 变(4.5%),余均未发现EGFR 敏感基因突变和间变性淋巴瘤激酶 (anaplastic lymphoma kinase,ALK)融合基因突变。

图2 间质性肺疾病合并肺癌患者肿瘤病理特点

表1 间质性肺疾病合并肺癌患者肿瘤位置、病理类型和活检方式 [例 (%)]
2.4 ILD 合并肺癌临床治疗及转归 50例ILD 合并肺癌患者中,3例口服糖皮质激素治疗ILD,余患者未针对ILD 进行特殊治疗。ILD 合并肺癌患者生存期分析结果显示,不同治疗方式和氧合指数是影响患者生存期的独立危险因素。见表2。

表2 影响ILD 合并肺癌患者生存期的Cox多因素回归分析
手术治疗组 (12 例)中位生存期为36 个月,化疗组(25例)中位生存期为12个月,支持治疗组(13例)中位生存期3.5个月,三者生存期差异有统计学意义(P<0.001)。见图3。
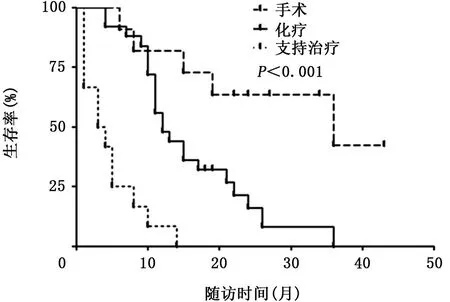
图3 50例间质性肺疾病合并肺癌患者选择不同治疗方式的生存期分析
对25例接受化疗的ILD 合并晚期肺癌患者生存期进行亚组分析,在调整年龄、肿瘤病理类型、ILD 影像表现类型 (UIP 和非UIP)、合并基础疾病数量、FVC、FEV1/FVC、DLCO、肿瘤分期等因素后,氧合指数仍是影响患者生存期的独立危险因素(HR=0.157,95%CI:0.034~0.711,P=0.016 3)。以化疗组患者氧合指数中位数338 mm Hg (1 mm Hg=0.133 k Pa)为界值,氧合指数>338 mm Hg 组生存期显著长于氧合指数≤338 mm Hg组(P=0.010 9)。见图4。
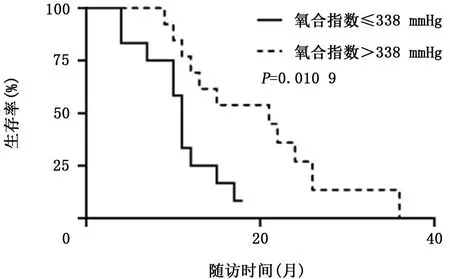
图4 不同氧合指数的晚期肿瘤患者化疗后生存曲线
3 讨论
ILD与肺癌关系密切已经受到越来越多的学者关注。不同国家回顾性研究结果均提示,与普通人群相比,肺癌在ILD 患者中发病率和病死率更高[4-5]。特发性肺纤维化是一种不明原因,以慢性、进行性加重的肺纤维化为主要特点的ILD,其影像和病理特征均表现为UIP。特发性肺纤维化与肺癌发病机制存在诸多相似之处[6-7]。荟萃分析报道,特发性肺纤维化患者中肺癌发病率为3.0%~48.0%[4]。在本研究观察的50例患者中,ILD 影像表现为UIP 的患者占78.0%,这提示以纤维化改变为主要特点的ILD 更易合并肺癌。本文中肺癌以周围型为主 (78.0%),分布于中下肺(58.0%)多见,这些区域也是ILD 最常累及的部位。而且,ILD 的网格和蜂窝多与肿瘤叠加在一起(82%),这也间接提示肿瘤的发生可能与ILD 反复炎症损伤、纤维化形成的过程中出现细胞的异常分化、增殖有关[8]。在我国普通人群中,多数肺癌患者(75%)首诊已处肿瘤中晚期,这也是肺癌预后差的主要原因[9]。在ILD 合并肺癌患者中,肺癌多在无意中发现,肺癌早期诊断病例相对更多[5,10]。本 研 究 观 察 的50 例 患 者 中,18 例(36.0%)在ILD 常规随诊时发现肺部占位性病变,早期肺癌占32.0% (12例非小细胞肺癌,4例局限期小细胞肺癌),这可能与ILD 需要动态观察影像变化,更能及时发现肿瘤有关。因为存在基础ILD,这部分患者常有咳嗽、呼吸困难等症状,一旦合并恶性肿瘤,临床表现无明显特异性。在本研究观察的50例患者中,多数仅表现为原有呼吸道症状不同程度加重,部分患者新发胸痛、咯血,这些新发症状更容易引起患者和接诊医师关注。
ILD合并肺癌患者临床症状较重,肺结构破坏明显,有创操作出现气胸等并发症风险增高,因此这部分患者取得组织病理诊断难度相对高。有研究显示,约19%ILD 合并肺癌患者因配合度差无法取得组织病理诊断证据[11]。本研究的50 例患者中,肺癌均经组织病理诊断,68.0%采用经皮肺穿刺的方式获取肺组织,这也与肿瘤多数外周分布,经皮肺穿刺可操作性强,取到肺组织可能性大有关。文中5例中央型肺癌患者也采用经皮肺穿刺获取肺组织,3例与肿瘤体积大,患者呼吸困难症状较重,经皮肺穿刺患者配合度更高有关,2例因肺外周出现转移病灶,经皮肺穿刺获取转移病灶肺组织诊断。在获取病理组织过程中,3 例患者(6.0%)出现少量气胸,其中2例发生在经皮肺穿刺,这2例肺内病变与胸膜间有间隙,且病变内可见到支气管充气征象,这可能与活检过程中出现气胸有关;另外1例发生在经支气管镜肺活检,肺内病变表现为大片实变影,伴支气管充气征,气胸发生与经支气管镜肺活检损伤胸膜有关。3例患者均未行胸腔闭式引流,吸氧联合对症治疗后,气胸吸收,这也提示选择适宜的活检方法可提高有创操作的安全性。与其他回顾性研究结论[12]类似,本研究发现ILD 合并肺癌患者中腺癌较多见,其次是鳞癌和小细胞癌。与普通人群相比,ILD 合并非小细胞肺癌患者EGFR 活化突变发生率明显降低(0%~5.8%比24.3%~47%)[13-16]。本研究的21例腺癌和1例腺鳞癌患者中仅1例检测到EGFR21外显子L858 突变,未发现ALK 融合基因突变,这可能与ILD 患者多有吸烟史且部分为鳞癌有关[8]。
近年来,肺癌的治疗在放疗、化疗、分子靶向等领域都取得了重大进展。但是,这些治疗方式在推广至ILD 合并肺癌的患者中遇到一些困难,例如,分子靶向药物可能诱发急性肺损伤[17],放疗所致的重度放射性损伤在ILD 合并肺癌中发生率显著增高[18],部分ILD 合并早期肺癌手术切除后诱发间质性肺疾病急性加重(acute exacerbation of interstitial lung disease,AEILD)等[19]。因此,ILD合并肺癌治疗方式的选择及预后判断是临床难点。对于合并ILD 且分期较早的肺癌,具备手术条件的患者,手术切除仍然是目前首选的治疗方案[20]。但是,术后并发症,如感染、AEILD 等是影响术后存活率主要因素。有研究发现,术后AEILD 的发生与手术操作和患者自身因素均有相关性[21],手术切除范围大,手术时间长的患者,术后出现AEILD 风险增加。患者既往曾经有过AEILD 史、术前肺活量明显降低、ILD 影像特点符合UIP,涎液化糖链抗原-6 明显增高都是术后发生AEILD 的危险因素。为降低手术导致AEILD的风险,外科医师可能对较小的肿瘤选择肺段切除术,这也是造成术后复发和远期预后差的重要原因[22]。在本研究中,12例Ⅰ期和Ⅱ期非小细胞肺癌患者均接受手术治疗,术后无严重并发症发生,这与患者手术切除范围小,ILD 肺功能受损程度轻有关,此组患者中位生存期为36个月,明显长于化疗组和支持治疗组。
与单纯Ⅲ期和Ⅳ期的肺癌患者比较,ILD 合并肺癌患者预后更差[23],且化疗出现并发症风险增高。文献报道年龄>70岁,ILD 影像表现以UIP为主,都是ILD 合并晚期肺癌化疗效果差的危险因素,而且对于已有ILD 患者,化疗药物诱发的药物性肺损伤发生风险增高[24]。本研究中25例接受化疗的患者中位生存期为12个月,较支持治疗组 (3.5个月)延长,亚组分析提示氧合指数>338 mm Hg的患者化疗生存期较氧合指数≤338 mm Hg的患者延长。
本研究仍有许多不足之处,入选患者例数相对较少,受回顾性研究所限,部分关注资料记录有缺失,无法客观评价。笔者期待未来有临床设计严谨的前瞻性、大样本研究能够提供更多的信息,为这类疾病患者后续的治疗和管理提供依据。
总之,与普通人群相比,ILD 患者合并肺癌风险增高。虽然在ILD 合并的肺癌中,非小细胞肺癌占半数以上,但是EGFR 和ALK 基因突变发生率低,且因顾及靶向药有诱导ILD 加重的风险,少有ILD 合并肺癌患者有机会选择靶向药物治疗。对于ILD 合并早期肺癌且具备手术条件的患者,手术切除仍然是首选治疗方式,术前需谨慎评估术后并发症风险。对于无法手术切除的ILD 合并肺癌患者,条件许可时可考虑选择针对肿瘤的化学治疗,氧合指数是化疗患者预后的重要预测因素。
利益冲突 所有作者均声明不存在利益冲突

