基于UPLC指纹图谱的陈皮饮片及其配方颗粒质量相关性研究*
黎桃敏,余欣彤,陈伟媚,徐东婷,胡 懿,施文婷,黄 瑶
(广东一方制药有限公司/广东省中药配方颗粒企业重点实验室,广东 佛山 528244)
陈皮为芸香科植物橘Citrus reticulata Blanco及其栽培变种的干燥成熟果皮,性苦、辛,味温,具有理气健脾、燥湿化痰的功效[1]。药材可分陈皮和广陈皮,主产于广东、浙江、江西、湖南、福建、四川、重庆等地[2]。陈皮以“橘柚”之名首载于《神农本草经》,被列为上品,且在众多医药类古籍中都有记载,具有良好的药用价值[3]。现代研究表明,陈皮活性成分主要为黄酮类化合物,包括芸香柚皮苷、橙皮苷、川陈皮素、橘皮素等[2],此外还含挥发油类、生物碱类和柠檬苦素等多种成分[3-5]。其主要药理作用包括降血脂、调节胃肠平滑肌运动、化痰、抗肿瘤、抗氧化、抗炎和保肝等[6-8],体现了中药的物质基础是由多分子、多成分组成的复杂整体[9]。
中药饮片是中药临床用药的主要形式,而中药配方颗粒是依据中医药理论和患者需求,由单味中药饮片经水提、浓缩、干燥、制粒而成,是对中药饮片的补充[10]。陈皮饮片经加工制成配方颗粒后,已不具饮片外形,仅依据2020年版《中华人民共和国药典》对其指标成分进行含量测定难以实现整体质量评价。相较于传统的经验鉴别和单组分分析,中药指纹图谱可以整体、宏观地表征被测样品主要化学成分的特征,实现对中药内在质量的综合评价[11-12]。为了全面客观地评价陈皮传统饮片与配方颗粒之间的关联性,本研究采用UPLC法分别测定了陈皮饮片和配方颗粒的指纹图谱,比较两者之间的相关性和差异性,以期为陈皮相关制剂的研究提供实验依据,更好地开展陈皮配方颗粒质量控制工作。
1 仪器与试药
1.1 仪器 Waters H-CLASS型超高效液相色谱仪(美国Waters公司);XP26型百万分之一天平、ME204E型万分之一天平(瑞士METTLER TOLEDO公司);Milli-Q Direct型超纯水系统(德国Merck公司);B-290型喷雾干燥仪(瑞士BUCHI有限公司);LGS20型干法制粒机(南京迦南科技有限公司);YRE-501型旋转蒸发仪(巩义市予华仪器有限责任公司);DLSB-5/20型低温冷却液循环水泵(郑州长城科工贸有限公司);111B型二两装高速中药粉碎机(浙江瑞安市永历制药机械有限公司);TC-15型套式恒温器(海宁市新华医疗器械厂);HWS28型恒温水浴锅(上海一恒科技有限公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药 芸香柚皮苷对照品(批号:wkq19041908,纯度98.0%)、川陈皮素对照品(批号:wkq20031701,纯度98.0%)均购自四川省维克奇生物科技有限公司;橙皮苷对照品(批号:110721-202019,纯度95.3%)购自中国食品药品检定研究院;橘皮素对照品(批号:18031501,纯度98.0%)购自成都普菲德生物技术有限公司;乙腈、冰醋酸、甲醇为色谱级(德国Merck公司);水为超纯水;其余试剂均为分析纯。
15批陈皮饮片(编号:S1~S15)经广东一方制药有限公司魏梅主任药师鉴定为正品,均为芸香科植物橘Citrus reticulata Blanco的干燥成熟果皮。根据《中药配方颗粒质量控制与标准制定技术要求》中“研究表征标准汤剂用汤剂的制备”项的指导原则[13],确定陈皮配方颗粒的制备方法:取陈皮饮片,加水煎煮2次,第一次加入投料量8倍的水,浸泡30 min,加热煎煮30 min,煎液用350目筛趁热过滤;第二次加投料量6倍的水,加热煎煮25 min,煎液用350目筛趁热过滤,合并两次滤液,得陈皮提取液。提取液低温减压浓缩至适量,浓缩液过250目筛网得陈皮清膏。清膏进行喷雾干燥,收集喷干粉,再加辅料适量,混匀,干法制粒,得陈皮配方颗粒。15批陈皮配方颗粒样品(编号:E1~E15)分别由15批饮片对应制备,饮片产地、饮片及对应配方颗粒编号见表1。

表1 样品信息表
2 方法与结果
2.1 色谱条件[14]色谱柱:Acclaim RSLC 120 C18Column(100 mm×2.1 mm,2.2 μm);流动相:乙腈(A)-0.5%冰醋酸溶液(B)梯度洗脱(0~15 min,13%~20%A;15~25 min,20%~34%A;25~44 min,34%~42%A);流速:0.40 mL/min;柱温:25 ℃;检测波长:283 nm;进样量:1.0 μL。
2.2 混合对照品溶液的制备 分别取芸香柚皮苷、橙皮苷、川陈皮素、橘皮素对照品适量,精密称定,加入甲醇配制成每1mL含芸香柚皮苷106.82 μg、橙皮苷115.50 μg、川陈皮素123.97 μg、橘皮素69.09 μg的混合对照品贮备液。
2.3 供试品溶液的制备 取陈皮饮片粉末(过二号筛)约1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇100 mL,称定质量,超声处理(功率:300 W,频率:45 kHz)1 h,取出,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液,即得饮片供试品溶液。
取陈皮配方颗粒适量,研细,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定质量,超声处理(功率:240 W,频率:45 kHz)1 h,取出,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液,即得配方颗粒供试品溶液。
2.4 方法学考察
2.4.1 专属性试验 分别精密吸取空白溶剂、混合对照品溶液及供试品溶液,按“2.1”项下色谱条件进样测定,结果显示,供试品溶液色谱在与对照品溶液色谱相应的保留时间处具有相同的色谱峰,且空白溶剂无干扰,表明该方法专属性良好。(见图1)

图1 UPLC 色谱图
2.4.2 精密度试验 精密吸取“2.2”项下混合对照品溶液,按“2.1”项下色谱条件连续进样6次,以2号峰橙皮苷为参照峰,计算得各共有峰相对保留时间和相对峰面积的RSD。RSD范围分别为0.15%~0.25%和0.15%~0.21%,表明仪器精密度良好。
2.4.3 稳定性试验 取陈皮饮片S15,精密称定,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件分别在0、2、4、6、8、12、24 h进样测定,以2号峰橙皮苷为参照峰,计算得各特征峰相对保留时间和相对峰面积的RSD。RSD范围分别为0.43%~1.34%和1.62%~2.76%,表明陈皮饮片供试品溶液在24 h内稳定性良好。
2.4.4 重复性试验 取陈皮饮片S15,精密称定,平行称定6份,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定。以2号峰橙皮苷为参照峰,计算得各特征峰相对保留时间和相对峰面积的RSD。RSD范围分别为0.06%~0.09%和1.96%~2.91%,表明该方法重复性良好。
2.5 UPLC指纹图谱的确立与相似度评价
2.5.1 指纹图谱的确立 取15批陈皮饮片及其配方颗粒,分别按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,得15批陈皮饮片及其配方颗粒的UPLC指纹图谱,将采集到的UPLC色谱图导入国家药典委员会颁布的“中药色谱指纹图谱相似度评价系统2012版”软件进行匹配,分别生成对照指纹图谱R1和R2。15批陈皮饮片、配方颗粒指纹图谱的堆叠图见2~3。从15批陈皮饮片与配方颗粒的指纹图谱中,共标记出5个共有峰,通过与对照品图谱对比,确定1号峰为芸香柚皮苷,2号峰为橙皮苷,4号峰为川陈皮素,5号峰为橘皮素。

图2 15 批陈皮饮片的UPLC 指纹图谱堆叠图

图3 15 批陈皮配方颗粒的UPLC 指纹图谱堆叠图
2.5.2 相似度评价 将15批陈皮饮片及其配方颗粒指纹图谱的数据文件导入“中药色谱指纹图谱相似度评价系统2012版”软件,分别计算各批次陈皮饮片、陈皮配方颗粒指纹图谱与其对照图谱的相似度,结果见表2。15批陈皮饮片指纹图谱与其对照指纹图谱(R1)的相似度均≥0.990,表明不同批次陈皮饮片的质量较为稳定。15批陈皮配方颗粒指纹图谱与其对照指纹图谱(R2)的相似度均≥0.910,表明不同批次陈皮配方颗粒的质量和生产工艺均较稳定。

表2 15 批陈皮饮片和配方颗粒UPLC 指纹图谱与其对照指纹图谱的相似度结果
2.5.3 对照指纹图谱的比较 将15批陈皮饮片和陈皮配方颗粒指纹图谱生成的对照指纹图谱R1和R2导入“中药色谱指纹图谱相似度评价系统2012版”软件,计算得陈皮饮片对照指纹图谱R1与陈皮配方颗粒对照指纹图谱R2的相似度为0.962。通过对陈皮饮片和陈皮配方颗粒的对照指纹图谱的共有峰进行分析,可以看出陈皮饮片中主要色谱峰在陈皮配方颗粒的色谱图中均有体现,而陈皮配方颗粒的主要色谱峰也能在饮片的图谱中找到追溯,表明从陈皮饮片到陈皮配方颗粒成分无明显变化,化学成分基本一致,二者具有一定的等效性,也反映出陈皮配方颗粒的制备工艺稳定可行。(见图4)

图4 陈皮饮片对照指纹图谱(R1)与陈皮配方颗粒对照指纹图谱(R2)
2.6 共有峰的相关性研究 分别计算15批陈皮饮片及其配方颗粒指纹图谱共有峰的“峰面积/取样量”值,结果见表3。不同批次陈皮饮片UPLC指纹图谱中各共有峰的“峰面积/取样量”值有所差异,也进一步影响着陈皮配方颗粒UPLC指纹图谱中各共有峰的“峰面积/取样量”值,为确保陈皮配方颗粒质量的稳定性,应严格把控陈皮饮片质量。采用SPSS 20.0软件,以各特征峰的“峰面积/取样量”值为变量,并为了消除各数据量纲和各数据之间相对大小差异对分析结果产生影响,对数据进行标准化预处理后进行Preason相关分析,结果见表4。结果表明陈皮饮片与配方颗粒UPLC指纹图谱的5个共有峰中,除橙皮苷峰外,芸香柚皮苷、峰3、川陈皮素和橘皮素均具有高度正相关性。

表3 15 批陈皮饮片与配方颗粒指纹图谱共有峰的“峰面积/取样量”值(mV·s·g-1)

续表3:

表4 15 批陈皮饮片与配方颗粒指纹图谱共有峰的相关性研究结果
2.7 UPLC指纹图谱的相关性研究
2.7.1 主成分分析 主成分分析法(PCA)是一种应用广泛的多元统计方法,在不丢失原来主要信息的前提下,从多变量之间的相互关系对数据集进行降维,可快速实现对数据的可视化识别[15]。以各特征峰的“峰面积/取样量”值为变量,通过SPSS 20.0软件对其进行标准化预处理后进行因子分析,计算得特征值和方差贡献率,见表5,主成分因子载荷矩阵见表6。以特征值>1为提取标准提取主成分[16-17],由表5~6可知,前两个主成分累积贡献率为97.042%>90%,表明提取的2个主成分能基本反映全部指标的信息。主成分1的特征值为3.310,方差贡献率为66.208%,载荷较高的峰有川陈皮素、橘皮素和芸香柚皮苷,表明这3个峰主要反映主成分1的信息;主成分2的特征值为1.542,方差贡献率为30.834%,载荷较高的峰有橙皮苷,表明这2个峰主要反映主成分2的信息。上述对陈皮指纹图谱差异贡献较大的成分,保留了原始变量的绝大部分信息,是影响陈皮饮片和配方颗粒质量的主要成分。
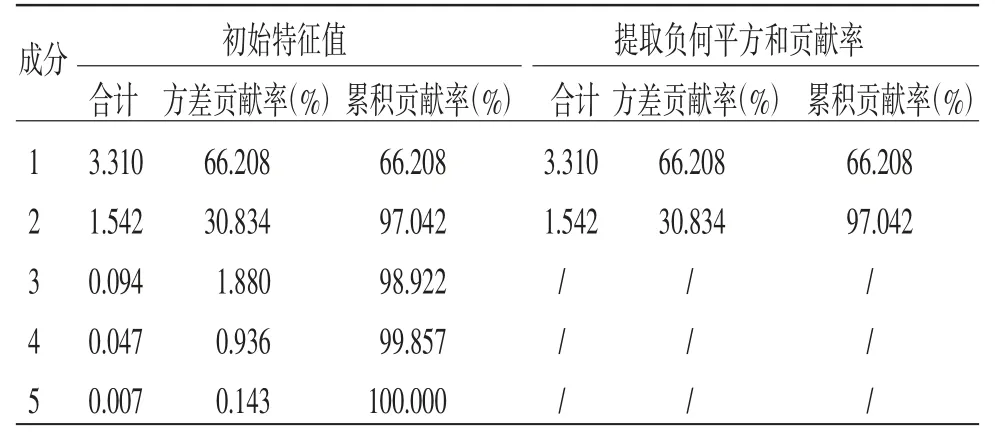
表5 特征值和方差贡献率
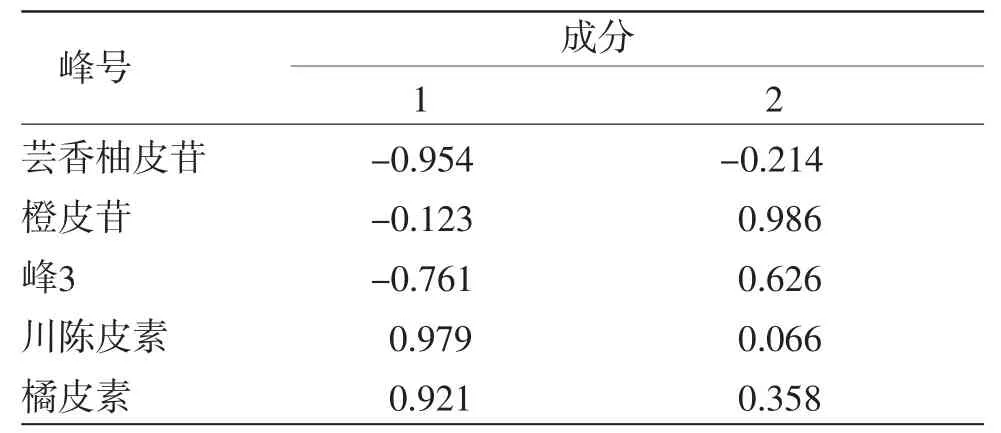
表6 主成分因子载荷矩阵
2.7.2 综合评分计算 采用SPSS 20.0 软件将15批陈皮饮片和配方颗粒的“峰面积/取样量”值进行标准化处理,得到Xi。由公式为特征值,由成分矩阵中的第j列载荷除以对应成分特征值的算术平方根所得),计算得到F1、F2,再根据综合评分函数F=F1*0.662 1+F2*0.308 3(其中F1、F2为2个主成分的得分,系数为各成分的方差贡献率),计算得到陈皮饮片及其配方颗粒指纹图谱的综合评分[18-19],结果见表7。15批陈皮饮片及其配方颗粒UPLC指纹图谱的综合评分变化趋势基本一致。
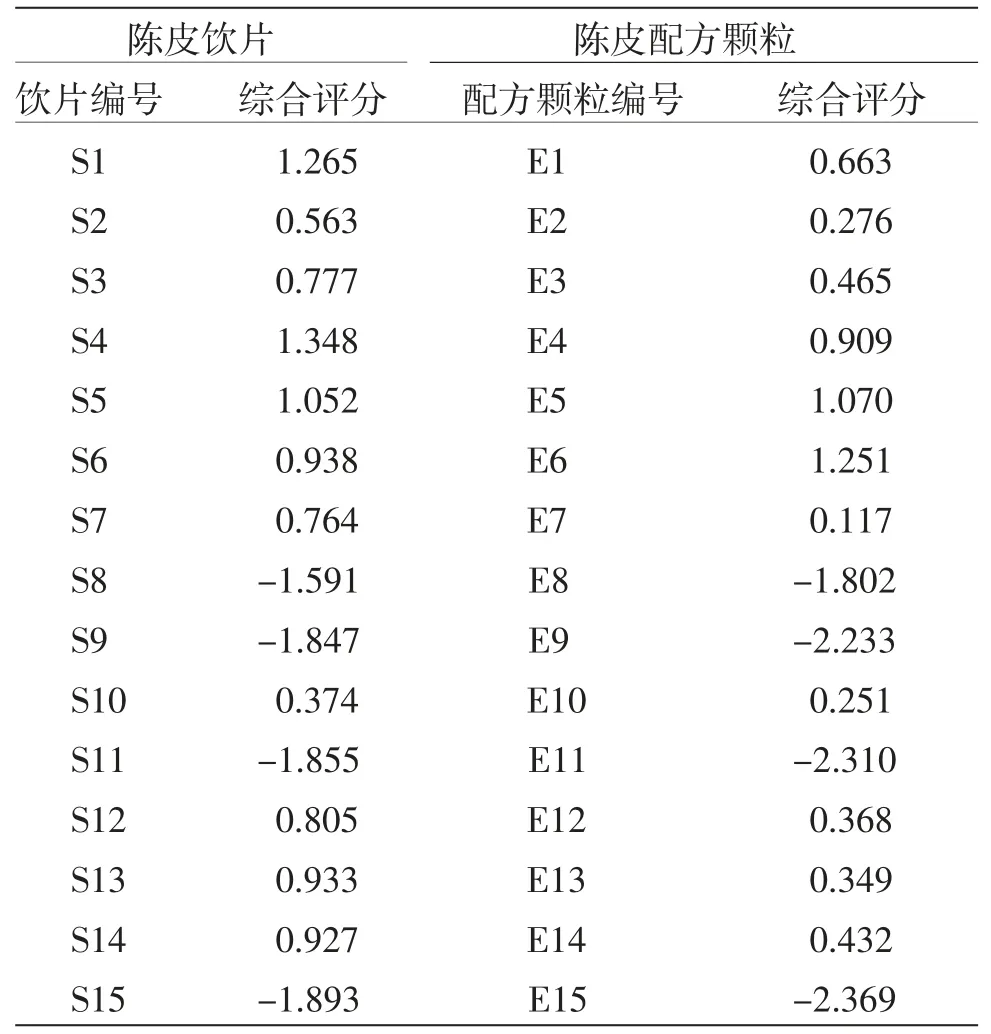
表7 15 批陈皮饮片和陈皮配方颗粒UPLC 指纹图谱的综合评分结果
2.7.3 相关性分析 以15批陈皮饮片及其配方颗粒UPLC指纹图谱的综合评分为变量,采用SPSS 20.0软件对其进行Pearson相关分析。主成分综合得分能够一定程度上反映样品质量[20],从主成分综合得分的Pearson相关分析结果可知,相关系数r值为0.980,P<0.01。表明陈皮饮片及其配方颗粒之间存在高度正相关性,陈皮饮片与配方颗粒的质量密切相关。
3 讨论
从共有峰相关性分析结果来看,陈皮饮片及其配方颗粒指纹图谱中芸香柚皮苷、橙皮苷、峰3、川陈皮素和橘皮素的相关系数分别为0.989、0.082、0.875、0.943、0.953,说明陈皮配方颗粒与陈皮饮片中芸香柚皮苷、峰3、川陈皮素和橘皮素的含量相关性极强;陈皮配方颗粒与陈皮饮片中橙皮苷的含量无相关性,因陈皮配方颗粒制备过程中其提取溶媒为水,该结果可能与橙皮苷化合物的水溶性较差[21-22]有关。后期可对陈皮饮片、标准汤剂与配方颗粒的质量相关性进行研究,以更加全面、客观地评价陈皮配方颗粒与标准汤剂物质基础的一致性,并从源头上做好质量控制工作。
影响中药饮片质量的因素众多,而中药饮片的质量与中药配方颗粒的质量紧密相关。本研究结果表明15批陈皮饮片及其配方颗粒UPLC指纹图谱综合评分的相关系数为0.980,陈皮饮片与配方颗粒对照指纹图谱的相似度为0.962,说明陈皮饮片与配方颗粒的质量正相关性强,两者的成分差异较小,为临床上陈皮配方颗粒作为陈皮饮片的补充提供了依据,也为陈皮相关制剂的质量控制奠定了基础。

