艾滋期HIV患者HAART后免疫重建不良的基线相关因素分析
王立洋 唐诗 闻颖
1沈阳市第六人民医院消化科(沈阳110001);2中国医科大学附属第一医院传染科(沈阳110001)
抗逆转录病毒治疗(antiretroviral therapy,ART)能显著降低HIV/获得性免疫缺陷综合征(Acquired Immunodeficiency Syndrome,AIDS)患者的病毒复制,但在病毒得到抑制情况下(HIV RNA <50 copies/mL)仍有15%~30%患者发生免疫重建不良(Suboptimal immune responders,SIR)[1]。SIR 患者容易发生机会性感染,远期病死率高[2]。SIR 的原因有年龄大、基线高病毒载量、基线低CD4+T 细胞计数、病毒学反弹、骨髓和胸腺功能不全等[3]。巨细胞病毒(Cytomegalovirus,CMV)作为HIV 患者最常见的共感染,CMV 共感染与SIR 的相关性受到关注。目前基线CMV IgM、CMV IgG、CMV DNA水平及抗CMV 治疗对SIR 影响尚无定论。笔者前期研究发现基线CMV DNA 水平对HIV 患者免疫重建无影响[4]。本文回顾性分析ART 后96 周并获得持续病毒学抑制者的32 个基线因素,评价各个基线因素与SIR 相关性,尤其是CMV 感染状态与SIR 相关性。
1 资料和方法
1.1 一般资料收集中国医科大学附属第一医院2009年1月1日至2014年12月31日确诊的HIV 感染者,诊断符合中华人民共和国卫生部制定的HIV 感染诊断标准“经酶联免疫吸附(enzyme linked immunosorbent assay,ELISA)及蛋白印迹(Western blot,WB)检测即确证试验”证实HIV 抗体阳性。入选标准:(1)年龄18 ~80 岁;(2)HIV首次确证试验阳性;(3)处于艾滋病期患者;(4)ART 并规律随访至少24 个月。排除标准:(1)ART耐药者;(2)随访过程中死亡者。病例筛选流程见图1。患者自愿签署知情同意书、提供相关信息并同意采集静脉血进行相关检测,伦理审批号:([2011]36)。
1.2 研究方法及评价指标
1.2.1 评价指标应用Excel 对入选患者的住院病历资料建立数据库,包括以下32 个指标,ART前基线的年龄、性别、体质量、白细胞总数(white blood cell count,WBC)、中性粒细胞计数(neutrophil count,NE)、血红蛋白(hemoglobin,HGB)、血小板(platelet,PLT)、谷氨酸-丙酮酸转氨酶(alanine Aminotransferase,ALT)、总胆红素(total bilirubin,TBIL)、血清白蛋白(albumin,ALB)、凝血酶原时间(prothrombin time,PT)、钠离子浓度、肌酐(creatinine,Cr)、C-反应蛋白(C-reactive protein,CRP)、低钠、卡氏肺孢子菌肺炎(pneumocystis cariniiPneumonia,PCP)、普通细菌感染、中枢神经系统性疾病、肝炎、肿瘤、结核、基线CD4+T 计数、基线CD8+T 计数、HIV RNA、WHO 临床分期、一线ART 方案含富马酸替诺福韦二吡呋酯(fumaricacid tenofovir two imidacloprid furosemide esters,TDF)与否、CMV 感染与否、CMV DNA、CMV IgM、CMV IgG、CMV 视网膜炎、抗CMV 治疗与否等作为评价与SIR 相关性的指标。
1.2.2 定义艾滋病期定义:世界卫生组织(WHO)临床分期IV 期的疾病或CD4+T 细胞计数<200 个/μL。SIR 定义:本研究将HIV/AIDS 患者经ART 后96 周并获得持续病毒学抑制(HIV RNA<50 copies/mL)CD4+T 计数小于200 个/μL 定义 为SIR[2]。CMV 感染定义:CMV DNA、CMV IgG(CMV IgG >12 AU/mL)、CMV IgM(CMV IgM >18 U/mL)其中有一项阳性。高水平CMV IgG 定义:CMV IgG >22(AU/mL)。CMV 感染状态分类:CMV 无感染、潜伏性感染、活动性感染及引起CMV 器官疾病。阳性CMV 血症定义:指通过聚合酶链式反应方法检测到外周血CMV DNA >500 copies/mL。CMV 视网膜炎定义:眼底镜检查发现CMV 视网膜特征性的改变且抗CMV 治疗有效或房水穿刺检测出CMV DNA。抗CMV 治疗定义:应用抗CMV 药物至少7 d。
1.3 统计学方法应用SPSS 17.0软件进行数据处理,计量资料正态分布用()表示,组间比较采用两组独立样本t检验,非正态分布用M(P25,P75)表示,组间比较采用非参数Mann-WhitneyU检验。计数资料组间率的比较采用χ2检验。多因素分析采用logistic 回归分析,将进行单因素分析P<0.1的基线因素代入多元回归模型中。P<0.05 为差异有统计学意义。
2 结果
2.1 一般基线因素特征在2009年1月1日至2014年12月31日确诊的中国医科大学附属第一医院传染科与关爱门诊随访的符合入组条件的HIV 感染者共104 例。其中17 例患者因在随访治疗中耐药更换治疗方案而被排除,包括10例患者一线ART 方案含TDF,7 例患者一线ART 方案为不含TDF治疗方案,17例患者随访96周后SIR 5例,免疫重建良好(optimal immune responders,OIR)12 例。共入组87 例,以ART 后96 周CD4+T 计数分为2 组:OIR组58例(ART后96周CD4+T计数≥200个/μL)、SIR 组29 例(ART 后96 周CD4+T 计数<200 个/μL)。结果发现,基线两组在基线CD4+T 计数、CD8+T 计数、CMV DNA、卡氏肺孢子菌肺炎、WHO 临床分期、CMV 感染差异有统计学意义(P<0.05,表1)。
2.2 CMV 感染状态的基线特征
2.2.1 CMV感染状态的基线特征与SIR的分析本研究中CMV 感染率为55%。阳性CMV 血症者22 例,OIR 组10 例,占19.6%,SIR 组12 例,占41.4%(P= 0.036);基线CMV IgM >18 U/mL 共5 例,OIR组4 例,占11.4%,SIR 组1 例,占4.5%(P= 0.679);基线CMV IgG >22 AU/mL 共17 例,OIR 组10 例,占30.3%,SIR 组7 例,占31.8%(P= 0.905);CMV视网膜炎共7 例,OIR 组2 例,占3.4%,SIR 组5 例,占17.2%(P= 0.07);抗CMV 治疗共21 例,OIR 组11 例,占19.0%,SIR 组10 例,占34.5%(P=0.111)。CMV 感染共44 例,OIR 组23 例,占45.1%,SIR 组21 例,占72.4%(P=0.018,表1)。
表1 OIR 组与SIR 组基线各指标比较Tab.1 data comparision between group OIR and group SIR ±s

表1 OIR 组与SIR 组基线各指标比较Tab.1 data comparision between group OIR and group SIR ±s
注:*代表P <0.05;△代表P <0.1
指标OIR 组例数SIR 组例数P 值年龄(岁)性别(男)体质量(kg)WBC[M(P25,P75),×109/L]NE HGB(g/L)PLT(×109/L)ALT[M(P25,P75),U/L]TBIL[M(P25,P75),μmol/L]ALB(g/L)PT[M(P25,P75),S]Na(mmol/L)Cr[M(P25,P75),μmol/L]CRP[M(P25,P75),mg/L]基线CD4+T 计数[M(P25,P75),个/μL]基线CD8+T 计数[M(P25,P75),个/μL]CMV IgM>18(U/mL)LogHIV RNA >5 CMV IgG >22(AU/mL)CMV DNA >500(copies/mL)低钠PCP WHO 临床分期Ⅳ期普通细菌感染中枢神经系统性疾病肝炎肿瘤结核CMV 视网膜炎一线ART 方案含TDF抗CMV 治疗CMV 感染39.9±13.2 89.7%60.5±10.1 5.0(3.6,6.6)2.7(1.6,4.7)120.2±23.0 191.2±92.4 30.5(15.3,81.0)8.2(6.2,11.4)38.3±8.5 13.5(12.7,14.1)139.6±3.7 62.0(51.0,71.8)14.3(4.9,50.0)117.5(46.5,197.5)75.0(481.5,1127.5)11.4%55.3%30.3%19.6%9.1%34.5%58.6%13.8%3.4%12.1%0.0%29.3%3.4%44.8%24.1%45.1%58 52 47 58 57 57 57 56 56 56 53 54 56 51 58 56 4 26 10 10 5 20 34 8 2 7 0 17 2 26 14 23 45.6±11.9 89.7%58.1±8.6 4.7(3.1,7.1)3.6(1.7,5.0)116.7±21.5 217.1±86.7 23.0(14.0,46.5)7.4(4.7,11.3)35.6±8.0 13.4(12.9,14.3)138.5±4.9 64.0(52.5,70.5)38.5(3.5,79.3)45.0(14.0,74.5)578.0(373.5,903.5)4.5%47.6%31.8%41.4%24.1%58.6%93.1%20.7%6.9%10.3%3.4%34.5%17.2%34.5%37.9%72.4%29 26 28 29 29 29 29 29 29 29 29 29 29 26 29 28 1 10 7 12 7 17 27 6 2 3 1 10 5 10 11 21 0.053△1.000 0.299 0.756 0.419 0.490 0.212 0.174 0.091△0.156 0.938 0.279 0.725 0.425 0.000*0.039*0.679 0.557 0.905 0.036*0.122 0.032*0.002*0.409 0.856 1.000 0.722 0.623 0.070△0.356 0.180 0.018*
2.2.2 CMV 感染状态的基线特征与基线CD4+T计数及增长的亚组分析阳性CMV 血症组基线CD4+T计数、96周CD4+T计数低于阴性CMV血症组(P=0.008,P=0.020)。CMV IgM >18 U/mL组基线CD4+T计数高于CMV IgM <18 U/mL组(P=0.031),而两组96 周CD4+T 计数差异无统计学意义。CMV IgG >22 AU/mL 组与CMV IgG <22 AU/mL 组基线CD4+T 计数、96 周CD4+T 计数差异无统计学意义。CMV 视网膜炎组基线CD4+T 计数低于无CMV视网膜炎组(P=0.024),而两组96周CD4+T计数差异无统计学意义。抗CMV治疗组与未抗CMV治疗组基线CD4+T 计数、96 周CD4+T 计数差异无统计学意义。CMV 感染组与CMV 未感染组基线CD4+T计数、96周CD4+T计数差异无统计学意义(表2)。

表2 基线的CMV 感染状态与基线及96 周CD4+T 计数的分析Tab.2 Baseline CMV infection status and baseline or 96 weeks CD4+T counts analysis
2.3 ART后96周SIR的基线危险因素将单因素分析中P<0.1 的以下9 个因素:包括年龄≥50 岁、基线CD4+T 计数<100 个/μL、基线CD8+T 计数>800 个/μL、基线CMV DNA >500(copies/mL)、PCP、WHO 临床分期Ⅳ期、CMV 视网膜炎、总胆红素>17.1 μmol/L、CMV 感染代入多因素Logistic 回归模型中,采用向前LR 法,结果显示:年龄≥50 岁、基线CD4+T 计数<100 个/μL 是ART 后96 周SIR 相关基线危险因素(表3)。
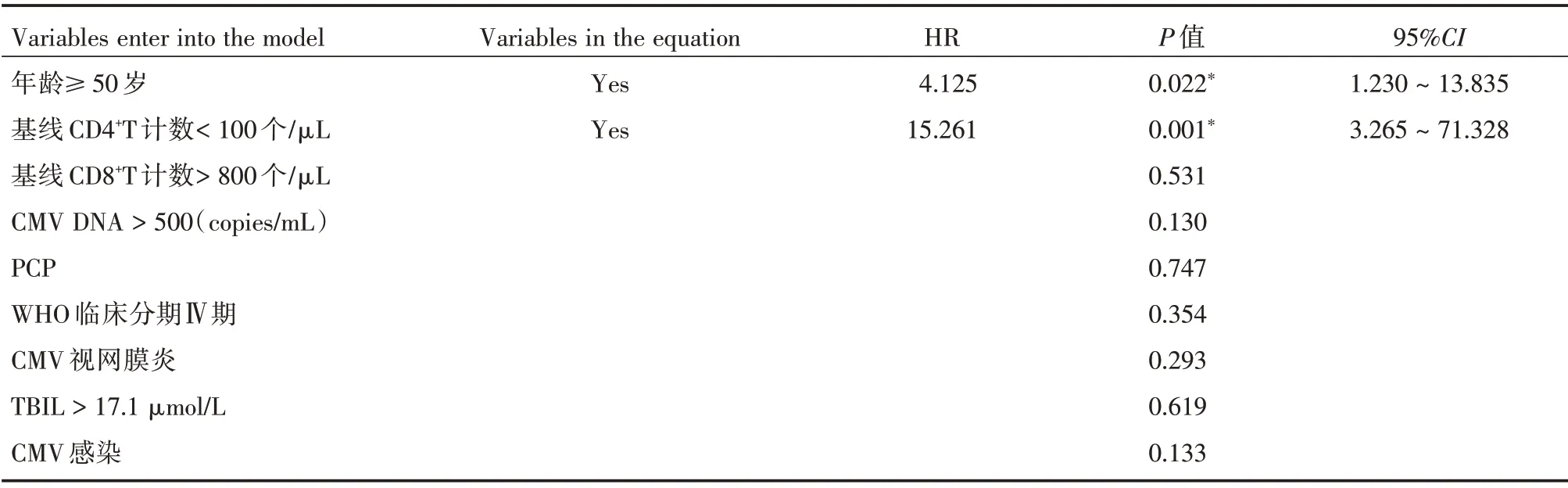
表3 ART 后SIR 基线危险因素Tab.3 Baseline risk factors corrrelated with SIR post-ART
3 讨论
艾滋病患者的SIR 机制尚未明确,但胃肠道微生物易位、共感染、炎性介质等是重要原因。CMV感染增加远期非AIDS 相关的病死率[5]。本研究发现:基线CD4+T 计数<100 个/μL 与ART 后96 周的SIR 有关。MANAYE 等[6]研究显示,大多数治疗前CD4+T 计数<200 个/μL 的患者,ART 后无法达到良好免疫重建。而SMITH 等[7]研究显示,ART 前CD4+T 计数<100 个/μL 对长期免疫重建没有影响,最终40%患者CD4+T 细胞计数能够超过500个/μL。本研究发现:年龄≥50 岁与ART 后96 周SIR 有关,与前期报道一致。SIR 的现象更容易出现在老年HIV/AIDS 患者[8]。
本研究发现:基线CMV 感染状态与ART 后96周的SIR 无关。关于CMV IgG 水平,前期文献证实:高水平CMV IgG 对ART 后的免疫重建有不良影响[9]。本研究中高水平CMV IgG 并不与ART 后免疫重建相关,分析原因如下:本研究中发现约10%的病例尽管存在CMV 血症,却缺乏CMV 的血清学抗体,可能与本研究均入组的是艾滋期患者,存在严重细胞免疫缺陷与体液免疫缺陷,这与部分前期文献不同[10]。关于抗CMV 治疗,前期文献报道抗CMV 治疗可以促进ART 后HIV 患者的CD4+T 细胞增长[11],而本研究中抗CMV 治疗与免疫学重建不良的发生并不相关,分析原因如下:本研究是回顾性研究,采用的标准以是否接受了抗CMV 药物至少7 d 作为标准;而既往文献是在患者CMV DNA 阳性的基础上分为抗CMV 治疗组与非抗CMV 治疗组[11],一些文献仅针对外周血CMV DNA 高载量患者(大于5 000 copies/mL)给予抗CMV 治疗[12]。关于CMV 病毒血症,近年文献报道:活动性CMV 血症预示着不良预后表现为增加了机会性感染的发生[24]。但也有不同报道:CMV病毒血症对HIV 患者的CMV 器官损害以及远期生存率有影响,是因为高水平的CD8+T 计数导致了更低的CD4/CD8 比率[13]。本研究中CMV 病毒血症与免疫学重建不良的发生并不相关,分析原因如下:(1)采用CMV 血症的标准存在差异,不同的研究分别以CMV DNA 大于250、500、1 000 copies/mL为CMV 病毒血症定义,本研究是以500 copies/mL为定义。(2)样本量偏小可能导致数据存在偏倚,需要大样本研究。(3)免疫学重建不良的定义不同,部分研究是按照随访时间点的CD4+T 计数增长数,而本研究是按照观察时间点96 周的CD4+T 计数。(4)观察时间点也不一致,不同文献观察时间点分别48 周、96 周、5年,因此需要区分短期与长期研究结果的差异。关于基线CMV 感染状态的亚组分析,阳性CMV 血症组基线及96 周CD4+T 计数均低于阴性CMV 血症组,提示基线CMV 血症的存在是细胞免疫缺陷更加严重的标志。本研究发现:基 线HIV RNA 水平与ART 后96 周 的SIR 无关。但既往认为基线HIV RNA 水平对免疫重建有不良影响。本研究数据部分缺失,随访时间点不同,可能造成结果不一致。
本研究首次全面地针对艾滋期患者基线各种CMV 感染状态与SIR 的相关性进行研究,数据真实可靠。但仍有不足之处:样本量偏小、随访时间短、个别患者存在某个指标的部分随访数据不完整、抗病毒治疗方案不同、缺乏ART 后CMV 感染各项指标的动态变化监测。
综上所述,CMV 感染是影响HIV/AIDS 患者预后的重要因素,其对SIR 的影响目前尚未明确。本研究得出基线的年龄≥50 岁及基线CD4+T 计数<100 个/μL 是ART 后96 周SIR 的基线危险因素,及早开始ART 治疗是预防SIR 的关键。虽然在本研究中,基线CMV 感染状态均不是SIR 危险因素,这可能与不同研究背景有关。近期研究发现了CMV 复制在肠道免疫调节、肠粘膜炎症、微生物易位、肠黏膜上皮功能受损方面的作用[14-15],需要进一步研究CMV 感染与SIR 相关性的分子生物学机制,寻求未来的靶向治疗。

