新型冠状病毒抗体检测在疑似病例排查中的应用研究
高会霞,李雅楠,刘玉珍,黄 颖,许 怡,张 志,郭 云,卢建华,李 力,王瑜玲,江 平,戴二黑
2019新型冠状病毒肺炎是新发急性呼吸道传染病,目前仍在全球范围内大流行。我国的疫情已基本得到控制,目前监测重点是疑似和高危人群的筛查以及境外输入病例,及早发现、及时控制传染源是疫情防控的关键。病毒核酸检测是最早应用于确诊新型冠状病毒感染的实验室检测方法[1-2]。但是,由于核酸检测采样等问题容易出现假阴性结果,抗体检测是核酸检测的有效补充。基于特异性免疫球蛋白M(Ig M)和免疫球蛋白G(IgG)抗体的血清免疫学检测是临床实验室常用的病原体感染检测方法[3]。国家卫生健康委发布的《新型冠状病毒肺炎诊疗方案(试行第8版)》中将抗体血清学检测纳入确诊病例辅助诊断标准。但是,由于抗体免疫学检测性能与检测原理密切相关,不同检测原理、不同工艺方法的检测试剂检测性能具有较大的差异,因此,深入评价和了解不同原理抗体检测试剂的性能,针对新冠疑似病例建立一套包含抗体检测的高效排查策略,快速准确的识别可能的感染人群、减少因核酸检测阴性而漏检,从而更好的控制传染源,也是疫情防控工作重点之一。本研究以隔离点76例被隔离观察的核酸检测阴性的疑似病例为研究对象,以隔离期不同时间点血清微量病毒中和抗体试验以及3种基于不同原理开发的新冠抗体检测方法,结合影像学等检查,综合判断疑似病例中确诊病例和排除病例的可能性,提出一套对疑似病例快速排查的抗体检测策略和方案。
1 材料与方法
1.1 研 究 对 象 本 研 究 选 取2020年4月1日 至2020年5月28日期间,因隔离点检测2019-nCo V血清Ig M特异性抗体阳性,转入石家庄市第五医院进行隔离观察的76例新冠疑似病例为研究对象。疑似病例的一般临床资料、流行病学资料和辅助检查资料通过电子病历系统获得。本研究遵守国际协调理事会临床试验规范和赫尔辛基宣言,经石家庄市第五医院医学伦理管理委员会批准实施(批准号:2020006)。
1.2 标本收集 在新冠疑似病例入院隔离的第1、7、14 d采集病例空腹静脉血5 m L,置于干燥的无抗凝剂的真空负压采血管内,室温静置30 min,2 500 r/min离心10 min,收集血清于无菌螺口塑料管中。同期采集患者鼻咽拭子标本,将拭子头浸入含病毒保存液的专用样本保存管中,弃去尾部,旋紧管盖。所有样本采集均严格按照要求进行。
1.3 2019-nCo V血清学检测 磁微粒化学发光法(CMIA法)2019-nCo V总抗体检测使用新型冠状病毒(2019-nCo V)抗体检测试剂盒(厦门万泰凯瑞生物技术有限公司,国械注准20203400198);直接化学发光法(CLIA法)2019-nCo V Ig M/IgG抗体检测使用新型冠状病毒2019-nCo V Ig M抗体检测试剂盒(国械注准20203400769)和新型冠状病毒2019-nCoV IgG抗体检测试剂盒(国械注准20203400770)(深圳亚辉龙生物科技股份有限公司);胶体金法(GICA法)2019-nCo V Ig M/IgG抗体检测使用新型冠状病毒(2019-nCo V)Ig M/IgG抗体检测试剂盒(唐山英诺特生物技术有限公司,国械注准20203400177)。所有操作步骤均严格按照厂家说明书进行。
微量病毒中和抗体试验:先进行假病毒包装和假病毒滴定,然后将患者血清倍比稀释,浓度梯度为1∶20、1∶40、1∶80、1∶160、1∶320、1∶640、1∶1 280、1∶2 560,并加入到96孔细胞培养板,每孔加入50μL 2019-nCo V假病毒颗粒混匀,置于37℃细胞培养箱中孵育1 h,每孔加入100μL h ACE2-hela细胞悬液(5×105个/m L),5% CO2培养48 h。与此同时,分别设置血清对照组、病毒对照组和正常细胞对照组。弃去培养基,每孔加入50μL荧光素酶检测试剂,室温避光孵育2 min。反应结束后,用移液器将反应孔中的液体反复吹吸6~8次,使细胞充分裂解,从每孔中吸出35μL液体,加入对应96孔化学发光检测板中,置于化学发光检测仪中,测定荧光值。计算中和抑制率(Inhibition dilution,ID),抑制率=[1-(样品孔的发光强度均值-正常细胞对照孔发光强度均值)/(病毒对照孔的发光强度VC均值-正常细胞对照值孔发光强度均值)]×100%。利用Graphpad prism软件计算ID50。ID50对应的血清稀释度即为该血清的中和抗体效价。当中和抗体效价≥1∶20即为阳性反应,<1∶20为阴性反应。
1.4 2019-nCo V核酸检测 采用荧光RT-PCR技术,核酸提取、扩增试剂盒和全自动核酸提取仪来自中山大学达安基因股份有限公司,7500型荧光PCR仪购自美国Thermo Fisher公司。所有操作步骤均严格按照厂家说明书进行。
1.5 类风湿因子检测 采用类风湿因子(rheumatoid factors,RF)测定试剂盒(胶乳凝集法)(上海捷门生物技术有限公司)。所有操作步骤均严格按照厂家说明书进行。
1.6 统计学方法 资料比较采用卡方检验或Fisher确切概率检验,不同检测方法的比较采用配对四格表χ2检验。所有假设检验均为双侧检验,检验水准α=0.05。
2 结 果
2.1 研究对象基本信息 在76例疑似病例中,男性43例(57.1%),女性33例(42.9%)。患者平均年龄为40.3岁,其中40~60岁占比最大,为46.8%,其次为20~40岁,占39.0%。54例(71.1%)患者无合并症,22例(28.9%)患者存在合并症,其中以过敏性疾病(10.5%)和自身免疫性疾病(3.9%)最多见。流行病学调查结果显示,50例(65.8%)患者近期有武汉地区旅居史,9例(11.8%)为境外回国人员,3例(3.9%)为新冠感染者密切接触者,共62例病例有明确的流行病学史。所有病例Ig M抗体初次检测阳性,并有发热、乏力、咳嗽等新冠肺炎相关临床表现;其中73例病例早期白细胞总数正常或降低,75例病例淋巴细胞计数正常或减少;经CT检查73例无影像学改变,3例有多发条索等新冠肺炎影像学特征。76例病例符合《新型冠状病毒肺炎诊疗方案(试行第八版)》中疑似病例判断标准(表1)。
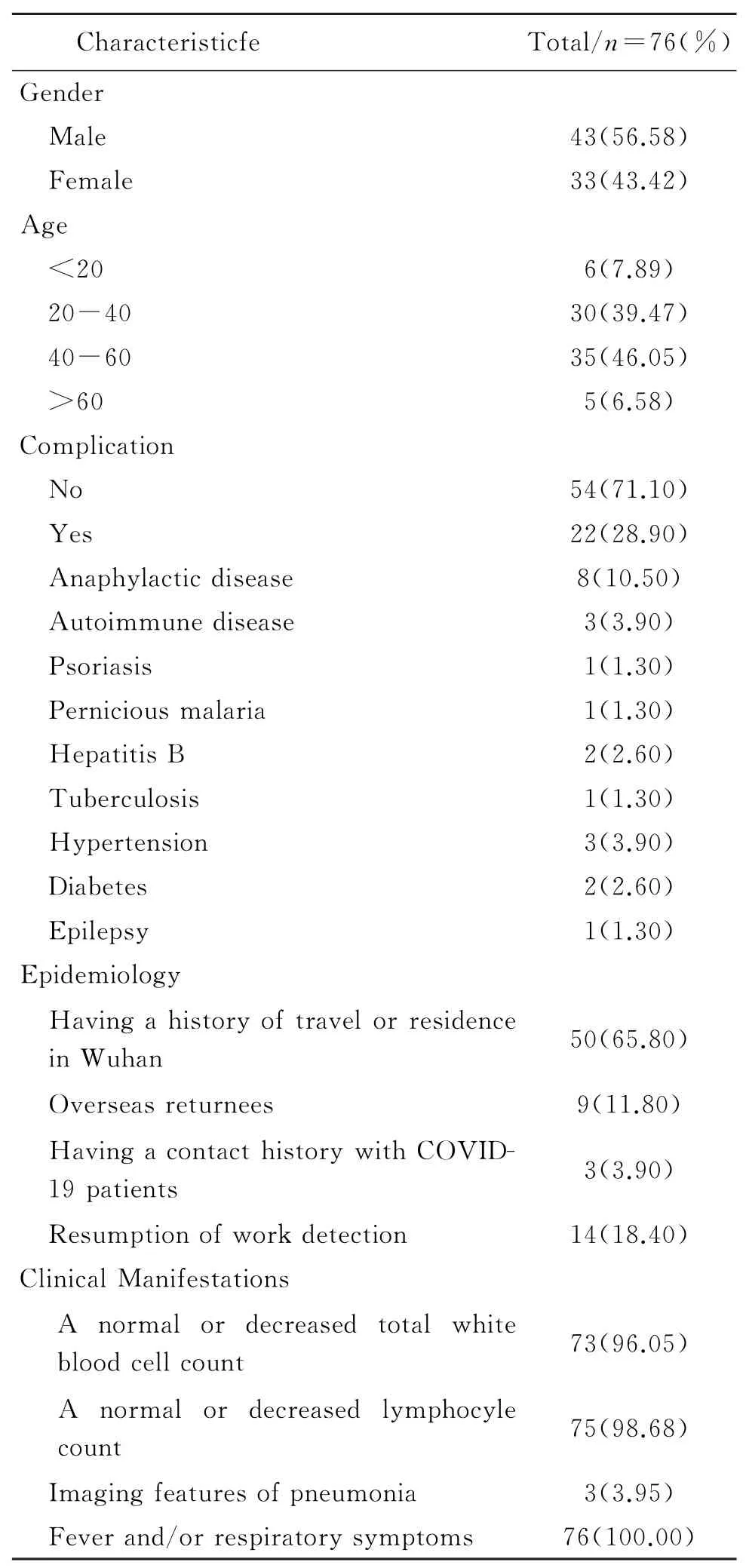
表1 新冠疑似病例一般资料及流行病学资料(n=76)Tab.1 Characteristics of IgM antibody positive suspected cases
在76例疑似病例中,类风湿因子均呈阴性反应,3例(3.9%)出现白细胞升高,4例(5.2%)C反应蛋白(C reaction protein,CRP)升高,1例(1.3%)降钙素原(Procalcitonin,PCT)升高,所有病例入院第1、7、14 d鼻咽拭子核酸检测结果均为阴性。
2.2 疑似病例中3例判定为确诊病例 通过CT检查、临床症状、微量病毒中和抗体试验以及3种不同抗体检测试剂检测结果,76例疑似病例中,有3例病例CT检查出现多发条索等影像学改变,中和抗体在入院隔离第1 d和第14 d均为阳性,CLIA检测IgG和CMIA检测总抗体在第1、7、14 d均为阳性(表2),均有武汉地区旅居史。病例1 GICA试剂检测出现IgG阴转阳的现象,是确诊病例的标志;病例2和病例3 IgG抗体CLIA试剂检测值从隔离第1 d至第14 d分别上升2.16倍和3.15倍,虽然未达到急性感染期4倍升高的标准,但是在病毒感染的中晚期IgG水平也呈持续上升的状态,并且由于中和抗体检测持续强阳性,因此,即使这3例疑似病例在隔离过程中核酸检测持续阴性,综合CT检查结果、流行病学史、中和抗体和3种抗体检测结果,这3例疑似病例判断为确诊病例。这3例病例中有2例CLIA法和GICA法检测Ig M阴性、IgG阳性,1例CLIA法Ig M弱阳性、IgG阳性,提示这3例病例可能在入院前已经处于病毒感染后期,所以核酸检测一直呈阴性。
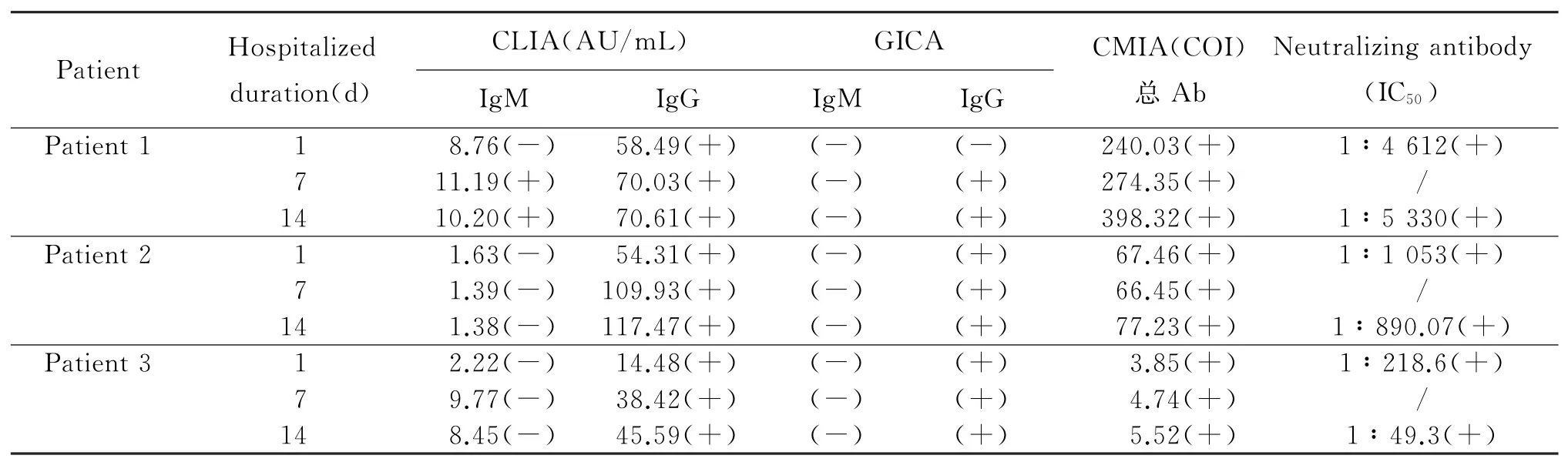
表2 3例确诊病例的血清抗体检测结果Tab.2 Serum antibody test results of 3 confirmed cases
2.3 疑似病例中73例判定为排除病例 76例病例中,除上述3例判定为确诊病例外,其余73例病例经CT检查无影像学改变,血清中和抗体检测在入院第1 d和第14 d均为阴性,核酸持续阴性,综合抗体检测结果判定为排除病例。这73例情况具体如下:①40例疑似病例入院所有时间点、所有试剂检测Ig M、IgG、总抗体均为阴性,判断为排除病例,入院前Ig M初次检测为假阳性。②30例疑似病例入院后一个以上时间点、一个以上试剂出现Ig M检测阳性,但所有时间点两种试剂IgG检测阴性,总抗体阴性,由于14 d内没有IgG转换,同时中和抗体持续阴性,因此判定为排除病例,入院前Ig M初次检测以及入院后Ig M检测为假阳性。③3例疑似病例不同抗体试剂检测结果不一致(表3)。3例疑似病例中,病例5和病例6两个厂家试剂在不同时间点Ig M均检测为阴性,没有出现Ig M和IgG同时阳性,病例5 CLIA、GICA和中和抗体检测结果均为阴性,病例6 CLIA法虽在第7 d和14 d IgG检测为阳性,但检测结果均在阳性判定值(10 AU/m L)附近,为弱阳性,IgG检测值无明显升高,同时GICA法IgG检测为阴性,中和抗体也检测为阴性。虽然病例4入院第1 d和7 d GICA法试剂检测Ig M和IgG同为阳性,但入院第14 d同为阴性,由于通常IgG持续时间长,一般不会在短时间内阴转,且不同时间点总抗体和中和抗体检测均为阴性,并且CLIA法检测IgG阳性值均在阳性判断值(10 AU/m L)附近。因此,结合CT检查和核酸阴性结果,综合判定这3例病例抗体检测为假阳性,疑似病例为排除病例。

表3 3例排除病例的血清抗体检测结果Tab.3 Serum antibody test results of 3 excluded cases
2.4 3种不同原理的抗体试剂检测结果比较 在3例确诊病例中,CLIA法Ig M或IgG检测以及CMIA法总抗体检测在入院后的第1、7和14 d共9次检测均为阳性,检出为9/9(+/+);GICA法Ig M或Ig G检测其中1例入院第1 d为阴性,其他8次检测均为阳性,检出为8/9(+/+),CLIA法和CMIA法检出性能优于GICA法。
在73例排除病例入院第1 d的检测中,CMIA总抗体检测阴性71例,特异性97.26%;CLIA和GICA法Ig M/IgG检测同时阴性均为54例,特异性均为73.97%。
在73例排除病例入院第14 d的检测中,CMIA总抗体检测阴性71例,特异性97.26%;CLIA和GICA法Ig M/IgG检测同时阴性分别为55例和65例,特异性分别为75.34%和89.04%(表4)。

表4 3种不同原理抗体检测试剂与临床诊断结果比较Tab.4 Comparison of three different principles of antibody detection reagents and clinical diagnosis results
3 讨 论
目前,2019新型冠状病毒肺炎仍在全球范围内大流行。据世界卫生组织(WHO)统计,截至2021年2月12日,全球2019新型冠状病毒感染确诊病例超过1亿人,累计死亡病例达237万。庞大的感染人群和超强的传染性对全球医疗卫生系统带来巨大压力和新的挑战。我国的疫情防控取得阶段性重要成果,目前的监测重点是高风险人群以及入境人员筛查,及早发现、及时控制传染源是疫情防控的关键。病毒核酸检测是最早应用于确诊新型冠状病毒感染的实验室检测方法。核酸检测具有快速、灵敏等优点。但是,核酸检测对实验室和人员的要求较高,并且会受到病程、标本采集、检测过程、检测试剂等多因素影响,往往需要多次采样才能达到确诊目的[4-5]。据统计,新型冠状病毒肺炎确诊病例的核酸检测阳性率在30%~50%之间[6],且不同实验室检测结果存在差异。在《新型冠状病毒肺炎诊疗方案(试行第8版)》的诊断标准中,将“血清学检测”作为确诊依据,即疑似病例“新型冠状病毒特异性Ig M抗体和IgG阳性”或“新型冠状病毒特异性IgG抗体由阴性转为阳性或恢复期较急性期4倍及以上升高”也可确诊[7],并将Ig M抗体阳性并具有相关临床症状或流行病学史作为疑似病例的诊断标准。很多隔离点采用胶体金法Ig M检测试剂进行疑似病例筛查,由于隔离点一般是基层检验人员,大部分采用的胶体金检测法,不同厂家试剂盒的检验性能存在一定的差异并且胶体金Ig M检测普遍特异性不高,结果判读依靠肉眼观察反应条带显色,受检测人员个人能力和主观因素影响较大,容易出现假阳性结果,对Ig M初检阳性的疑似病例统一转入定点医院隔离观察,使定点医院有限的医疗资源难以合理分配,并对Ig M阳性疑似病例个人和社会产生巨大心理压力。
本研究以76例因2019-nCo V Ig M抗体阳性转入定点医院进行隔离观察的疑似病例为研究对象,综合临床症状、CT检查、中和抗体检测以及3种不同原理抗体检测试剂对疑似病例是否是确诊或排除病例进行判定,并探讨不同血清学抗体检测方法的准确性,提出抗体检测在疑似病例排查中的应用策略。研究发现,76例疑似病例中,通过综合分析只有3例可以判断为确诊病例,其余73例均判断为排除病例。值得注意的是,疑似病例入院第1 d采用统一的抗体检测试剂复查结果显示,70%以上的患者血清学检测呈Ig M/IgG双阴性或总抗体阴性,提示这76例患者在隔离点进行的2019-nCo V Ig M抗体入院前检测中存在较大比例的假阳性。由于试剂本身阳性判断值原因,或者体内存在干扰物质(类风湿因子、嗜异性抗体、补体、溶菌酶等),或者标本原因(标本溶血、标本被细菌污染、标本贮存时间过长、标本凝固不全等),抗体检测可能会出现假阳性。本研究对76例疑似病例进行了血清类风湿因子检测,结果均为阴性,可排除类风湿因子对结果的干扰,提示可能是隔离点Ig M初检使用的试剂采用的胶体金方法学、间接法检测原理等其他因素导致隔离点Ig M抗体检测呈阳性反应。
对比3种不同原理市售抗体试剂与临床综合判断结果显示,CMIA法检测总抗体和CLIA法检测Ig M/IgG法对确诊病例的检出能力最好,对3例确诊病例不同时间点采集的样本均能检出,CMIA法检测总抗体和CLIA法检测Ig M/IgG对73例排除病例的检测特异性分别为97.26%和73.97%,CLIA法检测Ig M/IgG对3例确诊病例不同时间点采集的9份样本可检出8份,对73例排除病例的检测特异性为73.97%,Ig M/IgG单独检测的特异性显著低于CMIA法检测总抗体,假阳性反应大部分为Ig M检测。从方法学上分析,总抗体检测采用的是双抗原夹心法,而Ig M/IgG单独检测的原理为捕获法和间接法,双抗原夹心法检测过程中只有抗体分子的两个Fab臂分别结合到包被抗原和标记抗原才能被检出,能够降低杂蛋白的非特异性干扰。另外,从被检测物分析,总抗体检测能够同时检测Ig M、IgG和Ig A等多种抗体类型,能够明显提高检测的灵敏度。在对重点人群开展抗体检测排查疑似病例时,由于双抗原夹心法检测总抗体具有高灵敏度和特异性,并且只需要检测一个测试,出结果快速准确。因此,先检测总抗体,出现阳性结果时再检测Ig M/IgG,将有效避免Ig M检测假阳性高的问题,最大化提高排查效率。
2019-nCo V核酸检测存在一定的假阴性率,血清抗体检测假阳性率高。如何将核酸检测和血清学检测有效结合起来,做到准确筛查、精准防控,成为影响新冠肺炎疫情防控工作值得关注的问题。基于此,我们提出针对疑似病例和高危人群的2019-nCo V感染筛查路径(图1):针对重点人群筛查,应首先进行2019-nCo V核酸检测,若核酸检测阳性,收住入院隔离;若核酸检测阴性,则检测血清总抗体。若血清总抗体阳性,则需要进行至少2次以上连续核酸检测(采样时间至少间隔24 h),若核酸阳性,收住入院隔离;若核酸阴性,进行血清学Ig M/IgG抗体检测。若Ig M抗体阳性,无论IgG抗体阴性或阳性,提示急性期或感染期;若Ig M抗体阴性,IgG抗体阳性,应观察IgG抗体滴度变化,如出现4倍及以上升高,则为急性感染;如滴度升高小于4倍,则为既往感染。若血清总抗体阴性,排除新冠感染,必要时选择另外一种试剂复检。

图1 新型冠状病毒感染高危人群临床筛查策略Fig.1 Clinical screening strategies for people at high risk of new coronavirus infection
利益冲突:无
引用本文格式:高会霞,李雅楠,刘玉珍,等.新型冠状病毒抗体检测在疑似病例排查中的应用研究[J].中国人兽共患病学报,2021,37(12):1102-1107,1134.DOI:10.3969/j.issn.1002-2694.2021.00.160

