不同配伍比例麻黄-桂枝药对单煎与合煎化学成分对比分析
鲁 云,刘佩仪,徐 杰,邝 敏,陈巧华,梁志毅,程钰洁,魏 梅
(广东一方制药有限公司/广东省中药配方颗粒企业重点实验室,广东 佛山 528244)
中药配方颗粒是以单味中药饮片为原料,利用现代化工业技术精制而成,仅供临床调剂用的纯中药制剂,不仅具有免煎、易携带、服用方便等优点,同时保留了传统汤剂辨证施治、随证加减、复方配伍的特色[1-2]。近年来,关于中药配方颗粒“单煎合用”与传统汤剂“群药合煎”物质基础的一致性一直是大众比较关心的问题[3-4]。药对源于中医临床实践,系指通过相对固定的组合形式形成配伍单位而发挥综合效应的两味中药[5]。与经典方剂相比,药对也符合七情配伍理论,且仅有两味药,大大降低了多种药物复杂化学成分的干扰,可以实现以点带面的降维研究[6]。通过对比药对单煎与合煎的化学指纹图谱,可较为直观的反映二者整体物质基础的差异性。麻黄-桂枝药对来源于《伤寒论》中的麻黄汤,是发汗解表之峻剂[7]。本研究以不同配伍比例的麻黄-桂枝药对为例,进行单煎与合煎化学成分的对比分析,以期为单味中药配方颗粒合用与群药合煎的化学成分一致性研究提供参考。
1 材料与方法
1.1 仪器与试药
H-Class 型UPLC 仪(美国沃特世公司);Milli-QDirect 型超纯水系统(德国Merck 股份有限公司);ME204E 型万分之一天平(瑞士梅特勒-托利多公司);JJ3000B 型百分之一天平(常熟市双杰测试仪器厂);B-290 型喷雾干燥机(瑞士步琪有限公司);DLSB-5L/20 型低温冷却液循环泵(巩义市予华仪器有限责任公司);YRE-501 型旋转蒸发仪(巩义市予华仪器有限责任公司);KQ-700DE 型数控超声波清洗器(昆山市超声仪器有限公司)。
盐酸麻黄碱(批号:171241-201508,纯度为99.8%)、盐酸伪麻黄碱(批号:171237-201208,纯度为99.9%)、肉桂酸(批号:z110786-201604,纯度为98.8%)对照品均购自中国食品药品检定研究院;甲醇、乙腈(德国Merck 股份有限公司,色谱级);磷酸(天津市科密欧化学试剂有限公司,色谱级);其余试剂均为分析纯,水为超纯水。
10 批麻黄药材分别购自内蒙古吉隆生态科技有限责任公司(批号:2005017)、国药集团冯了性(佛山)药材饮片有限公司(批号:2003031、2003032、2003033)、内蒙古泰润药业有限公司(批号:1806023、1808024、1812013)、内蒙古亿利甘草有限公司(批号:1906041、1908003)、甘肃药材有限公司(批号:1911045);10 批桂枝药材分别购自广西南药药业有限公司(批号:2002019、2001021、2001016、2004054)、肇庆市高要区绿福农业种植专业合作社(批号:2006006、2001007)、广州市药材公司中药饮片厂(批号:2002001)、四川天雄药业有限公司(批号:2008036、2009011、2009005)。所有药材均经广东一方制药有限公司魏梅主任药师鉴定为正品。
1.2 方法
1.2.1 麻黄-桂枝药对样品的制备 精密称取麻黄/桂枝饮片适量,分别加水煎煮两次,煎液滤过,减压浓缩,喷雾干燥,即得麻黄、桂枝单煎样品。根据麻黄、桂枝的出膏率(出膏率=浓缩液重量×含固率/饮片量×100%)情况,分别按麻黄、桂枝饮片配伍比例(3 : 2、1 : 1、1 : 2、2 : 1)称取单煎样品(膏粉量=饮片量×出膏率),混匀,平行3 份,即得麻黄-桂枝药对单煎样品。
按照麻黄、桂枝饮片配伍比例(3 : 2、1 : 1、1 : 2、2 : 1) 精密称取上述同批次麻黄、桂枝饮片适量,平行3 份,分别加水煎煮两次,煎液滤过,合并两次煎液,减压浓缩,喷雾干燥,即得麻黄-桂枝合煎样品。
1.2.2 供试品溶液的制备 取麻黄-桂枝药对样品适量,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇25 mL,密塞,称定重量,超声处理(功率:250 W,频率:40 kHz)30 min,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,用0.22 μm 微孔滤膜滤过,取续滤液,即得。
1.2.3 对照品溶液的制备 分别取盐酸麻黄碱对照品、盐酸伪麻黄碱对照品、肉桂酸对照品适量,置于同一量瓶中,加甲醇溶解制成质量浓度分别为125.149 2、103.096 8、32.999 2 μg/mL 的混合对照品溶液。另取甲醇溶液作为空白对照溶液。
1.2.4 色谱条件 Waters ACQUITY HSS T3 (2.1 mm ×150 mm,1.8 μm)色谱柱;以乙腈为流动相A,以体积浓度为0.1%的磷酸水溶液为流动相B,梯度洗 脱(0 ~ 10 min,3% ~ 7%A;10 ~ 17 min,7% ~9%A;17 ~ 35 min,9% ~ 10%A;35 ~ 36 min,10% ~17%A;36 ~ 50 min,17% ~ 24%A;50 ~ 70 min,24% ~ 45%A);柱温:35 ℃;流速:0.25 mL/min;检测波长:0 ~ 35 min,波长为210 nm;35 ~ 70 min,波长为280 nm;进样量:1 μL。
1.2.5 统计学方法 用SPSS 20.0 软件进行数据分析,计量资料用均数±标准差(x±s)表示,两组间比较采用t检验。以P< 0.05 为差异具有统计学意义。
2 结果与分析
2.1 方法学考察结果
2.1.1 精密度实验 取同一份供试品溶液,按“1.2.4”项下色谱条件连续进样6 次,以2 号峰(盐酸麻黄碱)为参照峰S,计算各共有峰相对保留时间与相对峰面积的RSD 值均小于3%,表明仪器精密度良好。
2.1.2 重复性实验 取麻黄-桂枝药对样品6 份,按“1.2.2”项下方法制备供试品溶液,按“1.2.4”项下色谱条件测定,以2号峰(盐酸麻黄碱)为参照峰S,计算各共有峰相对保留时间与相对峰面积的RSD 值均小于3%,表明方法重复性良好。
2.1.3 稳定性实验 取同一份供试品溶液,分别于0、2、4、8、16、24 h,按“1.2.4”项下色谱条件进样测定,以2 号峰(盐酸麻黄碱)为参照峰S,计算各共有峰相对保留时间与相对峰面积的RSD 值均小于3%,表明样品在24 h 内稳定性良好。
2.2 指纹图谱的建立
按重量比为1 ∶1 称取10 批麻黄、桂枝饮片,分别按“1.2.1”项下方法制备10 份麻黄-桂枝药对合煎样品,编号S1-S10。分别按“1.2.2”项下方法制备供试品溶液,按“1.2.4”项下色谱条件测定,采集S1-S10 号样品的指纹图谱,并导入“中药色谱指纹图谱相似度评价系统(2012 版)”软件进行数据处理,建立对照指纹图谱R,见图1。各样品与对照指纹图谱R 的相似度分别为0.942、0.952、0.962、0.907、0.983、0.980、0.994、0.980、0.993、0.937,相似度均在0.9 以上,满足指纹图谱研究的要求。建立的麻黄-桂枝药对指纹图谱共标定了11 个共有峰,通过对照品比对,指认了峰2、峰3、峰9 分别为盐酸麻黄碱、盐酸伪麻黄碱、肉桂酸,见图2。
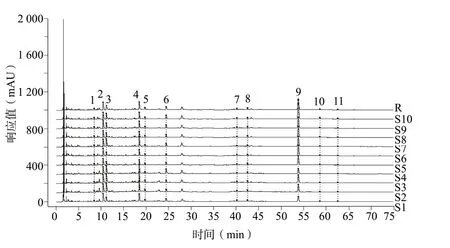
图1 10 批麻黄-桂枝(1 : 1)药对指纹图谱叠图Fig. 1 Fingerprints of 10 batches of Ephedra-Cinnamon(1 : 1)herbal pairs
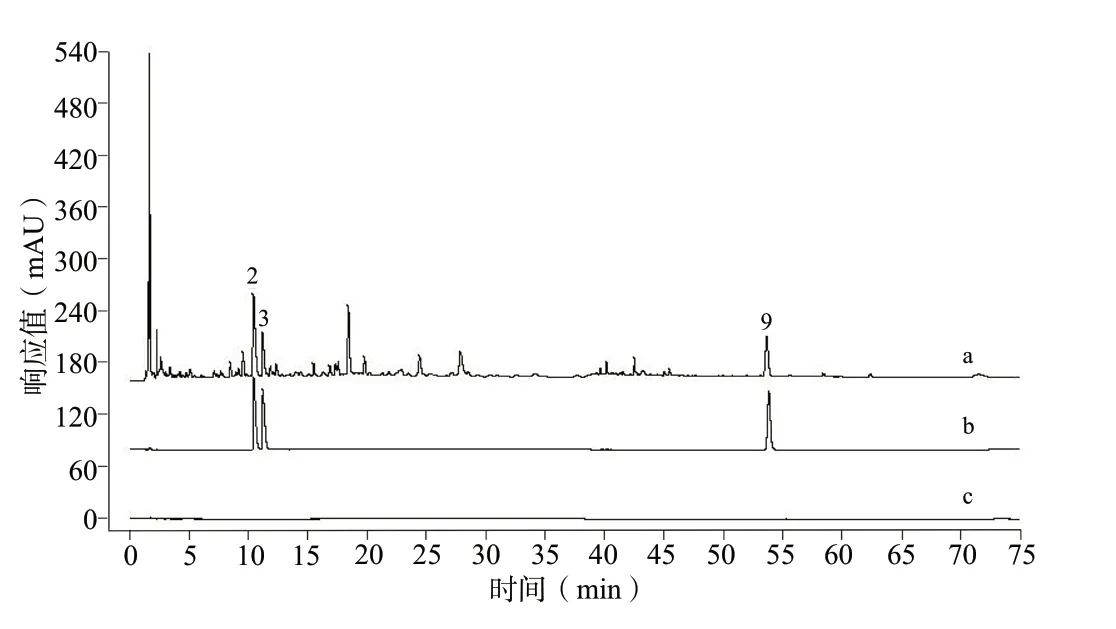
图2 麻黄-桂枝药对指纹图谱特征峰指认Fig. 2 Identification of the characteristic peaks of the fingerprints of Ephedra-Cinnamon herbal pair
2.3 指纹图谱测定与统计学分析
分别按“1.2.1”项下方法制备不同配伍比例的麻黄-桂枝药对单煎与合煎样品,按“1.2.2”项下条件制备供试品溶液,按“1.2.4”项下色谱条件测定,采集各样品的指纹图谱,见图3。

图3 不同配伍比例麻黄-桂枝药对单煎与合煎样品指纹图谱Fig. 3 Fingerprints of Ephedra-Cinnamon herbal pair with different compatibility ratios for single decoction and mixed decoction
计算各样品共有峰的“峰面积/称样量”值,并采用“1.2.5”项下方法进行数据处理与分析,见表1。
结果显示,不同配伍比例麻黄-桂枝药对单煎与合煎样品的指纹图谱均呈现与对照指纹图谱相同的11 个色谱峰,但单煎与合煎样品中各色谱峰的“峰面积/称样量”值存在一定差异。表1 结果表明:(1)4 组不同配伍比例麻黄-桂枝药对单煎与合煎样品峰1、峰4 的“峰面积/称样量”值的差异有统计学意义(P<0.05);峰9、峰10、峰11 的“峰面积/称样量”值的差异无统计学意义(P>0.05)。 (2) 当麻黄、桂枝配伍比例为2 : 1、3 : 2、1 : 1 时,单煎与合煎样品峰6 的“峰面积/称样量”值的差异有统计学意义(P<0.05)。(3)当麻黄、桂枝配伍比例为1 : 1 时,单煎与合煎样品指纹图谱的差异最大,峰1-峰8 的“峰面积/称样量”值的差异有统计学意义(P<0.05)。(4) 4 组不同配伍比例中,有且仅当麻黄、桂枝配伍比例为1 :1 时,单煎与合煎样品峰2(盐酸麻黄碱)和峰3(盐酸伪麻黄碱)的“峰面积/称样量”值的差异有统计学意义(P<0.05)。随着麻黄、桂枝配伍比例的变化,各共有峰“峰面积/称样量”值的变化规律见图4。结果显示,随着麻黄比例的减少,峰1-峰5、峰7-峰8 的“峰面积/称样量”值均呈现下降的趋势,而峰6、峰9、峰10、峰11 均呈现上升的趋势。因此,初步判定峰1-峰5、峰7-峰8 是麻黄中的化学成分,而峰6、峰9 -峰11 为桂枝中的化学成分。
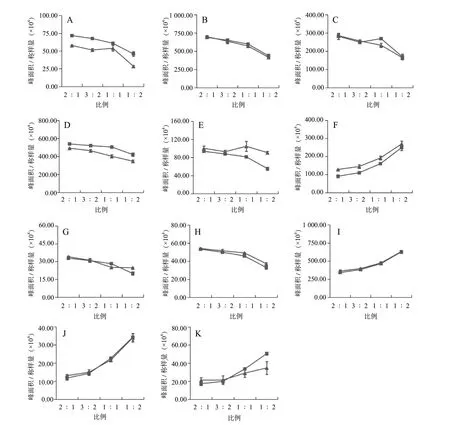
图4 不同配伍比例的麻黄-桂枝药对样品各共有峰“峰面积/称样量”值的变化趋势Fig. 4 Variation trend of the “peak area/sample weight”value of the common peaks of Ephedra-Cinnamon herbal pair with different compatibility ratios
表1 不同配伍比例麻黄-桂枝药对单煎与合煎样品各共有峰“峰面积/称样量”值(±s,n = 3)Tab. 1 The “peak area/sample weight” value of Ephedra-Cinnamon herbal pair with different compatibility ratios for single decoction and mixed decoction(±s,n = 3)
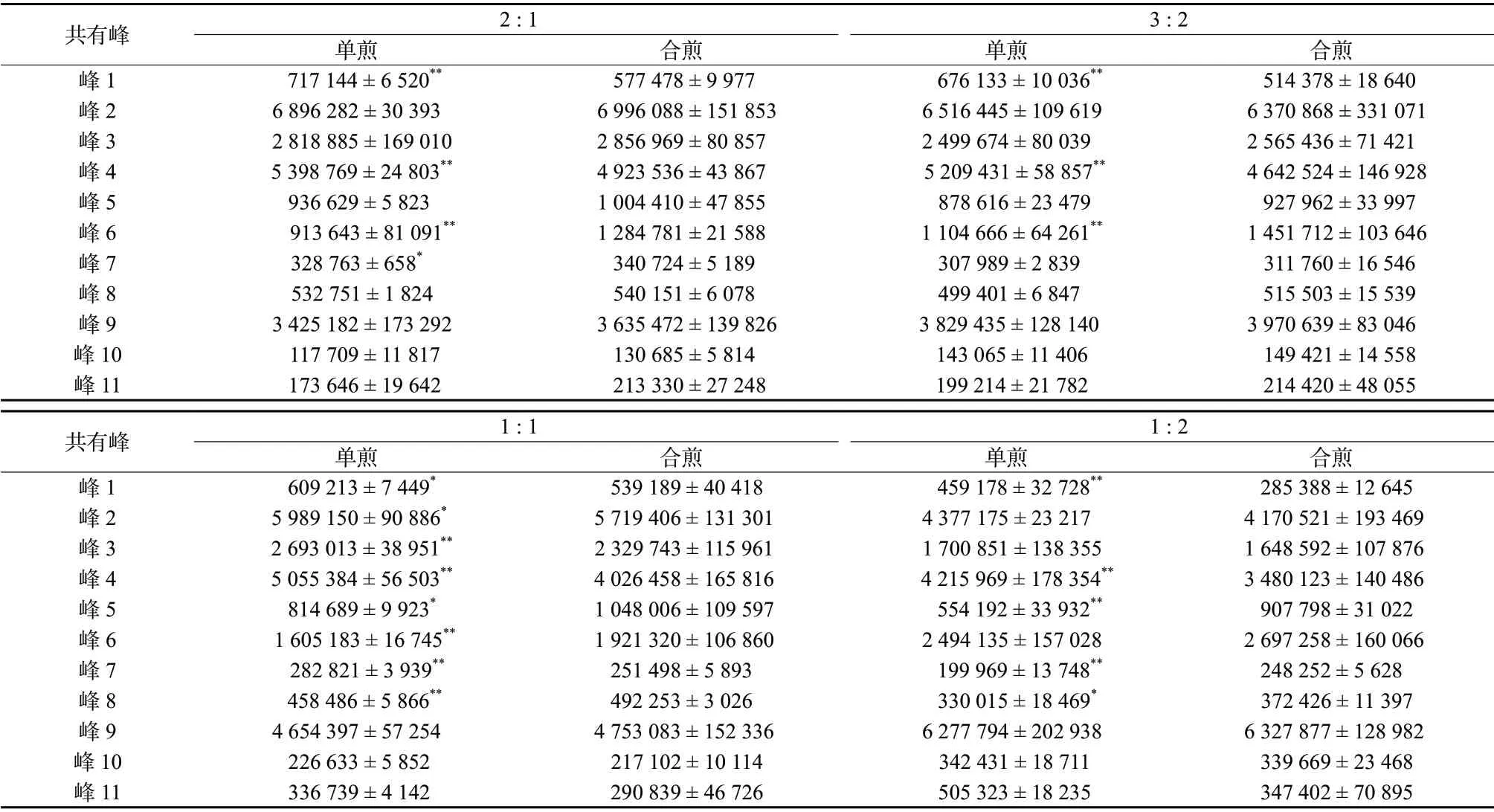
表1 不同配伍比例麻黄-桂枝药对单煎与合煎样品各共有峰“峰面积/称样量”值(±s,n = 3)Tab. 1 The “peak area/sample weight” value of Ephedra-Cinnamon herbal pair with different compatibility ratios for single decoction and mixed decoction(±s,n = 3)
注:不同配伍比例麻黄-桂枝药对单煎与合煎同一共有峰相比,*P <0.05,**P <0.01。
共有峰2 : 13 : 2单煎合煎单煎合煎峰1 717 144 ± 6 520** 577 478 ± 9 977 676 133 ± 10 036** 514 378 ± 18 640峰26 896 282 ± 30 393 6 996 088 ± 151 853 6 516 445 ± 109 619 6 370 868 ± 331 071峰3 2 818 885 ± 169 0102 856 969 ± 80 8572 499 674 ± 80 0392 565 436 ± 71 421峰4 5 398 769 ± 24 803**4 923 536 ± 43 867 5 209 431 ± 58 857** 4 642 524 ± 146 928峰5 936 629 ± 5 8231 004 410 ± 47 855 878 616 ± 23 479 927 962 ± 33 997峰6 913 643 ± 81 091**1 284 781 ± 21 588 1 104 666 ± 64 261** 1 451 712 ± 103 646峰7328 763 ± 658* 340 724 ± 5 189 307 989 ± 2 839 311 760 ± 16 546峰8 532 751 ± 1 824 540 151 ± 6 078 499 401 ± 6 847 515 503 ± 15 539峰9 3 425 182 ± 173 292 3 635 472 ± 139 826 3 829 435 ± 128 1403 970 639 ± 83 046峰10 117 709 ± 11 817 130 685 ± 5 814 143 065 ± 11 406 149 421 ± 14 558峰11 173 646 ± 19 642 213 330 ± 27 248 199 214 ± 21 782 214 420 ± 48 055共有峰1 : 11 : 2单煎合煎单煎合煎峰1 609 213 ± 7 449* 539 189 ± 40 418 459 178 ± 32 728** 285 388 ± 12 645峰2 5 989 150 ± 90 886* 5 719 406 ± 131 3014 377 175 ± 23 217 4 170 521 ± 193 469峰3 2 693 013 ± 38 951** 2 329 743 ± 115 961 1 700 851 ± 138 355 1 648 592 ± 107 876峰4 5 055 384 ± 56 503** 4 026 458 ± 165 816 4 215 969 ± 178 354** 3 480 123 ± 140 486峰5 814 689 ± 9 923* 1 048 006 ± 109 597 554 192 ± 33 932** 907 798 ± 31 022峰6 1 605 183 ± 16 745** 1 921 320 ± 106 860 2 494 135 ± 157 028 2 697 258 ± 160 066峰7 282 821 ± 3 939**251 498 ± 5 893 199 969 ± 13 748**248 252 ± 5 628峰8 458 486 ± 5 866**492 253 ± 3 026 330 015 ± 18 469* 372 426 ± 11 397峰94 654 397 ± 57 254 4 753 083 ± 152 336 6 277 794 ± 202 938 6 327 877 ± 128 982峰10 226 633 ± 5 852 217 102 ± 10 114 342 431 ± 18 711 339 669 ± 23 468峰11 336 739 ± 4 142 290 839 ± 46 726 505 323 ± 18 235 347 402 ± 70 895
3 讨论
麻黄-桂枝药对为常见辛温解表药对,在麻黄汤(麻黄 : 桂枝 = 3 : 2)、小青龙汤(麻黄 : 桂枝 =1 : 1)、桂枝芍药知母汤(麻黄 : 桂枝 = 1 : 2)、麻黄桂枝汤(麻黄 : 桂枝 = 2 : 1)中均有应用,故本研究以上述4 组麻黄、桂枝比例为例,比较单煎与合煎样品中化学成分的差异。结果表明,4 组不同配伍比例麻黄-桂枝药对中,单煎与合煎样品峰1 和峰4 的“峰面积/称样量”值的差异有统计学意义(P<0.05),而峰1、峰4 所表征的化学成分均来源于麻黄,猜测在合煎过程中,桂枝中溶出的某些物质成分与麻黄中的峰1 和峰4 所表征的化学成分发生反应,导致峰1和峰4 的峰面积减小。因此有必要对峰1 和峰4 进行指认,明确其发挥的药理/毒理作用。另外,麻黄、桂枝配伍比例为1 : 1 时,单煎与合煎样品中峰2(盐酸麻黄碱)、峰3(盐酸伪麻黄碱)的“峰面积/称样量”值的差异有统计学意义(P<0.05),而盐酸麻黄碱和盐酸伪麻黄碱是麻黄平喘的主要药效成分[8],此二者含量的差异极可能导致麻黄-桂枝药对单煎与合煎临床药效的差异。
根据各共有峰“峰面积/称样量”值的变化规律可推断峰1-峰5、峰7-峰8 所表征的化学成分来源于麻黄,而峰6、峰9-峰11 所表征的化学成分来源于桂枝。麻黄、桂枝配伍比例为1 : 1 时,单煎与合煎样品中麻黄化学成分含量差异有统计学意义(P<0.05),说明麻黄、桂枝配伍比例为1 : 1 时,对麻黄化学成分的溶出影响较大。4 组不同配伍比例麻黄-桂枝药对单煎与合煎样品峰9、峰10、峰10的“峰面积/称样量”值之间的差异均无统计学意义(P>0.05),说明麻黄、桂枝配伍比例对单煎与合煎样品中桂枝化学成分含量影响不大。
4 结论
本研究建立的麻黄-桂枝药对UPLC 指纹图谱,方法重复性和稳定性良好。通过比较指纹图谱中各共有峰“峰面积/称样量”值,证实了不同配伍比例的麻黄-桂枝药对单煎与合煎样品中部分化学成分的含量存在差异,且麻黄、桂枝配伍比例是影响化学成分差异的重要因素。本研究可为单味中药配方颗粒合用与群药合煎的化学成分一致性研究提供参考。

