BRCA1/2突变状态对乳腺癌患者外科手术方式选择的影响
付芬芬,孙 洁,张冬洁,褚福涛,张 春,张国锋,解云涛,
乳腺癌是严重威胁中国女性健康的恶性肿瘤。据全国肿瘤登记中心统计的数据显示,2015年中国新发乳腺癌30.4 万例,位居女性恶性肿瘤发病率第1 位[1]。家族遗传性乳腺癌的发生与肿瘤易感基因密切相关,其中乳腺癌易感基因(breast cancer susceptibility gene,BRCA)1 和BRCA2 是最重要的2 种BRCA。中国乳腺癌人群的BRCA1/2 突变率为5.3%[2]。BRCA1/2 突变乳腺癌患者的对侧乳腺癌发生风险显著高于散发性乳腺癌人群[3-4]。国外研究报道,BRCA1/2 突变的接受保乳术的患者,其同侧乳腺癌的复发风险相较于无BRCA1/2 突变的乳腺癌患者可增加2 倍左右[5]。鉴于BRCA1/2 突变乳腺癌存在潜在的复发或新发乳腺癌的风险,因此临床上对于BRCA1/2 突变乳腺癌患者的手术方式存在分歧。一方面,临床医师对于保乳术是否安全存在顾虑;另一方面,预防性乳房切除术作为一种有创的干预手段,可使乳腺癌发生风险降低90%以上。北京大学国际医院乳腺外科在国内较早开展了家族遗传性乳腺癌的基因检测和个体化手术治疗。本研究旨在探讨BRCA1/2 突变对乳腺癌人群手术方式选择的影响,以期为家族遗传性乳腺癌人群的临床诊疗提供参考依据。
1 资料与方法
1.1 病例选择标准
病例纳入标准:(1)初次确诊为原发性乳腺癌的住院患者,病理诊断为浸润性乳腺癌或乳腺原位癌;(2)符合BRCA1/2 检测标准,手术之前接受BRCA1/2 检测,并且获得检测结果;(3)完成乳腺癌手术治疗。
病例排除标准:(1)病理诊断为非乳腺癌,或者未确诊;(2)复发或转移性乳腺癌;(3)治疗中断或失访。
1.2 研究对象及资料收集
研究对象为2017 年12 月—2021 年6 月北京大学国际医院乳腺外科收治的符合病例选择标准的130 例原发性乳腺癌患者。
收集患者的临床病理资料,包括发病年龄、乳腺癌和(或)卵巢癌家族史、单侧或双侧乳腺癌、病理类型、组织学分级、肿瘤大小、免疫组织化学结果、治疗前腋窝淋巴结转移情况、是否接受新辅助化疗以及手术方式等。
1.3 BRCA1/2 检测
所有患者均自愿接受BRCA1/2 检测。抽取2 mL 外周静脉血,送至具备检测资质的基因检测机构进行BRCA1/2 检测。
1.4 统计学方法
应用SPSS 25.0 软件进行统计学分析。符合正态分布的计量资料的均数比较采用2 独立样本t检验,计数资料的比较采用Pearsonχ2检验或Fisher 精确概率法。P<0.05 为差异有统计学意义。
2 结果
2.1 BRCA1/2 突变状态与临床病理特征的关系
130 例患者中,BRCA1/2 致病胚系突变率为17.7%(23/130),其 中12 例为BRCA1 致病胚系突变,11 例为BRCA2 致病胚系突变(表1)。130 例患者的平均发病年龄为(44.9±11.4)岁;64 例(49.2%)患者有乳腺癌和(或)卵巢癌家族史;11 例(8.5%)患者为同时性或异时性双侧乳腺癌;56 例(43.1%)患者的肿瘤直径≤2 cm(T 分期为T1期);26 例(20.0%)患者为三阴性乳腺癌;65 例(50.0%)患者治疗前有腋窝淋巴结转移;76 例(58.5%)患者接受新辅助化疗。
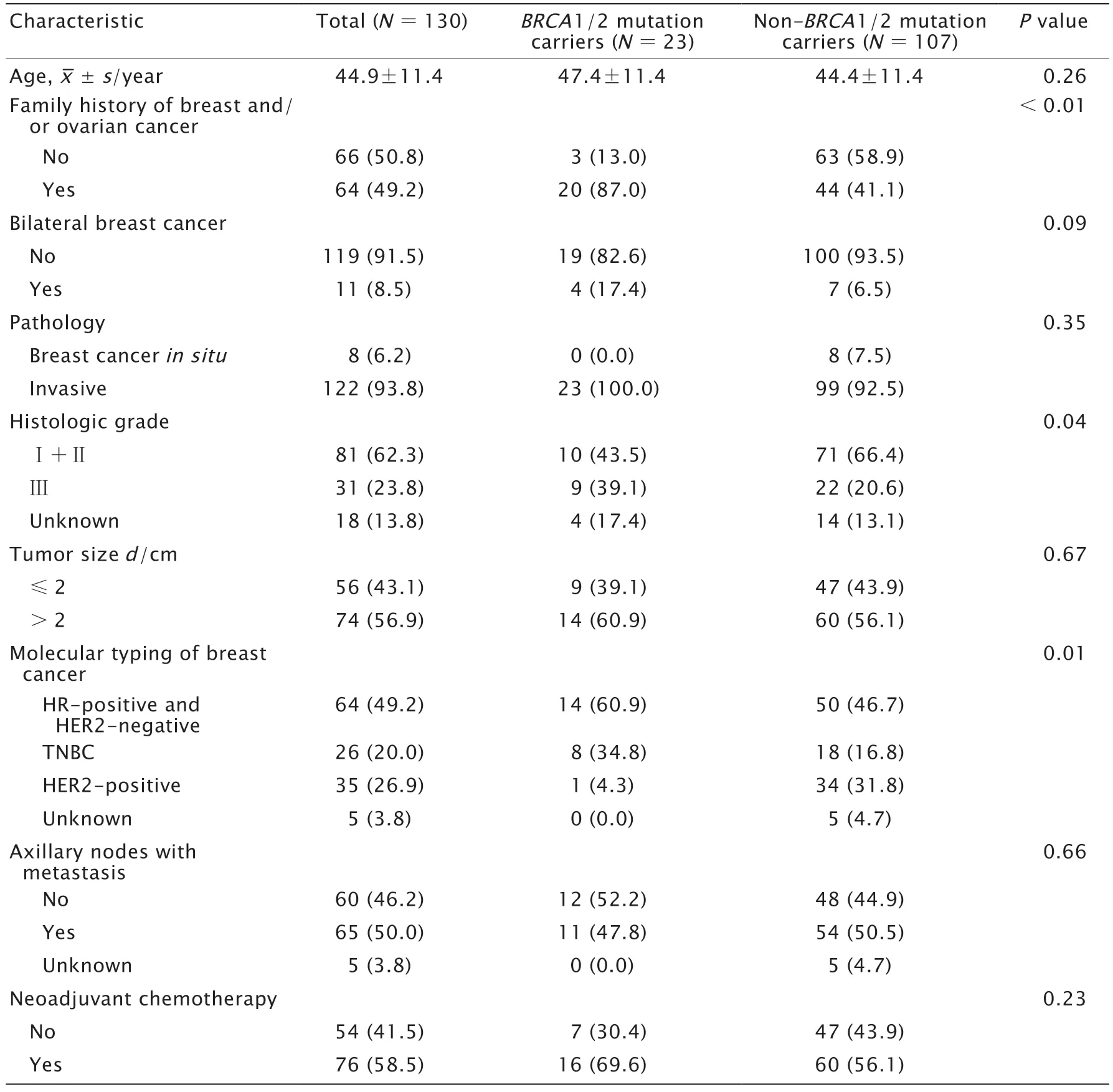
表1 130 例乳腺癌患者的BRCA1/2 突变状态与临床病理特征的关系Table 1 Relationship between BRCA1/2 mutation and clinicopathological features in 130 patients with breast cancer[n (%)]
与无BRCA1/2 致病胚系突变者相比,携带BRCA1/2 致病胚系突变的乳腺癌患者显示出明显的乳腺癌和(或)卵巢癌家族聚集倾向(87.0%vs41.1%),组织学分级更高(Ⅲ级:39.1%vs20.6%),三阴性乳腺癌所占比例也更高(34.8%vs16.8%),差异均有统计学意义(P<0.05);但是发病年龄、单侧或双侧乳腺癌、病理类型、肿瘤大小、治疗前腋窝淋巴结转移情况以及是否接受新辅助化疗与BRCA1/2 突变状态均无显著关联(P>0.05)。
2.2 BRCA1/2 突变状态与选择手术方式的关系
130 例患者中,59 例(45.4%)接受保乳术,60 例(46.1%)接受患侧单纯乳房切除术,11 例接受患侧乳房全切术联合对侧预防性乳房切除术(8.5%)。
BRCA1/2 致病胚系突变携带者与未携带者的手术方式存在显著差异(P<0.01,表2)。23例BRCA1/2 致病胚系突变携带者中,仅5 例接受保乳术,保乳率显著低于未携带者(21.7%vs50.5%);7 例(30.4%)接受患侧单纯乳房切除术,而未携带BRCA1/2 致病胚系突变患者的患侧单纯乳房切除术比例为49.5%;11 例(47.8%)接受患侧乳房全切术联合对侧预防性乳房切除术,而未携带BRCA1/2 致病胚系突变患者均未接受对侧预防性乳房切除术(0.0%)。
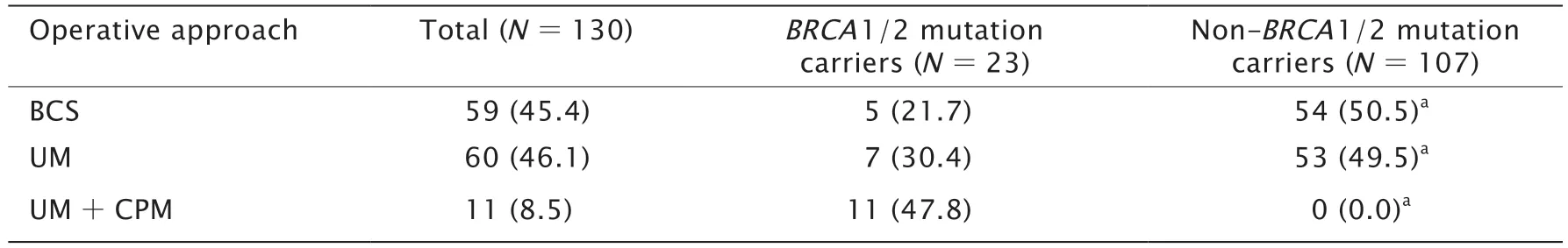
表2 130 例乳腺癌患者的BRCA1/2 突变状态与选择手术方式之间的关系Table 2 Relationship between BRCA1/2 mutation and choice of operative approach in 130 patients with breast cancer[n (%)]
2.3 对侧预防性乳房切除术的治疗情况
接受对侧预防性乳房切除术的11 例患者均为BRCA1/2 致病胚系突变携带者,年龄为41~60 岁,并且均有明确的乳腺癌和(或)卵巢癌家族史。本研究中,对侧预防性乳房切除术的病理检查结果均为阴性。11 例患者中,4例(36.4%)同时接受保留乳头-乳晕复合体的乳房切除术(nipple-areola complex-sparing mastectomy,NSM)联合Ⅰ期假体植入的乳房重建术,其中1 例的伤口出现愈合延迟(约4 个月后愈合),其余3 例均为Ⅰ期愈合,未发现乳头-乳晕坏死、感染、包膜挛缩和假体变形等术后并发症。
3 讨论
随着保乳术和前哨淋巴结活检技术的推广,现代乳腺癌的手术方式趋于将有创最小化。然而,对于携带BRCA1/2 致病胚系突变的乳腺癌患者而言,潜在的“乳腺癌遗传易感体质”让临床医师在制定手术方式时存在顾虑。目前,有关BRCA1/2 突变乳腺癌患者手术方式的系统性研究并不多见。北京大学国际医院乳腺外科自2017 年底开始,在乳腺癌临床诊疗过程中有意识地关注乳腺癌遗传高风险人群,谨慎挑选合适的BRCA1/2 突变患者,对其实施对侧预防性乳房切除术。
本研究发现,BRCA1/2 突变携带者的保乳率显著低于未携带者,提示临床在对BRCA1/2 突变携带者是否选择保乳术时仍存有顾虑。对于一般的乳腺癌人群而言,既往研究已证实保乳术后的长期生存不劣于乳房全切术;在早期乳腺癌患者中,保乳术后的长期生存甚至可能优于乳房全切术[6]。因此,欧美国家一般乳腺癌人群的保乳率可达50%以上。近年来,中国的保乳率也呈上升趋势。然而,保乳术是否适用于有保乳意愿的BRCA1/2 突变携带者,却一直存在争议。目前有关BRCA1/2 突变患者保乳术后局部控制率的研究尚未得出一致的结论。尽管一些随访时间已超过7 年的研究显示,BRCA1/2 突变携带者接受保乳术后,其同侧乳腺癌的复发风险呈持续升高趋势,但是近年来的研究却认为同侧乳腺癌事件的增多主要归因于同侧的新发事件,而非真正的同侧复发事件[7-8]。更重要的是,BRCA1/2 突变状态并没有显著影响保乳术后的总生存和远处转移生存,BRCA1/2 突变患者接受乳房全切术后与接受保乳术后的总生存和乳腺癌特异生存的差异均无统计学意义[7,9]。另一方面,术后放疗并没有额外增加BRCA1/2 突变患者的放疗相关不良反应[10]。本中心的一项大样本回顾性研究对187 例BRCA1 突变患者和304 例BRCA12 突变患者在接受保乳术、乳房全切术或乳房全切术联合术后放疗后进行中位随访7.5 年,结果发现无论是生存结局还是同侧乳腺癌复发事件,差异均无统计学意义(P>0.05)[11]。
无论接受何种手术方式,BRCA1/2 突变患者与散发性乳腺癌患者相比,其对侧乳腺癌的发生风险显著增加。BRCA1 和BRCA2 突变患者的10 年累计发病风险分别为25%~42% 和18%~32%[5,12]。有研究报道,中国BRCA1 和BRCA2 突变乳腺癌患者的对侧乳腺癌10 年累计发病风险分别为15.5%和17.5%,显著高于无BRCA1 和BRCA2 突变人群[4]。国外已有多项研究证实,与未选择预防性手术或严密监测的患者相比,实施对侧预防性乳房切除术可使BRCA1/2突变患者的对侧乳腺癌发生风险降低90%以上。尽管对于对侧预防性乳房切除术是否能够改善BRCA1/2 突变患者的总生存尚存有一定的争议,但是现有的证据表明,临床分期较早的年轻乳腺癌患者有可能从中获益[13-14]。
即便是在发达国家,BRCA1/2 突变患者对侧预防性乳房切除术的普及率也存在较大的差异,美国可高达49.3%,而以色列和挪威仅为0%~1.9%[15]。在中国,由于对BRCA1/2 突变相关乳腺癌的认识不足等原因,因此罕见有关对侧预防性乳房切除术的报道。本研究中,在与患者反复沟通手术风险并且权衡利弊之后,近半数(47.8%)的BRCA1/2 突变患者愿意同时接受对侧预防性乳房切除术,提示在中国的乳腺癌遗传高风险人群中开展对侧预防性乳房切除术具有可行性。
预防性乳房切除术联合乳房重建术具有良好的美容效果,可以有效缓解女性尤其是年轻女性的术后心理压力,提高生活质量。长期随访的资料显示,在接受对侧预防性乳房全切术联合乳房重建术的患者中,80%的患者表示满意[16]。NSM联合乳房重建术可以为女性患者提供更好的术后美容效果。国外的一项多中心研究证实,NSM在BRCA1/2 突变患者中是安全且可行的[17]。当然,术后发生组织皮瓣坏死、感染和包膜挛缩等并发症的风险也有所增加。因此,临床医师应严格把握手术适应证,与BRCA1/2 突变患者进行充分沟通,权衡预防性手术的利弊。
许多因素可以影响临床医师对于对侧预防性乳房切除术的选择,例如患者的年龄、肿瘤家族史、临床病理特征、教育背景和经济水平等。本研究结果提示,除BRCA1/2 突变状态以外,乳腺癌和(或)卵巢癌家族史以及年龄是影响对侧预防性乳房全切术选择的重要因素,这与国外的研究结果一致[18-19]。既往研究表明,家族史是影响BRCA1/2 突变患者对侧乳腺癌发生风险的重要因素[3]。中国人群的相关数据也显示,家族史可使BRCA1/2 突变携带者的对侧乳腺癌发生风险增加2 倍以上[4]。值得注意的是,有乳腺癌和(或)卵巢癌家族史的患者更易获得家庭成员的理解和支持。因此,有明显家族史的患者更愿意选择预防性乳房全切术。尽管国外报道,较早的确诊年龄(例如18~49 岁)是影响对侧预防性乳房全切术的重要因素[18-19],但是基于中国的国情,就如本中心既往报道的双侧预防性乳房全切术的手术条件[20],作者倾向于对年龄>30 岁且完成生育或预期寿命>10年的BRCA1/2 突变患者实施对侧预防性乳房切除术。
综上所述,本研究建议临床医师在为BRCA1/2 突变的乳腺癌患者制定手术方案时,除了对常规的临床病理因素进行考量之外,还需要结合患者的手术意愿、肿瘤家族史、年龄以及婚育等情况,并且与患者进行反复沟通。对于有保乳意愿且具备保乳条件的BRCA1/2 突变携带者,应充分告知保乳术及术后放疗是可行的,但是保乳术后仍然存在患侧新发乳腺癌或对侧新发乳腺癌的高风险,因此应进行严密的术后监测。对于有强烈愿意、愿意接受预防性手术的BRCA1/2突变携带者,应严格筛选乳腺癌和(或)卵巢癌家族史等高危因素,并且选择合适的年龄(如已完成生育或预期寿命>10 年),同时向患者充分告知预防性手术的利弊,给予患者充足的考虑时间,在获得家人理解和支持的前提下,可慎重开展患侧乳房全切术以及对侧预防性乳房全切术±Ⅰ期假体植入的乳房重建术。

