先天性膈疝死亡危险因素分析
崔甜甜 谢 伟 饶维暐 夏 昊
上海交通大学医学院附属新华医院(上海 200092)
先天性膈疝(congenital diaphragmatic hernia,CDH)是指因胚胎时期膈肌发育停顿导致膈肌缺损、腹腔脏器疝入胸腔[1],每3 000例活产儿中有1例发生[2],病死率为27%~46%[3-5]。CDH 导致肺发育不全和肺动脉高压,是患儿致死的主要因素[6-7]。近年来产前检查、护理以及新生儿医疗和外科管理的改进使得CDH存活率得到提高[8],但部分患儿面临术后多种远期合并症(如胃食管反流、胸廓畸形、哮喘等)[9-10],仍需加强监护。现回顾性分析CDH患儿的死亡危险因素,为后续临床诊治提供参考。
1 对象和方法
1.1 研究对象
选择2017 年1 月至2021 年2 月在上海交通大学医学院附属新华医院小儿急危重症医学科收治的CDH 患儿作为研究对象。纳入标准:①年龄≤28天;②初诊确诊为CDH;③排除病例资料不完整者。
根据治疗结局,CDH患儿分为存活组及死亡组。
1.2 方法
1.2.1 临床资料收集 通过病例信息系统回顾性收集分析患儿的临床资料,包括性别、胎龄、出生体质量、出生方式(剖宫产/顺产)、Apgar 评分(1 分钟≤7 分)、转运时间(从产房到病房时间)、儿科重症监护病房(PICU)住院天数、有创机械通气时间、有无混合感染;疾病及治疗相关信息包括膈疝位置(左/右)、肺动脉压力(生后首次心脏超声检测)、观察与预期肺头比(observed/expected lung to head ratio,o/eLHR)、有无肝脏疝入[7]、有无疝囊;入院后1 小时内动脉血气分析指标包括pH 值、乳酸、氧合指数(oxygenationindex,OI)。OI=MAP×FiO2×100/PaO2,其中PaO2为动脉氧分压,MAP 为平均气道压,FiO2为吸入氧浓度百分比。
1.2.2 CDH诊断标准[11]①产前诊断:产前超声检查对膈疝部位及相关脏器的异常改变可清晰检出。②产后诊断:症状为呼吸困难、紫绀、呕吐等;体征为肺部叩诊清浊音、心音偏移、肠鸣音减弱或消失等;X线胸片表现为膈上下阴影相连、膈影消失,提示纵隔显著移位。
1.3 统计学分析
采用SPSS 24.0 统计软件进行数据分析。计量资料符合正态分布的以均数±标准差表示,两组间比较采用两独立样本t检验;非正态分布的以中位数(P25~P75)表示,组间比较采用秩和检验。计数资料以例数(百分比)表示,组间比较采用χ2检验或Fisher精确概率法检验。采用二分类logistic回归分析影响CDH患儿死亡的因素。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况
纳入68 例CDH 患儿,男42 例、女26 例,中位胎龄39.0(37.5~39.4)周,平均出生体质量(2 996.9±549.8)g,PICU住院时间19.2(5.3~28.0)d,有创通气时间9.1(3.9~13.9)d。死亡组23例(33.8%)、存活组45例。手术59例,手术后死亡14例(23.7%)。左侧膈疝54例,右侧膈疝14例。
2.2 存活组和死亡组临床资料比较
与存活组比较,死亡组胎龄较小,出生体质量较低,PICU住院和有创机械通气时间较短,oeLHR较小,pH值较低,1分钟Apgar评分≤7和肝脏疝入比例较高,肺动脉压力和OI 较高,差异均有统计学意义(P<0.05)。见表1。
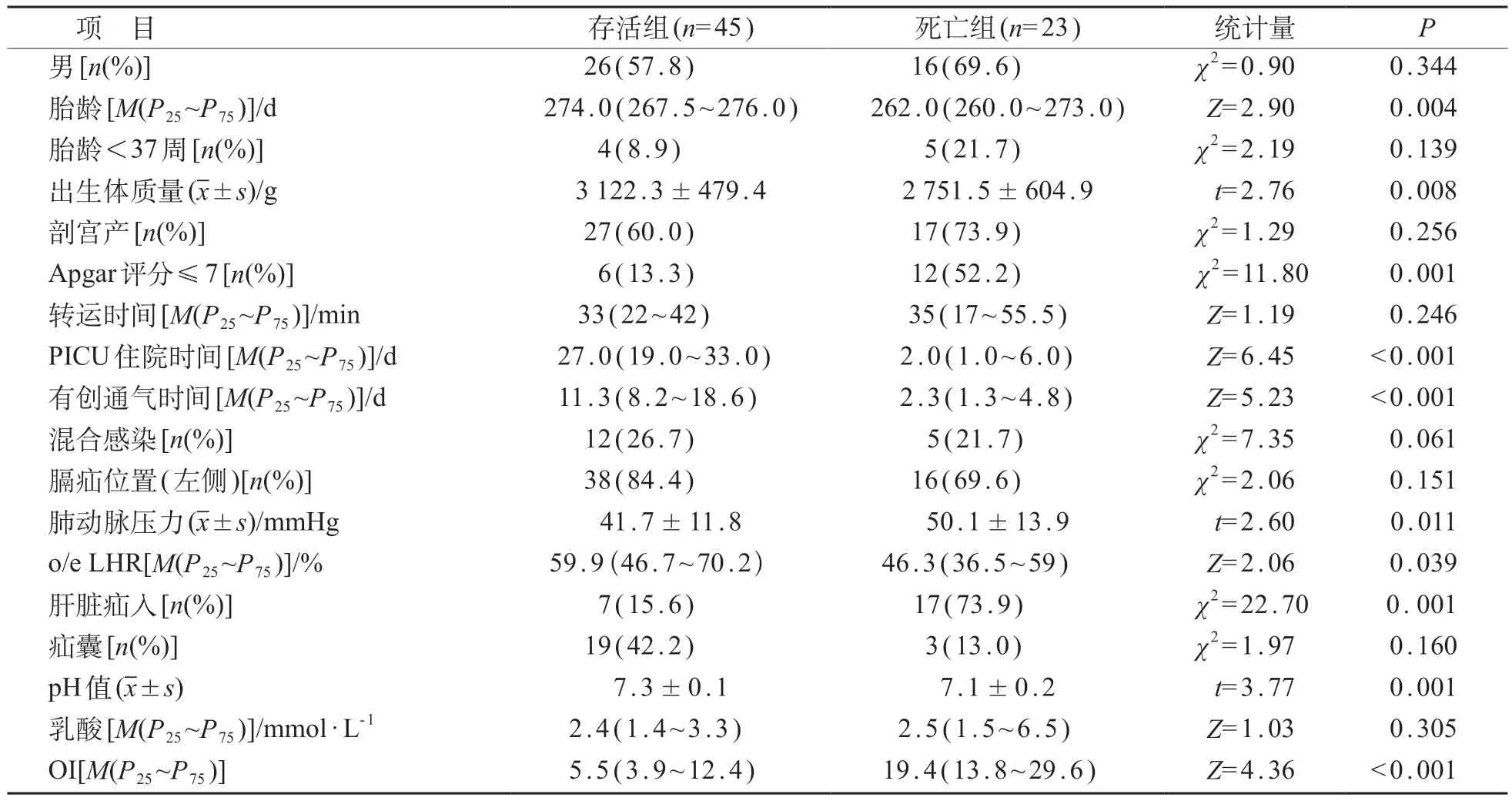
表1 CDH患儿存活组与死亡组临床资料比较
2.3 影响CDH患儿死亡的多因素分析
以死亡为因变量,将单因素分析中有统计学意义(P<0.05)的因素纳入二分类logistic 回归分析,结果显示,OI及肝脏疝入为死亡的影响因素。见表2。

表2 二分类logistic回归分析影响CDH患儿死亡因素
3 讨论
CDH通常与腹腔脏器疝入胸腔和肺发育异常有关,肺发育异常导致肺发育不全和肺循环的结构和功能异常,是一种罕见的膈肌发育缺陷,病死率较高[12]。相关研究通过统计分析1988 年—2015 年在体外生命支持组织(ELSO)登记处初诊为CDH 的7 564 例患儿,发现CDH 总病死率为50%[13]。另有研究通过国际CDH 研究组数据库,探讨2001 年—2015年3 906例产前诊断CDH患儿的分娩方式对预后的影响,发现其总病死率为36%[14]。另一项研究分析了82例CDH患儿,其病死率为33%[15]。本研究中CDH病死率为33.8%,与其他研究相比相对较低,可能与多学科联合诊治,转运时间短以及近年来围手术期的监护改善有关。
相关研究表明左侧CDH发病率更高,且男性占主导地位[2]。本研究中左侧膈疝54例(79.4%),男性42 例(61.8%)。部分研究报道右侧膈疝总死亡率高于左侧膈疝[16]。本研究中,右侧CDH 病死率50%(7/14),左侧CDH 病死率29.6%(16/54),但差异无统计学意义。本研究存活组的住院时间明显长于死亡组,说明CDH在早期有较高的病死率。相关研究指出,体质量每增加100 g,病死率下降7%,低出生体质量和低Apgar评分是CDH患儿的独立危险因素[17]。另有研究表明,1分钟和5分钟Apgar评分越低,CDH患儿死亡率越高[18]。本研究中低体质量、1 分钟Apgar 评分≤7 比例与 CDH 患儿病死率有关;存活组有创机械通气时间明显长于死亡组,考虑与部分重症CDH 患儿生后未手术即死亡,住院时间短有关。相关研究显示肺动脉压力及oeLHR与CDH 患儿的预后相关[19-20]。本研究中存活组肺动脉压力低于死亡组,oeLHR在死亡组与存活组的比较显示有统计学意义,可能与CDH 患儿病死率相关。
CDH 患儿的早产与不良结局相关。相关研究表明,妊娠37 周前分娩的CDH 患儿存活率为35%~43%[21-22]。另有研究发现在孤立性左侧膈疝中,胎龄与28天存活率有关[23]。本研究中存活组与死亡组的胎龄比较无统计学差异,可能与多学科联合诊治以及早产患儿偏少有关。CDH的预后也与胎儿肝脏位置有关,胸内肝脏提示膈肌缺损大,早期内脏疝会导致严重肺发育不全,中重度的CDH常合并有肝疝[6-7]。相关研究通过系统回顾和荟萃分析发现,超声和MRI在胎儿胸部发现肝脏与围生期不良结局相关[24]。肝脏占据胸部的百分比可预测CDH 胎儿的新生儿存活率[25]。本研究中死亡组有肝脏疝入者比例明显高于存活组,多因素logistic回归分析提示有肝脏疝入是CDH患儿死亡的独立危险因素。
CDH主要的病理生理是肺动脉高压,其主要造成肺血管阻力异常、右向左分流,从而出现严重低氧血症和持续胎儿循环[6]。近年来,利用血气分析预测患者预后的工作在积极开展。其中根据血气分析计算的OI被报道为呼吸衰竭患者预后的重要预测指标[26]。此外,据报道,OI是CDH死亡率的预测因子[27]。相关研究表明,24 小时平均OI 与24 小时最佳OI 对CDH 的死亡率有很高的预测价值[28]。有研究发现24 小时最佳OI 是CDH 30 天死亡率的独立预测因子[29]。本研究通过多因素回归分析发现,OI是CDH患儿死亡的独立危险因素,提示OI越高,与CDH相关的低氧血症越重,病死率越高。
综上所述,肝脏疝入及OI是CDH死亡的独立危险因素。因此,对上述因素需加强警惕,提高临床诊治能力,进一步改善预后,降低病死率。本文为单中心回顾性分析,部分数据收集不完整,样本量相对较小,存在一定局限性,多中心更大的样本量分析可能有助于提高统计数据的有效性。

