放射性同位素制品技术标准建设的现状与思考
张 云,徐 卓,杨 柳,隋艳颖
(原子高科股份有限公司,北京 102413)
放射性同位素制品主要应用于民用核技术应用领域[1],其研究始于20世纪50年代末至90年代中期,基本形成了放射性同位素(反应堆和加速器)、医用放射性同位素制品与药物、医疗和工业用放射源与示踪剂等在内的放射性同位素制品较为完整的研制生产体系[2-9]。2016年11月29日,国务院印发《“十三五”国家战略性新兴产业发展规划》,规划中明确提出,支持发展非动力核技术,包括离子、中子等新型射线源、医用放射性同位素、中子探伤、辐射改性等新技术和新产品,持续推动核技术在工业、农业、医疗健康、环境保护、资源勘探、公共安全等领域应用。近期,国家原子能机构等八部门联合发布《医用同位素中长期发展规划(2021—2035年)》(以下简称《规划》),这是我国首个针对民用核技术在医疗领域的指导纲领性文件,该《规划》的颁布将我国放射性同位素制品行业彻底推入快车道行列。
在核医学领域,根据统计数据可知[10-12],近几年,我国在核医学科建设、放射性药物和显像设备使用等方面均有较大幅度提升。这主要得益于放射性药物在医学诊断和肿瘤治疗领域的独特优势,随着全球人口老龄化加剧,放射性药物的应用将随着需求不断扩大而扩大。根据Medraysintell数据统计,2019年全球放射性药物市场规模约为60亿美元,同比增长8%,预计2030年全球放射性药物市场达到300亿美元规模[13-15]。而2019年中国放射性药物市场规模为35.93亿人民币,同比增长了21.9%,到2028年放射性药物的市场规模有望超过200亿人民币[16]。
在放射源领域,随着其在医疗与工业领域应用的不断深耕以及市场规模不断扩大,截至2017年,放射源市场规模为4.3亿,根据弗若斯特沙利文行业报告预测,预计到2022年放射源产品将达到5.35亿元,年复合增长率约4.4%。特别是随着国产钴-60源芯实现自给自足、伽马刀配置审批权限由国家卫生健康委员会下放到省级卫生健康委员会,以及植入式密封籽源在肿瘤治疗领域的需求不断扩大,未来医用放射源会出现迅猛增长。
市场规模的快速扩张,能够促进行业内产品的质量和检验标准不断完善,而标准体系的系统建设又能助推行业高质量发展。然而,在本领域内,与市场规模快速发展形成鲜明对比的是其产品的质量和检验标准发展却较为缓慢。这主要源于:(1) 与欧美国家相较,我国在该领域尚处于发展初期,尽管近年来受益于生命科学、航天和工业辐照等领域发展,促使该行业迅速崛起,但由于在放射性同位素制品专属理化分析方法、生物检验技术及关键质控设备检定等方面的欠缺,导致我国在质量检验标准建设方面相对落后,现阶段主要采用国际标准;(2) 我国放射性原料液主要依赖进口,在原料液质量标准建设中处于弱势地位;(3) 随着放射性同位素制品的应用范围不断扩大,特别在新兴行业和领域内,会有质量和检验标准与产品不匹配的问题。
1 技术标准体系现状
目前,国内放射性药物生产企业执行的产品质量标准主要为《中华人民共和国药典》(简称《中国药典》)和国家药品监督管理局给申报药品批准的企业标准(不作为通用质量标准)。其中,《中国药典》作为最重要的质量标准,同《美国药典》(USP43-NF38版)和《欧洲药典》(10.5版)一样,主要收载放射性药品质量控制、分析技术指导原则和品种质量标准,而其他如《裂变钼99-锝99m色层发生器》(GB/T 13172-2009)、《放射性药品的放射性化学纯度测定》(EJ/T 841-94)、《放射性核素活度测量 井型电离室法》(EJ/T 843-94)和《放射性药品溶液pH值测定方法》(EJ/T 845-94 ),以及检定规程如《γ放射免疫计数器》(JJG 969-2002)等,则为放射性核素及药品检验、仪器检定提供技术参考,基本满足上市产品的质量控制。但存在放射性原料液产品标准缺失和理化分析方法及设备检定标准老旧等问题。
目前国内放射源生产厂家遵循的产品质量标准主要为《密封放射源 一般要求和分级》(GB 4075-2009)、《密封放射源的泄漏检验方法》(GB/T 15849-1995)和《放射性物品安全运输规程》(GB 11806-2019),前两项标准主要对密封放射源的一般要求进行了规定,如表面污染检验、泄漏检验、辐射输出量测量和分级实验等方面,第三项标准则主要对非密封源和货包的表面污染和辐射水平等方面进行了规定。同时,在上述三项通用标准的基础上,行业内如原子高科股份有限公司等生产单位起草编制了《镅铍中子源》(GB/T 12714-2009)、《工业仪表用铯-137γ辐射源》(GB/T 13366-2009)等常规放射源的产品标准,基本满足常规放射源产品的质量控制。但对于其他领域产品,如各种新型反应堆的启动中子源以及氪-85测厚源等方面缺少相应的产品质量标准。
2 技术标准体系存在的问题
2.1 放射性药物
2.1.1缺乏分析检验技术标准 《中国药典》收载的放射性药品质量标准中存在分析方法不明确、杂质分析不精确等情况,例如锝[99mTc]亚甲基二膦酸盐注射液的放化纯度测定,未明确参考放化纯度测定法三法(通则1401)实验的纸色谱法或者薄层色谱法;高[99mTc]锝酸钠注射液中未收载α和β杂质的分析方法;《中国药典》(2020年版)放射性药品检定法未收载α核素的分析方法以及对纯β核素的鉴别,正电子核素放射性核纯度、放射性活度的测定技术上内容较少。除《中国药典》以外,有关放射性药物检验的国家标准或者行业标准有《放射性药品的放射化学纯度测定纸色谱法》(EJ/T 841-1994)、《放射性药品的载体含量测定分光光度法》(EJ/T 949-1995)和《高纯锗γ能谱分析通用方法》(GB/T 11713-2015)等,数量少且多年未更新,尤其是近几年采用高效液相色谱法在放射性药品放化纯度中的应用研究越来越广泛,但缺乏相应的核行业标准作为技术指导;另外,对于分析方法的验证与确认,《中国药典》收载了9101分析方法验证指导原则和9099分析方法确认指导原则,未明确放射性药品分析方法的适用范围,而放射性药品具有衰变且不恒定性等特点,放化纯度、放射性核纯度等有别于普通药品的检验项目方法验证和确认,如完全按照通则9101和9099执行,存在一定差异性,实施难度较大。
2.1.2放射性核素质量标准缺乏 医用同位素的制备是制约放射性药物研发以及核医学科发展的“卡脖子”问题。我国自主生产的碘[131I]、锶[89Sr]仅满足国内20%的需求,镥[177Lu]仅满足国内5%的需求,其他常用堆照医用同位素全部依赖进口[18]。《欧洲药典》(10.5版)收录了碘[131I]化钠溶液、磷[32P]酸钠溶液、钼[99Tc]酸钠溶液、三氯化镥[177Lu]溶液、碘[123I]化钠溶液等质量标准,而在国内,曾在1977年版《中国药典》中收录125I溶液标准,但由于难以实现125I的国产化而最终取消了该核素质量标准的收录,截至目前,《中国药典》尚未收录任何一种放射性原料的质量标准,存在标准盲区。近两年中国同位素与辐射行业协会组织相关单位进行了放射性核素标准的编制,补充了三氯化镥[177Lu]溶液、氯化铜[64Cu]溶液和碘[123I]化钠溶液三项核素标准,但缺乏碘[131I]化钠、氯化锶[89Sr]及钼[99Mo]酸钠溶液等常用核素的质量标准。
2.1.3质控关键设备检定标准不完善 放射性药物检验用关键设备的检定标准不完备,锝分析仪的检定工作参考《γ放射免疫计数器检定规程》(JJG 969-2002)进行,该计量标准存在适用范围以及应用要求没有与时俱进等问题;另外,用于检验放射性药物放化纯度的色层扫描仪、放射性流量检测仪等关键设备的检定缺乏计量标准,国内部分企业采用自校验的方式,存在校验项目不齐全,评判标准不一致等情况,对于设备的使用以及检验结果的准确性缺乏强有力的保证。
2.2 放射源
2.2.1标准老旧 通过国家标准化管理委员会官网查询可知,我国现行的放射源标准主要分为国家标准和行业标准两类。其中,国家标准10个,行业标准28个,包括3个通用类检验标准和35个产品标准。
根据《标准化法实施条例》规定,标准实施后,制定标准的部门应当根据科学技术的发展和经济建设的需要适时进行复审。复审周期一般不超过5年。但从表1中能够看出,2000年前修订及发布的标准占比65.79%,2016年后修订及发布的标准却仅有1个,占比仅为2.63%,在放射源行业,标准内容老旧、更新缓慢的问题尤为突出。
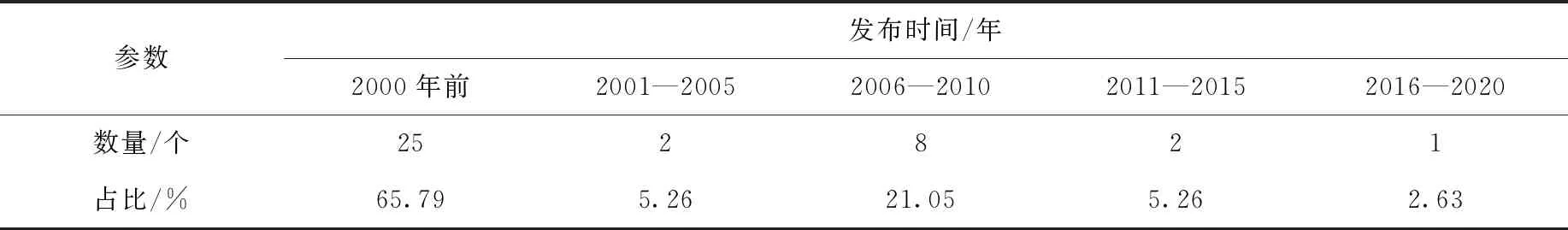
表1 放射源标准制定年份统计
特别对于通用类检验标准,由于未能及时更新,随着行业的不断发展创新,可能会产生检验方法不适用或合格判定限值变化等诸多问题。以《密封放射源的泄漏检验方法》(GB/T 15849-1995)为例,该标准等效采用国际标准ISO 9978-1992第一版,距今已有“26岁”高龄,而最新版ISO 9978已于2020年07月发布。与旧版相较,新版ISO 9978在实验人员资质、各项方法及技术指标等方面有较大变动,例如:新版标准明确了对于从事无损检测人员需经培训合格并取证,修改了标准中关于“6.1氦质谱泄漏检验”的计算公式和“6.2.1—6.2.4鼓泡泄漏检验”方法的探测阈值,同时增加了关于自发热源鼓泡检验的注意事项。由此可见,标准滞后带来的问题不容忽视,其中的重要因素就是国际标准与国家标准的脱节。
农业机械的保养要严格按照使用说明书及当地农机管理部门规定的内容进行。机车的高级保养应在机务管理人员指导下在室内进行。燃油动力机械要做到四小漏 (小漏油、小漏水、小漏气、小漏电)、五净(油、水、气、机器、工具)、六封闭(柴油箱口、汽油箱口、机油加注口、机油检视口、汽化器、磁电机)、一完好(技术状态完好);配套农具要实行常年修理,做到三灵活(操作、转动、升降灵活)、五不(不旷、不钝、不变形、不锈蚀、小不件)、一完好(技术状态完好)。
2.2.2国际标准制定参与程度低 国际标准制定参与程度低、自主创新性不足的问题在放射源行业同样较为突出。放射源的生产和销售在我国均受到严格管控,国内具备生产资质的单位较少。因此我国放射源行业的同行业竞争主要以国外厂家为主。这就更加需要我们重视参与国际标准的制定并积极投身其中,紧跟技术发展动态。然而,我国在放射源领域参与国际标准制定的项目却寥寥无几,以通用类检验标准为例,我国现行放射源检验类标准主要有两项:《密封放射源的泄漏检验方法》(GB/T 15849-1995)和《密封放射源 一般要求和分级》(GB 4075-2009),二者均为等效采用国际标准而制定的国家标准。我国尚未参与其中任何一项国际标准的制定。意味着在放射源检验领域,我国的检验技术处于跟随者和执行者状态,一旦检验技术出现重大变革,对于我国放射源行业将是较为沉重的打击。同时,标准国际化参与程度低,也会降低行业话语权、使得放射源产品在国际市场的竞争力和行业发展均受到影响。
2.2.3标准覆盖面小 近年来,随着放射源在医疗、辐照、辐射育种等方面应用范围不断扩大,与之相适应的产品标准、检验标准却未能及时覆盖。
在进口原料液领域,以放射源用核素标准为例,除钴-60伽玛刀放射源的钴-60原料在2018年实现国产化外,我国放射源生产的原料液大部分从欧美等国家进口,不仅存在放射性核素的断供和涨价风险,同时还因为标准覆盖不到该领域,导致放射源生产单位对进口原料液的质量指标,只能以生产厂家的各项出厂指标为准,缺少放射性原料液的验收标准。
在放射源产品领域,以工业仪表用氪-85测厚源为例,国内市场上的氪-85测厚源均从俄罗斯和欧美等国家进口。2019年,原子高科股份有限公司停产的氪-85测厚源成功复产,然而,国内放射源行业中却未找到与之匹配的产品标准,直至2020年12月,在原子高科股份有限公司等三家单位的共同努力下,发布了《工业仪表用氪-85测厚源》(T/CIRA 12-2020)团体标准,填补了现有标准中的空白,完成了对该产品的标准覆盖。
3 对策与建议
完善的标准体系是支撑产业可持续发展的重要保障。相比硬件方面取得的进步,放射性同位素制品在标准化方面取得的进展相对滞后。近年来,在政府部门的大力支持下,行业协会及科研、生产单位的共同努力下,我国放射性同位素制品应用领域标准化工作取得了一定成绩,但仍然存在制订、修订速度较慢、覆盖范围较窄、更新缓慢、跟不上产品发展需求等问题。加快推进本领域标准化进程,健全完善我国辐射技术应用领域标准体系,对于推动我国核技术产业加快发展,促进我国产业升级具有重要意义。
3.1 系统完善与更新放射性同位素制品标准体系
(1) 建议国家有关部门高度重视,在放射性同位素制品领域的标准体系建设工作中加强投入,给予相关政策配套,通过加大人力、物力、资金和渠道等方式,对标准编制、修订和宣贯等活动给予支持,并为相关协会和科研、生产单位参与各项标准的制定和审议明确途径,进一步提升我国放射性同位素制品领域标准体系的完整性和科学性。
(3) 建议发挥国内相关科研机构、协会团体和放射性同位素相关企业的积极性,提高创新意识,对标准进行动态跟踪、实时更新、扎实推进标准的制定、审查和发布,促进我国核技术的创新和产业发展,同时推动国内标准与国际接轨,进一步提升标准的自洽性。
(4) 建议国家自上而下结合我国同位素制品发展现状及特点,设立专项研究课题,系统开展放射性同位素制品领域的基础性技术和核心技术研究,如提高《中国药典》标准与企业标准的衔接;国家药监局对放射性药品的标准与行业内自发开展的标准建立的结合;国际放射源检验标准与国内标准的接轨等,进一步提升我国放射性同位素制品领域标准体系的先进性。
3.2 补充现有标准体系的空白区和薄弱区,做好各级标准衔接
针对放射性同位素制品,做好国家标准与行业标准、团体标准的衔接,并强化标准推广,促进企业标准在国家标准、行业标准、团体标准基础上建立与完善,形成同品同类同标准的行业发展模式,使各级标准有机结合,达到日常工作标准化和一致性。
同时对现有国家标准中不适用、未更新的内容进行修订;在现有国家标准的基础上,行业标准和团体标准应针对国家标准的空白区、薄弱区发力,补充完善,逐渐形成系统性的放射性同位素制品标准体系。
3.2.1核素制备 目前,我国大部分放射性核素依赖进口,因此,放射性核素“国产化”便成为了解决行业发展“卡脖子”问题的关键一环。在自主研制核素制备国产化进程中,要同步进行核素标准的建立,破解核素制备的难题,国内有关部门,社会团体及相关生产、科研单位发挥自身优势,设立专项研究课题,同时积极与国际标准对标,共同建立我国放射性核素的生产、质控标准,填补现有标准体系的空白。在2020年已发布《三氯化镥[177Lu]溶液》团体标准的基础上,逐步建立碘[131I]、钼[99Mo]、碘[125I]、磷[32P]等常用核素的团体标准。
3.2.2放射性药物检验技术 对于《中国药典》、国家药监局以及放射源领域的通用检验技术标准,普遍存在标准更新不及时,与国际标准有差异的情况,需要行业内发挥主观能动性,在检验技术方面不断革新,跟上蓬勃发展的放射性同位素制品行业发展。一是放化纯度检验用纸色谱法、薄层色谱法、高效液相色谱法等各类方法进行系统研究,明确各类放化杂质分离方法适用范围,并给予方法指导;二是核纯度检测中α和β杂质检测方法进行研究,以及纯β核素的鉴别等检验技术进行研究;三是放射性药品的生物分布实验,在锝[99mTc]聚合白蛋白注射液已有检测方法的基础上进行再研究,对标国际扩充品种,并形成指导原则;四是参考《中国药典》9101和9099通则,提出适用于放射性药品检验方法的方法学确认与验证指导原则。在标准化管理部门及行业协会的组织下,系统性建立和不断完善,引领行业技术与国际接轨。同时,在提升行业整体技术创新水平,完善标准编制背后的理论依据,夯实标准编制基础,切实提高标准体系建设的科学性和适用性。
3.2.3放射源检测 针对目前现有放射源标准老旧,对放射源生产行业无法形成有效指导,建议首先对应用最广泛的《密封放射源的泄漏检验方法》(GB/T 15849-1995) 和《密封放射源 一般要求和分级》(GB 4075-2009)进行修订;再对常用的放射源检验方法如氦质谱检漏法等方法进行规范;逐步更新和完善国内应用范围较广泛的镅铍中子源、铯137Cs辐射源等放射源技术标准,推动放射源技术标准和质控标准的发展。
3.2.4检测仪器 积极响应国家药监机构对于计算机化系统和数据完整性的管理要求,同时,为保证检测仪器准确可靠,就放射性同位素制品检测仪器的校验方法进行标准化建设,结合行业内自校验的现状,组织建立检测仪器校验的团体标准。
3.3 强化标准宣贯,推动标准在行业内广泛推广及应用
建议标准管理部门、行业团体协会通过宣讲培训、技术交流和讲座等方式,多渠道、多层次开展标准宣贯工作,帮助企业掌握标准基本内容,正确理解和使用标准。并组织搭建标准实施反馈平台,优化实施反馈机制,实现标准实施、反馈、提升的良性循环。
建议放射性同位素行业内相关企业加强标准的应用及推广,并将其与企业精益管理、质量体系建设和绩效考核机制相结合,引导并强化标准在企业中的作用。通过标准执行促进企业提高自身生产能力,优化生产、研发和质控方面的工艺水平,并最终促进放射性同位素制品行业的发展,提升其国际竞争力,为放射性同位素制品“走出去”奠定坚实基础。
3.4 提升标准国际化水平
随着2021年10月10日《国家标准化发展纲要》的正式颁布,更是将“提升标准国际化水平,加快构建推动高质量发展的标准体系”作为发展重点。因此,建议在放射性同位素制品领域,积极推进国内该领域内的科研院所及企事业单位承担ISO/IEC专业技术机构(TC/SC)秘书处工作,通过与其开展更多的合作交流,不仅能够紧跟该领域内技术发展趋势,还能不断强化国际标准意识,加强标准化人才培养、储备和输出,提升标准国际化水平。
4 结论
本文对放射性同位素制品标准体系进行了概要性的总结:在放射性药物领域,以《中国药典》为主的标准体系整体框架较为完整,但在分析检验方法、放射性核素产品以及质控关键设备检定等方面需进行标准补充;在放射源领域,以《密封放射源的泄漏检验方法》(GB/T 15849-1995)和《密封放射源 一般要求和分级》(GB 4075-2009)为主,再辅以常规产品标准,共同构建了放射源检验的通用技术标准,基本满足常规放射源产品的质量控制,但普遍存在标准老旧、国际标准制定参与程度低和覆盖面小等问题。
针对上述问题,本文提出了“完善与更新放射性同位素制品标准体系、补充现有标准体系的空白区和薄弱区,做好各级标准衔接、强化标准宣贯,推动标准在行业内推广及应用以及提升标准国际化水平”等相关建议,希望国家对放射性同位素制品标准体系建设能够投入更多的关注与支持,同时希望行业内的科研单位和企业共同努力解决标准体系建设中存在的问题,以推动行业更高质量、高速度的发展。

