探究CO2催化重整中镍基催化剂的抗积碳性
丁远鑫,马晓茜,唐玉婷,陈新飞
(华南理工大学 电力学院 广东省高效清洁能源利用重点实验室,广东 广州 510640)
生物质作为一种可再生能源[1],具有丰富、无污染的优势,对降低温室气体排放具有重要意义[2-4]。生物质气化是一种广泛应用的将生物质转化为H2和CO合成气的技术[5-8],但气化过程生成的焦油[9-12]对设备造成堵塞和损坏[13-14],限制了生物质气化的规模化应用。
本文采用二氧化碳催化重整技术,将焦油转化为CO和H2[15-17]。针对二氧化碳催化重整过程丝状碳沉积导致的催化剂失活问题[18-23],探究了Ni-Fe双金属催化剂在焦油二氧化碳催化重整过程的抗丝状积碳性能以及催化性能,为合成抗丝状积碳性能强的催化剂提供参考。
1 实验部分
1.1 试剂与仪器
硝酸镍、无水硝酸铁、二氧化锆、甲苯均为分析纯。
OTF-1200X立式管式炉;LD-P2020蠕动泵;D08-1F型流量显示仪和质量流量控制器;纯水氢气发生器。
1.2 催化剂制备
采用浸渍法制备Ni/ZrO2、Fe/ZrO2和Ni-Fe/ZrO2催化剂。
1.2.1 Ni/ZrO2和Fe/ZrO2催化剂制备 分别在两杯100 mL去离子水中加入14.55 g硝酸镍和20.2 g硝酸铁,搅拌溶解后,分别取20 mL,分别加入2 g ZrO2载体,转移到电磁搅拌器中搅拌。将粘性固体置于105 ℃的干燥箱中12 h,直至大部分水分蒸发。干燥的固体在700 ℃ (N2)下煅烧2 h。冷却到室温,研磨,筛分,并放在一个密封的袋子里。
1.2.2 Ni-Fe/ZrO2催化剂制备 14.55 g硝酸镍溶于100 mL去离子水中,制成0.5 mol/L硝酸镍溶液,加入20.2 g硝酸铁。以下操作与Ni/ZrO2催化剂制备过程相同。
1.3 催化剂活性测试
甲苯CO2重整实验在垂直管式炉中进行,见图1。

图1 催化重整反应装置示意图Fig.1 The catalytic reforming reaction unit was depicted in a schematic diagram
由图1可知,在反应器中加入0.1 g催化剂(内径8 mm,长度420 mm),在50% H2/Ar气氛下(30 mL/min)在800 ℃下还原2 h。通过吹扫氩气(30 mL/min)将反应器冷却到室温。通过移动Ar (40 mL/min)和CO2(20 mL/min)通过反应器,提取残余气体。然后将实验反应温度提高到850 ℃。向反应器中泵入1 mL/h的甲苯,直至温度达到850 ℃。
采用排水法测定CO2重整过程中的气体体积。通过气体采样袋收集反应器出口的气体产物。采用安捷伦7890B GC-FID/TCD法测定气体产物中H2、CO和CO2的百分含量。每次实验都重复2次,以确保结果的准确性和可靠性。
由产氢转化的甲苯摩尔质量(nToluene,H2)与甲苯总摩尔质量(ntotal)之比计算甲苯转化率(XT);同样,碳的转化率(XC)计算为产CO转化的甲苯的摩尔质量(nToluene,CO)比甲苯的总摩尔质量(ntotal)。气体产率由H2(VH2)和CO(VCO)的体积与甲苯(VToluene)的体积之比得到。

(1)

(2)

(3)

(4)
式中XT——甲苯转化率,%;
XC——碳转化率,%;
PH2——H2产率,%;
PCO——CO产率,%;
nToluene,H2——产氢转化的甲苯摩尔质量,g;
ntotal——甲苯总摩尔质量,g;
nToluene,CO——产CO转化的甲苯的摩尔质量,g;
VH2——产生H2体积,mL;
VCO——产生CO体积,mL;
VToluene——甲苯体积,mL。
2 结果与讨论
2.1 催化剂表征
2.1.1 XRD 还原后Ni/ZrO2、Ni-Fe/ZrO2和Fe/ZrO2催化剂的XRD谱图见图2。

图2 Ni/ZrO2、Ni-Fe/ZrO2和Fe/ZrO2催化剂的XRD变化趋势Fig.2 XRD trends of Ni/ZrO2,Ni-Fe/ZrO2,and Fe/ZrO2 catalysts
由图2可知,3种催化剂均表现出较强的ZrO2特征衍射峰。Ni/ZrO2催化剂在H2还原后出现了3个明显的Ni特征衍射峰,分别位于2θ=44.447,51.771,76.334°的位置。与Ni/ZrO2催化剂相比,Fe/ZrO2催化剂在2θ=44.658°时仅表现出一个Fe特征衍射峰。Ni-Fe/ZrO2催化剂在XRD谱图上没有明显的Ni和Fe峰。而Ni-Fe合金的特征衍射峰出现在2θ=35.644°处,说明催化剂上的金属活性位点不是单金属颗粒,而是Ni-Fe合金[24]。镍铁合金是由镍和铁的金属作用产生的。Ni-Fe合金的形成可以大大提高催化剂的催化效率[3]。
2.1.2 N2吸附-脱附 图3和表1为还原后复合催化剂的N2吸附等温线和孔参数。


图3 复合催化剂还原后的N2吸附-脱附等温线(a)和孔径分布(b)Fig.3 N2 Adsorption-desorption isotherms (a) and pore size distributions (b) composite catalysts after the reduction
由图3可知,复合催化剂的N2吸附等温线为带有H3滞后环的Ⅳ型等温线,揭示了煅烧和还原催化剂的介孔结构。粒子聚集在H3迟滞环上产生了一个小开口。同时,由图3(a)可知,在相对较低的压力(<0.5)下,所有样品都有N2吸收,说明存在微孔。由图3(b)可以看到中孔和微孔的存在。还原后,3种催化剂不仅在3~4 nm范围内出现了峰,而且在1~2 nm 范围内出现了较宽的峰[25]。还原后催化剂的峰值强度较高,说明还原后催化剂产生了更多的中孔和微孔。与Ni/ZrO2、Ni-Fe/ZrO2和Fe/ZrO2催化剂相比,只有Ni/ZrO2、Ni-Fe/ZrO2和Fe/ZrO2催化剂在0~2 nm之间出现了较大的峰。这表明,在Ni-Fe/ZrO2催化剂中加入Fe可以使其多孔性增强。中孔和微孔的增加使得反应物反应迅速,易于分散。前人研究发现[26],镍基介孔催化剂在CO2重整过程中表现优异。
由表1可知,还原后的催化剂的比表面积、孔容、孔径均按比例减小。由表可知,还原后的Ni/ZrO2催化剂具有最高的比表面积、孔容和孔径。Ni-Fe/ZrO2催化剂排名第二,Fe/ZrO2催化剂排名最后。铁的加入在一定程度上降低了Ni-Fe/ZrO2催化剂的效率。金属浓度的上升,填补了通道,是造成这种现象的原因。数据下降的另一个原因可能是铁堵塞了一些小孔和/或存在与铁密切相关的结晶镍物种[27]。

表1 复合催化剂的表面积、总孔容和孔径Table 1 Composite catalyst surface areas,gross pore volumes,and pore diameter
2.1.3 扫描电镜 SEM结果(图4)显示了3种催化剂的形貌。

图4 还原后(a) Ni/ZrO2, (b) Ni-Fe/ZrO2,(c) Fe/ZrO2的SEM图Fig.4 SEM diagrams of (a) Ni/ZrO2,(b) Ni-Fe/ZrO2,(c) Fe/ZrO2 after the reduction
由图4可知,Ni/ZrO2催化剂上分布着小颗粒,同时,其表面没有明显的凸起现象。与Ni/ZrO2催化剂相比,Fe/ZrO2催化剂粒径较大,表面相对粗糙。Ni-Fe/ZrO2催化剂中存在大颗粒,且大颗粒分布均匀,小颗粒随机镶嵌。然而,由于这些大颗粒的存在,表面也变得相对粗糙[24],这可能与合金的形成有关。在合金的生成过程中,在催化剂的结构中产生了较大的颗粒。Ni与Fe相互作用形成Ni-Fe合金。Ni-Fe/ZrO2催化剂中Fe的加入改变了催化剂的结构,使其具有不同的催化性能。
2.2 催化剂的催化性能
图5显示了不同催化剂的甲苯转化率(XT)和碳转化率(XC),图6显示了不同催化剂上甲苯CO2重整产物中H2,CO和CO2的比例[28]。由式(5)可知,CO方程前面的系数高于H2,说明CO比H2形成更多。生成的H2可能会进一步与二氧化碳反应生成更多的CO。生成的CO可以分解为二氧化碳和C。由于H2消耗高于CO消耗,H2转化率较低。同时,浓度越高,CO含量越高。相应地,H2的含量较低。

图5 由氢转化率(a)和碳转化率(b)计算的甲苯转化率Fig.5 Conversion efficiencies of toluene calculated by the hydrogen conversion (a) and carbon conversion (b)
由图5可知,与Ni/Fe/ZrO2催化剂相比,Ni/ZrO2催化剂在20 min内的反应效果更好,这意味着Ni/ZrO2催化剂在反应开始时比Ni-Fe/ZrO2催化剂具有更高的催化活性。然而,随着反应进行(≥20 min),Ni/ZrO2催化剂上的逐渐减少,这是由碳沉积引起的式(7),积碳会在反应过程中覆盖催化剂上的活性位点,导致催化剂活性降低。随着反应的进行,式(7)的负面影响变得更加明显。而在Ni-Fe/ZrO2催化剂中,铁的掺杂可以与镍反应生成Ni-Fe合金,提高了催化剂的抗积碳性能。Ni-Fe/ZrO2在CO2催化重整过程中保持较高的反应活性。

(5)

(6)

(7)
由图6可知,Ni/ZrO2催化反应CO2重整甲苯生成的H2(8.18%)和CO(29.51%)含量在前20 min高于Ni-Fe/ZrO2催化反应生成的H2(6.58%)和CO(28.91%)含量,说明Ni/ZrO2催化剂在反应开始时比Ni-Fe/ZrO2催化剂具有更高的活性。随着反应的进行,Ni/ZrO2催化剂释放的H2和CO量逐渐减少,导致Ni/ZrO2催化剂表面进一步积炭。如果在催化剂上沉积焦炭,催化剂上的活性位点就会被覆盖。降低催化剂的活性。在Ni-Fe合金的作用下,Ni-Fe/ZrO2催化剂上甲苯CO2重整生成的H2和CO量保持在一定范围内。实验还证实,在催化剂中加入铁可以提高催化剂的催化活性。由图6(c)可知,整个反应在CO2气氛下进行催化重整,CO2的输入量约为33.3%。在前20 min,Ni/ZrO2催化剂比Ni-Fe/ZrO2催化剂吸收更多的CO2。Ni/ZrO2催化剂活性更高,将更多的CO2转化为CO,当反应时间超过20 min时,Ni-Fe/ZrO2催化剂消耗的CO2比Ni/ZrO2催化剂消耗的CO2更多,说明在反应过程中有更多的CO2转化为可燃气体CO。Ni-Fe/ZrO2催化剂在反应过程中的作用由于合金的形成而增强,导致CO2消耗增加。

图6 甲苯在Ni/ZrO2、Ni-Fe/ZrO2和Fe/ZrO2上CO2重整气态产物的气体含量Fig.6 The gas content of gaseous products from CO2 reforming of toluene over Ni/ZrO2,Ni-Fe/ZrO2 and Fe/ZrO2(a)H2;(b)CO;(c)CO2
结果表明,Ni/ZrO2催化剂的活性(>20 min)高于Ni-Fe/ZrO2催化剂。随着反应的进行,Ni-Fe/ZrO2催化剂的催化效率优于Ni/ZrO2催化剂。在ZrO2上,Ni和Fe之间的强烈相互作用可导致高度分散的合金(Ni-Fe合金)的形成[29]。合金的形成可以增加耐焦性,减少催化剂表面积碳量。同时,焦炭沉积所覆盖活性位点的减少,导致催化剂活性的提高,有助于提高催化剂的稳定性和使用寿命。
2.3 积碳分析
沉积在催化剂上的碳会覆盖催化剂的活性位点,这是CO2催化重整甲苯过程中催化剂失活的主要原因之一。本研究从固定床反应器中收集反应后催化剂,并通过SEM、XRD、TGA和元素分析仪对催化剂进行表征。
2.3.1 扫描电镜 SEM结果(图7)显示了3种废催化剂的形貌。

图7 反应后(a) Ni/ZrO2,(b) Ni-Fe/ZrO2,(c) Fe/ZrO2的SEM图Fig.7 SEM diagrams of (a) Ni/ZrO2,(b) Ni-Fe/ZrO2,(c) Fe/ZrO2 after the reaction
碳纳米管是Ni/ZrO2催化剂上最常见的碳沉积形式,富含大量的“晶须”碳形成,阻止反应物进入催化剂孔隙,使催化剂失活[30-31]。在Ni-Fe/ZrO2方面,已有研究报道Ni-Fe合金可以抑制碳纳米管的生长。因此,与Ni/ZrO2催化剂相比,Ni-Fe/ZrO2催化剂表面几乎没有可见的碳沉积。Ni-Fe/ZrO2催化剂比Ni/ZrO2催化剂表面的焦炭分解少。
2.3.2 XRD 催化剂样品的XRD谱图见图8。
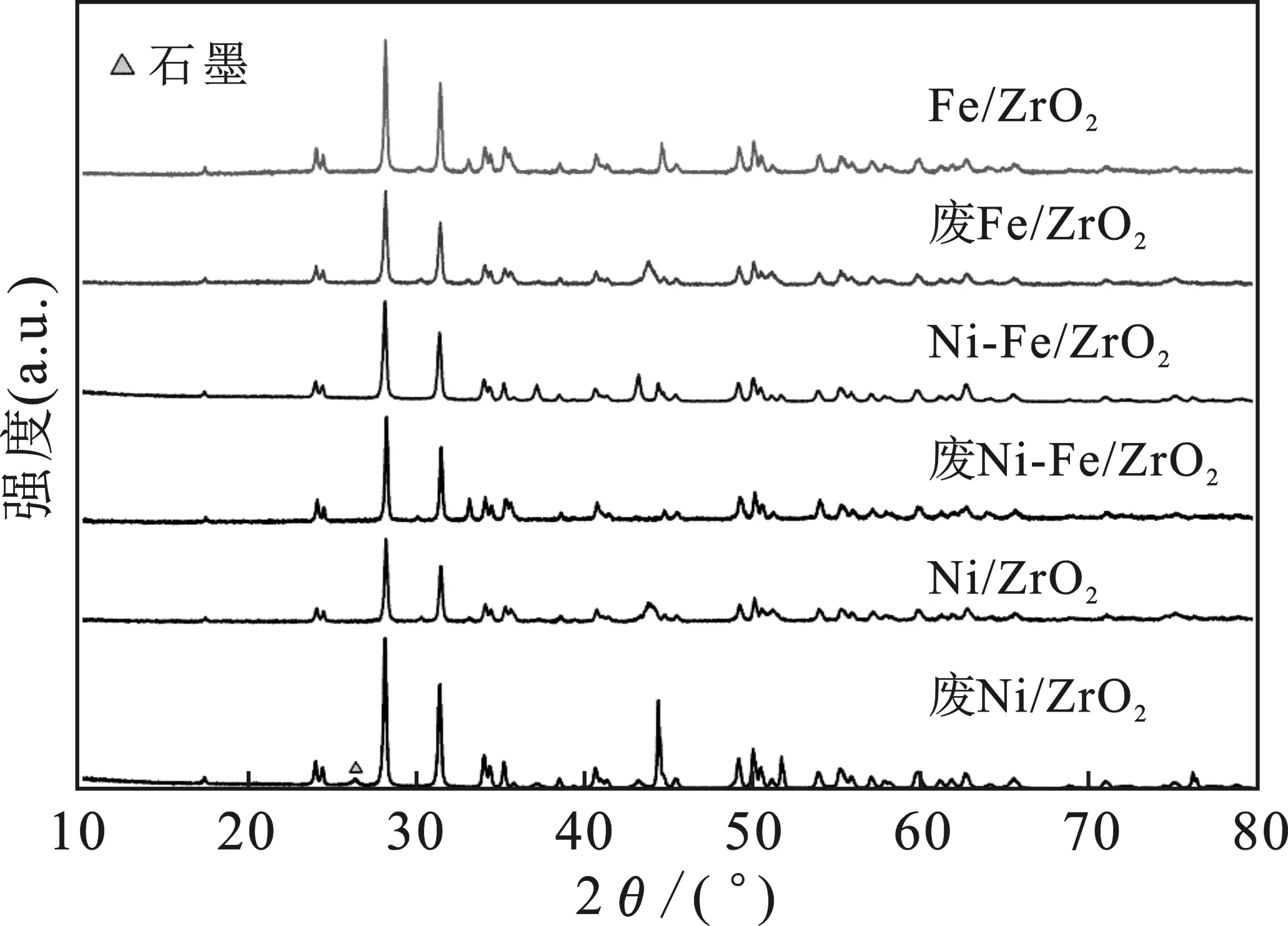
图8 反应前后3种催化剂的XRD谱图Fig.8 XRD patterns of the three catalysts before and after the reaction
由图8可知,3种样品中载体ZrO2的特征衍射峰占多数。反应后Ni/ZrO2催化剂,在2θ=26.396°处出现了较明显的石墨特征衍射峰,说明反应80 min后出现了较明显的积碳现象。结合之前的研究结果,在反应达到80 min之前,催化活性降低,催化剂稳定性下降[28]。而Ni-Fe/ZrO2催化剂没有明显的碳型石墨特征衍射峰。Ni-Fe合金的形成提高了催化剂的抗积碳性能,使更多的碳处于高游离态,减少了碳沉积量[13]。这进一步证实了Ni-Fe/ZrO2比Ni/ZrO2具有更好的抗积碳性能。
2.3.3 热重分析 废催化剂在空气气氛中的TG/DTG曲线见图9。
由图9可知,Ni/ZrO2和Ni-Fe/ZrO2催化剂的质量在300~521 ℃温度范围内开始增加。在521 ℃时,Ni/ZrO2催化剂的质量达到极限。重量的增加是由于金属的氧化作用。Ni/ZrO2催化剂的质量从521 ℃ 急剧下降到700 ℃,重量损失约10%,累积碳的氧化导致重量损失[18]。与此相反,Ni-Fe/ZrO2催化剂的质量没有明显的损失,而是持续增加。这主要与金属的连续氧化有关。铁的加入增强了催化剂的抗积碳性,减少了催化剂表面的积碳。

图9 废催化剂热重分析结果Fig.9 Thermogravimetric analysis results of waste catalyst(a) TG;(b) DTG
相应的,由图9(b)的DTG曲线可知,Ni/ZrO2催化剂在300 ℃以下有一个较小的失重峰,这也证实了本节的TG解释。在第二部分中,重量增加的峰值在500 ℃左右达到最大值。第三部分的DTG峰值约为650 ℃,这归因于石墨碳。这也是催化剂失活的主要原因[32]。Ni-Fe/ZrO2催化剂在稳定之前一直处于增重状态,表明Ni-Fe/ZrO2催化剂具有良好的抗积碳性能。Ni-Fe/ZrO2催化剂由于其优异的抗积碳效果,不会产生失重。这与活性分析得出的结论一致。
2.3.4 元素分析 用元素分析测试来计算沉积在废催化剂上的碳量。80 min时,Ni/ZrO2催化剂上的碳含量为27.54%,而Ni-Fe/ZrO2催化剂上的碳含量仅为5.48%。结合以上XRD和TGA结果,Ni/ZrO2催化剂表面沉积的碳导致催化剂活性降低。Ni-Fe/ZrO2催化剂中Ni和Fe的强烈相互作用形成了Ni-Fe合金。在合金的作用下,催化剂保持低碳含量长达80 min,而且很难失活,Ni-Fe/ZrO2具有比Ni/ZrO2更高的抗积碳性能。
从废催化剂的表征来看,Ni-Fe/ZrO2比Ni/ZrO2表面的焦炭分解少。这表明Ni-Fe/ZrO2比Ni/ZrO2更抗积碳。结果表明,铁的掺入可以显著提高镍基催化剂在焦油CO2重整过程中的抗积碳性能。
3 结论
随着反应的进行,Ni/ZrO2催化剂的活性显著降低,甲苯转化率由25.3%降至10.86%。然而,Ni-Fe/ZrO2双金属催化剂上的甲苯转化率仍在19%~25%范围内。Ni/ZrO2上的积碳含量(27.54%)高于Ni-Fe/ZrO2上的积碳含量(5.48%)。同时,由于积碳的存在,Ni/ZrO2催化剂的还原量降低了10%左右,Ni-Fe/ZrO2催化剂的积碳量仅为5.48%,铁掺杂镍基催化剂提高了催化剂的抗积碳性,提高了CO2焦油重整过程的催化操作稳定性。Ni-Fe合金的发展抑制了Ni-Fe/ZrO2催化剂表面积碳,提高了抗焦效率,使Ni-Fe/ZrO2催化剂保持了运行稳定性。
——会偷偷侵蚀你的发动机!

