金属盐对阴离子表面活性剂紫外吸收特性的影响
刘子龙,侯晓楠,郭丰志,吴冲,李雪,矫玉秋,卢贵武
(中国石油大学(北京) 理学院 油气光学探测北京市重点实验室,北京 102249)
表面活性剂为主剂的化学驱油技术常被用于三次采油[1-4]。地层油藏的复杂性对表面活性剂提出了更高的要求[5-7],而阴离子表面活性剂因其界面活性高、耐温性好等优点常被用于化学驱[8-9]。紫外吸收光谱法是测量表面活性剂浓度的常用方法[10-12],但金属盐对表面活性剂浓度测定影响的研究较少。本文利用紫外吸收光谱法研究金属盐对阴离子表面活性剂紫外吸收特性的影响,通过分析Ca2+、Mg2+、K+盐对SDBS和AOS溶液吸光度的影响,拟合了加入金属盐时SDBS和AOS溶液浓度与吸光度间的经验公式,为阴离子表面活性剂的耐盐性研究提供了重要的理论基础。
1 实验部分
1.1 试剂与仪器
无水氯化钙(CaCl2)、氯化镁(MgCl2)、氯化钾(KCl)均为分析纯;十二烷基苯磺酸钠(SDBS)、α-烯基磺酸钠(AOS)均为分析纯;去离子水。
FA2014电子天平;P5比例双光束紫外可见分光光度计;DHG-9240A电热鼓风干燥箱;HMS-6D磁力搅拌器。
1.2 溶液配制及光谱分析
1.2.1 十二烷基苯磺酸钠和α-烯基磺酸钠溶液的制备 利用电子天平称取十二烷基苯磺酸钠和 α-烯基磺酸钠各1 g,配成100 mL质量浓度均为1%的SDBS和AOS溶液作为母液。然后用去离子水将母液稀释成不同浓度,SDBS溶液质量浓度范围 0.001%~1.000%,AOS溶液质量浓度范围 0.1%~1.0%。再分别配制500 mmol/L CaCl2、MgCl2、KCl溶液以备用。由于实验发现氯化钠和氯化钾对阴离子表面活性剂吸光度影响的区别不大,氯化钠的研究较多[13-15],故选用研究较少的氯化钾试剂。实验中两种表面活性剂浓度的选择是基于其紫外吸光特性和耐盐性的不同。
1.2.2 光谱分析 紫外光谱分析使用P5比例双光束紫外可见分光光度计,使用10 mm光程长度的石英比色皿,吸收光谱波长范围400~200 nm,取样间隔1 nm,扫描速度6 nm/min,光程 10 mm。开始测量前,先将去离子水放入石英比色皿中做背景去除,去掉水溶液吸光度的影响。然后再将配制好的溶液分别做吸光度测量,每组做3次,记录每组吸收峰位置和吸光度。所有实验均在恒定室温下进行。
2 结果与讨论
2.1 SDBS的紫外吸收特性研究
2.1.1 SDBS的紫外吸收特性 图1给出了不同质量浓度的SDBS紫外吸收光谱图。


图1 不同质量分数SDBS在吸收波长224 nm(a)和 261 nm(b)处紫外吸收光谱图Fig.1 UV absorption spectra of SDBS with different mass fractions at absorption wavelengths of 224 nm(a) and 261 nm(b)
由图1可知,SDBS在波长224 nm和261 nm左右分别有强吸收峰和弱吸收峰,其吸收峰强度随溶液中SDBS浓度的升高而增强。224 nm处的强吸收峰出现在低浓度处,由SDBS结构中的共轭双键发生的π→π*跃迁所产生,出现的浓度范围为 0.001%~0.02%,这符合Lambert-beer定律。而261 nm处的吸收峰出现的浓度范围为0.01%~0.5%,该吸收峰是苯环的特征吸收峰,由环状共轭双键中的π→π*跃迁所引起,同时伴有精细结构的产生。
由Lambert-beer定律可知,紫外吸光度与溶液质量浓度在一定范围内存在线性关系,但超出一定质量浓度范围后,线性关系将不存在。图2给出了SDBS溶液在224 nm和261 nm波长处的吸光度值与质量分数的关系。
由图2可知,224 nm波长处吸收峰出现的浓度范围为0.001%~0.02%,但其吸光度在质量分数0.001%~0.01%时呈现良好的线性关系,超过 0.01% 时,线性关系变差,因此拟合了质量分数在 0.001%~0.01%时吸光度与质量浓度的关系曲线,线性关系为:y=241.258 4x-0.014 0,线性相关系数R2=0.999 4。

图2 SDBS的质量分数和吸光度的线性关系Fig.2 The linear relationship between the mass fraction and absorbance of SDBS
在261 nm波长处的吸收峰出现的浓度范围为0.01%~0.5%,该波长处吸光度在质量分数 0.001%~0.3%时线性关系较好,因此拟合了质量分数在0.001%~0.3%时吸光度与质量浓度的关系曲线,线性回归方程为:y=7.645 8x-0.035 1,线性相关系数R2=0.998 0。
从图中可以得到,SDBS溶液的吸收峰在 224 nm 处的拟合曲线斜率为241.258 4,比吸收峰在261 nm处的斜率更高,斜率高灵敏性更强,但线性拟合范围窄,适合浓度在0.01%以下SDBS溶液的定量测量。261 nm处的拟合曲线浓度范围较宽,更适合对浓度在0.01%~0.3%的SDBS溶液进行定量测量,但在低浓度(<0.01%)时,由于吸光度强度较低,灵敏性较弱,更适合用224 nm处拟合的曲线方程进行定量测量。
2.1.2 金属盐对SDBS紫外吸收特性的影响 当在SDBS溶液中各加入50 mmol/L Ca2+、Mg2+、K+盐,可以发现Ca2+盐和Mg2+盐容易使SDBS溶液产生沉淀。但Ca2+盐和Mg2+盐在小于0.006%质量分数时溶液较为澄清,加入钾盐溶液始终澄清。由于溶液产生沉淀会使SDBS溶液浓度下降,造成测量的吸光度误差过大,因此选用质量分数小于0.006%范围研究金属盐对SDBS溶液吸光度的影响。
图3给出了在不同浓度的SDBS溶液中加入Ca2+盐、Mg2+盐、K+盐对224 nm处吸收峰和 261 nm 处吸收峰强度的影响。
由图3a可知,对于224 nm处的吸收峰,在0.001%~0.003%浓度范围加入金属盐,吸光度变化微小。在0.003%~0.006%浓度加入金属盐,吸光度有明显降低,同时可以观察到Ca2+盐的影响最大,K+盐的影响最小。图3b为金属盐对SDBS溶液在261 nm处吸收峰强度的影响,由图可知,溶液中加入K+盐吸光度没有变化,与原溶液的曲线几乎重合。而Ca2+盐和Mg2+盐的加入都使原溶液吸光度明显升高,溶液浓度越高,吸光度升高越多。从金属盐对两处吸收峰的影响可以看到,随着金属盐的加入会对波长224 nm处的吸收峰发生明显的减色效应,对波长261 nm处的吸收峰发生明显的增色效应,同时得出金属阳离子对SDBS溶液吸光度影响顺序为:Ca2+>Mg2+>K+,这可能与金属阳离子的带电荷量和原子半径的差异有关,具有较大电荷量和原子半径更大的阳离子更容易与SDBS作用,影响其吸光度。


图3 金属盐对SDBS溶液在吸收峰 224 nm(a)、261 nm(b) 处吸光度影响Fig.3 The effect of metal salt on the absorbance of SDBS solution at the absorption peaks 224 nm(a) and 261 nm(b)
表1给出了SDBS溶液中加入不同金属盐质量浓度与吸光度的线性关系拟合方程。

表1 加入不同金属盐SDBS溶液的质量 浓度与吸光度线性关系Table 1 The linear relationship between the mass concentration and absorbance of SDBS solutions with different metal salts
由表1可知,与SDBS原溶液方程相比,加入金属盐224 nm处的吸收峰拟合方程斜率减小,261 nm处的吸收峰拟合方程斜率增大,加入Ca2+盐斜率变化最大,加入K+盐拟合方程斜率变化最小,同时由线性相关系数(R2)也可以得到,Ca2+盐拟合方程的线性相关度相对较差,加入K+盐拟合方程的线性相关度最好,表明K+盐对溶液影响最小,Ca2+盐影响最大。
2.2 AOS的紫外吸收光谱研究
2.2.1 AOS的紫外吸收特性 图4给出了AOS在不同质量浓度的紫外吸收光谱图。

图4 不同质量分数AOS的紫外吸收光谱Fig.4 UV absorption spectra of AOS with different mass fractions
由图4可知,AOS在波长238 nm处有一个最大吸收峰,此吸收峰是由AOS结构中的共轭双键产生的π-π*跃迁所引起。随着AOS溶液浓度的升高,238 nm处吸收峰强度逐渐升高。与SDBS的紫外吸收光谱(图1)相比,AOS溶液吸收峰在较高浓度 0.1% 时才初显。当AOS溶液浓度增加到1%时光谱波形依然良好,而SDBS溶液在1%时特征吸收峰已经因吸光度过高而消失。这是由于SDBS结构中的苯环会增强溶液吸光度,而AOS结构中不含苯环,使AOS溶液在较高浓度才可以观察到明显的吸收峰。
图5给出了用紫外分光光度计测量不同质量分数的AOS在238 nm波长处的吸光度与质量分数的关系曲线。

图5 AOS的质量分数和吸光度的线性关系Fig.5 The linear relationship between the mass fraction and absorbance of AOS
由图5可知,AOS溶液在0.1%~1%范围内线性关系很好,线性回归方程为:y=1.452 8x-0.019 64,线性相关系数R2=0.999 2。
2.2.2 金属盐对AOS紫外吸收特性的影响 当在AOS溶液中加入50 mmol/L CaCl2时,AOS溶液极易产生沉淀。而当在AOS溶液中加入50 mmol/L MgCl2、KCl时,AOS溶液在0.1%~1%范围内都很澄清,因此测量不同浓度AOS溶液中加入50 mmol/L MgCl2、KCl的吸光度变化。
图6给出了在不同浓度的AOS溶液中加入Mg2+盐、K+盐对吸光度的影响。
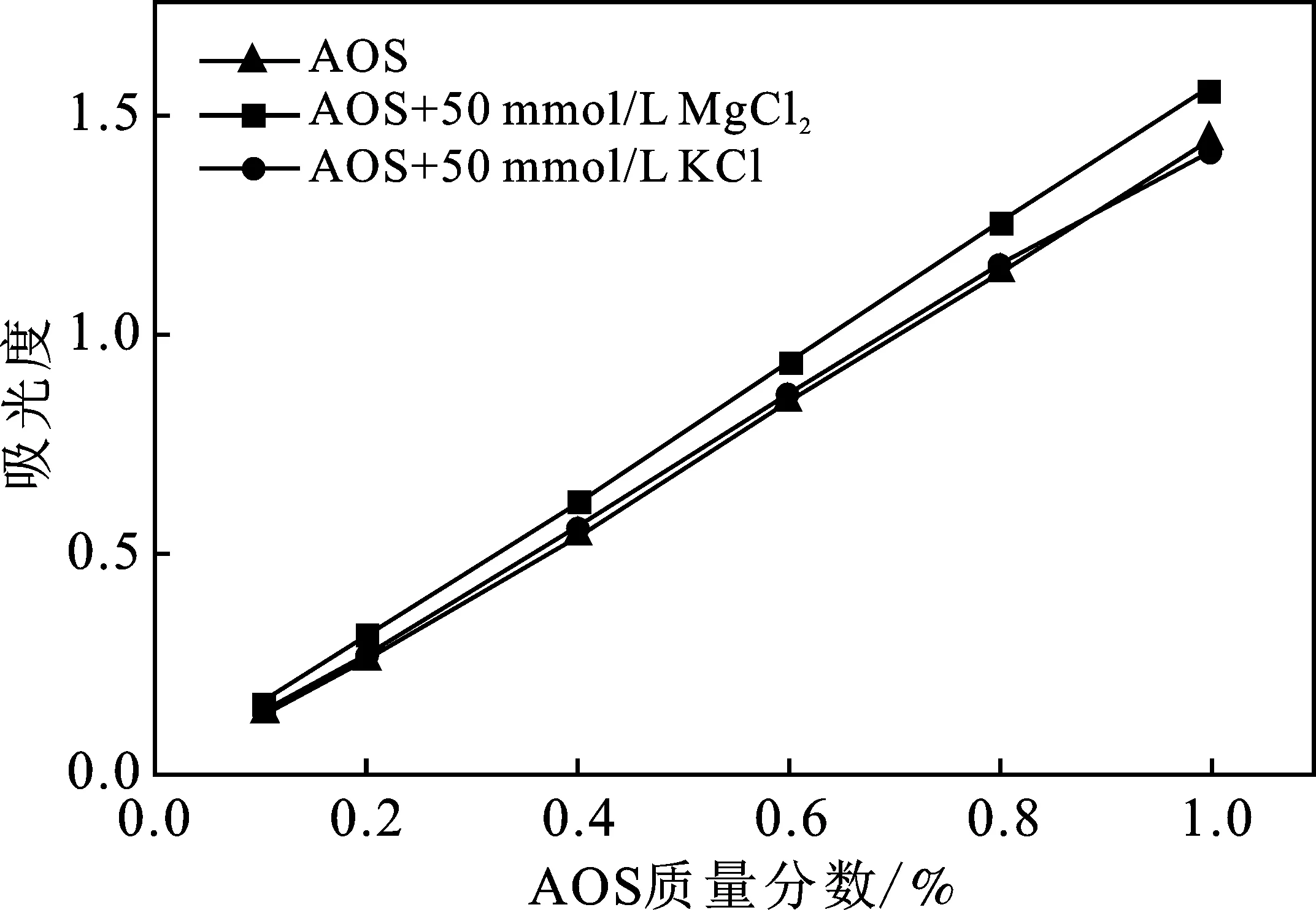
图6 Mg2+盐和K+盐对AOS吸光度的影响Fig.6 The influence of Mg2+ and K+ salt on the absorbance of AOS
由图6可知,AOS溶液中加入MgCl2溶液,其吸光度会升高,且升高后的曲线线性关系良好,线性关系方程由表2给出,可以看出加入Mg2+盐的溶液拟合曲线斜率有明显升高。当在AOS溶液中加入KCl溶液,可以发现溶液的吸光度变化微小。表明三种金属盐中钾盐对AOS溶液吸光度影响最小,其次是镁盐,最后是钙盐。
表2给出了AOS溶液中加入不同金属盐质量浓度与吸光度的线性关系拟合方程。

表2 加入不同金属盐AOS溶液的质量浓度与 吸光度线性关系Table 2 The linear relationship between the mass concentration and absorbance of different metal salt AOS solutions
由表2可知,在AOS溶液中加入Mg2+盐和K+盐,拟合的线性方程相关度都可以达到0.99以上,线性拟合度比SDBS溶液更好。加入K+盐后拟合的曲线方程斜率变化很小,加入Mg2+盐后拟合的曲线方程斜率有明显升高。表明Mg2+盐比K+盐对AOS溶液的影响更大。
3 结论
本文采用紫外吸收光谱法研究了三种金属盐对阴离子表面活性剂(SDBS和AOS)紫光吸收特性的影响。结果表明,由于SDBS的芳香烃结构,SDBS的紫外吸收光谱在224 nm和261 nm处出现一强一弱两个吸收峰。当在SDBS溶液中加入金属盐,发现在吸收峰224 nm处产生减色效应,溶液吸光度有所下降,在吸收峰261 nm处产生增色效应吸光度升高。而AOS的紫外吸收光谱仅在238 nm处有一个吸收峰,该吸收峰由AOS结构中的共轭双键所产生。当在AOS溶液中加入金属盐,发现钙盐易和AOS溶液产生沉淀,镁盐的加入会使AOS溶液吸光度升高,钾盐的加入对AOS溶液吸光度的影响最小。最终得到三种金属盐对SDBS和AOS溶液吸光度影响顺序为Ca2+>Mg2+>K+,这与金属阳离子的带电荷量和原子半径大小有关。

