冻融胚胎过夜培养后移植患者妊娠情况分析
王晓婷,陈宥艺,韩晓艳,张 祥,闫春芳
(西安市第四医院生殖医学中心,陕西 西安 710004)
对于新鲜取卵周期未移植行全胚冷冻,或移植后未孕仍有剩余冻存胚胎的患者,冻融胚胎移植(frozen-thawed embryo transfer,FET)是一个有效的临床策略。它具有冻融移植周期子宫内膜容受好、能有效预防卵巢过度刺激综合征、降低治疗成本并能增加累计临床妊娠率等优势。虽然影响冻融胚胎移植妊娠率的因素很多,但是冻融胚胎的质量及继续发育潜能无疑是最重要的影响因素之一。本研究回顾性分析了西安市第四医院536例冻融胚胎移植周期,旨在探索冻融胚胎过夜培养后卵裂球增长与否及继续发育的情况对临床妊娠结局的影响,并为需要进行单胚胎移植的患者,提供最佳的胚胎选择方案。
1资料与方法
1.1患者资料
收集2018年1月至2019年3月在西安市第四医院进行冻融胚胎移植患者的536个周期的临床资料。研究对象的纳入标准:①女方因盆腔输卵管、排卵障碍、子宫内膜异位症、不明原因等因素,男方因少弱畸形精子症或无精子症等因素进入常规体外受精与胚胎移植(in vitro fertilization,IVF)或卵胞浆内单精子显微注射(intracytoplasmic sperm injection,ICSI)周期;②所有患者的解冻胚胎均是胚龄为第3天卵裂期的冷冻胚胎、过夜培养后移植2枚胚胎的冻融移植周期。排除标准:①患者有明确影响胚胎着床的因素,包括子宫畸形、输卵管积水、子宫腺肌症等;②夫妇一方染色体核型异常;③女方有未控制至正常的糖尿病、结核、甲亢,以及其他自身免疫系统疾病者。
1.2方法
1.2.1内膜准备
所有患者均于月经周期第2~4天行阴道超声及基础性激素检查,根据既往月经周期、基础疾病及患者的意愿,采用自然周期、促排卵周期、人工周期或降调节+人工周期方案行移植前的内膜准备,子宫内膜厚度≥7mm作为冻融胚胎移植的标准。
1.2.2解冻胚胎
所有纳入研究对象的胚胎均为常规IVF或ICSI受精、体外培养、采用玻璃化冷冻保存的第3天卵裂期胚胎。所有胚胎均采用玻璃化冷冻方法冷冻,冷冻前根据卵裂球个数、均匀程度及碎片情况对胚胎进行分级[1],冷冻胚胎均评级为Ⅰ~Ⅲ级。使用玻璃化解冻试剂盒(日本加藤公司)对第3天卵裂期胚胎进行解冻复苏。试剂盒包括解冻液TS、稀释液DS、冲洗液WS1和WS2,解冻过程:将胚胎从液氮中取出,迅速置于37℃的TS液中,1min后将其依次转移至DS、WS1、WS2中分别放置3min、5min、5min。最后转移至预先平衡好的37℃胚胎培养液G2 PLUS(瑞典vitrolife公司),置于37℃、6%CO2、5%O2的培养箱中继续培养18~20h。
1.2.3解冻胚胎存活标准
解冻后胚胎有半数及以上卵裂球存活视为存活胚胎[2]。
1.2.4分组方法
依照移植的2枚胚胎过夜培养后(18~20h)卵裂球增长与否分为3个大组:A2组(n=425),有2枚胚胎均有卵裂球增长;A1组(n=89),只有1枚胚胎有卵裂球增长;A0组(n=22),有2枚胚胎均无卵裂球增长。再根据每个胚胎卵裂球增长的数目及发育情况将A2组分层为5个小组,即aa组、ab组、ac组、bb组、cc组(a:胚胎致密化、融合或者形成早期囊胚;b:胚胎增长卵裂球个数>2个;c:胚胎增长卵裂球个数≤2个)。
1.2.5确定妊娠结局
移植后14d测血人绒毛膜促性腺激素(β-human chorionic gonadotrophin,β-hCG),血β-hCG≥50IU/L者判断为生化妊娠并继续黄体支持。移植后30d阴道超声检查,见孕囊及心管搏动为临床妊娠。
1.3统计学方法

2结果
2.1一般临床结果
冻融移植的536个周期,获得临床妊娠周期293例,临床妊娠率为54.7%;孕囊数389个,胚胎种植率为36.3%;早期流产49例,早期流产率为16.7%。A2、A1、A0组的年龄、内膜厚度、身体质量指数(body mass index,BMI)和不孕年限比较差异均无统计学意义(P>0.05),见表1、表2。
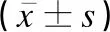
表1 A2、A1、A0 组患者的基本情况
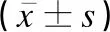
表2 A2组的5个小组患者的基本情况
2.23组胚胎继续发育情况与患者临床妊娠情况的关系
冻融胚胎经培养18~20h后进行移植,A2、A1、A0 3组的临床妊娠率分别为60.9%、36.0%、9.1%,差异有统计学意义(χ2=37.76,P<0.05);3组胚胎种植率分别为41.1%、21.3%、4.5%,差异有统计学意义(χ2=44.73,P<0.05);3组早期流产率分别为16.2%、18.8%、50.0%,差异无统计学意义(P>0.05),见表3。

表3 A2、A1、A0 3组的临床妊娠情况的总体比较[%,(n/N)]
3组间的临床妊娠率(A2组vs A1组:χ2=18.704;A2组vs A0组:χ2=23.146)和胚胎种植率(A2组vs.A1组:χ2=24.359;A2组vs.A0组:χ2=23.389)两两比较差异均有统计学意义(P<0.05);3组早期流产率两两比较差异均无统计学意义(P>0.05)。
2.3 A2组的5个小组临床妊娠情况比较
分两个层次比较A2组内5个小组(aa组、ab组、ac组、bb组、cc组)的临床妊娠情况,首先将至少移植含有1枚胚胎出现致密化、融合或者形成早期囊胚的3个小组(aa组、ab组、ac组)进行比较,在至少有1枚a类胚胎的前提下,观察另一枚胚胎发育情况对临床妊娠结局的影响;其次再对aa组(2枚胚胎均出现致密化、融合或者形成早期囊胚)、bb组(2枚胚胎卵裂球增长个数均>2个)、cc组(2枚胚胎增长卵裂球个数均≤2个)3个小组之间妊娠情况进行比较,结果如下。
2.3.1 aa、ab、ac 3组间比较
aa、ab、ac 这3个小组中,均至少有1枚胚胎出现致密化、融合或者形成早期囊胚。结果显示,随着另一枚胚胎增长卵裂球数目的下降,临床妊娠率和胚胎种植率有下降趋势,早期流产率呈上升趋势,见表4。组间两两比较显示:aa组的临床妊娠率(χ2=5.976)和胚胎种植率(χ2=15.906)均显著高于ac组,且ab组的胚胎种植率显著高于ac组(χ2=9.839),差异均有统计学意义(P<0.05),3组间的早期流产率差异无统计学意义(P>0.05)。
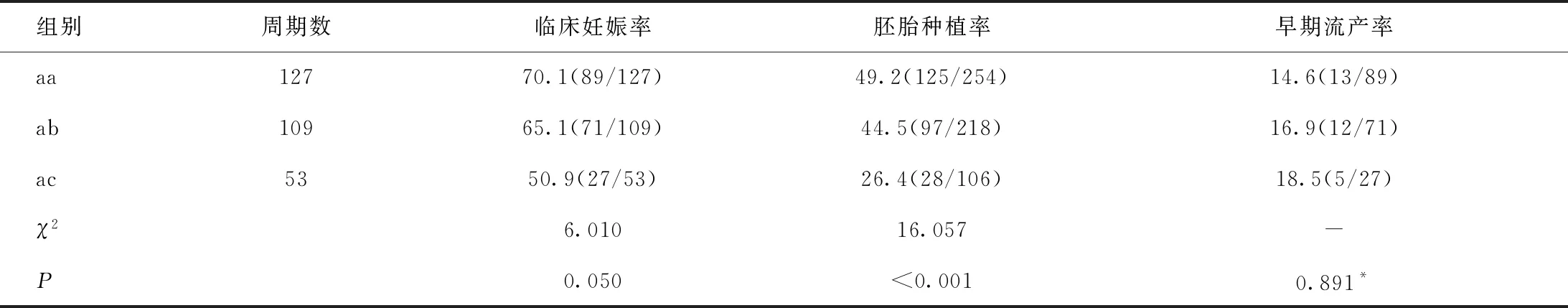
表4 aa、ab、ac 3组的临床妊娠情况的总体比较[%,(n/N)]
2.3.2 aa、bb、cc 3组间比较
aa、bb、cc 3个小组中,随着2枚胚胎卵裂球增长数目的减少,临床妊娠率和胚胎种植率依次出现下降趋势,见表5。组间两两比较显示:其中,aa组的临床妊娠率显著高于cc组(χ2=8.108),aa组的胚胎种植率显著高于cc组(χ2=6.971),bb组的早期流产率显著低于cc组(χ2=3.890),上述差异均有统计学意义(P<0.05)。
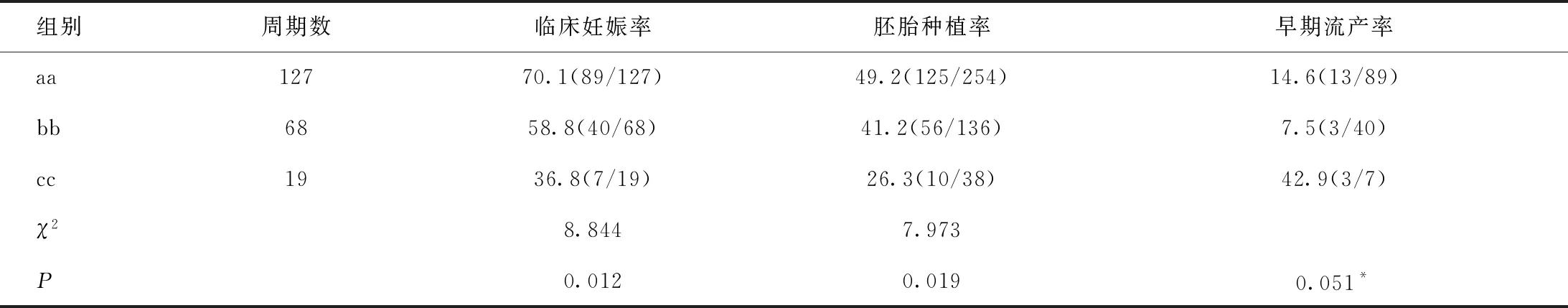
表5 aa、bb、cc 3组临床妊娠情况的总体比较[%,(n/N)]
3讨论
3.1对冻融胚胎复苏后继续发育情况进行评估的重要性
随着FET技术的普及,广大人类辅助生殖技术专家及工作者希望可以在提高妊娠率和种植率的同时,降低多胎率和流产率,增加FET的安全性[3]。这就要求我们对FET周期中的胚胎发育潜力进行判断,不仅仅要评估冷冻前的胚胎评分,还需结合解冻后胚胎的继续发育情况进行综合考量。
有研究认为冻融胚胎复苏后即使有卵裂球损伤或死亡,过夜培养后如能继续生长,仍可获得较好的种植率,而且是否能继续生长对此类胚胎的种植潜力非常关键[4]。还有研究发现,随着胚胎复苏后卵裂球增长数目的增加,临床妊娠率似有升高的趋势[5]。卵裂期胚胎解冻后过夜培养如能继续发育并且发生致密化将会有更高的活产率[4]。低质量胚胎过夜培养后如能获得更多的卵裂也会有比较不错的妊娠率,尽管这个比率会低于高质量胚胎[6]。众多研究表明,复苏后胚胎的发育潜能至关重要,且其影响因素需要从多个角度进行探索,本研究旨在通过观察解冻后过夜培养的2枚胚胎继续发育情况与患者妊娠情况的关系,以期更加细化、精准地评价胚胎的种植潜能,为临床解冻移植策略提供最优的胚胎选择依据。
3.2为优化临床结局制定最佳的胚胎选择策略
本研究中,A2、A1、A0这3个组间的临床妊娠率和种植率比较均有统计学差异,且A2组>A1组>A0组,说明胚胎解冻过夜培养后是否有卵裂球增长与临床妊娠情况息息相关,这与之前研究一致[7]。本研究结果还显示:A0组(2枚胚胎均无卵裂球增长)临床妊娠率和胚胎种植率大大降低,表明如果解冻胚胎过夜培养18~20h后仍无卵裂球增长,提示妊娠失败的可能性较大。Laverge等[8]在1998年研究报道,对复苏后经过夜培养后没有卵裂球增长的胚胎,进行荧光原位杂交发现染色体异常比例很高,仅有20%左右的胚胎为正常二倍体。若移植此类胚胎,不但胚胎着床率低,且因染色体异常而发生流产的几率增加[9-10]。如此高的染色体异常比例,临床结局可想而知。因此本研究提示,提前解冻胚胎过夜培养时,应该把是否有卵裂球增长作为一个重点观察指标,来指导冻融胚胎移植策略;2枚胚胎均无卵裂球增长的周期、除非患者不同意其它移植策略或已经没有冻存胚胎可供选择,否则建议继续行胚胎培养至囊胚移植,尤其对于反复种植失败的患者,不建议对此类胚胎进行移植。
对A2组(即2枚胚胎均有卵裂球数生长组)进一步分层分析,aa、ab、ac这3个小组的比较数据表明,无论临床妊娠率还是胚胎种植率均与胚胎继续增殖发育情况有关。而且随着另一枚胚胎增长卵裂球数的下降,临床妊娠率和胚胎种植率均出现下降趋势,这与之前的研究报道一致[11]。aa组在临床妊娠率和种植率上均高于ac组(P<0.05),且ab组的胚胎种植率高于ac组(P<0.05)。可以看出,从临床妊娠角度来看,a类胚胎(即过夜培养后出现致密化、融合或者形成早期囊胚的胚胎)发育潜能有明显的优势,其次为b类胚胎(即胚胎增长卵裂球个数>2个)。aa、bb、cc这3个组比较,aa组的临床妊娠率和胚胎种植率显著高于cc组(P<0.05);bb组的早期流产率显著低于cc组(P<0.05),aa组和bb组早期流产率差异无统计学意义(P>0.05)。从早期流产率的角度来看,b类胚胎继续发育的潜能优于c类胚胎,后期需要加大样本量进一步研究。本研究结果表明,过夜培养后胚胎卵裂球个数增长越多,尤其是已经出现致密化、融合或形成早期囊胚的胚胎,患者将获得较好的临床结局,与Solé等2011年研究结果一致,因此,我们有理由认为选择过夜培养后出现致密化、融合或形成早期囊胚的a类胚胎及卵裂球数目增长较多的b类胚胎进行移植,是获得成功妊娠的一个很关键的胚胎选择策略。
胚胎种植率增加的同时必然会伴有临床多胎妊娠率的增加,冻融胚胎过夜培养后,如果同时移植2枚都能达到b类以上的胚胎,则胚胎种植率均可达到40%以上,从患者妊娠安全性角度考虑,移植前需要综合考虑各方面因素尽量降低多胎率。如果是单角子宫、剖宫产术后的疤痕子宫及任何原因期望为单胎妊娠的患者,最好继续培养至囊胚行单囊胚移植或选择a类或b类胚胎进行移植,在保证较高临床妊娠率的前提下,能有效地降低多胎率,增加FET的安全性。当然,对于获得胚胎非常不容易且胚胎较少的患者,可能面临囊胚培养后无可移植囊胚的风险,在临床实际工作中,要根据患者的胚胎发育情况、子宫内膜、身体状况、家庭经济及患者意愿进行综合分析,最终决定冻融胚胎移植的最优方案。
3.3总结
综上所述,冻融胚胎过夜培养后移植2个以上卵裂球增长的胚胎,尤其是已经发生致密化、融合或形成早期囊胚的胚胎,能获得比较高的临床妊娠率、种植率和相对较低的流产率;单胚胎移植时可优先选择胚胎已经致密化、融合或者形成早期囊胚的胚胎。对于反复移植失败的患者,不建议移植卵裂球数目未增加或者卵裂球数增加≤2个的胚胎,可考虑继续培养至囊胚再移植。
——以1985—2020年为例

