基于石墨烯量子点的类过氧化物酶活性用于过氧化氢的检测
马 纳,秦莉莉,尚冰冰,2,齐宝平,2†
1. 湖北民族大学生物资源保护与利用湖北省重点实验室,湖北恩施445000;2. 湖北民族大学化学与环境工程学院,湖北恩施445000
0 引言
纳米酶(nano-enzyme) 是具有类酶活性的纳米催化材料,与天然酶和传统人工酶相比,具有稳定性好、成本低、可重复利用、便于修饰等优点[1~3]。纳米酶已经成功模拟了包括氧化酶、过氧化物酶、过氧化氢酶、超氧化物歧化酶和水解酶等天然酶,在生物传感、癌症诊断、组织工程、环境保护等多个领域得到应用[4~9]。碳质纳米材料作纳米酶具有稳定性好、廉价易得、生物毒性低以及易于化学修饰等特点,受到广泛的关注[10]。1996 年,Dugan 等[11]首次报道富勒烯及其衍生物具有类似超氧化物歧化酶(SOD) 的活性[11],随后越来越多的碳质纳米材料,包括 碳 纳 米 管[12,13]、石 墨 烯 量 子 点(GQDs)[14,15]、氮 化碳[16,17]等相继被发现具有类酶活性。Zheng 等[18]报道了GQDs 具有高效的类过氧化物酶催化活性,其活性远远高于大尺寸氧化石墨烯。Sun 等[15]通过选择性失活特定的含氧官能团,探究了GQDs 表面官能团对GQDs 衍生物作为过氧化物酶模拟物的催化活性,发现GQDs 表面的羰基(—C=O) 是催化活性位点,羧基(—COOH) 可作为底物的结合位点,羟基(—OH) 对催化反应起到抑制作用。Nirala等[14]研究了外界因素对GQDs 作为类过氧化物酶的催化活性的影响,发现GQDs 的催化活性与催化剂的用量、底物的浓度、检测液的pH 值和温度密切相关。目前,GQDs 的过氧化物酶性质研究还处于初期阶段,尚缺乏深入的基础研究。因此,如何提高GQDs 作过氧化物酶的活性以促进GQDs 在催化领域的应用,具有重要意义。
本文采用超声剥离法与化学氧化法分别制备了含氧量较低的GQDs 与含氧量较高的GOQDs,用于3,3′,5,5′-四甲基联苯胺(TMB)与过氧化氢(H2O2) 体系(TMB/H2O2)的催化,探讨了GQDs 表面的含氧量对其类过氧化物酶催化活性的影响,并在此基础上构建的一种基于GOQDs 的H2O2分析方法。
1 实验部分
1.1 主要试剂与仪器
试剂:石墨纳米颗粒(GNPs,纯度高于93%,平均直径为3~4 nm)购自SkySpring 纳米材料公司;C2H5OH、H2SO4、K4[Fe(CN)6]‧3H2O、K3[Fe(CN)6]、KMnO4、H2O2(30%)、HCl等试剂均购自上海阿拉丁生化科技股份有限公司;3,3′,5,5′-四甲基联苯胺购自上海麦克林生化科技有限公司;实验室用水均为超纯水。
仪器:JEM-2100F 型高辨透射电子显微镜(TEM, JEOL 公司)、Autolab PGSTAT302N 型 电化学工作站(Metrohm 公司)、Avatar 360 型Fourier变换红外光谱仪(FT-IR, Thermo Nicolet 公司)、RF-6000 型 荧光分光光度计(Shimadzu 公司)、TU-1901 (UV-Vis)型双光束紫外-可见光光度计(北京普析通用仪器有限责任公司)。
1.2 GQDs、GOQDs 及修饰电极的制备
1.2.1 GQDs 的制备
将30 mg GNPs 加入到100 mL 圆底烧瓶中,加入30 mL 乙醇/水(体积比1∶1),在冰浴中超声振荡6 h,所得悬浊液以10 000 r/min 转速离心20 min,收集上层清液,旋转蒸发去除溶剂,重新分散到超纯水中,所得浅棕色分散液记为GQDs。
1.2.2 GOQDs 的制备
将0.5 g GNPs 加入到含17 mL H2SO4与0.38 g NaNO3的250 mL 圆底烧瓶中,置于冰浴中,剧烈搅拌下缓慢加入2.5 g KMnO4,反应2 h 后,向反应体系中加入50 mL 超纯水。然后,向上述溶液中滴加2 mL 30% 的H2O2,将反应体系转入到250 mL HCl/H2O(体积比为1∶10)溶液中,以20 000 r/min转速离心20 min,去除上清液,反复加入超纯水洗涤,直至悬浮液接近中性。将上述悬浮液在冰浴中超声3 h,以10 000 r/min 转速离心30 min,收集上层棕色清液,记为GOQDs。
1.2.3 修饰电极的制备
采用粒径为0.3 mm 和0.05 mm Al2O3粉末依次对玻碳电极(GCE,直径3.0 mm) 进行抛光,超声清洗后,用N2吹干电极表面。电极倒置,将5 μL GQDs 溶液滴在GCE 表面,室温风干,得到GQDs修饰的GCE 电极,记为GQDs/GCE。
同上述步骤,制备GOQDs 修饰的GCE 电极,记为GOQDs/GCE。
1.3 电化学检测
循环伏安法(CV)、电化学阻抗法(EIS)与电流-时间曲线(I-t)测试均在电化学工作站上进行。以饱和甘汞电极作参考电极、铂丝作对电极、GCE及其修饰电极(GQDs/GCE、GOQDs/GCE)作工作电极,组成三电极体系。
CV 测试在0.2 mol/L pH 3.8 的柠檬酸-磷酸盐缓冲溶液(CPBS)中进行,电势扫描范围为-1.0~+0.2 V,扫描速率为50 mV/s,测试过程中采用N2保护。 EIS 测试在含10 mmol/L K3Fe(CN)6/K4Fe(CN)6(摩尔比1∶1)的0.1 mol/L KCl溶液中。在0.2 mol/L pH 3.8 CPBS 中,连续加入不同浓度的H2O2,采集GOQDs/GCE 修饰电极的I-t数据。
1.4 GQDs 和GOQDs 的类过氧化物酶活性测试
以TMB/H2O2体系的显色反应考察GQDs 和GOQDs 的类过氧化物酶活性,操作步骤如下:依次将10 μL GQDs (0.2 mg/mL)、100 μL H2O2(50 mmol/L)、100 μL TMB (0.8 mmol/L) 和1 mL 乙酸盐缓冲液(0.2 mol/L, pH 3.5) 加入到离心管中,置于50 ℃水浴中反应10 min,测试反应后的溶液在500~800 nm 波长范围内的吸收光谱。
同上述步骤,考察GOQDs 的类过氧化物酶活性。
2 结果与讨论
2.1 材料表征
2.1.1 TEM 分析
采用TEM 对GQDs 与GOQDs 的粒径与形貌进行表征,结果如图1 所示。由图1 可知,所制备的GQDs 与GOQDs 粒径较均一,形状接近圆形,且具有较好的分散性。分别对200 颗左右的GQDs 与GOQDs进行粒径统计,GQDs 与GOQDs 的平均粒径分别为(3.3±0.2)nm 与(3.4±0.5)nm,两种碳质纳米颗粒的粒径接近。

图1 GQDs (a)与GOQDs (b)的TEM 表征Fig.1 TEM images of GQDs (a)and GOQDs (b)
2.1.2 FT-IR 分析
采用FT-IR 对GQDs 与GOQDs 表面的官能团进行表征,结果如图2 所示。由图2 可知,位于3 440、1 610、1 110 cm-1处的吸收峰分别归属于GQDs 与GOQDs 表面上羟基(—OH)伸缩振动、羰基(C=O) 伸缩振动及(C—O—C)醚键伸缩振动。而GOQDs 谱图在1 740、1 242 cm-1处有羧基中的C=O 伸缩振动和C—O 伸缩振动。由此可知,与GQDs 相比,GOQDs 表面具有更丰富的含氧官能团,这归因于GOQDs 制备过程中采用了强氧化反应体系。

图2 GQDs 与GOQDs 的FT-IR 图Fig.2 FT-IR spectra of GQDs and GOQDs
2.1.3 XPS 分析
采用XPS 技术对GQDs 与GOQDs 的组成进行表征,结果如图3 所示。由图3 可知,GQDs 与GOQDs 均 由C 和O 组 成,位 于284. 2 eV 和534.5 eV 的特征峰分别归属于C 1s 与O 1s。对目标元素C 1s 和O 1s 的峰面积进行积分,采用相对灵敏度因子法[19]得到各目标元素的百分含量,GQDs 与GOQDs 中O/C 的含量之比分别为0.11 与0.52。由此可以得出,与GQDs 相比较,GOQDs 表面具有更丰富的含氧官能团,与FT-IR 测试结果一致。
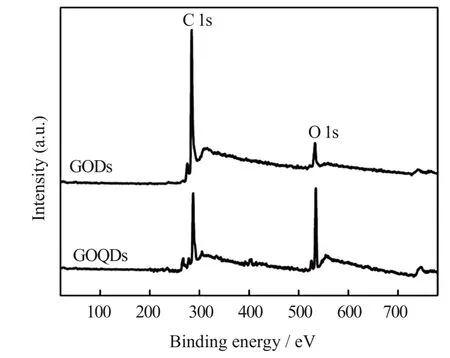
图3 GQDs 与GOQDs 的XPS 图Fig.3 XPS spectra of GQDs and GOQDs
2.1.4 荧光分析
采用荧光分光光度计,在240~500 nm 波长范围内,以20 nm 幅度改变激发波长,观察GQDs 与GOQDs 的水溶液发射波长的变化,结果如图4 所示。由图4 可知,GQDs 与GOQDs 的荧光发射波长随激发波长的改变而改变,其荧光性能表现出激发依赖性;GQDs 的最佳发射波长位于390 nm,GOQDs 的最佳发射波长位于536 nm;在365 nm 紫外灯照射下,GQDs 水溶液呈现蓝色荧光,而GOQDs 水溶液呈现蓝绿色荧光。与GQDs 相比较,GOQDs 的荧光发射波长有比较明显的红移,这归因于GOQDs表面含氧官能团的增加[19,20]。

图4 GQDs (a)与GOQDs (b)水溶液的荧光发射光谱插图:GQDs(a)与GOQDs(b)水溶液在365 nm 紫外灯照射下的照片Fig.4 Fluorescence emission spectra of GQDs (a)and GOQDs (b)dispersed in water Inset:photos of GQDs (a)and GOQDs (b)under 365 nm UV lamp excitation
2.2 GQDs 与GOQDs 的类过氧化物酶催化活性
2.2.1 GQDs/GCE 与GOQDs/GCE 修饰电极的CV分析
将GQDs 与GOQDs 分别修饰到GCE 电极上,在含6 mmol/L H2O2的0.2 mol/L pH 3.8 CPBS 中采用CV 测试考察GQDs 与GOQDs 作为类过氧化物酶对底物H2O2的催化能力,结果如图5 所示。由图5 可知,在相同实验条件下,相对于裸电极GCE,GQDs/GCE 与GOQDs/GCE 对 底 物H2O2均 有 较大的响应电流,这归因于GQDs 与GOQDs 的类过氧化物酶催化活性[14,15];相 对 于GQDs/GCE,GOQDs/GCE 上的响应电流增加显著,在-0.92 V附近,GQDs/GCE 与GOQDs/GCE 对H2O2的还原电流峰值分别为0.38、1.65 mA,GOQDs 展现出更好的催化活性。CV 测试结果表明,GQDs 与GOQDs 均对H2O2展现出类过氧化物酶活性,含氧量较高的GOQDs 展现出更好的催化活性。
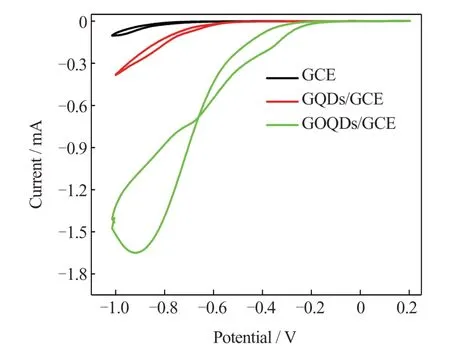
图5 GCE、GQDs/GCE 及GOQDs/GCE 在含6 mmol/L H2O2的0.2 mol/L pH 3.8 CPBS 中的CV 曲线Fig.5 CV curves of GCE, GQDs/GCE, and GOQDs/GCE in 0.2 mol/L pH 3.8 CPBS containing 6 mmol/L H2O2
2.2.2 GQDs/GCE 与GOQDs/GCE 修饰电极的EI S分析
采用EIS 技术测试GQDs/GCE 与GOQDs/GCE 在含10 mmol/L K3Fe(CN)6/K4Fe(CN)6(1∶1)的0.1 mol/L KCl 溶液中对电子的转移能力[21],结果如图6 所示。由图6 可知,以[Fe(CN)6]3-/4-作探针的交流阻抗图谱中,裸电极GCE 的电子转移阻碍常数(Ret) 为780 Ω;修饰电极GQDs/GCE 的Ret几乎为0,表明GQDs 碳质纳米材料具有良好的导电性能;修饰电极GOQDs/GCE 的Ret增加至8 780 Ω,表明GOQDs 对探针具有较强的排斥作用,这归因于GOQDs 表面丰富的含氧官能团降低了碳质纳米材料的导电性能,抑制了电极表面的电子传递。
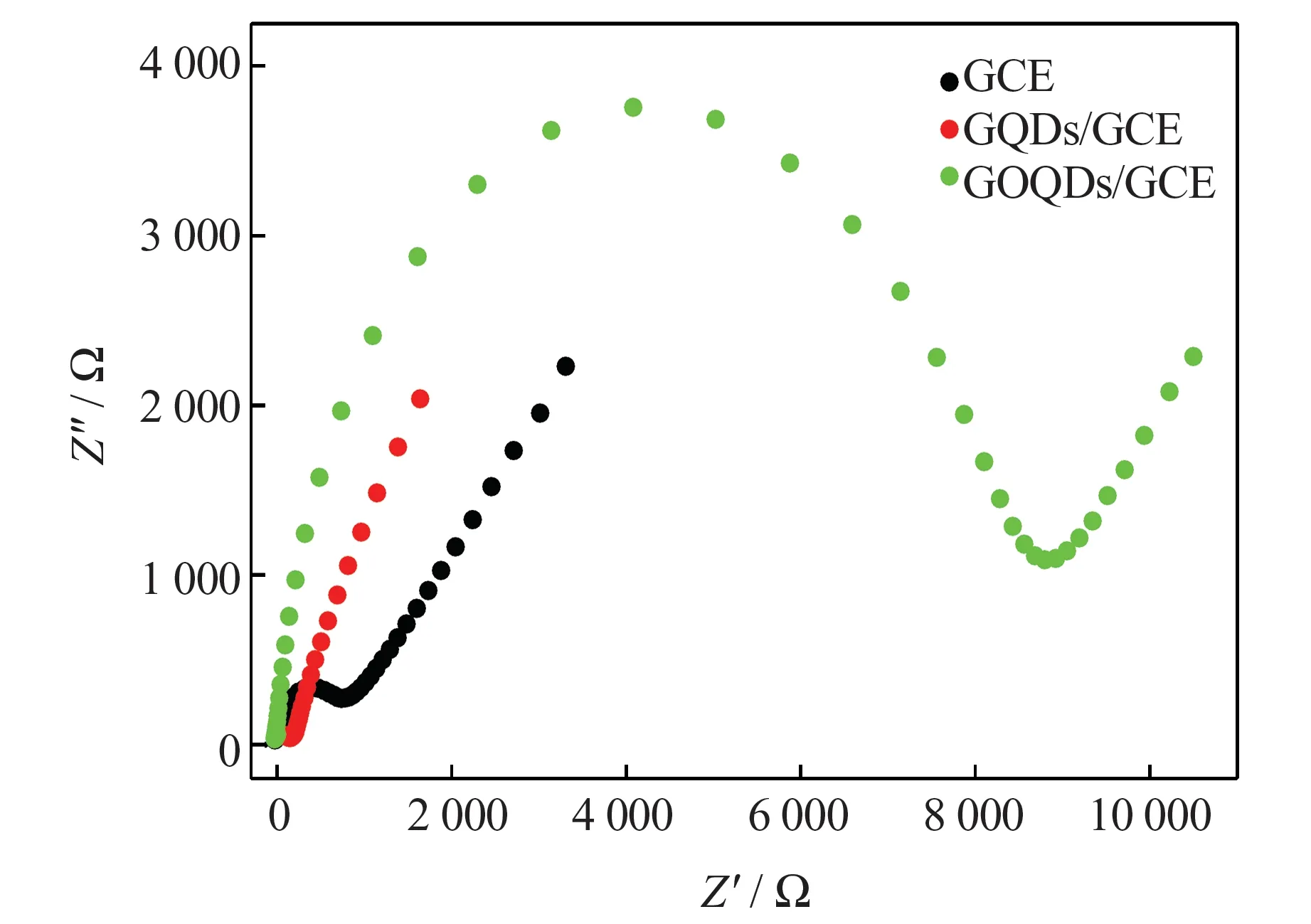
图6 GCE、GQDs/GCE 及GOQDs/GCE 在0.1 mol/L KCl 溶液(含10 mmol/L K3Fe(CN)6/K4Fe(CN)6(1∶1))中的EIS 曲线Fig.6 EIS curves of GCE, GQDs/GCE and GOQDs/GCE in 0.1 mol/L KCl solution (containing 10 mmol/L K3Fe(CN)6/K4Fe(CN)6 (1∶1))
2.2.3 GQDs 与GOQDs 的类过氧化物酶活性
采用TMB/H2O2体系的显色反应考察GQDs和GOQDs 的类过氧化物酶活性。如图7(a)(b)所示,GQDs 和GOQDs 均可通过催化H2O2的反应,将溶液中的TMB 氧化为氧化态TMB (oxTMB),溶液由无色变为蓝色,oxTMB 在652 nm 处具有特征吸收峰(曲线e 与f)[22];当GQDs 或者GOQDs 单独与TMB 反应时,溶液仍然为无色,无法被氧化(曲线c与d),从而证实GQDs 与GOQDs 具有类过氧化物酶活性。图7(b)显示了GOQDs 催化H2O2氧化TMB 显色的过程。
采用酶动力学实验探究GQDs 与GOQDs 的类过氧化物酶活性,在保持TMB 或H2O2浓度不变的条件下,通过改变另一底物的浓度,进行酶促反应[22]。如图7(c)~(f)所示,底物TMB 的浓度在0~0.12 mmol/L 或底物H2O2的浓度在0~300 mmol/L的范围内,GQDs 或GOQDs 与TMB/H2O2体系的催化反应遵循Michaelis-Menten 动力学模型[23],即满足1/v=Km/(vmax[S])+1/vmax,其中,v为不同底物浓度下的初始反应速率;[S]为底物的浓度;Km为米氏常数(为反应速度达到最大速度一半时的底物浓度,通常用于表示酶与底物的亲和力,Km数值越小,酶与底物的亲和力越强);vmax为最大初始反应速率。通过方程式的斜率和截距可以得出Km和vmax。
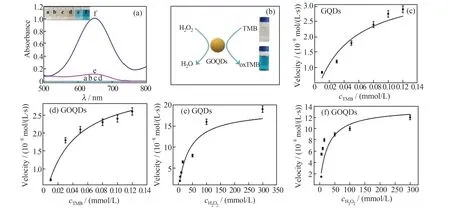
图7 (a)TMB、TMB+H2O2、TMB+GQDs、TMB+GOQDs、TMB/H2O2+GQDs 和TMB/H2O2+GOQDs(曲线a~f)的吸收光谱及对应颜色变化;(b)GOQDs 催化H2O2氧化TMB 显色的示意图;GQDs(c)与GOQDs(d)以TMB 为底物时的Michaelis-Menten动力学;GQDs (e)与GOQDs (f)以H2O2为底物时的Michaelis-Menten 动力学Fig.7 (a)Absorption spectra and the corresponding color changes of the TMB, TMB+H2O2, TMB+GQDs, TMB+GOQDs,TMB/H2O2+GQDs and TMB/H2O2+GOQDs (a-f)solutions;(b)Schematic diagram of GOQDs catalyzed oxidation of TMB into oxidized TMB (oxTMB)in the presence of H2O2;Michaelis-Menten kinetics of GQDs (c)and GOQDs(d)towards TMB;Michaelis-Menten kinetics of GQDs (e)and GOQDs(f)towards H2O2
GQDs 的类过氧化物酶活性:对于TMB,Km=0.040 mmol/L,vmax=3.69×10-8mol/(L·s);对 于H2O2,Km=26.19 mmol/L,vmax=30.92×10-8mol/(L·s)。GOQDs 的类过氧化物酶活性:对于TMB,Km=0.011 mmol/L,vmax=3.11×10-8mol/(L·s);对于H2O2,Km=15.880 mmol/L,vmax=13.64×10-8mol/(L·s)。 GOQDs 的Km值低于GQDs,说明GOQDs 对于底物H2O2具有更好的亲和力。与目前报道的其他碳质纳米材料的类过氧化物酶活性相比(见表1),本文中GOQDs 的Km值更低,具有更高的催化活性[15]。
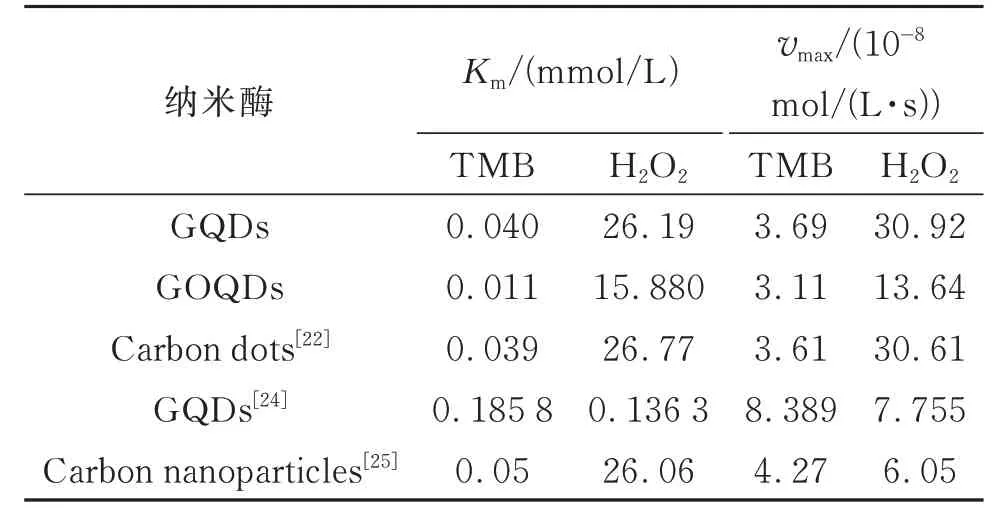
表1 GQDs、GOQDs 与其他碳质纳米材料作为类过氧化物酶的动力学常数Table 1 Enzymatic kinetic constants of GQDs and GOQDs in this work with other carbon nanomaterials as peroxidase
2.2.4 GOQDs/GCE 的I-t曲 线 分 析
通过施加-0.92 V 外加电场,在0.2 mol/L CPBS (pH 3.8) 中连续加入H2O2,测试GOQDs/GCE 对目标物H2O2的响应电流。如图8(a)所示,加入低至0.002 mmol/L H2O2时,催化电流有明显的增加,随着H2O2的连续加入,相应电流呈阶梯式增加。如图8(b)所示,在0.002~2.4 mmol/L 范围内,GOQDs/GCE 的电流响应与H2O2的浓度有较好的线性关系,线性拟合方程为I(mA)=-0.357 3c(mmol/L) -0.120 9 (R2=0.995),检 出 限 为0.4 μmol/L (信噪比S/N=3)。在H2O2浓度低至0.002 mmol/L 时,响应电流在3 s 内能达到稳态,表明GOQDs/GCE 对小分子有较好的响应,归因于GOQDs 表面上存在类过氧化物酶的活性位点[15]。
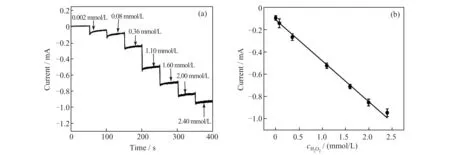
图8 (a)GOQDs/GCE 对连续加入H2O2的电流响应;(b)GOQDs/GCE 的稳态电流响应信号对H2O2浓度的线性关系Fig.8 (a)Amperometric response of GOQDs/GCE to continuous addition of H2O2;(b)the linear relationship between the steady-state current GOQDs/GCE and the different concentrations of H2O2
3 结 语
本文以GNPs 为原料,制备了含氧量低的GQDs 与含氧量高的GOQDs,探究了含氧量对GQDs 类过氧化物酶活性的影响。实验结果表明,相对于修饰电极GQDs/GCE,GOQDs/GCE 对电子具有较大排斥作用,但对小分子H2O2具有更大响应电流;GQDs 与GOQDs 均具有类过氧化物酶活性,相对于GQDs,GOQDs 的Km数值更小,对底物具有更好的亲和力;含氧量高的GOQDs 展现出更好的类过氧化物酶活性,证实丰富含氧官能团对GQDs 的类过氧化物酶活性具有重要作用,为提高GQDs 过氧化物酶催化活性提供了思路。在此基础上,构建GOQDs/GCE 的检测平台对H2O2的检出限为0.4 μmol/L (S/N=3),在0.002~2.4 mmol/L范围内具有较好的线性关系,为H2O2检测提供了一种简便有效的方法。

