颈动脉粥样硬化治疗用药规律及作用机制探析*
李珊珊,喻正科,赵梦雪,陈静
1 湖南中医药大学 湖南长沙 410208
2 湖南中医药研究院附属医院 湖南长沙 410006
《中国心血管健康与疾病报告2020》[1]表明目前我国心血管疾病患病率仍有逐年上升的趋势。动脉粥样硬化是一种全身性疾病,是导致心脑血管疾病的病理基础,涉及一条甚至多条血管,以血管内膜出现粥样沉积物,管壁增厚,管腔狭窄为主要特征,早期虽无明显临床表现[2],但随着病情进展,可能会危及生命。动脉粥样硬化其危险因素较多,包括年龄、性别、吸烟史、饮酒史等,与高血压、糖尿病、血脂异常、肥胖等疾病均有较大关联[3]。现动脉粥样硬化保守治疗手段包括抗血小板聚集、降脂稳斑等,若管腔狭窄严重,则需手术治疗。
颈动脉粥样硬化(Carotid Atherosclerosis,CAS)是全身动脉粥样硬化性疾病形成及演变的反应窗口[4],与心脑血管疾病存在相关性。其主要病位为颈部血管。CAS早期进展较为缓慢,通过控制危险因素、中医药干预等手段于疾病初期可逆转病情,如若颈部动脉狭窄严重,斑块不稳则可能危及生命。故而减轻动脉粥样硬化及斑块程度,有利于减少心血管系统疾病的发生,改善预后,降低危急重症发生率及致死率。
资料与方法
1 数据来源及检索方式
以“颈动脉粥样硬化”“颈动脉斑块”中英文为主题词,“中医”“中药”“中西医”中英文为副主题词,主副主题词之间以“AND”连接。检索中国知网自2002年01月至2021年12月期间的所有相关文献。
2 入组标准
2.1 纳入标准 ①文献明确符合颈动脉粥样硬化诊断标准[5];②文献为临床随机对照试验,临床疗效明确,治疗组患者疗效优于单纯常规西医治疗的对照组,且有统计学意义;③中药口服治疗,明确方剂的组成及用法,包含中药汤剂及中成药。
2.2 排除标准 ①排除非临床研究试验,如综述类文献、动物实验研究类文献、病例分析、专家经验总结类文献等;②药物组成不完整的文献;③虽有明确药物组成,但属敷贴、定向透药等外治法的文献;④疗效评价标准不合理,研究结果无统计学意义的文献;⑤中药治疗方案为同一中成药的文献或中药汤剂药物组成完全相同的文献,仅取1篇。
3 中药数据规范
参照《中华人民共和国药典2020年版》[6]及《中药学》[7]对文献中所出现的中药进行规范处理:①处方中应用简化名称、别名:如薏米、薏仁、苡仁等均统一为薏苡仁,仙灵脾统一为淫羊藿等;②中药经炮制后,若为同一类药物,则不予区分,如姜半夏、清半夏、法半夏统一为半夏等;若为非同一类药物,如生地黄、熟地黄,则分别统计。③中药性味归经按《中华人民共和国药典2020年版》统一规范。
4 数据处理
由两人“背对背式”通过CNKI搜索文献,阅读初步筛选出的文献,依照数据纳入、排除及剔除标准获得符合条件的文献,进行预处理,如涉及争议文献则交由第三人处理,一人应用Excel记录筛选与规范后的数据,后由三方共同校对查验数据的正确性及非主观性。
5 数据挖掘分析
将数据录入中医传承辅助平台v2.50“方剂管理”模块,分别进行单药分析、关联规则分析及聚类分析,并获得核心药物组合。
6 获取核心药物靶点信息
通过TCMSP数据库查找核心药物的分子信息,以口服生物利用度(OB)≥30、类药性(DL)≥0.18为标准筛选药物活性成分,预测药物可能作用靶点,并于Uniprot蛋白质数据库规范靶点信息,获得药物作用靶点集合。
7 建立疾病相关靶点集合
以“Carotid atherosclerosis”为检索词在Genecards数据库获取CAS疾病的所有相关靶点,建立Excel文档,以关联系数(Relevance score)降序排序,关联系数越大,则表明两者间相对关联度越大,设定关联系数≥中位数,获得合适的CAS疾病基因靶点集合。
8 构建药物-活性成分-靶点-疾病网络
利用jevnn平台绘制venn图并得到药物及疾病靶点集合的交集靶点,将交集靶点与药物活性成分相对应,应用Cytoscape 3.9.1构建药物-活性成分-靶点-疾病网络。
9 构建PPI网络及核心靶点网络
交集靶点导入String平台,要求最低互动分数为0.40,删除游离节点,构建PPI网络,并得到相应信息tsv文件,文件导入Cytoscape 3.9.1,利用插件CytoCNA构建核心靶点网络,以靶点≥Degree、Betweenness(BC)、Closeness(CC)、Eigenvector(EC)、LAC、Neighborhood Connectivity(NC)中位数为标准筛选2次,获得核心靶点。
10 富集分析
在David平台录入药物及疾病交集靶点,选择智人类别,通过富集分析,探讨CAS主要生物学过程及通路。
数据挖掘结果
本次研究分析共纳入228个有效方剂,其中主要治疗CAS的方剂为163个,主要治疗CAS合并高血压、脑梗死、糖尿病、冠心病的的方剂分别为35个、20个、12个、8个。
1 单味药物分析
1.1 药物频次分析 所有处方共涉及214味中药,总使用频次为2080次,使用频次前20的药物分别为丹参、黄芪、川芎、半夏、水蛭、茯苓、甘草、三七、山楂、当归、地龙、赤芍、泽泻、白术、陈皮、牛膝、红花、何首乌、天麻、葛根。见表1。
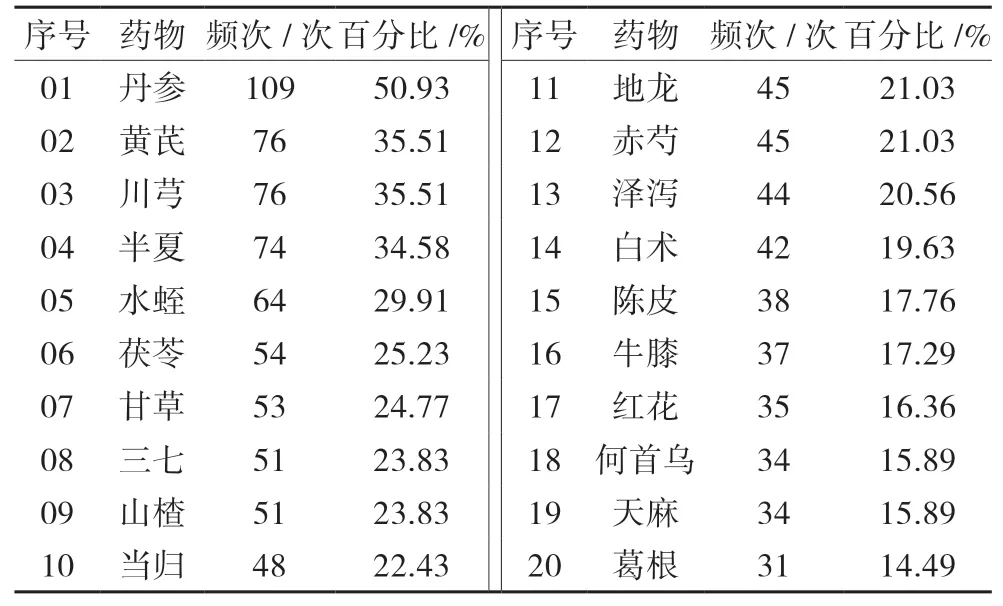
表1 治疗CAS处方中使用频次为前20的高频中药
1.2 药物性味归经分析 治疗CAS处方中涉及的中药:药性以温性为最多,药味以甘、苦、辛为主,归经以肝经(23%)、脾经(17%)、心经(13%)、胃经(12%)、肺经(11%)为主。见表2。
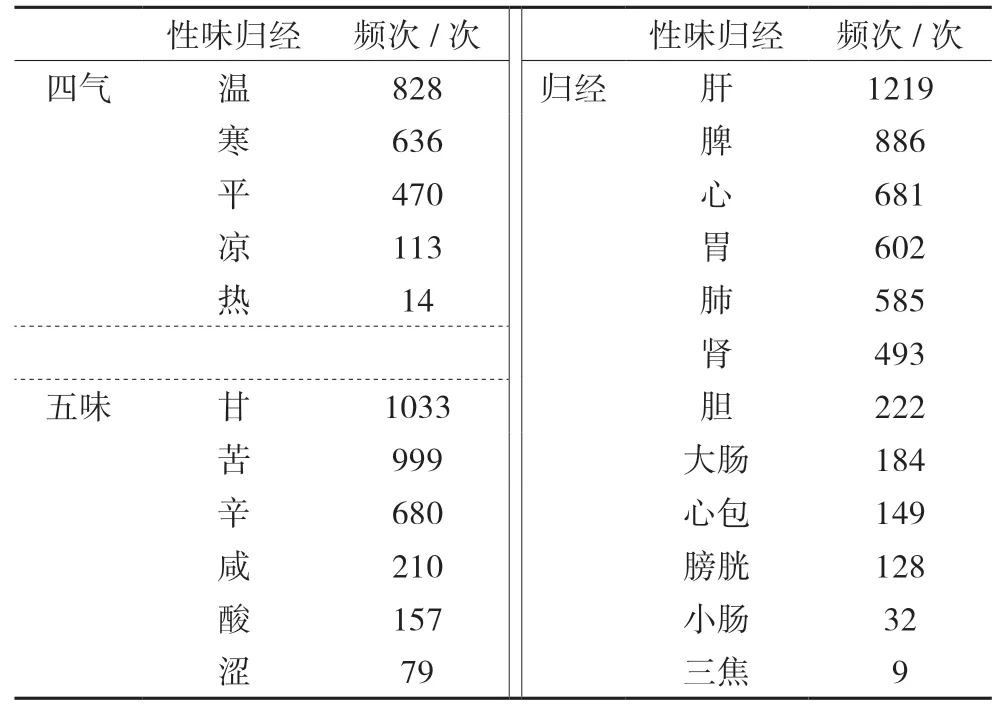
表2 治疗CAS处方中中药性味归经频次分布
1.3 关联规则分析 设置支持度个数为23,置信度0.6,得到27个同时出现频次≥23次的药物组合,包括“丹参-黄芪”“川芎-丹参”“半夏-丹参”“半夏-茯苓”等。见表3。

表3 治疗CAS处方中频次≥23(次)的中药组合
其中共涉及丹参、黄芪、川芎、半夏、茯苓、水蛭等16味中药,可认为此16味中药较为核心,其关联关系经由网络分析展示。见图1。

图1 药物组合网络分析图
在此基础上行进一步关联规则分析,置信度越高,代表“->”左右的药物于中药处方中同时出现的概率越大。见表4。

表4 治疗CAS处方中中药关联规则分析
1.4 聚类分析 设置相关度为8,惩罚度为8,通过聚类分析后得到潜在药物组合14个。见表5。

表5 治疗CAS处方中中药潜在药物组合
潜在药物组合共组潜在处方7个,借由网络分析图展示。见图2。
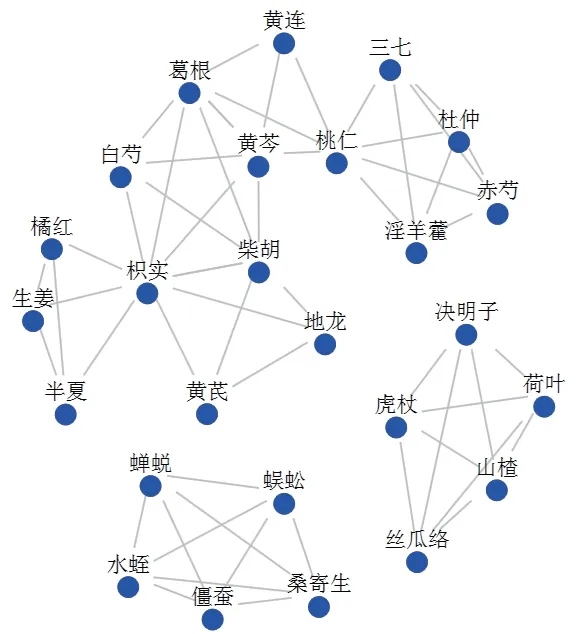
图2 潜在组方网络分析图
2 网络药理学分析结果
基于数据挖掘分析,选取“丹参、黄芪、半夏、川芎、茯苓”组成核心药物,以此进行网络药理学分析。
2.1 核心药物作用靶点 核心药物组合共获得活性成分120个,剔除重复及未查询到靶点的活性成分23个,总计97个活性成分,其中以丹参最多,包含59个活性成分。应用Uniprot蛋白质数据库规范靶点信息,共获得人源非重复的药物可能作用靶点253个。
2.2 疾病基因靶点 以“Carotid atherosclerosis”为检索词在Genecards数据库共获取CAS疾病的所有相关靶点2099个,以靶点关联系数≥其中位数“1.63”为标准获得CAS疾病基因靶点1052个。
2.3 药物-活性成分-靶点-疾病网络 药物作用靶点及疾病基因靶点分别导入jevnn平台,并绘制venn图。见图3a。据此获得药物靶点及疾病靶点的交集128个,依交集靶点查询五药总计90个药物活性成分起抗CAS作用,通过Cytoscape3.91构建药物-活性成分-靶点-疾病网络,图中各节点面积越大,则代表其连接度越大,所起作用愈加显著。丹参治疗CAS的有效成分最多,其次为黄芪、半夏,其中以Mol000098(槲皮素)、Mol000006(木犀草素)、Mol000422(1.7-二羟基-3.9-二甲氧基紫檀烯)、Mol007154(丹参酮IIA)等活性成分作用较为显著。见图4。
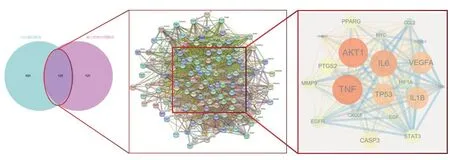
图3 a venn b基于String平台的PPI网络 c核心靶点网络
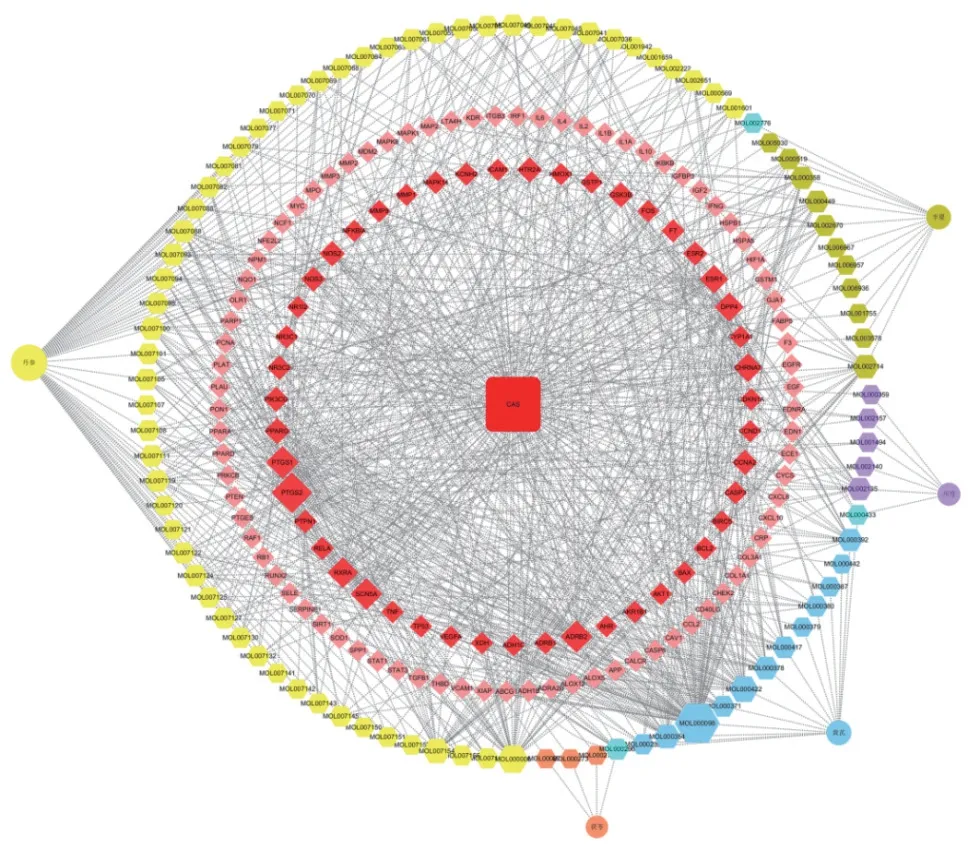
图4 药物-活性成分-靶点-疾病网络
2.4 PPI及核心靶点网络 通过String数据库平台构建PPI网络,分析靶点蛋白与蛋白间相互作用,其中未见游离节点,包含128个节点,2624条无向连线。见图3b。应用Cytoscape 3.9.1插件CytoCNA分析构建核心靶点网络,计算得到Degree、BC、CC、EC、LAC、NC中位数行两次筛选,共得到核心靶点20个,可合理认为靶点其Degree值越大,则与其他靶点的关联度越大,愈加重要,其中最为核心的靶点包括TNF(肿瘤坏死因子)、AKT1(丝氨酸/苏氨酸蛋白激酶)、IL6(白细胞介素6)、VEGFA(血管内皮生长因子A)等。见图3c,表6。

表6 核心靶点
3 富集分析
3.1 生物进程分析 2.3中获取的交集靶点进一步分析,共得到生物学过程(biological process,BP)、细胞组分(cellular component,CC)、分子功能(molecular function,MF)986条,以P<0.05且FDR<0.05筛选后余518条,以P值升序排序,BP前10条目包括:细胞因子介导的信号通路(cytokine mediated signaling pathway)、凋亡过程负调控(negative regulation of apoptotic process)、细胞增殖正性调节(positive regulation of cell proliferation)等;由CC可见CAS疾病主要是发生在细胞外,前10通路中extracellular space、extracellular region、cell surface均属此意;此外该病也作用于大分子复合物(macromolecular complex)、核质(nucleoplasm)等;MF富集较为显著的包括蛋白质结合(protein binding)、转录因子结合(transcription factor binding)、酶结合(enzyme binding)等。见图5。
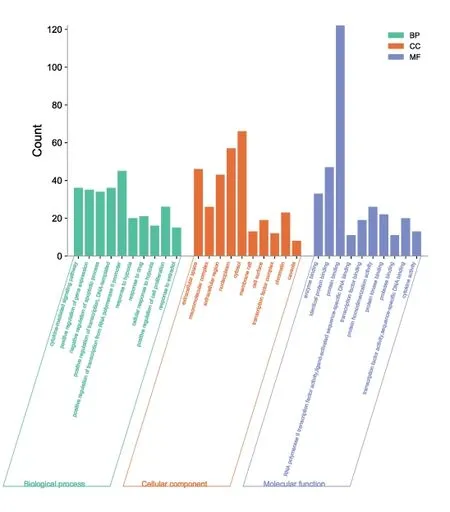
图5 生物进程分析图
3.2 KEGG分析 KEGG分析共得到162条通路,以P<0.05且FDR<0.05筛选后共计151个通路,以P值升序为序可见筛选前20条通路,可见:核心药物较为富集化的通路包括癌症的途径(Pathways in cancer)、AGE-RAGE信号通路在糖尿病并发症中的作用(AGE-RAGE signaling pathway in diabetic complications)、脂质和动脉粥样硬化(Lipid and atherosclerosis)、流体剪切应力和动脉粥样硬化(Fluid shear stress and atherosclerosis)等。见图6。
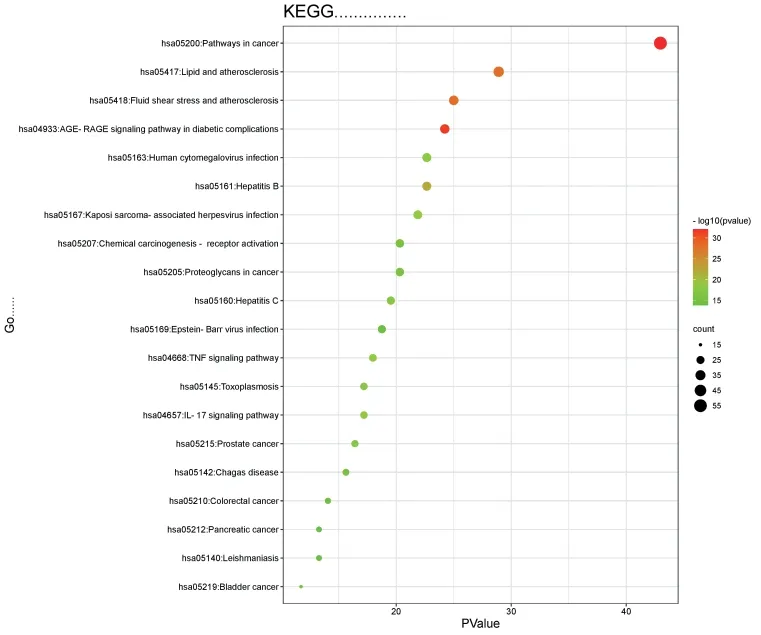
图6 KEGG分析气泡图
讨 论
1 病因病机
《灵枢·经脉第十》言“脉道以通,气血乃行”“经脉者,所以能决死生,处百病,调虚实,不可不通”,脉道通利对人机体有着重要作用,脉管阻塞,血液运行不畅,五脏六腑无充足的血液滋养,则生理机能受损。心主血脉,脉道通利为心脏正常生理功能运行的必要条件之一。古代中医学没有明确提出颈动脉粥样硬化并斑块形成这一疾病,国医大师朱良春认为其属于“脉痹”范畴,乃“本虚标实”之证:本虚为脾肾亏虚,脾气不足,气血生化乏源,水液输布代谢失常[8];标实为痰瘀互结,朱老认同痰湿瘀致病学说,指出动脉硬化及斑块形成的核心与痰瘀二邪紧密相关。《动脉粥样硬化中西医防治专家共识(2021年)》[2]认为CAS是由于先天禀赋不足、久食肥甘厚味、七情内伤、劳倦等多种因素致使五脏生理机能受损,气血阴阳亏虚,即本虚,继而形成痰湿、血瘀、气滞、寒凝、热毒等病理因素,痰、湿、瘀血又再次成为机体的致病因素,日久则邪气聚于脉道,不散而结聚成块,此为标实。本研究在此病因病机基础上,通过分析临床治疗CAS的用药规律,进一步讨论不同病理因素致病的针对性用药,以期提供参考。
2 数据挖掘分析
治疗CAS的中药药性以温寒平为主,药味以甘苦辛为主。寒邪收引筋脉、热毒生风动血,均为导致CAS的病机,寒凉者热之寒之,温热者寒凉治之,为辨证论治基础,平味药物作用和缓,若寒热病机不甚明显,不失为良好选择。甘味药补益和中,CAS本属虚症,气虚为根本,甘味药如黄芪、甘草等,多甘温或甘平,补中气,行血有力,益脾气,水液输布畅达。利水消肿类如茯苓、泽泻等亦甘淡为主。苦味药能泄能燥,疏理条畅气机,苦寒清湿热,苦温除寒湿。辛味药行散之力峻,行气、行血,治疗气血阻滞功效较强,理气药、活血化瘀类药物多味辛,三棱、莪术、水蛭、虻虫等破血消癥类药物走而不守,药味均属辛苦。归经以肝、脾、心、胃、肺经多见。肝疏泄全身气机,促进血液津液运行;脾主运化,运化水谷,通调水道;心主血脉,推动血液行于脉中,助脉道通利,血流顺畅;肺朝百脉,肺气宣发肃降推动一身之气、水液及血液的正常运行;胃又称“水谷气血之海”,为机体的一切生理活动提供能量。
治疗CAS的药物中使用频次较多的药物为丹参、黄芪、川芎、半夏、茯苓、水蛭等。丹参属活血化瘀类中药,《本草纲目》谓其能“破宿血,生新血”,主治“寒热积聚,破癥除瘕”。现代药理学研究认为丹参可通过多成分多靶点起到抗CAS作用。黄芪性甘温,归脾肺二经,为补益脾气之要药,兼行滞通痹。气虚则行血无力,血行不畅,流滞脉络,日久则生瘀血及斑块。《本经疏证》言黄芪“利营卫之气,故凡营卫间阻滞,无不尽通”,补益脾气,行血化瘀,故标本同治。川芎善治气滞血瘀,古称其“血中气药”。茯苓健脾利水,脾气居中枢运转津液,脾气充足,水液方能运行顺畅。水蛭、地龙均为虫类药物,善于走窜,通经活络力强,水蛭亦可破血逐瘀,消癥积。水蛭主要成分为水蛭素,地龙主要成分为蚓激酶、蚓胶质酶、纤维蛋白溶解酶等,两种药物可通过不同的代谢途径阻止凝血因子的活化,均能有效抑制血小板聚集、抗凝抗栓、改善血液流变学、降低血脂等[9-10]。
药物组合分析图中共涉及到16味中药,据药物功效,大致分为7类:1)活血化瘀类:丹参、川芎、水蛭、三七、红花、赤芍;2)补益气血类:黄芪、甘草、当归、白术;3)利水渗湿类:茯苓、泽泻;4)理气类:陈皮;5)化痰类:半夏;6)消食类:山楂;7)通经活络类:地龙。可见CAS的治疗以补气、活血化瘀为主,同时根据兼证的不同,辅以行气、利湿、化痰等。其中“丹参”“半夏”“川芎”“黄芪”“茯苓”五种药物与其他关联较多。近半数药物组合含有丹参,“丹参-黄芪”为使用频率最高的药物配伍,可用于气虚血瘀证型CAS。川芎、丹参、黄芪为三药组合,在补气活血基础上加以行气,以防过补反致气滞。“黄芪-当归”,这一药对见于李东垣名方当归补血汤,方中当归及黄芪含有阿魏酸、黄芪甲苷及毛蕊异黄酮等药理成分,可以促进并调控大鼠体内脂质代谢,促进胆固醇的排泄,抑制颈动脉粥样硬化及斑块的形成[11]。
聚类分析后共得到7个潜在药物组方:方1:黄芩、黄连、葛根、桃仁:乃葛根黄芩黄连汤去甘草加桃仁,此方可用于治疗热毒血瘀证型,其中葛根、黄芩、黄连均具清热解毒之功,桃仁活血,可治瘀血蓄积之癥瘕痞块;方2:白芍、黄芩、葛根、枳实、柴胡:为大柴胡汤的基础用药,本方较方2清热力弱,但消斑块功用更甚,枳实为行气通塞要药,与葛根、白芍配伍,破气活血,通经活络;方3:半夏、枳实、橘红、生姜:半夏白术天麻汤之基础方,半夏、橘红、生姜皆可燥湿化痰,橘红,枳实都属理气药物,善治气滞痰凝所致CAS;方4:水蛭、蜈蚣、蝉蜕、僵蚕、桑寄生:《素问·阴阳应象大论》“血实者宜决之”,本方多为虫类药物,功擅化瘀消癥,搜络剔邪,药性峻猛。但是虫类药多属有毒之品,临床应用时应对药物用量予以把握,不可过量反戕伐正气;方5:决明子、虎杖、山楂、荷叶、丝瓜络:方中虎杖、决明子润肠通便,山楂、荷叶化浊降脂,对于形体肥胖的CAS患者具有良好的治疗效果;方6:三七、桃仁、赤芍、淫羊藿、杜仲:方中杜仲、淫羊藿温阳,补益肝肾,配以活血化瘀,本方可用于阳虚血瘀证型CAS。
3 网络药理学分析
基于数据挖掘分析,合理认为CAS多见“气虚血瘀、痰湿内停”证型,故拟“丹参-黄芪-川芎-半夏-茯苓”这一核心药对。
中药具有多成分、多靶点的治疗优势,中药复方可通过不同成分间的相互作用治疗疾病。西医认为CAS发病机制包括脂质浸润学说、血小板聚集及血栓形成学说、内皮损伤-反应学说、炎症学说等。TNF、IL-6、IL1B均为炎性因子,三者在血管内协同作用促使血管内皮因子的产生[12],山柰酚、槲皮素、隐丹参酮、木犀草素等均可作用于TNF,槲皮素为黄芪抗CAS重要活性成分之一,江扬[13]等研究认为槲皮素可以抑制LDL诱导的内皮细胞氧化损伤,亦可以通过ceRNA调控氧化应激情况,多方干预动脉粥样硬化的形成及发展。丹参活性成分木犀草素可以抑制炎症生成、抑制氧化应激反应、抑制TLR-4/NF-κB信号通路,起到抗CAS作用[14-15];丹参酮IIA其分子结构与胆固醇高度相似,通过竞争机制抑制胆固醇在血管内的沉积,降脂及保护血管内皮细胞,从而抑制CAS形成[16]。VEGFA为VEGF家族的一个亚型,能促进血管内皮细胞的分裂与增生,在CAS形成过程中具有较强的调节作用[17],研究认为VEGF在人体多脂组织中的表达显著高于低脂组织,更易致动脉硬化及斑块形成[18]。
核心药物作用于机体主要作用于细胞外组分,调控细胞增殖、细胞凋亡、细胞因子介导反应等以抗CAS形成。通过分析KEGG通路,认为大部分通路均与炎症相关,如:IL-17信号通路、NF-κB信号通路,慢性炎症持久刺激血管内表皮细胞,使其增生,内膜增厚;脂质和动脉粥样硬化通路、脂肪细胞中脂解的调节等部分通路属脂质代谢性,LDL将脂质由肝脏转移至血管内,血管内脂肪代谢障碍,沉积于血管内皮,导致粥样斑块形成;补血及凝血通路作用于血栓调节素(THBD)、凝血因子VII(F7)、尿激酶型纤溶酶原激活链(PLAU)、内皮纤溶酶原激活物抑制剂(SERPINE1)、组织型纤溶酶原激活链(PLAT)、凝血因子III(F3),血管内皮细胞受损时,血小板凝集于血管局部,凝血酶作用使纤维蛋白原转化为纤维蛋白,而形成血栓[19],核心药物可通过该通路调控体内凝血系统,而抑制粥样硬化的形成。此外还有流体剪切应力和动脉粥样硬化通路、血管内皮生长因子信号通路、钙信号通路等多种通路。
核心药对“丹参-黄芪-川芎-半夏-茯苓”主要是通过调控体内脂质代谢及炎症反应抗CAS,而其中起到最主要功效当属“丹参-黄芪”药对。

