油酸钠与含苯环类羟肟酸盐对金红石可浮性的影响及协同作用机理研究
郭万中,印万忠,刘明宝,池冬瑞,班小淇,殷学明
(1.东北大学资源与土木工程学院,辽宁 沈阳 110819;2.陕西省尾矿资源综合利用重点实验室,陕西 商洛 726000)
金红石理论含钛量高,杂质少,是制备高品级钛白粉及各类高端钛基复合材料的优质原料来源[1]。到目前为止,我国已发现原生金红石矿床、矿化点88处,探明TiO2储量大约1.53×107t,分布于全国17个省、市、自治区,其中以湖北、河南、陕西、江苏、山西为主(占全国总储量的96%)[2]。工艺矿物学研究显示我国绝大多数原生金红石矿具备有价矿物嵌布粒度细、共伴生关系复杂的特性,所以其选别工艺一直未获得突破性进展,只能进口金红石或者采用高成本的人造金红石来满足我国高端钛工业的发展需求[3]。生产实践及理论研究表明,浮选是解决金红石矿分离问题的关键技术之一,最具发展前景,而高效浮选药剂的研发则往往是浮选工艺取得突破的瓶颈所在[4]。
目前,脂肪酸类及羟肟酸类药剂是金红石浮选工艺中极具代表性的两类药剂体系,其中研究较多的脂肪酸类药剂为油酸钠,而羟肟酸类药剂的代表则是苯甲羟肟酸钠和水杨羟肟酸钠[5]。油酸钠虽然捕收能力强,但其选择性及低温耐受性均不足,而苯甲羟肟酸钠或水杨羟肟酸钠则具有对细粒级选择性好,但捕收能力较低,用量大,成本高,因此,如能将油酸钠与苯甲羟肟酸钠或水杨羟肟酸钠组成二元协同浮选体系,则有可能使捕收能力和选择性均得到一定程度的提高,从而达到1+1>2的效果[6]。但金红石在上述协同药剂体系中的浮选行为及机理很少见到报道,因此,本论文利用单矿物浮选实验确定了金红石在油酸钠与苯甲羟肟酸钠及油酸钠与水杨羟肟酸钠组成二元协同体系中的浮选行为,并结合一系列界面化学测试手段探索了组合药剂在金红石表面的作用行为,为我国金红石资源的高效利用提供一定的理论支撑。
1 实验
1.1 实验原料
本实验选取粒度小于-0.074 mm商洛市商南钛业有限公司重选-磁选的金红石精矿作为实验样品,矿样XRD见图1。样品中TiO2含量在96.5%左右,杂质为少量的含铁物相,实验所用油酸钠、苯甲羟肟酸钠和水杨羟肟酸钠,纯度均不小于99%,NaOH和HCl为化学纯,实验用水为实验室自制去离子水。
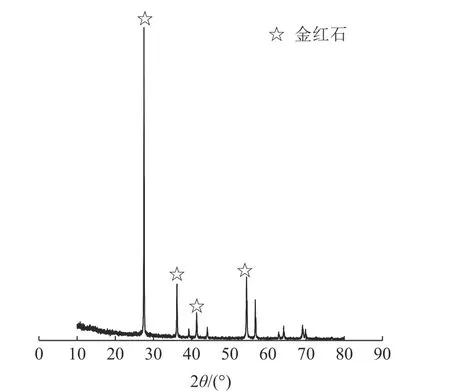
图1 矿样X射线衍射Fig.1 X-ray diffraction spectrum for mineral sample
1.2 主要实验方法
(1)浮选实验
浮选实验在XFG型挂槽式浮选上进行,浮选温度为(20±2)℃,矿浆浓度为34%,实验过程依次加入金红石矿样、去离子水后开机搅拌并调节pH值,按不同添加顺序及质量比例依次加入捕收剂,每种捕收剂加入后搅拌3 min,浮选3 min,泡沫产品烘干后计算回收率。
(2)动电位测试
称取-5µm的金红石样品10 mg,将其加入含有一定数量去离子水的烧杯中,按不同添加顺序及质量比例依次加入两种捕收剂后分别搅拌2 min并调节pH值,最终药剂总浓度为1 g/L,矿浆体积为40 mL,采用JS94H为电泳仪测定金红石动电位。在进行药剂预先混合对动电位的影响实验时,首先将药剂按照不同质量比例预先在10 mL离心管中混合,然后再加入到矿浆中并搅拌2 min。
(3)接触角测试
将5 g粒度-5µm的金红石样品置入50 mL锥形瓶中,加入一定体积的去离子水,搅拌1 min后加入第一种药剂并调节pH值,振荡1 h,然后加入第二种药剂继续振荡1 h。药剂预先混合对接触角的影响实验过程的操作步骤为先将药剂按照不同质量比例预先在10 mL离心管中混合,然后再加入到矿浆中搅拌1 h。该实验中药剂总浓度为2 g/L,矿浆总体积为20 mL,矿浆过滤后阴干,称取2 g阴干后的样品压片测定接触角,其余样品留用,压片时压力为20 MPa,保压2 min。
(4)药剂协同效应的计算方法
根据前人研究结果,药剂的协同效应值采用式(1)计算:

其中,ε实验、ε理论分别为不同条件下金红石回收率的实验值和理论值,可由图2中虚线拟合得到[7]。
2 结果与讨论
2.1 捕收剂对金红石可浮性的影响
两种药剂总用量为500 mg/L,浮选pH值9.5左右时不同组合体系中金红石浮选行为与药剂比例及添加顺序的关系见图2,图中虚线为回收率理论变化值。
由图2(a)可以看出,单一油酸钠体系中金红石的回收率(49.2%)要大于单一苯甲羟肟酸钠体系(39.16%),说明油酸钠的捕收能力要超过苯甲羟肟酸钠。不同药剂添加顺序下组合体系中金红石的回收率大小顺序为:先添加苯甲羟肟酸钠后油酸钠>预先混合后再添加>先添加油酸钠后苯甲羟肟酸钠。由不同药剂比例下金红石回收率与理论曲线的关系可看出油酸钠和苯甲羟肟酸钠的组合对金红石浮选具有良好的协同效应。由图2(b)可以看出,单一油酸钠体系中金红石的回收率(49.2%)要远远大于单一水杨羟肟酸钠体系(3.47%),说明在实验pH值下油酸钠的捕收能力要远远超过水杨羟肟酸钠。不同顺序下金红石回收率大小为:先添加水杨羟肟酸钠后油酸钠>先添加油酸钠后水杨羟肟酸钠>预先混合后再添加。由实验数据与理论曲线的相对位置可看出,两种药剂对金红石回收率也存在着较好的协同效应。
由图2可得出,单一药剂体系中金红石回收率顺序为:油酸钠体系(49.2%)>苯甲羟肟酸钠体系(39.16%)>水杨羟肟酸钠体系(3.47%),这是由于三种药剂的分子结构不同引起的,油酸钠非极性基长度要远远超过其他两种药剂,故其对金红石的捕收能力最高。另外,羟肟酸类药剂为螯合类捕收剂,相对于苯甲羟肟酸钠,水杨羟肟酸钠分子中的苯环上多了一个羟基,该羟基也参与了药剂与金红石表面的相互作用,从而使水杨羟肟酸钠分子中苯环被“锚定”在矿物表面,而苯甲羟肟酸钠分子中的苯环却可以自由转动,从而强化了苯甲羟肟酸钠体系中矿物的疏水性能,所以苯甲羟肟酸钠体系中金红石回收率较高。
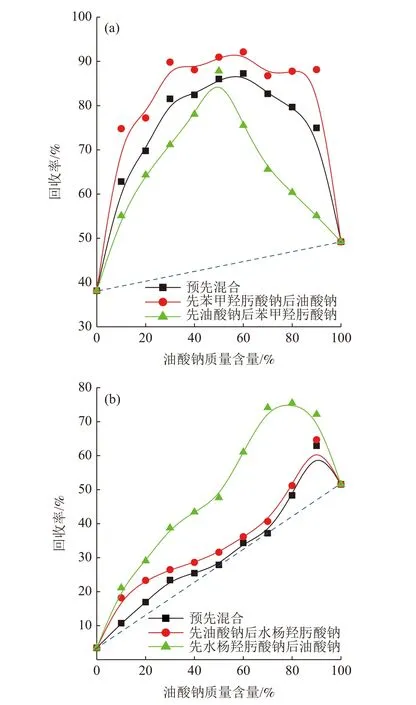
图2 金红石在不同混合体系中的浮选行为Fig.2 Flotation behavior of rutile in different mixed systems
2.2 捕收剂对金红石的协同作用机理
2.2.1 Zeta电位测试
不同实验条件下药剂比例对金红石动电位的影响见图3,动电位理论变化可用图中虚线来表示。
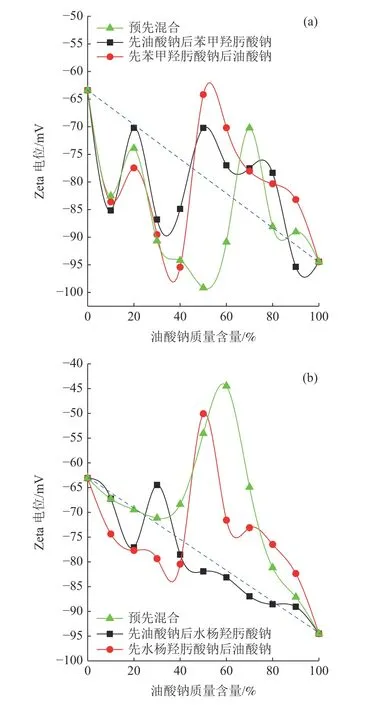
图3 不同体系中金红石动电位(药剂总浓度1 g/L)Fig.3 Zeta potential of rutilein different systems(total reagent concentration = 1g/L)
由图3(a)可以看出,单一苯甲羟肟酸钠体系中金红石的动电位为-63.4 mV,远远大于单一油酸钠体系中的动电位值(-94.5 mV),水溶液中苯甲羟肟酸根离子和油酸根离子均带一个负电荷,说明油酸钠在金红石表面的吸附量要远远超过苯甲羟肟酸钠。随组合药剂中油酸钠质量含量的增加,金红石动电位在不同药剂添加顺序下均呈现先低于理论值后大于理论值的变化规律。动电位小于理论值的现象说明两种药剂离子在金红石表面发生了相互诱导的共吸附行为,该吸附行为可导致组合药剂在矿物表面的吸附密度增加,动电位小于理论值;动电位大于理论值的实验现象表明金红石表面双电层厚度增加,滑移面外移,造成该现象的原因则是药剂分子间生成体积较大的缔合物。
由图3(b)可以看出,单一水杨羟肟酸钠体系中金红石的动电位为-63.1 mV,也远远大于单一油酸钠体系中的动电位值(-94.5 mV),因水溶液中油酸根离子带一个负电荷而水杨羟肟酸根离子则带两个负电荷,故油酸钠在金红石表面的吸附量要远远超过水杨羟肟酸钠。结合图3(a)可知,三种药剂体系中金红石动电位大小顺序为:苯甲羟肟酸钠体系(-63.4 mV)≈水杨羟肟酸钠体系(-63.1 mV)»油酸钠体系(-94.5 mV)。由不同药剂在溶液中的荷电情况得出三种药剂在金红石表面的吸附量大小顺序为:油酸钠>苯甲羟肟酸钠>水杨羟肟酸钠,这种现象引起上述三种单一药剂体系中金红石浮选回收率大小发生变化。两种药剂预先混合后再添加时金红石动电位均大于理论值,说明二者预先混合时生成的缔合物具有较大的空间体积。先添加油酸钠后加入水杨羟肟酸钠时金红石动电位基本上都位于理论线以下,说明此时两种药剂以相互诱导的单分子层共吸附为主。先添加水杨羟肟酸钠后油酸钠时金红石动电位的实验值位于理论线的两侧,说明此时组合药剂在金红石表面的吸附主要包括相互诱导的单分子层共吸附和缔合物吸附两种形式。
2.2.2 表面张力实验
图4为不同组合药剂溶液表面张力与浓度的关系,由图4(a)可见,苯甲羟肟酸钠几乎不具备表面活性,只有在浓度较大时才可小幅度的降低水的表面张力,而油酸钠则在浓度较低时即可大幅度降低其水溶液的界面张力,这是由于油酸钠对金红石捕收能力较苯甲羟肟酸钠高。在油酸钠与苯甲羟肟酸钠摩尔比为1∶1的混合水溶液中,在总浓度小于10-5mol/L时混合溶液的表面张力要低于相同浓度下的单一药剂体系,说明此时二者在气液界面生成缔合物,该缔合物的存在大幅度降低了水溶液的表面张力;混合药剂水溶液与单一油酸钠水溶液的最低表面张力及CMC值近似相等,进一步表明苯甲羟肟酸钠的存在促进了油酸钠在气液界面的聚集数目。由以上分析可以看出,油酸钠和苯甲羟肟酸钠分子之间具备生成缔合产物的作用能力。由图4(b)可以看出,水杨羟肟酸钠也几乎不具备表面活性,且因其分子中苯环上除了连接有肟基以外还连有一个羟基,该羟基的存在使其降低水的表面张力的能力要小于苯甲羟肟酸钠,这就引起苯甲羟肟酸钠对金红石捕收能力强于水杨羟肟酸钠。在油酸钠与水杨羟肟酸钠为1∶1的混合体系中,随组合药剂总浓度的增加,组合药剂水溶液与单一油酸钠水溶液的表面张力具有明显相似的变化规律,说明水杨羟肟酸钠促进了油酸钠在气液界面的吸附。
由以上分析可看出,油酸钠与苯甲羟肟酸钠或者水杨羟肟酸钠均具有缔合能力,并且从两类混合药剂体系水溶液表面张力值的大小得出水溶液中油酸钠与苯甲羟肟酸钠的缔合能力可能要强于其与水杨羟肟酸钠的缔合能力。通过分析两类药剂分子的结构得出,油酸钠与含苯环的羟肟酸类药剂之间的作用力除了非极性基间的疏水缔合作用力以外,更重要的是油酸钠分子中富电子的双键与含苯环羟肟酸类药剂分子中缺电子的苯环之间存在着电子共轭效应。
2.2.3 接触角实验
不同药剂体系中金红石接触角的变化见图5,图中虚线为接触角理论变化值。由图5可看出,两种体系内组合药剂对金红石接触角的协同效应值均表现为先增大后减小的趋势,与金红石浮选回收率的高低相一致。但值得注意的是不同药剂添加顺序下接触角的大小与相应的浮选指标并非是一一对应的,例如,单一油酸钠体系中金红石接触角最大但此时的浮选回收率并非为最高值。上述分析及实验现象表明影响矿物浮选的因素是多种多样的,说明矿物表面所生成的缔合物与浮选气泡的作用能力要高于单一药剂,缔合物的生成数量及空间构象是决定组合药剂捕收能力的重要因素。
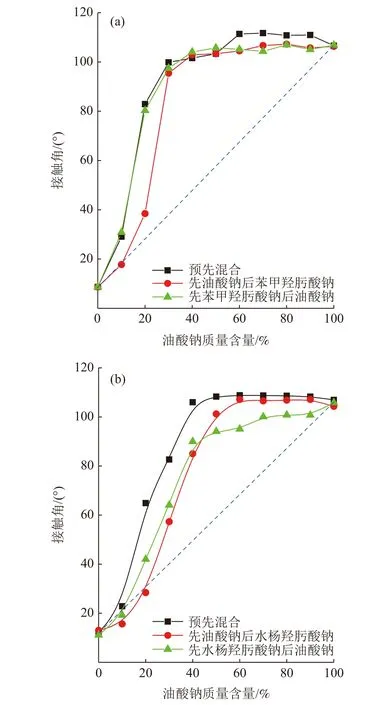
图5 不同药剂体系中金红石接触角与药剂比例和添加顺序的关系Fig.5 Plots of contact angle vs. reagent ratio under various adding sequences in different reagent systems
2.2.4 紫外漫反射实验
TiO2其对紫外线的吸收而具有良好的光催化性能,而金红石表面药剂的吸附则会在一定程度上影响TiO2晶格的应力,因此,金红石对紫外线的吸收特性会受到表面吸附的药剂种类和数量的影响。本论文分别测定了不同组合药剂体系中金红石粉末的紫外漫反射行为并计算了相应的带隙变化情况,以及从晶体化学角度探索组合药剂在金红石表面的吸附机理。不同体系及实验条件下金红石的紫外漫反射吸收光谱见图6。由图6可看出,不同体系及药剂添加顺序下金红石矿样的紫外漫反射光谱有较大差别,说明不同体系下组合药剂在金红石表面的作用特性不同。根据文献[8-10]的研究,金红石的带隙宽度采用公式(2)估算:

其中:Bg、λ为金红石带隙宽度和紫外吸收波长。λ的估算方法为:沿每条光谱中紫外吸收迅速上升位置做切线,切线在横轴上的交点即为λ值。
通过对图6的分析得知,光谱中紫外吸收迅速上升的部分在300~310 nm范围内,因此,本论文在此范围内做光谱切线。根据式(2)计算结果,油酸钠与苯甲羟肟酸钠混合浮选体系中金红石带隙变化规律为:先苯甲羟肟酸钠后油酸钠(3.65 eV)>二者预先混合(3.59 eV)>先油酸钠后苯甲羟肟酸钠(3.54 eV)。而油酸钠和水杨羟肟酸钠混合浮选体系中金红石带隙变化规律则改变为:二者预先混合(3.71 eV)>先油酸钠后添加水杨羟肟酸钠(3.69 eV)>先添加水杨羟肟酸钠后添加油酸钠(3.65 eV)。由以上带隙宽度的变化可看出,金红石与药剂作用后的带隙变化与其浮选回收率有较好的对应关系,回收率呈现出随带隙的增加而升高的变化趋势;而油酸钠和水杨羟肟酸钠混合体系中不同药剂添加顺序下金红石带隙宽度与其浮选回收率成反比关系,带隙越宽,金红石的浮选回收率越低。

图6 不同实验条件下金红石与组合药剂作用后的紫外可见漫反射光谱Fig.6 The UV-Vis DRSfor rutile after interaction with combined reagents under different conditions
2.3 讨论
如上所述,两种体系中组合药剂对金红石的回收率均有良好的协同效应,该效应的产生除了两种药剂在矿物表面的共吸附引起非极性基的长短搭配并由此改善了气泡的吸附特性以外更重要的是两种药剂在金红石表面生成了缔合物,该缔合物的生成大幅度改善了矿物的表面性质及气泡与矿物的作用能力。由图2(a)和图2(b)可知,两类体系均表现出先添加羟肟酸类药剂后添加油酸钠时金红石的回收率要大于其他两种情况,这是由于羟肟酸类药剂分子横断面积较大,在金红石表面吸附时所需空间较大,故该类药剂先加入到体系中时可首先以较佳空间构象吸附到矿物表面的高活性位点上,当油酸钠随后加入到矿浆中时,油酸根离子除了可以穿插吸附到矿物表面外,还可以与已经吸附的羟肟酸根离子生成缔合物,从而改善了矿物的可浮性。先加入苯甲羟肟酸钠后加入油酸钠时矿物的回收率高于先加入水杨羟肟酸钠后加入油酸钠时,说明此时苯甲羟肟酸钠和油酸钠之间生成的缔合物对金红石的捕收能力更强,因为苯甲羟肟酸钠分子非极性基的自由度较水杨羟肟酸钠高,故苯甲羟肟酸根离子的非极性基与油酸根离子的非极性基所生成的缔合物的数量更多、空间构象也更适合浮选气泡与之作用的缘故。油酸钠和苯甲羟肟酸钠预先混合时,二者在溶液中生成了分子间缔合物,当该药剂溶液添加到矿浆中后,各种药剂离子及缔合物种可吸附在金红石表面,从而提高了金红石的回收率,但由于存在竞争吸附,该药剂添加顺序下金红石的回收率要小于先添加苯甲羟肟酸钠后油酸钠的情况。因水杨羟肟酸钠分子中苯环上连接的羟基的影响,油酸钠与水杨羟肟酸钠分子所生成的缔合物的空间结构不利于其在金红石表面的吸附,故当将混合药剂溶液添加到浮选体系中时油酸根离子和水杨羟肟酸根离子的竞争吸附占主要地位,所以此时金红石的回收率也小于先添加水杨羟肟酸钠后添加油酸钠时的情况。当体系中先加入油酸钠时,油酸钠可首先在金红石表面发生吸附,给随后苯甲羟肟酸钠的吸附造成了较大的空间位阻,二者之间缔合物的生成数量及空间构象也受到抑制,故该药剂添加顺序下金红石的回收率最低,油酸钠与水杨羟肟酸钠体系中的情况也与此类似。两种浮选体系中,不同添加顺序下组合药剂的协同效应指数见表1。
由表1可看出,先加入羟肟酸类药剂后加入油酸钠时组合药剂的协同效应指数要大于其他两种药剂添加顺序,说明该药剂添加顺序可以强化两种药剂之间的相互作用。尽管先加入苯甲羟肟酸钠后加入油酸钠时金红石的回收率要远远高于先加入水杨羟肟酸钠后加入油酸钠体系,但两种药剂添加体系中协同效应的大小并没有明显的对应关系,进一步表明先加入苯甲羟肟酸钠后加入油酸钠时金红石表面生成的组合药剂的缔合物更有利于气泡在矿物表面的附着。
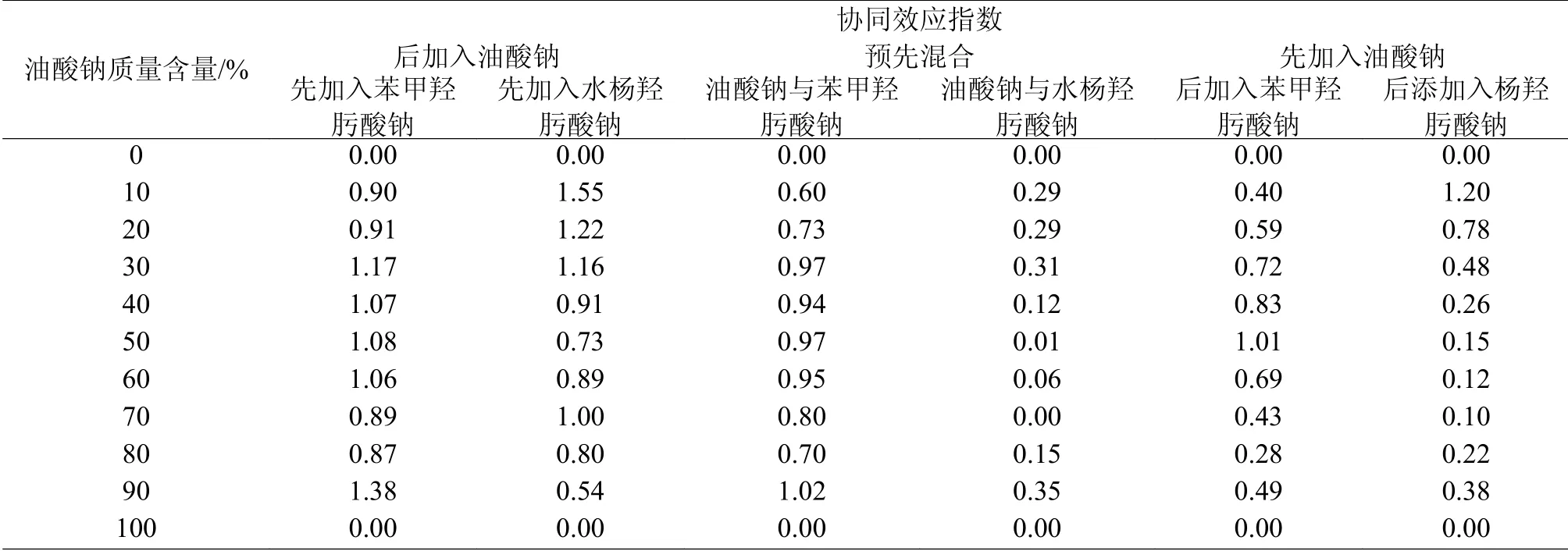
表1 不同体系中组合药剂的的协同效应指数Table 1 Synergism valuesof different combined reagentsfor rutile flotation
不同条件下金红石回收率与药剂比例的关系曲线见表2。由表2可看出,在拟合优度相近的情况下药剂预先混合后再添加和先添加油酸钠时,油酸钠与苯甲羟肟酸钠或水杨羟肟酸钠体系的回收率与药剂比例的关系可分别用4次和5次多项式拟合,显示前一混合体系中金红石的浮选行为较后者简单。而在先添加苯甲羟肟酸钠后加入油酸钠时金红石的浮选行为较先加入水杨羟肟酸钠后加入油酸钠时复杂,进一步说明油酸钠与苯甲羟肟酸钠混合对金红石的捕收能力超过其与水杨羟肟酸钠组合。由P-value可以看出,曲线拟合结果非常显著,可以用来预测实验结果。

表2 不同体系中金红石浮选回收率与药剂比例的拟合曲线Table 2 Curving fittingsfor rutile recovery against reagent ratioa in varioussystems
3 结论
(1)三种药剂对金红石捕收能力大小顺序为:油酸钠体系(ε=49.2%)>苯甲羟肟酸钠体系(ε=39.16%)>水杨羟肟酸钠体系(ε=3.47%)。相同药剂添加顺序下油酸钠与水杨羟肟酸钠混合体系中金红石的回收率要小于其与苯甲羟肟酸钠混合体系,显示油酸钠与苯甲羟肟酸钠组合对金红石的捕收能力较强。油酸钠和苯甲羟肟酸钠混合体系中回收率大小为:先苯甲羟肟酸钠后油酸钠>二者预先混合>先油酸钠后添加苯甲羟肟酸钠。油酸钠和水杨羟肟酸钠体系中则表现为:先添加水杨羟肟酸钠后油酸钠>先添加油酸钠后水杨羟肟酸钠>预先混合后再添加。
(2)油酸钠与羟肟酸类药剂分子之间具备缔合能力,该缔合力是由于油酸钠分子中富电子的双键与羟肟酸类药剂分子中缺电子苯环之间的电子共轭效应。先添加羟肟酸类药剂后添加油酸钠时金红石的回收率在三种药剂添加顺序下最高,显示此时组合药剂之间所生成的缔合物的数量及空间构象最适宜浮选气泡在矿物表面的附着。两种体系内组合药剂在金红石表面的吸附可分为互相诱导的单分子层共吸附和缔合物引起的多层吸附两大类。
(3)油酸钠与苯甲羟肟酸钠混合浮选体系中金红石回收率的高低与药剂作用后矿物的带隙宽窄成正比例关系,即带隙越宽,金红石的浮选回收率越高;而油酸钠和水杨羟肟酸钠混合体系中金红石带隙宽度与其浮选回收率成反比关系,深层次的原因则有待于进一步研究。

