表面端基对MXene材料电解水制氢的影响*
张萌玲,卢清杰,卢 强,柳清菊
(云南大学 材料与能源学院,昆明 650091)
0 引 言
工业革命以来,化石燃料一直是人类社会发展所依靠的主要能源。但能源危机与环境问题日益凸显,开发可再生能源,加快能源结构转型迫在眉睫。氢能作为可再生能源,依托于丰富的海水资源与太阳能或风能产生的剩余电能,通过电解水制氢技术既能解决新能源发电工程的大规模消纳问题,又能促进新能源产业和氢能产业的发展,对我国调整能源结构有着重要意义[2]。由于电化学界面阻力以及浓度差等影响因素,实际中电解水制氢所需的电压远高于其理论值1.23 V[3]。研究与开发催化剂用于减小过电位、加快电子转移速率是促进电解水制氢发展的关键。目前,贵金属催化剂为广泛应用的催化剂,主要指铂族金属(Pt、Ru、Rh、Ir、Pd) 及其氧化物(RuO2和IrO2等)。其中,Pt和RuO2、IrO2分别为析氢反应(HER)和析氧反应(OER)最理想的电催化剂[4]。贵金属因自身的自旋轨道耦合效应而具有高催化活性,其氢吸附自由能(ΔGH)近似于0,能有效降低HER所需要的过电位。但贵金属价格昂贵、储量稀少,虽有较高的催化活性,且单独使用时容易发生聚集,同时也存在毒性、易溶解、稳定性差等不足,极大地限制了其应用。
MXene(一般为过渡金属碳化物、氮化物和碳氮化物)是继石墨烯之后一类新兴的2D材料,在吸附[5]、光电催化[6-7]、气敏[8]、电池[9-10]、超级电容器[11-12]、半导体[13]、传感器[14-15]等领域极具应用潜力。目前,至少有超过100种化学计量的MXene成分和无限数量的固溶体[16],利用适当的手段插层、功能化、杂化[17]可以获得具有一定层间距的单层或少层材料。基于其高比表面积、载体功能、金属成分和表面端基带来的良好导电性和亲水性、多样的制备方法、高灵活度以及良好的化学稳定性,MXene材料用作电解水制氢催化剂吸引了大量的研究且取得了较快的进展。MXene催化水分解是放热过程。Gouveia等[18]利用密度泛函理论研究水在18个M2X MXene (M = Ti,Zr,Hf,V,Nb,Ta,Cr,Mo和W,而X=C或N)表面上的解离与键合。在MXene(0001)表面上,水分子吸附在桥(B)或顶部(T)(图1),分解为OH和H两部分并在各自最稳定吸附位点进行扩散。两者在MXene表面吸附自由能均为负值,其中H最有利吸附位点为HM中心,OH吸附位置取决于MXene种类,有时最有利吸附位点存在竞争关系。研究中涉及的MXene反应活化能垒都低于0.44 eV,氮化物势垒往往略大于相应碳化物的势垒,并且沿着元素周期表呈现周期增加趋势。
1 MXene材料的制备
MXene材料是由前驱体Mn+1AXn刻蚀而来,其中A为活泼金属,主要是Al、Si、In、Ga、Ge、Sn。由于M-X键以共价键和离子键为主,结合力较强;M-A键为金属键,结合力较弱,因此可以通过选择性刻蚀A原子层以获得二维层状MXene材料。MXene自身的结构特性决定了制备工艺的多样性。自2011年Ti3C2成功制备以来,短短十余年已有百余种MXene材料被成功合成并报道。如图2所示,随着时间的推移,MXene材料的制备方法越来越多样化。本文主要介绍含氟制备和无氟制备两种方法。
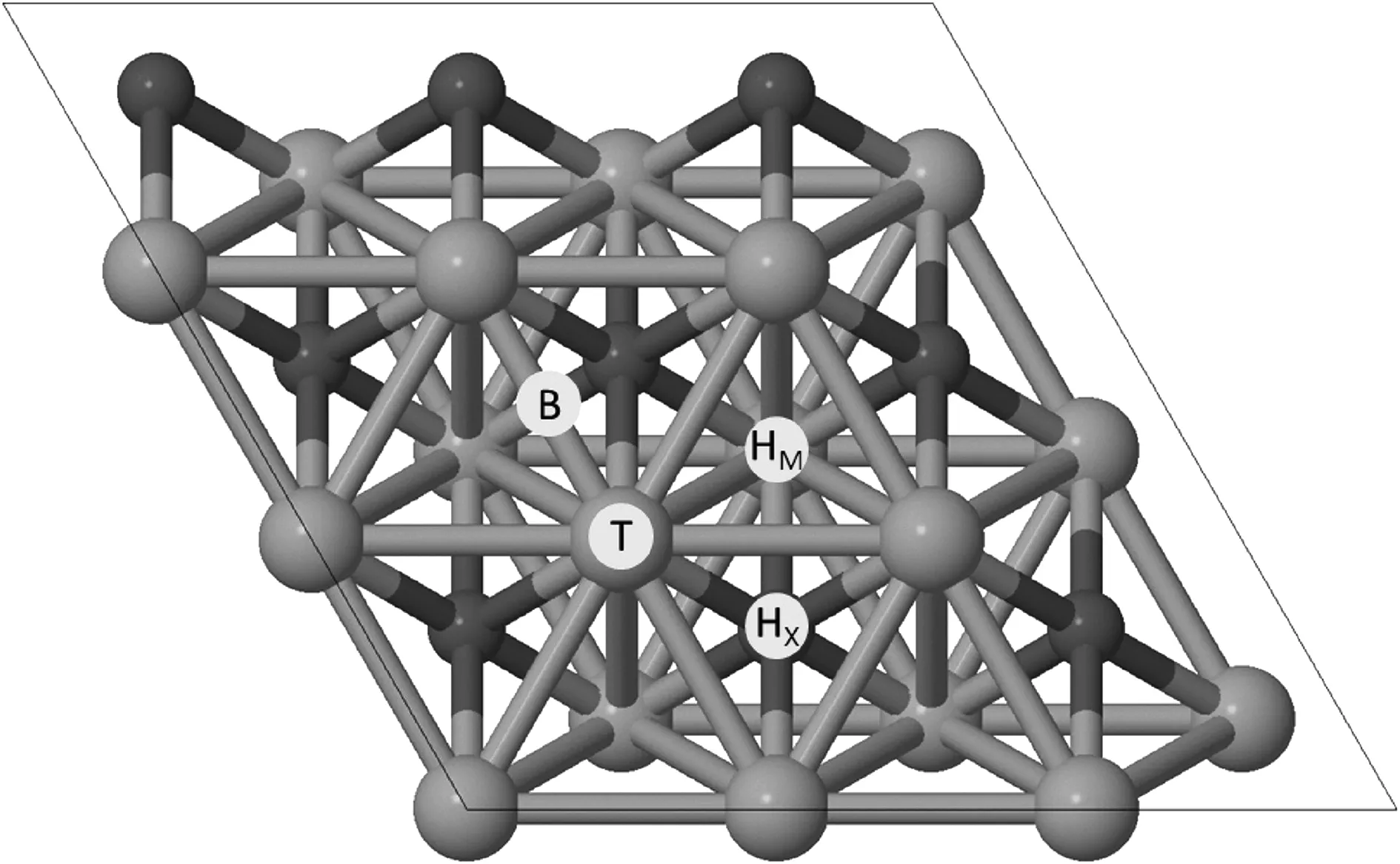
图1 MXene (0001)表面的超晶胞的俯视图。顶层和底层为过渡金属(M),中间层为碳或氮(X)。菱形为所用单元格边界。球内字母表示4个对称位置:桥(B)、顶(T)、中空金属(HM)和中空碳/氮(HX)[18]
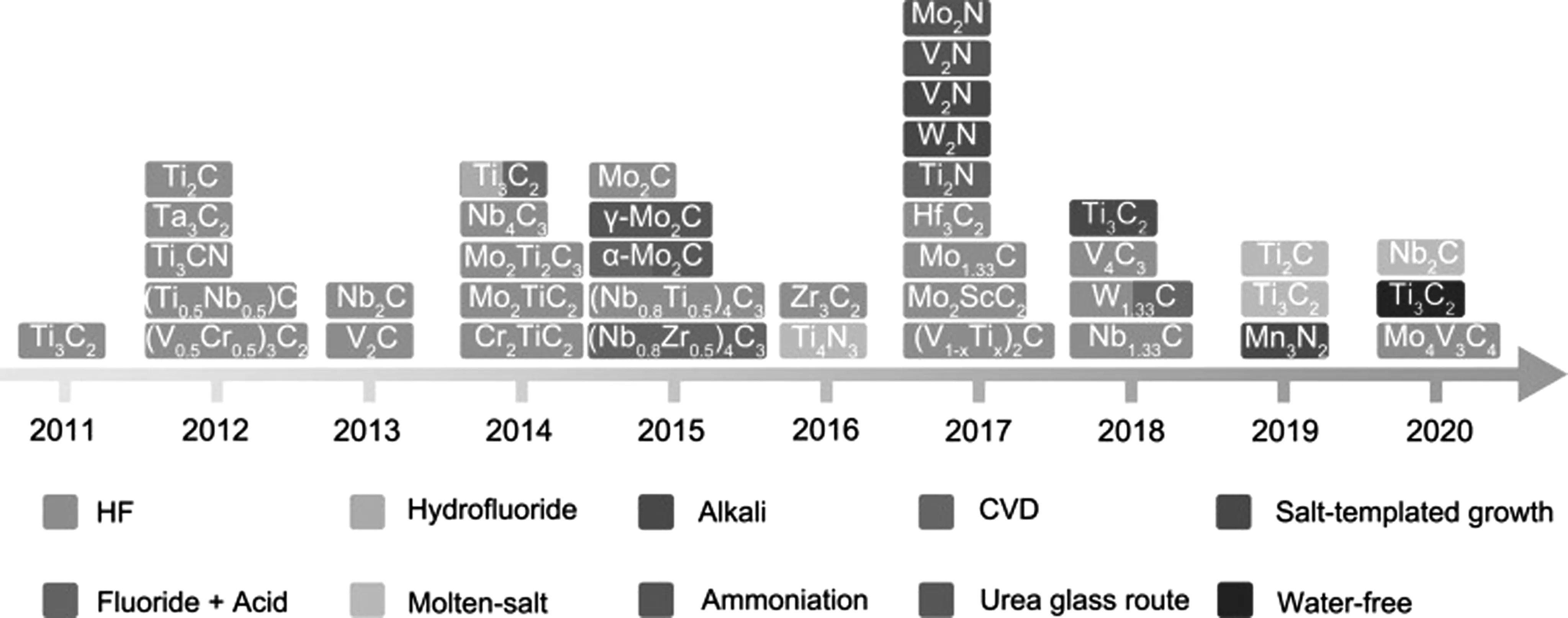
图2 MXene材料的合成历程[19]Fig.2 Timeline of a typical synthetic route for MXene in the past decade[19]
1.1 含氟制备工艺
使用HF刻蚀MAX相是制备MXene材料最常用的方法。以制备Ti3C2为例,Wang等[17]将其对应的MAX相缓慢浸泡至HF中,发生如下所示的化学反应,从而得到目标MXene材料(图3)。
Ti3AlC2+3HF=AlF3+3/2H2+Ti3C2
(1)
Ti3C2+2H2O=Ti3C2(OH)2+H2
(2)
Ti3C2+2HF=Ti3C2F2+H2
(3)

图3 HF刻蚀Ti3AlC2过程示意图[17]Fig.3 Schematic diagram of HF etching Ti3AlC2 process[17]
此外,Luo等[11]同样通过HF刻蚀Ti3AlC2成功制备出Ti3C2-MXene经过插层与Sn4+柱化处理后,将其应用于锂离子电容器,表现出更高的能量密度与功率密度。并且,作者通过XRD表征分析了刻蚀前后物相的变化并对比了采用普通烘干和冷冻干燥得到的MXene表面形貌上的区别,前者烘干的试样表面有微小的Al2O3纳米颗粒附着。
HF刻蚀MAX相所需要的时间、温度与HF浓度有关。利用HF刻蚀可以快速、大量的获得多层聚集态的MXene,其后一般需要经过液体插层剥离得到单层或少层的MXene。但是,由于HF是强酸,易挥发、有毒性、危险性高,寻找能代替HF的刻蚀剂显得尤为重要。
强酸和氟化物混合原位生成HF或利用双氟化物代替HF进行刻蚀是比较常见的替代方法。例如,黄等[20]利用LiF和HCl反应生成HF参与MAX相刻蚀,显著减少了HF的用量。与全部使用HF不同的是,由于氟化物阳离子和水分子的插层作用,刻蚀后层间距增加。Karmakar等[21]以HCl与LiF原位反应刻蚀Ti3AlC2并按逐层组装工艺制造Ti3C2Tx-MXene/CuI纳米颗粒异质界面,适用于光电和存储器件。Zhao等[22]通过LiF和HCl参与Ti3AlC2刻蚀出MXene,利用1-(3-氨丙基)-3-甲基咪唑溴化铵对MXene进行功能化后作为添加剂参与制备水性环氧树脂(WEP)的智能阻隔增强剂。Guo等[23]将HCl分别混合LiF、 NaF、KF、NH4F作为刻蚀剂在120~180 ℃下刻蚀Mo2Ga2C。NH4F + HCl作为刻蚀剂表现出优异的刻蚀能力,可以在更低的温度下获得Mo2C-MXene。
除了通过LiF和HCl反应生成HF之外,利用KHF2、NH4HF2等前驱体的热分解产生HF进行刻蚀也是比较常见的方法之一。Feng等[24]通过NH4HF2刻蚀Ti3AlC2制备出具有大晶面间距的Ti3C2-MXene材料,高温下表现出良好的稳定性。
含氟刻蚀方法选择性高、制得的MXene层间距较大且表面基团丰富,但同时在安全和环保等方面存在一定的隐患。
1.2 无氟制备工艺
熔融盐刻蚀[25-27]、碱液法刻蚀[28]、电化学刻蚀[29]、卤素刻蚀[30]、藻类刻蚀[31]、化学气相沉积法等[29]也是获得无氟MXene的重要方法,在过去的发展中已逐渐成为代替HF和通过原位反应生成HF刻蚀的重要途径。Yu等[32]提出液体刻蚀结合机械力辅助液体剥离制备Ti3C2纳米片新方法,实现无氟技术。Li等[26]第一次通过非氟化学方法获得仅有Cl作为表面终端基的MXene。利用熔融ZnCl2中的Zn元素与MAX相前驱体(Ti3AlC2、Ti2AlC、Ti2AlN和V2AlC)中的Al元素之间的置换反应,合成新的MAX相。同时,过量熔融ZnCl2具有很强的Lewis酸性,在剥离过程中形成以Cl作为表面端基的MXene。 Li等[27]将Ti3SiC2在CuCl2熔盐中浸渍制备得到Ti3C2,表现出高Li+存储容量和高倍率性能。刻蚀过程中,暴露的Si原子被Lewis酸Cu2+氧化成Si4+,形成具有挥发性的SiCl4,而剩余Cu2+与Ti3C2中部分暴露的Ti原子反应生成金属铜沉积在样品表面。依赖于A层原子的两性性质,可以利用碱性溶液刻蚀MAX相。Li等[33]以NaOH碱辅助水热法制备了无氟且高纯度的Ti3C2Tx-MXene(T=OH,O)。然而碱性刻蚀条件下MXene骨架容易发生腐蚀,改良刻蚀工艺是采用碱液法刻蚀所必须面临的挑战[29]。电化学刻蚀可以摆脱刻蚀剂对材料骨架的影响[34]。Yang等[35]采用无氟电化学刻蚀方法,在较短的刻蚀时间内(5 h)获得90%以上单层或双层Ti3C2Tx。以1M NH4Cl和0.2 mol/L四甲基氢氧化铵(TMA·OH)组成电解液,两块Ti3AlC2分别作为阳极和阴极,阳极进行蚀刻反应,阴极用作对电极。Shi等[30]在无水乙腈(CH3CN)中利用碘刻Ti3AlC2,随后在HCl溶液中分层制备出无氟MXene。所制备MXene具有O终端基和完整的晶格结构,可以进一步转化为具有中等尺寸(约1.8 mm)和高氧含量(18.7%(质量分数))的薄片,且在分散体系中可以稳定存在2周。与初始致密的层状Ti3AlC2相比,碘蚀刻MAX相由于引入了碘化物作为表面端基而有明显的膨胀。
2 表面端基的分类及其对性能的影响
裸露的MXene材料化学性质不稳定,极易被氧化或分解。表面端基的引入即为对MXene进行表面功能化的过程。官能团功能化的MXene具有裸露MXene的金属导电性同时更加稳定。以HF刻蚀Ti3AlC2为例,MAX相层间的Al原子被移除,导致单个Ti3C2层因失去金属键而彼此剥落。剥落的2D Ti3C2层具有两个暴露的Ti原子,连接环境中的官能团以建立稳定结构[29]。—O、—OH或—F属于MXene上天然、常见的官能团。依据Bader电荷与热力学稳定性分析,稳定性Ti3C2O2>Ti3C2F2>Ti3C2(OH)2[31]。
除此之外,表面端基会影响MXene材料的电化学性能、能带结构和功函数[36]。在不影响框架的基础上表面端基可以调节MXene材料的带隙[37-39]。没有表面端基的Ti3C2表现出金属性质,而Ti3C2F2与Ti3C2(OH)2具有半导体的能带结构。同时,MXene材料的性能很大程度上依赖于表面端基的种类。这些丰富的表面端基赋予了MXene丰富的表面化学性质和高度亲水性[40]。对MXene材料进行刻蚀是引入表面端基的重要方法。刻蚀液的选择直接影响表面端基的比例,刻蚀方法的多样性致使MXene表面端基多样化。目前已报道的表面端基可主要分为三大类,分别是卤族( —F、—Cl等);氧族(—O、—S等)和等相对分子质量官能团(—OH、—NH2、—CH3等)[41]。
2.1 卤族
卤族表面端基可以通过在卤化物熔盐中的Lewis酸性蚀刻接枝到MXene上[27]。这类带有负电荷的表面端基可以促进质子吸附动力学,同时降低电荷转移电阻,从而提高活性位点的反应性。Li[40]及其团队以10% HF溶液刻蚀、N-甲基吡咯烷酮(NMP)中超声剥离并在低温退火下制备出具有丰富表面F端基且不含O基团的Ti2CTx纳米片。结合密度泛函理论计算和实验表征,丰富的表面F端基赋予了MXene优异的电催化活性。如图4所示,—F、—O、—OH作为表面端基引入可以降低ΔGH。富有F端基的Ti2CTx纳米片的起始过电位为75 mV,比层状Ti2CTx(265 mV)和原始Ti2AlC(380 mV)小得多。并且当表面F端基减少时,其催化活性大大下降。Li等[26]基于MAX相与ZnCl2之间的置换反应利用熔融盐刻蚀制备出富含Cl表面端基的MXene。较富含F表面端基的MXene具有更优异的电化学行为。Sarfraz等[38]以CuCl2作为反应原料熔融法合成Cl作为表面终端基团的Ti3C2Cl2MXene。通过扫描电镜表征结果,单层Cl-MXene纳米片更透明、更薄厚度更小。作为碱性介质(KOH溶液)中的HER催化剂,Ti3C2Cl2过电位为259 mV,较Ti3C2Tx降低了185 mV,并且兼具更低的Tafel斜率。良好的HER催化活性可归因于Cl作为表面端基增加了层间距,为反应提供了更多的活性位点,同时,以Cl作为表面端基的MXene拥有更高的稳定性。

图4 Ti2C、Ti2CFx、Ti2CFx(OH)、Ti2CFx(O) 和 Ti2CFx(OH)(O) 的结构模型,括号内数值为一个氢原子吸附的吉布斯自由能[40]Fig.4 Structural models of Ti2C, Ti2CFx, Ti2CFx(OH), Ti2CFx(O) and Ti2CFx(OH)(O). The contents of the brackets represent the calculated Gibbs free energy for one hydrogen atom adsorption[40]
2.2 氧族
简单热处理可以在MXene表面形成O端基。在高温下,—OH易转化为—O[42]。 HER的活性与表面O原子的电荷状态有关,而O原子的电荷状态又受—OH覆盖率影响[43]。以O作为表面端基的MXene在HER中具有较低的ΔGH,是用于电催化产氢的重要催化剂。Lv等[44]研究具有2H对称结构以O作为表面端基的Ti2C、V2C、Nb2C、Mo2C和Ti3C2HER催化性能。通过分子动力学模拟,具有优异的热力学稳定性。并且电荷以稳定离子键的形式大都分布在碳原子和外部氧原子周围(图5),成为氢吸附的活性中心。Ling[45]等分析了以O作为表面端基的10个单金属碳化物和7个双金属碳化物MXene的HER活性,其中Ti2CO2和W2CO2具有较高HER催化活性。O在MXene上有两个能量上有利吸附方向,导致3种不同结构的M2CO2(M为过渡金属),如图6所示。图6(a)为O原子在一个表面上吸附在fcc位点,在另一个表面上吸附在hcp位点;6(b)中O原子更倾向于吸附在两侧的面心立方位点;6c为O原子在两个表面上吸附于hcp位点。IIIB族金属碳化物,O原子在一个表面上吸附于fcc位点,另一个表面上吸附于hcp位点。IVB和VB族金属碳化物,O原子倾向于吸附在两侧的面心立方位点。但VIB族金属,氧吸附最稳定的位点为两个表面的hcp位。由于外层过渡金属原子与表面O端基相结合,带有负电性的表面端基会从外层过渡金属接受电子,并在费米面以下形成一个新的能带,从而使材料具有不同是导电性能,显示具有O端面的IVB金属碳化物是半导体,而具有O端面的VB和VIB金属碳化物是金属。Lai等[40]将HF刻蚀制备出Ti2C-MXene在1 100 ℃下退火形成Ti2COx。Ling[46]等利用第一性原理计算过渡金属元素(Fe,Co和Ni)的引入对具有完全氧封端的碳化钒(V2CO2)的HER催化性能的影响。过渡金属引入削弱氢与氧之间的强结合力,促进了内部原子和表面O原子之间的电荷转移,降低MXene表面ΔGH直至为零并兼具良好的稳定性。Jiang等[47]通过简单化学处理将Ti3C2(OH)x转换为Ti3C2Ox。在10 mA/cm2下过电位为190 mV并兼具良好稳定性。Pandey[48]等发现MXene不同的层厚度与金属组成成分会影响其HER催化活性,ΔGH可以根据MXene结构中金属层的数量变化高达0.5 eV。Wu等[49]利用高温煅烧直接合成了2D层状化合物Ta2CS2-MXene。这种有序S封端的Ta2CS2-MXene具有双功能活性,在10 mA/cm2时,OER活性为243 mV,HER活性为73 mV。

图5 (a)Ti2CO2,(b)V2CO2,(c)Nb2CO2,(d)Mo2CO2和(e)Ti3C2O2的ELF图(上,0.5au)和ELF图(下,0.8au)的等值面垂直于(100)方向切片[44]Fig.5 Isosurfaces of ELFs (upper, 0.5 au) and ELF maps (lower, 0.8 au) sliced perpendicular to the (100) direction for (a) Ti2CO2, (b) V2CO2, (c) Nb2CO2, (d) Mo2CO2 and (e) Ti3C2O2[44]

图6 O-封端MXenes的三种不同结构的俯视图和侧视图[45]Fig.6 The top and side view of three different kind of structures of O-terminated MXenes[45]
2.3 等相对分子量官能团
—OH作为MXene表面端基的形成能通常大于相应结构形成以—F作为表面端基,这意味着—F在洗涤、储存在水中或碱溶液碱化都会转化为—OH[13]。Bai[13]等比较了Lu2CT2(T=F,OH)的稳定性、电子性质和载流子迁移率。结果显示F端基的存在可能导致中心Lu原子的F轨道分裂。而OH结构为直接带隙半导体,其带隙为1.28 eV,具有更低功函数。Peng[50]及其团队利用简单的密封热方法使—NH2取代—OH,在Ti3C2-MXene表面成功引入了端—NH2基团。
除此以外, P和Si属于MXene上非天然官能团,利用P和Si取代Ti2C和V2C的—F和—OH也被证实具有可行性[51-52]。
3 结 论
MXene材料作为一个冉冉升起的新星材料,因在能源、电池、超极电容器、摩擦纳米发电机、涂料材料、感应器件等领域具有重要的应用而收到重点关注。电解水制氢是解决能源危机的重要举措,当下催化剂的固有性质仍然存在电荷转移缓慢和活性中心局限在边缘或缺陷位的缺点[43]。改变M或X元素的比例[16]制备合成具有较大比表面积的层状结构的MXene,优化和丰富MXene的现有性能是攻克这一难点的解决方法。大量研究与计算证实表面端基功能化MXene是提高产氢效率的重要举措。表面端基功能化后的MXene具有优异的导电性与可作为HER反应活性位点的表面端基,可大幅降低反应中的ΔGH,甚至在某些程度上媲美贵金属催化剂。了解表面端基与MXene的整体构效对HER催化活性提高至关重要。作为日益扩大的家族,在理论与实践方面,未来仍需要不断完善与发展,以期尽快收获应用。

