大剂量甲氨蝶呤治疗淋巴瘤的血药浓度和不良反应影响因素分析Δ
叶嘉俊,黎泽钰,吴汉彪,王 佳,葛燕辉,仇志坤 (广东药科大学附属第一医院临床药学重点专科,广州 510080)
甲氨蝶呤(methotrexate,MTX)作为一种抗肿瘤药物,在淋巴瘤治疗中的临床使用剂量通常高于常规剂量,当给药剂量大于500 mg/m2称为大剂量甲氨蝶呤(high‑dose methotrexate,HD‑MTX)。2019年《大剂量甲氨蝶呤亚叶酸钙解救疗法治疗恶性肿瘤专家共识》指出,HD‑MTX在淋巴瘤的治疗方案中起重要作用,其剂量范围为1~8 g/m2,而20 mg/kg或500 mg/m2已达到致死量[1]。因此,临床使用HD‑MTX时必须合理使用亚叶酸钙进行解救,这种疗法被称为HD‑MTX亚叶酸钙解救疗法。HD‑MTX在化疗时毒性较大,常见不良反应有肝肾功能损伤、腹泻、骨髓抑制等。因此,血药浓度监测是安全应用HD‑MTX的前提。过往研究显示,合并使用质子泵抑制剂(proton pump inhibitors,PPIs)类药物会引起HD‑MTX的延迟排泄[2]。本文采用回顾性研究,探讨HD‑MTX治疗淋巴瘤的血药浓度和不良反应影响因素,旨在为HD‑MTX的研究和应用提供数据支撑,为其在临床上合理应用、减少毒副作用提供参考。
1 资料与方法
1.1 一般资料
通过查阅广东药科大学附属第一医院电子病历系统、医院管理信息系统(hospital information system,HIS)及检验系统,收集2020年7月至2021年11月接受HD‑MTX治疗的所有患者的病历信息,包括患者的病历号、年龄、性别、身高、体质量、化疗方案、给药剂量,以及给药前后丙氨酸转氨酶、天冬氨酸转氨酶、总胆红素、肌酐清除率(creatinine clearance,CrCl)、白蛋白(albumin,ALB)等检验指标,记录不同时间HD‑MTX的血药浓度(c6h、c24h、c48h)检测值,提取合并使用PPIs类药物信息,并评估用药后48 h内所有不良反应发生情况。本研究通过本院伦理委员会批准,伦理号:医伦审〔2023〕IIT‑第(9)号。
1.2 纳入、排除标准
本研究的纳入标准:(1)经临床诊断为淋巴瘤;(2)至少完成1个疗程的 HD‑MTX化疗;(3)化疗前及化疗期间进行了血常规和肝、肾功能检查;(4)化疗期间进行了HD‑MTX治疗药物浓度监测。本研究的排除标准:外院转入血药浓度超标的患者。
1.3 治疗方案
(1)HD‑MTX用量:HD‑MTX的总剂量根据不同淋巴瘤、不同患者的基本情况确定,一般给药剂量为2~5 g/m2,前30 min滴完总量的10%,余下90%经输液泵于5.5 h内匀速滴完;滴注结束后12 h开始,每6 h肌内注射亚叶酸钙至HD‑MTX血药浓度<1 μmol/L。(2)化疗前1 d进行水化操作并用碳酸氢钠碱化尿液,使尿量维持在3 000 mL/d以上且pH值≥7。(3)亚叶酸钙解救:常规解救共6次,一般在HD‑MTX滴注结束后12 h开始,首次剂量为负荷剂量75 mg,后5次剂量均为15 mg/m2,每隔6 h静脉注射1次;若测得HD‑MTX血药浓度仍然过高,则追加亚叶酸钙解救剂量,并继续监测HD‑MTX的血药浓度。
1.4 主要治疗药物、试剂及仪器
MTX注射液购自澳大利亚Pfizer(Perth)Pty Limited公司,注射用亚叶酸钙购自哈尔滨三联药业股份有限公司,MTX检测试剂、Viva‑E全自动免疫分析仪均购自西门子医学诊断产品(上海)有限公司,雷勃尔LD5‑2A离心机购自北京医用离心机厂。
1.5 统计学方法
使用SPSS 22.0软件进行统计分析。计量资料以±s表示,多组间比较采用单因素方差分析;以单因素分析差异有统计学意义的指标为自变量,以c6h、c24h、c48h为因变量,采用多元线性回归进行血药浓度影响因素的多因素分析,方差膨胀系数(variance inflation factor,VIF)在1~3.5之间,表明自变量之间无共线性问题;不良反应发生情况以率表示,组间比较采用χ2检验。检验水准α=0.05。
2 结果
2.1 一般资料结果
本研究最终纳入133例采用HD‑MTX治疗淋巴瘤的患者进行分析。其中14~35岁(青年组)54例,36~59岁(中年组)51例,60~73岁(老年组)28例;男性105例,女性28例;因9例为卧床患者,缺失身高或体质量数据,因此仅有124例患者,其中体质量指数(body mass index,BMI)<18.5(较轻组)27例,BMI 18.5~<24(正常组)69例,BMI≥24(超重组)28例;剂量<5 g/m2(小剂量组)45例,剂量≥5 g/m2(大剂量组)88例;根据肝功能正常范围(丙氨酸转氨酶>9~<50 U/L、天冬氨酸转氨酶>15~<40 U/L、总胆红素>5~<19 μmol/L)可知,肝功能正常组55例,异常组78例;因8例患者缺失身高或血清肌酐数据,因此仅有125例患者,其中CrCl>120 mL/min组49例,CrCl 90~120 mL/min组40例,CrCl 60~<90 mL/min组29例,CrCl 30~<60 mL/min组7例;合并使用PPIs组10例,未合并使用PPIs组123例;ALB<35 g/L(异常组)26例,ALB≥35 g/L(正常组)107例。
2.2 血药浓度影响因素单因素分析结果
HD‑MTX治疗淋巴瘤时,影响血药浓度的单因素分析结果显示:年龄、CrCl对c6h有影响,差异有统计学意义(P<0.05);年龄、CrCl、ALB对c24h有影响,差异有统计学意义(P<0.05);年龄、BMI、CrCl、合并使用PPIs、ALB对c48h有影响,差异有统计学意义(P<0.05)。结果见表1。

表1 影响不同时间HD‑MTX血药浓度的单因素分析结果
2.3 血药浓度影响因素多因素分析结果
采用多元线性回归对单因素分析差异有统计学意义的指标进一步进行多因素分析,结果显示,年龄、CrCl对c6h无影响,差异无统计学意义(P>0.05),VIF在1~3.5之间,表明数据之间相互独立,自变量之间无关联性,分析结果可接受;年龄是c24h的主要影响因素,差异有统计学意义(P<0.05),VIF在1~3.5之间,表明存在低度自相关性,自变量之间无关联性,分析结果可接受;CrCl、合并使用PPIs是c48h的主要影响因素(P<0.05),VIF在1~3.5之间,表明存在低度自相关性,自变量之间无关联性,分析结果可接受。结果见表2。
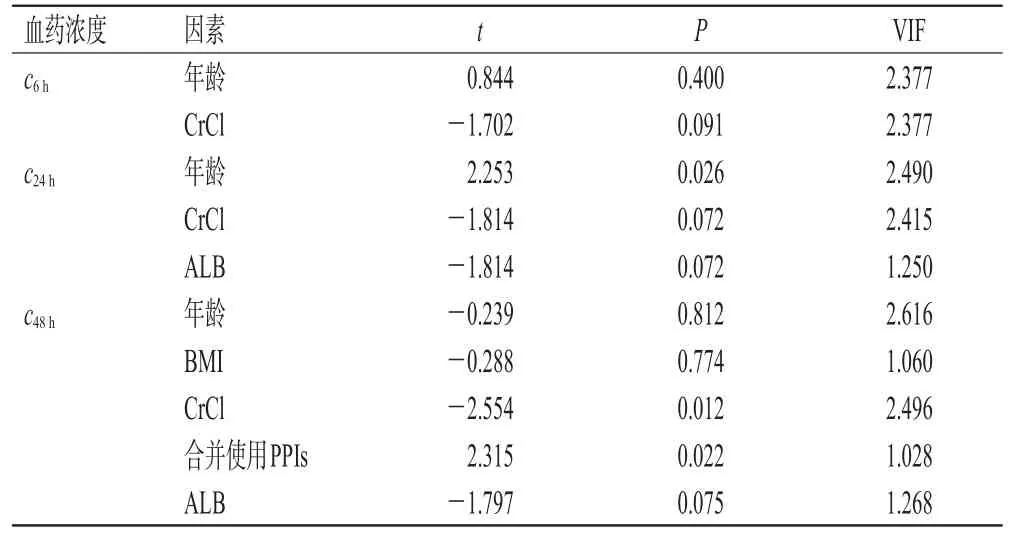
表2 影响不同时间HD‑MTX血药浓度的多因素分析结果
2.4 不良反应发生情况及影响因素分析结果
本研究收集了133例患者采用HD‑MTX治疗淋巴瘤48 h内的不良反应发生情况,有68例患者发生不良反应,总体不良反应发生率为51.13%,其中皮肤和超敏反应2例,血液和淋巴系统反应59例,胃肠道反应6例,其他不良反应1例。因BMI纳入例数为124例,CrCl纳入例数为125例,故两组不良反应例数均为62例。不同组别统计的不良反应发生率结果显示,年龄、BMI、肝功能、CrCl对不良反应发生率有影响,差异有统计学意义(P<0.05)。结果见表3。

表3 影响HD‑MTX不良反应的因素分析结果
3 讨论
本研究结果显示,年龄是c24h的主要影响因素,c24h与年龄呈正相关。既往研究显示,肾脏是MTX的主要排泄途径,年龄对肾脏功能有一定影响,血药浓度也随年龄增长有上升趋势[3]。本研究结果显示,CrCl与合并使用PPIs是c48h的主要影响因素。CrCl反映患者的基础肾功能,肾功能不全则会导致MTX排泄减少,从而导致血药浓度升高;另外,HD‑MTX以静脉给药方式给药,24 h内大部分的MTX会排出体外[4],提示药物在组织中分布积聚是影响MTX后期清除的主要因素。合并使用PPIs对HD‑MTX血药浓度的影响机制有较多说法,可能是由于PPIs抑制肾小管中的H+‑K+‑ATP酶,导致肾小管减少分泌MTX,从而使其血药浓度升高[5―6]。Wang等[7]的Meta分析结果显示,PPIs与HD‑MTX联合使用会致使MTX排泄减少,导致c48h升高,提示对于合并使用PPIs的患者,应加强血药浓度监测。
本研究结果显示,纳入133例患者的不良反应发生率为51.13%,其中血液和淋巴系统的不良反应占不良反应总数的86.76%,提示HD‑MTX治疗淋巴瘤需要密切关注不良反应发生情况,及时做好处理,尤其是血液和淋巴系统相关的不良反应。年龄对HD‑MTX治疗淋巴瘤的不良反应发生有影响,其原因可能是年龄越大的患者因其生理功能减退,器官代偿适应能力变差,机体的生物转化和排泄能力相对减弱,导致药物半衰期延长,在体内积蓄,血药浓度升高[8],更可能出现MTX排泄减少。这提示老年人更应加强血药浓度监测,以便及时给予亚叶酸钙解救。BMI对HD‑MTX不良反应发生有影响,原因可能是MTX表观分布容积和清除率随体质量的增加而增加,导致药物在体内积蓄,血药浓度升高。这提示给药时要根据BMI适当调整剂量,并加强血药浓度监测。CrCl<90 mL/min的患者HD‑MTX血药浓度较CrCl≥90 mL/min的患者高,可能是由于肾功能不全则会导致MTX排泄减少,从而使血药浓度升高,导致不良反应发生。肝功能异常的患者在使用HD‑MTX治疗后,不良反应发生率上升,有可能是由于HD‑MTX相关肝损伤以肝细胞型为主,HD‑MTX血液浓度升高会增加肝损伤趋势[9]。
综上所述,HD‑MTX在淋巴瘤治疗方案中,需考虑患者年龄、CrCl及合并使用PPIs情况,做好患者血药浓度监测,及时使用亚叶酸钙解救;同时,患者年龄、BMI、肝功能和CrCl对不良反应发生率有影响,使用HD‑MTX治疗淋巴瘤时,需注意不良反应的发生,尤其是血液和淋巴系统相关的不良反应情况。本研究仍有局限性,如样本量较少、未涉及不良反应的具体种类和严重程度分析,有待进一步深入研究。

