孟鲁司特联合依巴斯汀治疗老年咳嗽变异性哮喘的疗效观察
牛奉华,牛丽华
北京市西城区大栅栏社区卫生服务中心,北京 100051
咳嗽变异性哮喘(cough variant asthma,CVA)是由免疫、炎症、环境等因素综合作用而形成的一种特殊类型的哮喘,其发病机制与普通哮喘类似,均存在气道炎症、气道高反应性、气道重塑等致哮喘因素[1]。但CVA通常以单一的咳嗽症状为临床表现,多发生于夜间,常表现为反复发作的刺激性干咳,春秋季加重,常与上呼吸道慢性炎症相混淆,故既往也称为“过敏性咳嗽”“隐匿性哮喘”[2]。随着年龄的增长,老年人群的免疫-内分泌调节能力下降,为CVA发病的高危人群。CVA虽不会造成生命危险,但由于其长期存在而影响夜间休息,常造成患者失眠、抑郁,严重影响了老年人群的生活质量。基于CVA发病与免疫、炎症因素密切相关,本研究旨在利用高亲和力的组胺H1受体阻断剂依巴斯汀和高亲和力的白三烯受体阻断剂孟鲁司特,来发挥其抑制免疫应答高反应性和炎症反应的作用,从而干预老年CVA患者的疾病发展过程。本研究采用VAS评分用于评估患者咳嗽症状的严重程度;CET评分用于评估患者日间咳嗽、夜间咳嗽对睡眠的影响、咳嗽的剧烈程度、咳嗽对日常生活和心理的影响;LCQ评分用于评估咳嗽对生活质量的影响。
1 资料与方法
1.1 一般资料
选取2020年5月~2021年12月期间于该院就诊的80例CVA患者作为研究对象,采用随机数字表法分为对照组和联合组,每组40例。其中,有76例患者完成全程治疗,对照组38例,联合组38例。对照组:男性22例,女性16例;年龄61~82岁,平均年龄(67.2±9.2)岁。联合组:男性21例,女性17例;年龄62~85岁,平均年龄(68.5±10.0)岁。两组患者一般资料比较无统计学差异(P>0.05),具有可比性。本研究经该院伦理委员会批准[伦理批号2020年(审)001号],所有患者或家属知情并签署知情同意书。
纳入标准:①符合中华医学会呼吸病学会哮喘学组2017年发布的《上-下气道慢性炎症性疾病联合诊疗与管理专家共识》[3]中关于CVA的诊断标准者。②年龄60~90岁者。③病程4周以上者。
排除标准:①并发急性支气管炎、肺结核、感冒等呼吸系统疾病者。②合并严重器质性疾病或精神疾病者。③入组前2周内使用过依巴斯汀、孟鲁司特药物治疗者。④不能配合治疗及随访者。⑤不能耐受依巴斯汀、孟鲁司特药物治疗者。⑥需加用糖皮质激素/长效β2受体激动剂者。
1.2 治疗方法
对照组给予口服孟鲁司特钠片(N.V. Organon,国药准字J20130047,规格10mg)10mg,qd,睡前服用,疗程8周。联合组在对照组治疗基础上,加用依巴斯汀片(ALMIRALL, S.A.,进口药品注册文号H20140855、H20140856,规格10mg)10mg,qd,睡前与孟鲁司特钠片同服,疗程8周。所有患者均调整生活方式,如健康饮食、哮喘防治教育、适当运动、避免接触冷、热、致敏原等,且不予以其他抗炎、止咳类中药或西药治疗。
1.3 观察指标
分别在用药前、用药第2、4周和8周进行视觉模拟评分(visual analogue scale,VAS)、简易咳嗽程度评分表(cough evaluation test,CET)、莱切斯特咳嗽问卷(Leicester cough questionnaire,LCQ),以评估患者咳嗽症状的严重程度、咳嗽对健康的影响程度以及咳嗽对生活质量的影响。①VAS是常用的疼痛评分标准之一,是患者根据自己症状严重程度在0~10mm的直线上标记刻度,0代表没有咳嗽,10mm代表最剧烈的咳嗽,中间部分代表不同强度的咳嗽。VAS用以对比患者治疗前后咳嗽的严重程度[4]。②CET从患者日间咳嗽频率、夜间咳嗽对睡眠的影响程度、咳嗽的剧烈程度、咳嗽对日常生活的影响程度、咳嗽对心理的影响程度5个方面进行1~5分的评估打分[5]。分值越高代表咳嗽对患者的日常生活、心理影响越大,反之代表咳嗽对患者的日常生活、心理影响越小。③LCQ用以评估患者生活质量具有良好的信度、效度和反应度[6]。对患者就咳嗽相关生活质量的19个问题进行问卷调查及打分,其中11个问题涉及生理领域,5个问题涉及心理领域,3个问题涉及社交领域。分值越高代表咳嗽对患者的生命质量影响越大,反之代表咳嗽对患者的生命质量影响越小。
1.4 统计方法
采用SPSS 17.0 软件进行数据统计学分析。计量数据以x±s表示,采用t检验;计数资料以n(%)表示,采用χ2检验。P<0.05为具有统计学差异。
2 结果
2.1 基线资料比较
对照组:病程范围6~22周,平均病程(12.6±4.4)周;27例曾接受吸入糖皮质激素治疗(71.1%)。联合组:病程范围6~25周,平均病程(13.2±5.0)周;25例曾接受吸入糖皮质激素治疗(65.8%)。两组患者病程、接受糖皮质激素治疗情况等基线资料比较无统计学差异(P>0.05)。
2.2 治疗前后两组患者VAS评分比较
两组患者治疗前和治疗第2周后VAS评分比较无统计学差异(P>0.05)。联合组治疗第4周和8周VAS评分均低于治疗前(P<0.05);且联合组低于对照组(P<0.05)。见表1。提示联合组可在用药4周后改善患者咳嗽症状的严重程度,且起效时间比单用孟鲁司特更早。
表1 两组患者VAS评分比较 n=38,±s,分

表1 两组患者VAS评分比较 n=38,±s,分
与同组治疗前比较,a:P<0.05;与对照组比较,b:P<0.05
组别 治疗前 第2周 第4周 第8周对照组 6.61±1.41 5.95±1.69 5.88±1.83 4.23±1.93a联合组 6.55±1.39 5.92±1.66 4.96±1.32ab 3.20±1.22ab t值 0.187 0.078 2.513 1.250 P值 0.852 0.938 0.014 0.007
2.3 治疗前后两组患者CET评分比较
日间咳嗽方面,两组患者治疗第2、4周和8周CEF评分与治疗前比较均无统计学差异(P>0.05)。夜间咳嗽影响睡眠、剧烈咳嗽、咳嗽影响生活、咳嗽导致焦虑方面,联合组治疗第4周和8周均较治疗前降低(P<0.05);且联合组治疗第4周和8周较对照组降低(P<0.05)。见表2。
表2 两组患者CET评分比较 n=38,±s,分

表2 两组患者CET评分比较 n=38,±s,分
分类 组别 治疗前 第2周 第4周 第8周日间咳嗽 对照组 2.32±0.47 2.30±0.62 2.26±0.45 2.29±0.33联合组 2.41±0.51 2.35±0.57 2.38±0.53 2.30±0.60夜间咳嗽影响睡眠 对照组 4.31±0.69 4.28±0.66 3.92±0.60 3.01±0.58a联合组 4.35±0.72 3.61±0.88 3.28±0.70ab 2.35±0.64ab剧烈咳嗽 对照组 3.61±0.62 3.59±0.65 3.12±0.69a 2.51±0.72a联合组 3.73±0.74 3.58±0.65 2.29±0.59ab 1.82±0.83ab咳嗽影响生活 对照组 3.52±0.76 3.44±0.81 3.17±0.68 2.60±0.59a联合组 3.61±0.82 3.14±0.83 2.71±0.70ab 2.22±0.56ab咳嗽导致焦虑 对照组 3.10±0.71 3.05±0.88 2.93±0.85 2.38±0.77a

续表
2.4 治疗前后两组患者LCQ评分比较
生理领域、心理领域、社交领域评分和总分,联合组治疗第4周和8周均较治疗前升高(P<0.05);且联合组高于对照组(P<0.05)。见表3。
表3 两组患者LCQ评分比较 n=38,±s,分
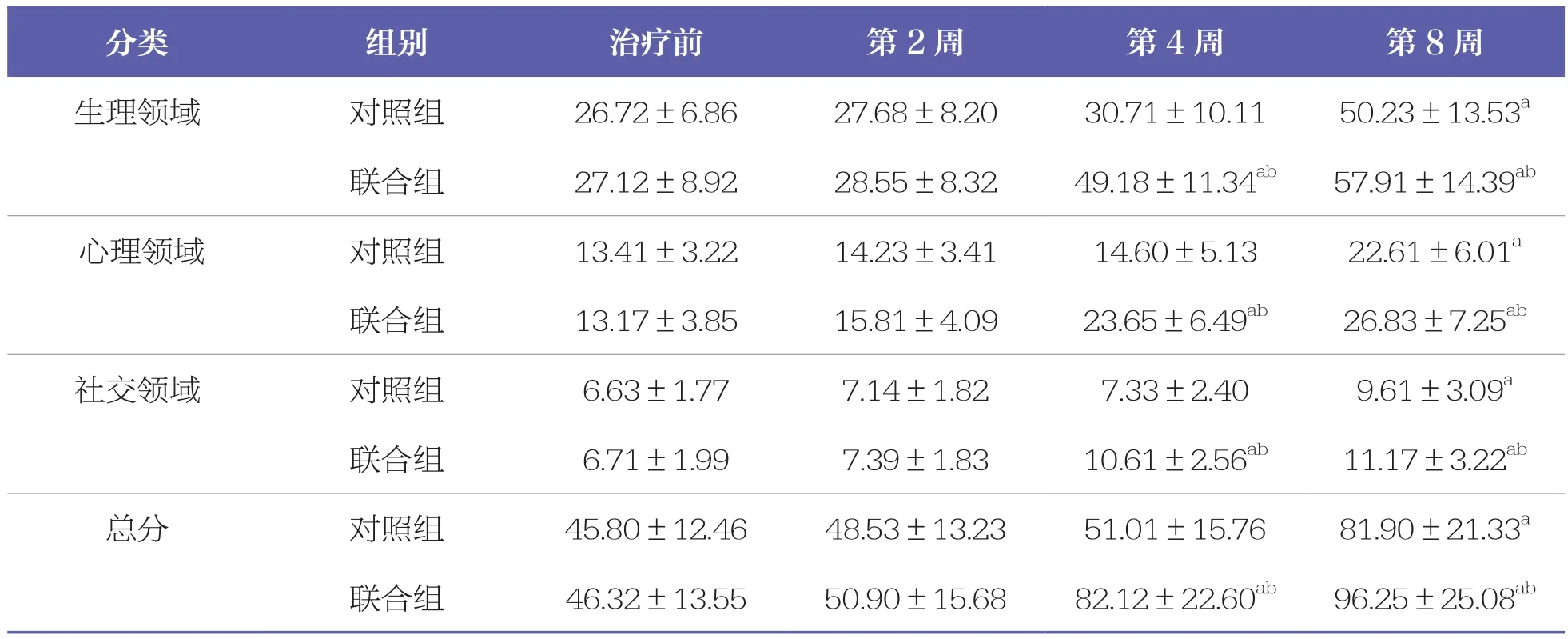
表3 两组患者LCQ评分比较 n=38,±s,分
与同组治疗前比较,a:P<0.05;与对照组比较,b:P<0.05
分类 组别 治疗前 第2周 第4周 第8周生理领域 对照组 26.72±6.86 27.68±8.20 30.71±10.11 50.23±13.53a联合组 27.12±8.92 28.55±8.32 49.18±11.34ab 57.91±14.39ab心理领域 对照组 13.41±3.22 14.23±3.41 14.60±5.13 22.61±6.01a联合组 13.17±3.85 15.81±4.09 23.65±6.49ab 26.83±7.25ab社交领域 对照组 6.63±1.77 7.14±1.82 7.33±2.40 9.61±3.09a联合组 6.71±1.99 7.39±1.83 10.61±2.56ab 11.17±3.22ab总分 对照组 45.80±12.46 48.53±13.23 51.01±15.76 81.90±21.33a联合组 46.32±13.55 50.90±15.68 82.12±22.60ab 96.25±25.08ab
3 讨论
CVA是一种以反复发作的刺激性咳嗽为主要症状表现的特殊类型哮喘,其发生机制与哮喘类似,是由多种免疫细胞参与形成以气道高反应性、气道炎症、气道重塑为特点的慢性气道炎症[7]。肥大细胞作为一种免疫细胞在CVA的病理生理过程中发挥了关键作用。当机体受到冷热变化等物理刺激或接触变应原时,肥大细胞会被激活而释放大量的组胺、白三烯、前列腺素等免疫介质,这些免疫介质共同作用,可引起气道收缩,导致气道高反应性,并刺激气道上皮细胞释放白介素-25(interleukin-25,IL-25)、白介素-33(interleukin-33,IL-33)等细胞因子,促进气道炎症的产生[8]。组胺是引起超敏反应的关键因素,主要由肥大细胞产生。组胺产生后,可与气道平滑肌中的组胺受体结合,引起支气管平滑肌收缩,同时使血管通透性增加,气管、支气管黏膜发生水肿,造成气道高反应性,致使患者在气道受刺激时产生干咳表现[9]。白三烯是人体内重要的炎症介质,白三烯肥大细胞被释放后可诱导炎症因子在气管内聚集,促进气道炎症的发展,同时白三烯可促进气道成纤维细胞、上皮细胞增殖,参与气道重塑[10-11]。本研究旨在通过不同的作用机制联合使用抗组胺及抗白三烯类药物,以评估对CVA病理过程的干预作用。
依巴斯汀是第2代抗组胺药物,与H1抗体具有高亲和力、高选择性,可有效地抑制组胺诱导的变态反应,拮抗组胺诱导的血管通透性增加及气道高反应性[12]。依巴斯汀不能透过血管屏障,不会与脑中H1受体结合。因此,在临床使用中较少出现嗜睡、头晕等神经系统不良反应[13]。在既往研究中,有学者应用依巴斯汀治疗儿童支气管哮喘,结果显示,患者的治疗有效率及肺功能均得到改善,同时激素使用率下降,显示出其治疗支气管哮喘的效果理想[14]。林振荣等[15]应用依巴斯汀治疗感染后咳嗽,亦取得了较好的治疗效果。孟鲁司特是一种高选择性白三烯受体拮抗剂,可竞争性拮抗白三烯与白三烯受体的结合,减少白三烯引起的白介素-4(interleukin-4,IL-4)、可溶性细胞间黏附因子-1(soluble intercellular adhesion molecule-1,sICAM-1)等炎症介质及细胞因子的释放,抑制气道平滑肌细胞增生及气道上皮纤维化,减少气道炎症和气道重塑[16]。本研究从拮抗组胺和白三烯的不同途径,使用孟鲁司特联合依巴斯汀治疗来抑制CVA的发病过程,结果显示,联合组治疗4周后,VAS和LCQ评分较治疗前均有所改善(P<0.05);到第8周时,患者评分改善更为明显(P<0.05)。值得注意的是,CET评分中联合组患者治疗前日间咳嗽评分较低,治疗后评分较治疗前未出现显著变化。而夜间咳嗽影响睡眠、剧烈咳嗽、咳嗽影响生活等评分则在治疗后第4周时较治疗前降低(P<0.05),治疗8周时降低更为明显(P<0.05)。推测这与CVA的发病机制有关:夜间腺体分泌旺盛,导致呼吸道黏膜充血、水肿、炎症因子渗出更加严重,从而加重夜间咳嗽而影响睡眠,大大降低了患者的生活质量。本研究结果表明,针对CVA的发病机制和临床特点,孟鲁司特联合依巴斯汀治疗从整体上改善了患者CET评分,对CVA具有较好的治疗效果。单用孟鲁司特在第4周时除CET评分中剧烈咳嗽评分较治疗前降低外(P<0.05),其他各项评分改善均不甚明显;到第8周时,夜间咳嗽影响睡眠、剧烈咳嗽、咳嗽影响生活等评分具有统计学差异(P<0.05)。综上所述,孟鲁司特联合依巴斯汀治疗相比单药治疗可更快地改善患者的临床症状,降低患者的咳嗽强度,提高患者的生活质量,值得临床推广使用。

