洋甘菊中2种咖啡酰基奎宁酸大孔树脂纯化工艺的优化
张柏生 ,热依木古丽·阿布都拉,信学雷,范芳芳 ,李 茜
(1. 新疆医科大学附属中医医院,新疆 乌鲁木齐 830000;2. 新疆中药炮制研究重点实验室,新疆 乌鲁木齐 830000;3. 中国科学院干旱区植物资源化学重点实验室,新疆特有药用资源利用省部共建国家重点实验室培育基地,中国科学院新疆理化技术研究所,新疆 乌鲁木齐 830011)
洋甘菊(Matricarla chamomillaL.)的药用历史悠久。新疆民族药中的多个处方含洋甘菊,《中华人民共和国卫生部药品质量标准》(维吾尔药分册)中就收录了3个包含洋甘菊的制剂。洋甘菊具有抗菌、抗炎、解痉、抗溃疡、增强免疫力、降低血脂、降低血糖等作用,主要用于治疗感冒、咳嗽,中风等症[1-2]。国内外的大量研究表明洋甘菊中含黄酮类、酚酸类、香豆素类、萜类、挥发油、多糖类及其他化学成分[3-6]。这些成分是洋甘菊药理作用的物质基础。其中咖啡酰基奎宁酸类已被证实具有抗炎、抗哮喘、抗肿瘤、抗类风湿性关节炎等作用[7-8]。在前期提取工艺研究基础上,本研究以3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸的含量为指标,考察具有不同物理结构和化学结构(不同极性)的10种树脂的静态吸附-解吸能力,筛选出纯化功能最好的树脂型号AB-8。进一步研究AB-8型大孔吸附树脂富集洋甘菊活性部位过程中吸附量、上样量、上样浓度、解吸参数等因素的影响,使工艺更加适应工业化生产。
1 仪器与材料
1.1 仪器
Waters e2695型超高效液相色谱系统,包括Waters 2489 UV/Visible Detector,Empower色谱工作站(美国Waters公司);UV-2550型紫外可见分光光度仪(日本岛津);R-210型旋转蒸发仪(瑞士Buchi);FDU-2100型冷冻干燥器(日本EYELA);DZF-6050B型真空干燥箱(上海齐欣);MOOEL ESJ-6020型电子分析天平(沈阳龙腾)。
1.2 试药
HPD-100,HPD-450,HPD-600,HPD-750型大孔吸附树脂(沧州宝恩);D101型大孔吸附树脂(上海摩速);D140,D4020,AB-8,NKA-9,X-5型大孔吸附树脂(南开大学化工厂);3, 4-二-O-咖啡酰基奎宁酸对照品,4, 5-二-O-咖啡酰基奎宁酸对照品(中国科学院新疆理化技术研究所自制);乙腈,甲醇为色谱纯(美国Fisher公司);超纯水。
1.3 药材
洋甘菊药材购自新疆伊犁地区昭苏县,为《国家药品标准维吾尔药分册》收载,经新疆维吾尔自治区中医医院李玲主任药师鉴定为菊科母菊属一年生或多年生草本植物,拉丁名Matricarla chamomillaL.[9]。
2 方法与结果
2.1 洋甘菊活性部位的制备
取洋甘菊全草4 kg,加70 %乙醇回流提取2次,每次2 h,料液比1:30,合并滤液,减压浓缩至无醇味,加水稀释至0.20 g/ml。
2.2 咖啡酰奎宁酸含量测定方法学研究
2.2.1 色谱条件 Thermo Golden Proshell C18(2.1 mm×100 mm,1.7 μm)色谱柱;以0.2 %甲酸-水溶液(A)和乙腈(B)为流动相,梯度洗脱,程序见表1。330 nm下采集指标成分的峰面积;柱温设置为35 ℃,流速设置为0.3 ml/min。
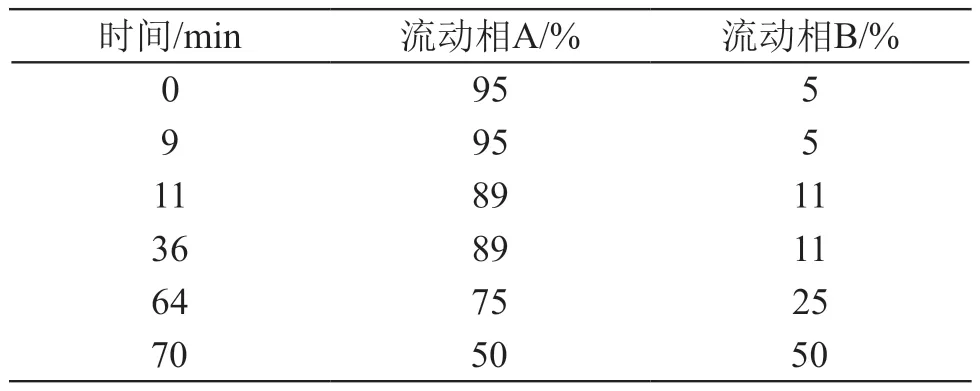
表1 梯度洗脱程序
2.2.2 对照品溶液的制备 精密称取3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸对照品适量,置于50 ml量瓶中,加60 %甲醇超声溶解,定容,摇匀,制成对照品溶液,每1 ml溶液中含3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸分别为43.3 μg/ml和33.5 μg/ml。
2.2.3 供试品溶液的制备 称取样品粉末(过40目筛)约1.0 g,精密称定,置具塞圆底烧瓶中,精密加入60 %乙醇100 ml,称定重量,浸泡30 min后加热回流40 min,取出,放冷,用60 %乙醇补足重量,摇匀,0.22 μm微孔滤膜滤过,取续滤液,即得。
2.2.4 测定法 按2.2.1项色谱条件,分别精密吸取对照品溶液与供试品溶液各5 μl,注入超高效液相色谱仪,测定峰面积,用外标一点法计算供试品中两种咖啡酰奎宁酸的含量。
2.2.5 线性关系考察 精密量取3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸对照品溶液1,2,3,4,5,6,7 ml于10 ml量瓶中,加60 %甲醇至刻度,摇匀,即得。按2.2.1项下条件测定,进样量10 μl。以对照品峰面积(Y)对其浓度(X,μg/ml)进行线性回归。分别得到3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸标准曲线,见表2。

表2 线性回归方程
2.2.6 精密度试验 精密量取3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸对照品溶液适量,置于10 ml量瓶中,加60 %甲醇稀释至刻度,摇匀,按2.2.1项色谱条件进样测定,连续进样6次,计算得3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸峰面积的RSD分别为0.048 %和0.088 %,表明方法精密度良好。
2.2.7 稳定性试验 精密称取供试品粉末适量,按2.2.3项下方法制备供试品溶液,按2.2.1项下色谱条件,在0,2,4,8,12,24 h进样测定,计算得3,5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸峰面积RSD值分别为1.23 %和0.68 %, 表明供试品溶液室温下24 h内稳定。
2.2.8 重复性试验 精密称取供试品粉末适量,按2.2.3项下方法制备供试品溶液,平行制备6份,按2.2.1项下色谱条件下测定,测得供试品中3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸的平均含量分别为0.173 %和0.12%,RSD值分别为0.44 %和0.46 %,表明方法的重复性良好。
2.2.9 加样回收试验 取同批次已知含量(3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸含量分别为0.173 %,0.12 %)的药材70 mg,精密称定,共6份,置10 ml量瓶中,按样品中咖啡酰奎宁酸含量1:1比例,精密加入两种咖啡酰奎宁酸对照品,按2.2.3项下方法制备供试品溶液,按2.2.1项下方法进样测定,3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸的平均加样回收率分别为96.90 %和99.89 %,RSD分别为0.83 %和2.26 %,结果见表3、表4。表明该分析方法准确。
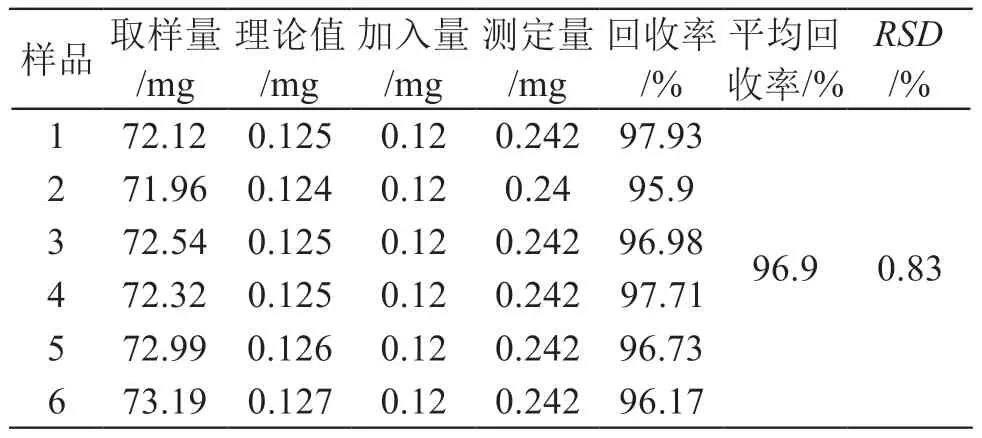
表3 3, 5-二-O-咖啡酰基奎宁酸加样回收试验结果
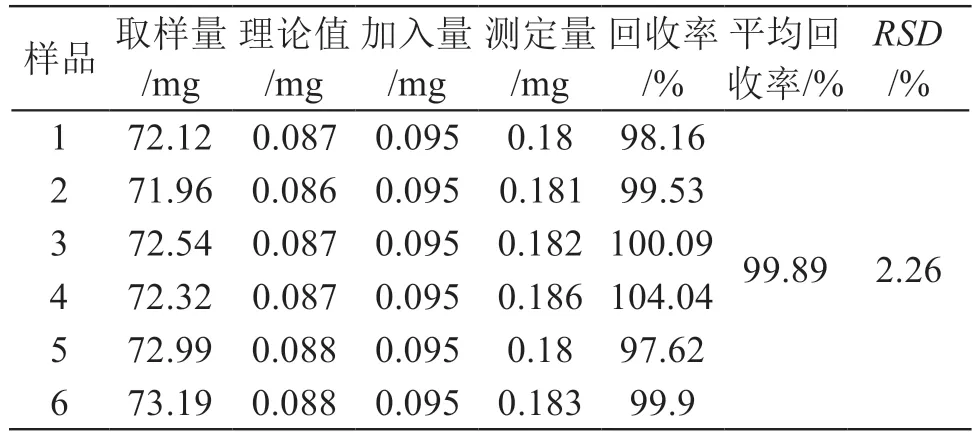
表4 4, 5-二-O-咖啡酰基奎宁酸加样回收试验结果
2.3 树脂处理
用95 %乙醇浸泡10种大孔树脂2~4 h,排出乙醇后,用蒸馏水反复冲洗至树脂在试管中不显浑浊为止,再用超纯水充分淋洗树脂至无醇味,抽滤。
2.4 大孔吸附树脂吸附率和解吸率的计算方法
按下式计算树脂吸附率和解吸率。
A0为原液中指标成分的峰面积;A流为流出液中指标成分的峰面积;A解为解吸液中指标成分的峰面积。
2.5 树脂的筛选
称取10种已处理好的大孔吸附树脂各2 g,加洋甘菊提取液30 ml,置于摇床,25 ℃、87 r/min振摇2 h,放置10 h,抽滤,测定指标成分的峰面积。滤去提取液后的大孔树脂水洗抽干,加70 %乙醇30 ml,25 ℃、87 r/min振摇2 h,放置2 h,进行静态解吸,测定解吸液指标成分的峰面积,计算吸附率和解吸率,结果见表5。
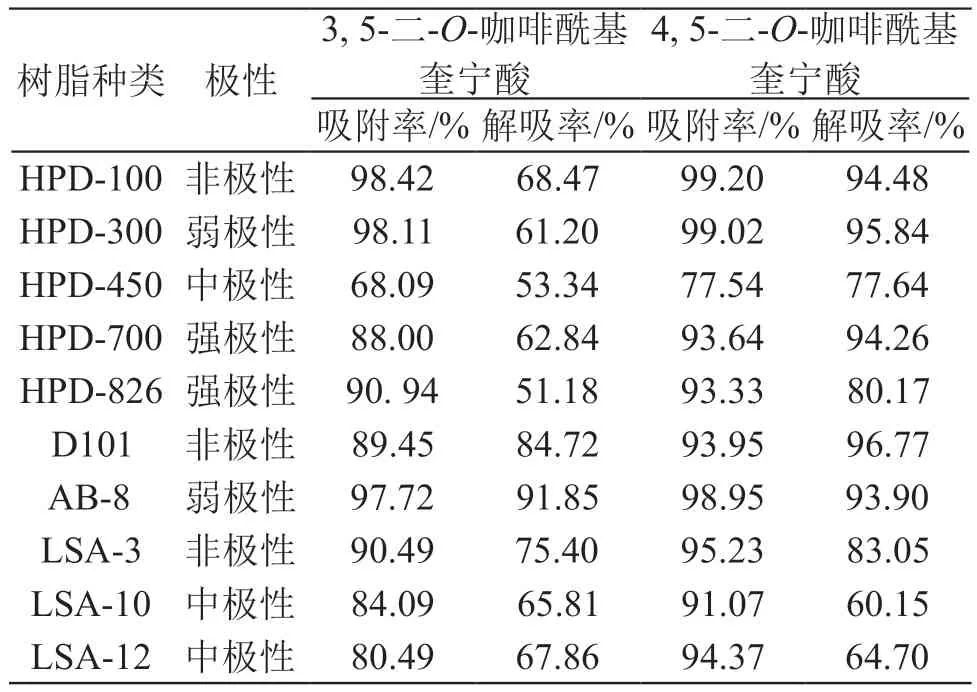
表5 10种大孔树脂静态吸附-解吸情况
由表3可见,综合考虑各树脂的吸附率和解吸率,选择AB-8进行后续试验。
2.6 上样浓度的考察
将AB-8树脂按2.3项下方法处理,装入树脂床体积(BV)为50 ml的树脂柱,分别加入生药浓度为0.20,0.16,0.12 g/ml的上样液10 BV,吸附流速为2 BV/h, 收集每1 BV(50 ml)流出液,离心,过滤,进行超高效液相色谱(UPLC)测定,计算吸附率,确定上样浓度。结果见表6。

表6 上样浓度考察结果
由表6可见, 随着上样浓度的降低,吸附量在持续增加。上样浓度为0.16,0.12 g/ml时,10倍上样体积时还未达到吸附饱和。上样液浓度为0.2 g/ml时,与其他上样浓度(0.16,0.12 g/ml)相比,上样时间短,且上样液总体积较小,考虑到实际生产需要,选择上样浓度为0.20 g/ml。
2.7 上样量的考察
根据上样浓度考察结果,选择吸附量为90 %以上的上样体积作为最终上样量。即,对于生药浓度为0.20 g/ml的提取液,最佳上样量为7 BV(见表6)。
2.8 吸附速率的考察
量取洋甘菊提取液(0.20 g/ml)400 ml,经50 ml(径高比为1:6)AB-8型大孔吸附树脂柱吸附,流速分别设计为 1,2,3 BV/h ,收集流出液,测定指标成分的峰面积,计算吸附率。结果见表7。

表7 洋甘菊提取液吸附速率的考察结果
由表7可见,当吸附速率成倍增加时,3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸的吸附量反而下降。当吸附速率为 3 BV/h时,吸附量显著减少。考虑到产业化生产需要,选择吸附速率为2 BV/h。
2.9 水冲洗用量的考察
将吸附饱和的树脂柱按5 BV/h流速,用纯净水洗脱树脂未吸附的溶液,收集流出液,测定目标成分的峰面积。结果表明,结合生产需要,用水量为1 BV最合适,见表8。
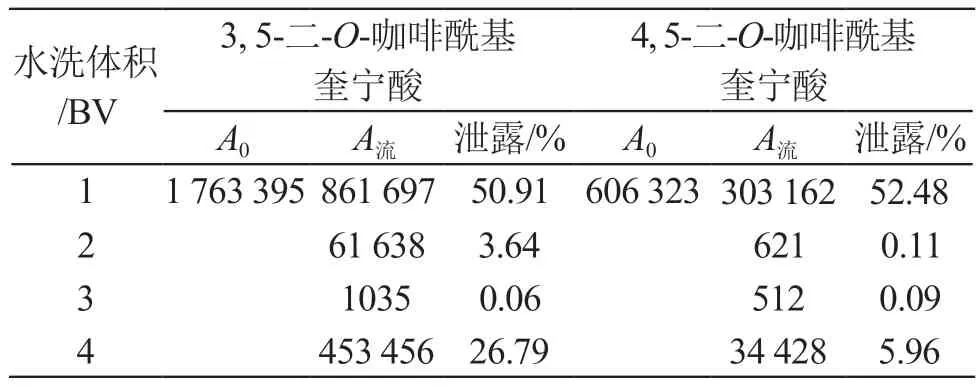
表8 水洗量的考察结果
2.10 洗脱溶剂的考察
分别量取洋甘菊提取液(生药浓度为0.2 g/ml)350 ml,以2 BV/h吸附速率,经50 ml(径高比1:6)AB-8树脂柱吸附,再以5 BV/h流速,用1 BV水洗后,分别用 50 %,70 %,95 %乙醇溶液洗脱目标化合物, 收集洗脱液4 BV,测定指标成分的峰面积,计算解吸率,结果见表9。
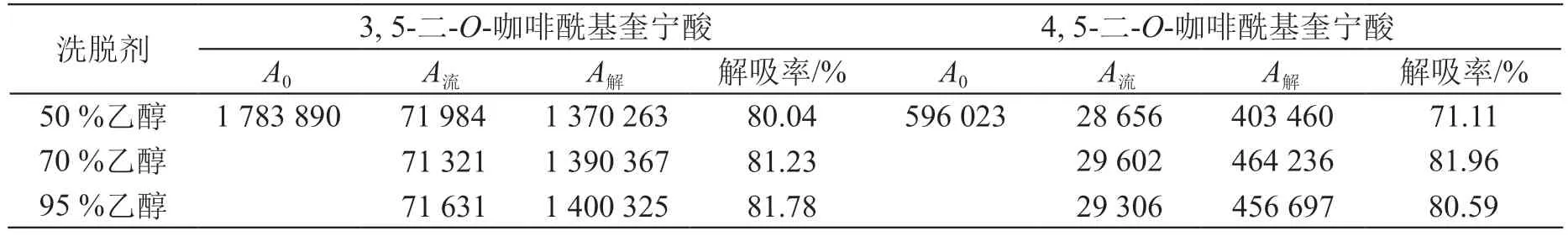
表9 洗脱溶剂的考察结果
由表9可见,几种溶剂对目标化合物的洗脱效果无明显差别。需进一步综合考察洗脱剂和用量。
2.11 洗脱溶剂和用量的考察
取洋甘菊提取液(生药浓度为0.2 g/ml)350 ml,以2 BV/h吸附速度,经50 ml(径高比1:6)AB-8树脂柱吸附,再以 5 BV/h流速,用1 BV水洗后,依次用50 %乙醇3 BV、70 %乙醇3 BV、95 %乙醇3 BV洗脱目标化合物,测定峰面积,计算解吸率。结果见表10。
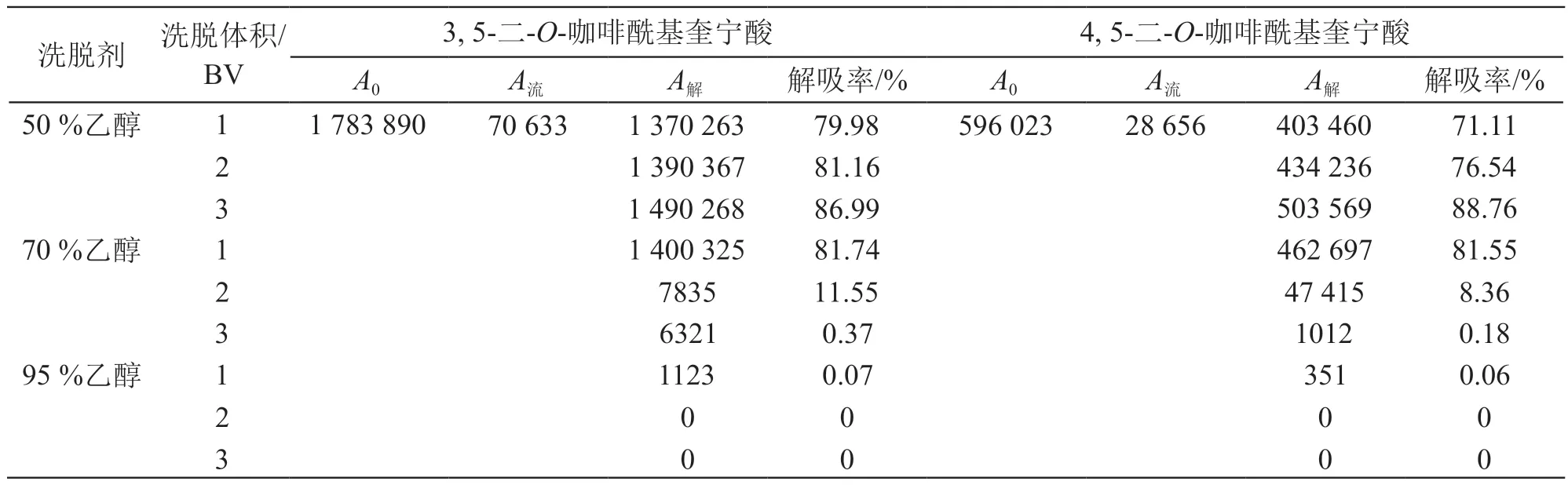
表10 洗脱溶剂的考察结果
由表10可见,用3 BV 50 %乙醇洗脱之后,1 BV 70 %乙醇基本上可把目标化合物洗脱出来。
3 讨论
本文以3, 5-二-O-咖啡酰基奎宁酸和4, 5-二-O-咖啡酰基奎宁酸两种特征成分为洋甘菊活性部位含量测定指标,对10种不同型号和功能的大孔吸附树脂进行静态吸附和解吸功能评价,选出适合洋甘菊活性部位富集功能的树脂型号AB-8。进一步对洋甘菊提取物纯化效率的影响因素(上样量、上样浓度、吸附速率、洗脱溶剂和用量等)进行考察。最终确定洋甘菊活性部位制备工艺:采用AB-8型大孔吸附树脂,药液浓度0.20 g/ml(相当于原生药),树脂柱径高比1:6,吸附速率2 BV/h,在此条件下,上柱量达到7 BV;吸附好的树脂先以5 BV/h流速的1 BV水洗净,再依次用3 BV 50 %乙醇和1 BV 70 %乙醇洗脱,合并洗脱液,浓缩,干燥。
咖啡酰基类衍生物种类繁多,具有抗炎、抗氧化、抗菌等广泛的生物活性,同时具有低毒、抗耐药、易制备等优点[10]。因此选择二咖啡酸奎宁酸化合物为提取工艺考察指标。
前期研究证明洋甘菊活性成分主要集中在中等偏大极性部位,同时考虑到大工业生产的需要,考虑直接使用50 %乙醇进行洗脱。50 %乙醇主要洗脱成分为酚酸类物质[11-13]。但活性部位的目标成分不止酚酸类物质,还有生物活性较好的黄酮类物质。同时有文献报道黄酮类物质一般需用70 %乙醇才能将其从大孔树脂上洗脱下来,最终确定采用3 BV 50 %乙醇洗脱后用1 BV 70 %乙醇继续洗脱,得目标活性部位[14-15]。该纯化工艺具有吸附量大、吸附速度快、易于解吸附、成分损失少、树脂使用周期长等优点,适合大规模工业化生产。

