2022年诺贝尔化学奖解读
——点击化学和生物正交化学
宋新强, 张 玉, 程永明,任雨轩,田梓煜,张 牧
(1. 信阳师范大学 a. 生命科学学院; b. 医学院; c. 校医院, 河南 信阳 464000;2. 河南中医药大学 第二临床医学院, 河南 郑州 450003; 3. 河南科技大学 动物科技学院, 河南 洛阳 471000)
0 引言
2022年,丹麦科学家莫滕·梅尔达尔(Morten MELDAL)、卡尔·巴里·夏普利斯(Barry SHARPLESS)和美国科学家卡罗琳·贝尔托齐(Carolyn BERTOZZI)被授予诺贝尔化学奖,表彰他们为生物正交化学(Bioorthogonal chemistry)和点击化学(Click chemistry)的发展所做出的贡献。其中, SHARPLESS和MELDAL 两位科学家开发了实现分子多样性与功能化的点击化学反应;而BERTOZZI则将点击化学的应用从化合物的合成推向生物学细胞的应用,即生物正交化学。点击化学和生物正交化学是化学学科发展的一次自我革新和进化[1]。
1 点击化学
自18世纪现代化学诞生以来,许多化学家都尝试通过人工合成来构建复杂的分子。然而,复杂的分子在合成过程中,通常产生很多不需要的产物,这些产物最终又需要很多步骤来纯化。在传统的有机合成过程中,科学家们更侧重于通过碳碳键(C-C)的构建,来合成复杂的分子结构,这一技术路线诞生了以WOODWARD和COREY 等为代表的全合成大师[2]。不过,这一技术路线的弊端也逐渐显现:如或操作难度高,或产率较低,或生产成本高。
2001年,SHARPLESS[3]提出了“点击化学”的概念,旨在避开前述传统技术路线,新开辟碳-杂原子键(C-X-C)这一方法作为有机合成基础,并借此来简单、高效地获得新的化学分子。2002年, SHARPLESS和MELDAL都发表了一价铜催化的叠氮化物-炔烃环加成反应(Copper-catalyzed azide-alkyne cycloaddition,CuAAC), 这种点击反应具有产率高、室温下可以进行、应用范围广、产物容易纯化的优点[4-5]。
“点击化学”的英文表述为Click chemistry,这句话来源于Click it or ticket it这句美国话。Click reaction意指化学反应像系安全带“喀哒”一声即可反应完成。“点击化学”意指小分子可以通过快速拼接即可以实现大分子的合成(见图1)。

注:A.点击反应卡通示意图,B.铜催化的叠氮化物-炔烃环加成反应示意图。图1 改变化学界的点击反应Fig. 1 The click reaction that changed chemistry
目前,常用的点击化学反应主要包括环加成反应(叠氮-炔-惠斯根1,3-二极环化反应和杂二阿尔德环化反应)、亲核开环反应(杂环化合物的亲核开环反应,如氮丙啶、环氧化物、氮丙啶离子、表磺离子和环状硫酸盐)、羰基缩合(非醛基羰基型反应,如形成腙、肟醚、酰胺和芳香杂环)和加成反应(对碳-碳多键的加成,主要是迈克尔加成,如胺-烯、硫醇-烯和硫醇-炔加成)4 类[6](见图2)。其中,铜催化的叠氮-炔基环加成反应(CuAAC) 是较为经典的点击化学反应,该反应是指由Cu+催化叠氮化合物与炔基化合物,生成三唑五元环化合物的共价加成反应。
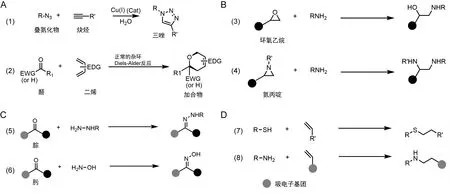
注:A. 环加成反应:(1)铜催化的叠氮-烯烃环化,(2)正常的杂环Diels-Alder反应;B. 亲核开环反应:(3)环氧化物亲核开环反应,(4)氮丙啶的亲核开环反应;C. 羰基缩合:(5)形成腙羰基缩合反应,(6)形成肟的羰基缩合反应;D. 加成反应:(7)硫醇-烯加成反应的代表例子,(8)迈克尔加成反应。图2 点击反应的类型Fig. 2 Types of click reactions
在这些早期应用实例中,CuAAC作为生物正交化学的能力得到了清楚的证明。然而,同时也暴露了局限性。第一个问题是CuAAC的效率与在有机溶液环境下相比大幅下降,这就需要加入三唑胺配体TBTA。TBTA在缓冲液或介质中均能提高反应速率和产率,但溶解性较差。第二个问题是副反应,在有机条件下,观察到副产物如二炔、双嘧唑和5-羟基三唑。当应用于缓冲条件时,表面标记和过量炔试剂的ABPP方法均出现了非特异性反应。末端炔在Cu(Ⅱ)催化下氧化偶联生成副产物二炔。第三个最严重的问题是铜离子引起的毒性,铜离子很容易被天然氨基酸残基螯合,破坏蛋白质的结构和功能,并能诱导活性氧(ROS)的形成,在细胞表面连接CuAAC的大肠杆菌细胞转移回正常培养基后无法分裂增殖,高于微摩尔浓度的铜离子会造成严重的细胞损伤甚至死亡;除了Cu(Ⅰ)的毒性外,高浓度含Cu(Ⅱ)的三唑产物可引起CPMV衣壳等生物分子复合物的分解和降解。考虑到这3个主要的局限性,虽然CuAAC在生物系统中证明了其正交性和有效性,但在细胞内的早期应用实例很少。为了进一步拓宽CuAAC作为生物正交化学在生命系统中的应用范围,必须克服这些障碍[7-8]。
2014年 SHARPLESS又与中国学者董佳家课题组[9]一起发现了第二个点击化学反应——六价硫氟交换反应(Sulfur fluoride exchange,SuFEx)。简言之,SuFEx 是磺酰氟(-SO2F)等与甲硅烷基醚反应生成磺酸酯等。硫氟键(S-F)具有很高的化学稳定性,又可通过亲核取代发生脱氟反应,硫氟交换反应利用硫氟(S-F)官能团,通过乙烯基磺酰氟(ESF)等含氟含硫砌块与胺等发生反应,得到硫氟交换底物,从而实现化学反应,被称为新一代点击化学,成为当前有机氟化学研究的新热点(见图3)。此反应受空气等环境因素影响,具有良好的热稳定性,解决了经典点击化学反应的许多问题。

图3 硫氟交换点击化学Fig. 3 Sulfur fluoride exchange (SuFEx) click chemistry
2 生物正交化学
自从SHARPLESS和MELDAL 等[4,10]报道了铜离子催化的叠氮和炔基快速反应的点击化学之后,很多科学家开始使用此方法对生物分子进行标记和应用。由于铜离子的细胞毒性,限制了其在生物活体内的应用。
BERTOZZI 也在研究这一难题,她在研究一类聚糖,聚糖通常位于细胞的表面,产于生物化学过程,唾液酸参与构成聚糖。BERTOZZI 通过实验设计,预先化学修饰唾液酸,修饰过的唾液酸又参与构成聚糖,通过培养基培养,使细胞表面聚集带有修饰的唾液酸参与的聚糖。例如,提前将荧光分子连接唾液酸,荧光就能在细胞中定位唾液酸参与构成的聚糖。但是,她必须保证,引入的化学基团不能与细胞中的其他物质发生反应,即不能干扰细胞的正常化学反应。为此,BERTOZZI 团队引入一个术语 “生物正交”反应( Bioorthogonal reaction)[11],即能够在生物体系中进行、且不会干扰天然生物化学过程。
2000 年,BERTOZZI[12-14]利用叠氮化物(Azide)成功将荧光分子与引入聚糖中的叠氮化物连接起来。叠氮基团不会影响细胞,甚至也可以被引入到活体生物中(见图4)。
后来她发现,将炔烃连接到环状化学结构上,即使没有铜催化,叠氮化物和炔烃也可以快速反应,因为张力产生的能量使反应平稳进行。2004 年,她发表 “环张力促进的叠氮-炔环加成”( Strain-promoted azide-alkyne cycloaddition,SPAAC) 反应的论文[15],指出该类生物正交化学在没有铜催化剂参与下,利用了环状炔烃本身的高环张力,进行的叠氮-炔环加成反应。在SPAAC 反应中,共轭和位阻效应对SPAAC 反应活性有影响(见图5)。环状炔烃的合理设计,是反应的关键,因为它为反应驱动提供动力来源,也是发展和完善SPAAC关键环节。 BERTOZZI 团队的工作使点击化学进入了无铜催化阶段,使点击化学在生物体内安全高效进行。这个里程碑式的研究,使科研人员可以用来探索生物分子在细胞定位和相互作用,以及探索疾病的发展规律与治疗方法。
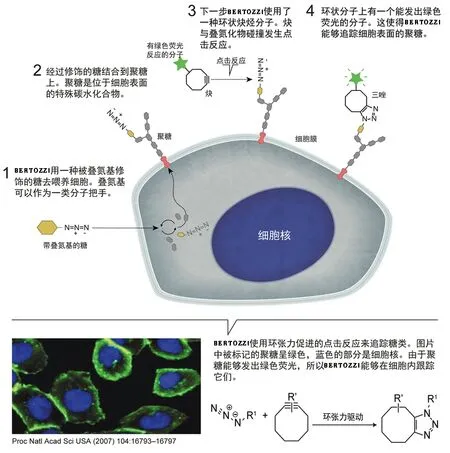
图5 SPAAC生物正交化学追踪聚糖的原理示意图Fig. 5 Schematic diagram of the principle of tracing glycans by SPAAC bioorthogonal chemistry
3 点击化学和生物正交化学在生命科学领域的应用
3.1 点击化学在蛋白质组学中的应用
近年来,点击化学结合蛋白质质谱法,在蛋白质组学研究方面得到广泛应用。通过在小分子活性基团加上接头,再连接炔基,这样就形成一个带有炔基的探针。报告基团通常与叠氮基相连,包括两类:一类荧光素、Cy3/Cy5 等的荧光基团,当被探针标记的蛋白质组在聚丙烯酰胺凝胶上分离时,被标记的蛋白就会显示出便于检测的特定荧光信号;另一类是生物素基团(Biotin), 被探针标记的蛋白既可以通过免疫印迹法检测,还可以被特异地富集并进行鉴定(见图6)。基于该方法,科学家们首先合成了一系列活性小分子探针,采用点击化学的方法在蛋白质组层面找到了其作用靶标,如穿心莲内酯、姜黄素、青蒿素等[16]。

图6 基于点击化学的天然产物靶点鉴定的方法Fig. 6 Identification of natural products targets based on click chemistry
3.2 生物正交化学在活体标记与示踪中的应用
在活细胞中,蛋白质、糖类和脂质都可以被生物正交基团修饰(见图7)。生物正交基团以化学合成的方法连接到代谢类似物上,在生成发育过程中,生物正交基团被引入到细胞,随后通过使用探针,即配对基团,可以标记和定位目标分子,进而确定细胞或目标分子的位置与功能。

图7 生物正交化学标记生物分子Fig. 7 Bioorthogonal labeling of biomolecules
点击化学被公认为可以提供多种多价新糖共轭物,包括糖聚合物、糖肽、糖二聚体、糖簇、糖胞、大分子和糖阵列。BERTOZZI 的团队[11,15]利用糖代谢工程与生物正交化学,分析了糖类在活斑马鱼的胚胎发育过程中的作用。在斑马鱼胚胎发育的不同阶段,加入环辛炔功能化的唾液酸,在生长的过程中,唾液酸被细胞摄取并被引入细胞表面的糖蛋白上,随后与配对基团修饰的荧光探针发生生物正交,通过此方法,可以直观地看见糖类在斑马鱼胚胎发展过程中定位表达和动力学过程(见图8)。
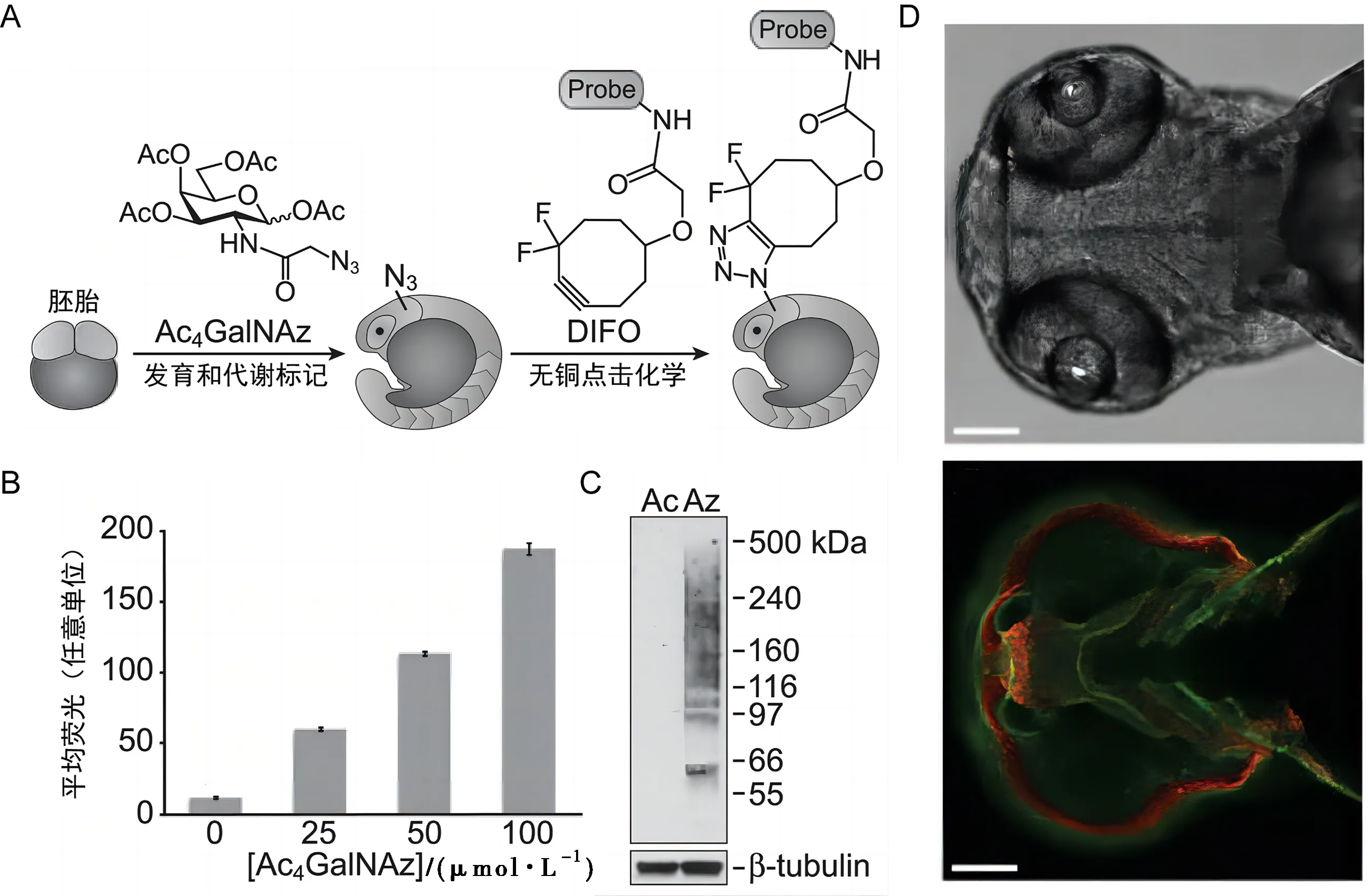
图8 叠氮修饰半乳糖在代谢过程中被加入到斑马鱼聚糖Fig. 8 Ac4GalNAz is metabolically incorporated into zebrafish glycans
3.3 生物正交化学在免疫治疗中的应用
免疫治疗通常需要治疗靶点,可以通过生物正交化学,将化学基团引入到肿瘤细胞或病原体的表面,形成人工靶点;也可以将此方法应用于药物的靶向传递,能提高药物的利用率和降低毒副作用。目前,生物正交化学反应已被应用于成像显示剂以及抗肿瘤药物的靶向运输,体内示踪和靶向肿瘤治疗效果明显(见图9)。

注:A.叠氮修饰的T细胞膜仿生纳米颗粒的制备;B.肿瘤的糖代谢标记与T细胞膜纳米药物的肿瘤光热靶向治疗。图9 细胞糖代谢生物正交标记用于抗肿瘤药物的靶向递送Fig. 9 Schematic illustration of tumor targeted drug delivery based on the metabolic glycoengineering and biorthogonal chemistry
免疫治疗也应用到了肿瘤治疗,生物正交化学反应也可用于免疫增强剂的传递,增加免疫治疗的效果。用叠氮化的糖预处理肿瘤细胞使其表达N3基团,将不同的免疫刺激物与二苯并环辛炔(Dibenzocyclooctyne,DBCO)基团进行偶联,随后通过生物正交化学反应将免疫增强剂连接到肿瘤细胞表面,成功引入的免疫增强剂可以激活动物的抗肿瘤能力,抑制肿瘤的发育[17](见图10)。

注:A.叠氮修饰的T细胞膜仿生纳米颗粒的制备;B.肿瘤的糖代谢标记与T细胞膜纳米药物的肿瘤光热靶向治疗。图10 基于点击化学的活体组织靶向技术Fig. 10 Active tissue targeting via anchored click chemistry
4 展望
生物正交化学已经成为一种可行的方法,可以在以前无法想象的情况下构建复杂的分子。生物正交化学性的影响已经广泛应用于蛋白质合成、药物发现、体内化学和聚合物科学。展望未来,生物正交化学将继续发展成为一种能够递送新药、创造新材料和回答现代分子生物学工具(如GFP和CRISPR-Cas9)或小分子配体无法解决的生物学问题的工具。尽管生物正交化学在开发和应用方面取得了巨大的进展,但仍有许多工作要做。
虽然所有的生物正交基团的分子量都比直接表达的蛋白质标签低得多,但生物正交连接物仍然代表着对所研究的生物系统的扰动,而且笨重的衍生物可能不被用于将标签合并到生物靶标的酶机制所接受。目前仍需要小型、安全、稳定、具有快速动力学的新试剂,对在活细胞和动物体内有效工作的试剂具有很高的价值。最初最小化生物正交基团的大小和改善生理特性的努力已经成功,但很少有双正交反应能产生天然的生物键,如酰胺。能够在生命系统中快速生成天然共价键的新型反应将是化学生物学的宝贵工具。“正交生物正交”反应的不断发展,使得在生命系统中同时使用多个生物正交化学物对成为可能,提供了对所研究的生物系统的另一种控制水平,具有十分重要的价值。
通过开发将生物正交化学与活体系统中的成像相结合的方法,生物成像已经取得了进展。荧光生物正交化学的发展以及体内放射化学的创新已经成为从细胞到整个动物水平的强大成像工具。需要通过改善非特异性相互作用或可能降低信噪比的副反应,继续推动检测的极限,从而实现成像的新领域,包括低丰度生物分子目标(如内源性蛋白质)的活体细胞成像,以及开发用于临床诊断、监测和分期人类疾病的体内方法。这些发展将受益于正在进行的合成复杂染料和荧光团的努力,这些染料和荧光团具有定制设计的物理特性,可以照亮复杂生物系统中的单个生物分子。
近年来,在生物大分子上定点附着生物正交手柄的化学技术取得了巨大的进步。安装独特的反应性多肽标签的重组方,法简化了在蛋白质目标上的位点特异性结合,具有广泛的底物范围。但这些方法确实存在转换不完全的问题,而且需要高浓度的试剂,这导致体内使用有限。遗传密码的扩展也有助于安装具有氨基酸精度的生物正交手柄,不需要额外的肽标签。然而,为了适应新的底物,往往需要对其进行广泛的重新设计。在一个具有广泛底物范围的活体系统中,将小分子定量、非侵入性、高纯度、位点特异性地附着在蛋白质上的简单方法是非常可取的,它代表了一种理想化的蛋白质共轭方法,值得努力。大量的努力都集中在蛋白质共轭策略上,将这些策略扩展到其他生物大分子和复杂代谢物在很大程度上仍尚待开发,这是新方法的关键领域。
炔烃与酰基叠氮化物在正常条件下的反应有时是非常复杂的。因此,除了已知的铜催化剂外,还需要发现更多合适的催化剂,譬如金属铱、钯、银等介导的生物正交偶联反应。通过使用简单的叠氮化物或烷基以外的支架,在温和条件下提供所需的区域选择性产品,还需要探索点击化学的多组分方法,因为这可以为该领域增加新的内容。光化学也为研究具有时空精度的细胞过程提供了一种强大的方法。展望未来,光导生物正交化学提供的控制可能使单个生物分子动态的实时成像成为可能,并为阐明生物分子在信号通路中的功能提供工具。基于组织渗透的近红外光的光诱导生物正交化学的发展,可提供在体内诱导快速反应的能力,为研究活体动物的发病机制提供新的精确水平。
从有机化学和生物学的交叉,生物正交化学已经成为构建生物分子和在其原生环境中研究它们的基本方法。随着不断增长的势头,生物正交化学正在推动生物学和生物医学的研究,并通过广泛的应用影响着各个学科的发展。

