盐湖水氯镁石合成三方硼镁石的结晶机理及动力学研究
彭姣玉,谈钰琴,杨克利,董亚萍,张 波,李 武
(1.中国科学院青海盐湖研究所,中国科学院盐湖资源综合高效利用重点实验室,青海西宁 810008;2.青海盐湖资源综合利用技术研究开发中心,青海西宁 810008;3.青海师范大学,青海西宁 810016;4.青海省盐湖资源化学重点实验室,青海西宁 810008)
硼是一种典型的非金属元素,外层电子构型为2s22p1,具有缺电子结构特性,可通过sp2或sp3杂化形式与氧原子配位,或者以这两种配位形式通过不同的结合而形成种类繁多、结构复杂的硼酸盐化合物。硼酸盐是一类重要的化工原料及光学材料,具有耐磨、高强、阻燃、耐热、防腐等优点及优良的非线性光学性质,广泛应用于冶金、机械、建材和医药等领域[1-4]。硼酸镁则是一类新型增强、减摩抗磨[5]、阻燃[6-8]和发光基质材料[9-10],可作为添加剂应用于高级玻璃[11]、陶瓷[12]和塑料高分子[13-14]等行业中,具有优越的增强改性效果。在无碱玻璃纤维生产中,硼酸镁是玻璃配料中引入氧化硼的主要原料之一,硼的加入可有效降低玻璃的熔化温度,调整玻璃液黏度和表面张力,防止断丝,提高纤维的成型;在陶瓷釉料中加入硼酸镁,可大幅降低釉的烧成温度和高温黏度,提高釉的坚固性和光泽度。
三方硼镁石(MgO·3B2O3·7.5H2O)是常见的六硼酸镁化合物,由于其硼含量较高,合成方法简单,是无碱玻璃纤维和陶瓷生产中一种重要的含硼原料,通常采用水热法合成三方硼镁石。由于硼酸镁溶液具有极大的过饱和性,硼酸根存在形式复杂,三方硼镁石的合成时间较长且纯度低[15-17],无法满足特种玻璃和陶瓷等行业的需求。因此,相关文献对快速合成三方硼镁石纯物质进行了报道。孟令宗等[18]研究了一种快速合成三方硼镁石的方法,活性MgO、H3BO3和H2O以一定的质量比于室温下搅拌反应3.5 h,静置澄清后过滤清液静置12 h,继续搅拌6 h 再静置,逐渐析出大量三方硼镁石沉淀,合成时间由文献[16-17]报道的30 d 缩短至24 h 之内。DERUN等[19]报道了0~70 ℃条件下,采用MgO、H3BO3和H2O 为原料合成三方硼镁石,结果表明,60 ℃时30 min即可结晶析出三方硼镁石。KIPCAKET 等[20]报道了60~100 ℃条件下MgCl2·6H2O、Na2B4O7·10H2O、H2O 及不同硼源(H3BO3和B2O3)组合对水硼镁石(MgO·B2O3·7H2O)和三方硼镁石(MgO·3B2O3·7.5H2O)物相的影响,得到了纯相水硼镁石,但三方硼镁石多为混合物;在此基础上,YILDIRIM 等[21]利用超声辅助条件研究了60~100 ℃快速合成水硼镁石和三方硼镁石,合成时间由6 h 缩短至20 min 以内,提高了反应速度,但是三方硼镁石仍为混合物。综上,较高温度(60 ℃)下,以活性MgO、H3BO3和H2O 为原料可实现三方硼镁石的快速合成,但活性MgO 由碱式碳酸镁高温分解制得,生产成本较高,不利于批量化生产。
中国盐湖含有大量镁资源。据统计,盐湖卤水钾肥生产过程中,每生产1 t氯化钾将产生质量分数30%以上的氯化镁老卤约40 m3,该老卤在盐田日晒中便可获得纯度高于95%的水氯镁石(MgCl2·6H2O)[22-23]。以MgCl2·6H2O为镁源代替活性MgO合成三方硼镁石,不仅可降低生产成本,同时还可实现盐湖水氯镁石的高值化利用,对盐湖资源的可持续开发具有重要的意义。然而,由于硼酸镁溶液结构的复杂性,以MgCl2·6H2O为镁源合成的三方硼镁石多数为混合物,其结晶相转化机理及动力学行为尚不清楚,不利于三方硼镁石纯物相的合成。基于此,本文以盐湖水氯镁石、五硼酸钠固体(或硼酸和氢氧化钠)为原料,开展了快速合成三方硼镁石的实验研究,并对其结晶机理和动力学过程进行了探究,可为后续三方硼镁石的规模化生产提供一定的借鉴作用。
1 实验部分
1.1 原料、试剂和仪器
原料和试剂:二次重结晶水氯镁石(MgCl2·6H2O,纯度≥99%);五硼酸钠固体(NaB5O8·5H2O,实验室制备);乙二胺四乙酸二钠(EDTA)、甘露醇、氢氧化钠、硼酸,均为分析纯;指示剂包括铬黑T、酚酞和甲基红;去离子水(18.25 MΩ/cm)。
仪器:DHG-9075-A 型鼓风干燥箱;UPT-l-40型超纯净水机;ZNCL-GS 型智能恒温磁力搅拌器;DXR 型激光拉曼光谱仪;X'Pert Pro 型X 射线衍射仪;SU8010型场发射扫描电子显微镜。
1.2 三方硼镁石(MgO·3B2O3·7.5H2O)的合成
称取一定量的五硼酸钠固体,加入一定体积水(总硼浓度约为1.3 mol/L),加热溶解,再分批加入一定质量的水氯镁石固体,溶解后放入一定温度条件下的恒温水浴磁力搅拌器中,反应一段时间结晶析出固体,固液分离,分别用去离子水、乙醇洗涤固相,于45 ℃烘干后进行物相表征。实验探究了温度(25、40、60 ℃)、原料(水氯镁石、氯化镁饱和老卤、五硼酸钠固体或溶液)、五硼酸钠与氯化镁物质的量比(1∶4、1∶8、1∶12、1∶16)对三方硼镁石产物的影响,确定最优合成条件。
1.3 三方硼镁石(MgO·3B2O3·7.5H2O)的结晶机理、动力学
根据实验优化条件,配制一定浓度的五硼酸钠和水氯镁石溶液,放入恒温搅拌器进行反应,每隔一段时间采用针头过滤器取液相分析测定硼含量,得到浓度-时间曲线,同时进行拉曼光谱液相结构检测。当溶液中硼浓度几乎保持不变时,进行固液分离,用水、乙醇洗涤固相,于45 ℃烘干后做物相鉴定;对拉曼、结晶数据进行处理,获得相转化机理和结晶动力学方程。
2 结果与讨论
2.1 温度、物质的量比、原料的影响
不同温度和物质的量比条件下合成产物的XRD 鉴定结果如表1 所示。由表1 可知,当五硼酸钠与氯化镁的物质的量比为1∶4和1∶8时,25~60 ℃合成的产物均为三方硼镁石的纯物相。随着镁含量的增加,溶液酸度增加,合成产物中伴随有六水氯化镁、硼酸及其他硼酸镁盐的结晶析出,不利于三方硼镁石的合成。实验发现,当温度为25 ℃、五硼酸钠与氯化镁物质的量比为1∶8时,2 h左右开始出现三方硼镁石沉淀,所需时间最短且产率高。由此可知,实验最优条件为温度为25 ℃或室温,五硼酸钠与氯化镁的物质的量比为1∶8。
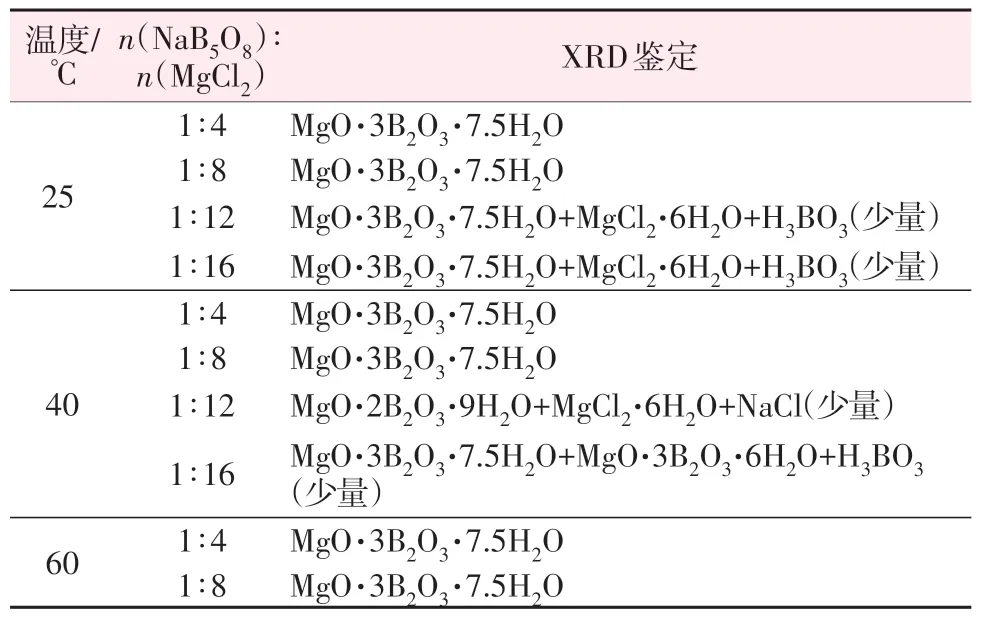
表1 不同温度、物质的量比对合成固相的影响Table 1 Effects of temperature and mole ratio on solid phase
表2为不同原料对合成三方硼镁石的影响。由表2 可知,采用水氯镁石或氯化镁饱和卤水均可合成三方硼镁石。氯化镁饱和卤水含有硼、镁等资源,可分别作为硼源、镁源合成三方硼镁石,有利于卤水硼、镁资源的综合利用。硼酸钠固体原料可由硼酸和氢氧化钠配制相应的溶液代替。因此,后续实验中可利用水氯镁石、硼酸和氢氧化钠为原料合成三方硼镁石,简化合成工艺、降低生产成本。
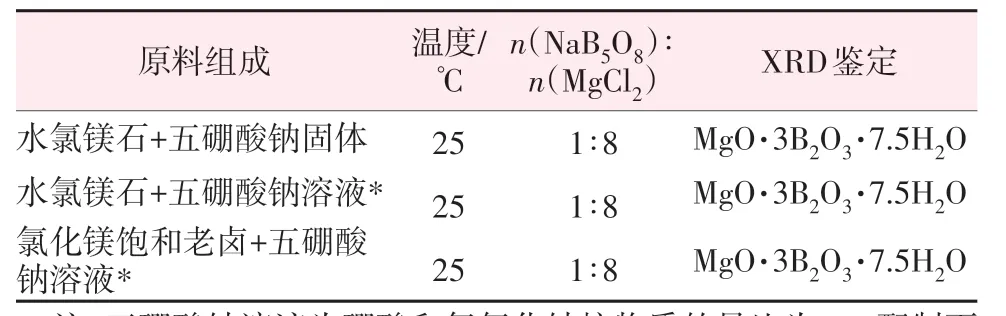
表2 不同原料对合成固相的影响Table 2 Effects of materials on solid phase
2.2 三方硼镁石(MgO·3B2O3·7.5H2O)的结构、形貌表征
图1 为25 ℃、五硼酸钠与氯化镁的物质的量比为1∶8 时合成三方硼镁石的XRD 和Raman 谱图。由图1a 可知,合成的三方硼镁石与标准纯物相(PDF#01-070-1902)吻合较好,各特征峰位置基本一致,无其他杂峰。根据文献报道,硼酸盐离子的拉曼特征峰在300~1 400 cm-1[24]。图1b 中1 257、1 076 cm-1处的弱峰分别对应于B—O 键三配位[B(3)—O]和B—O键四配位[B(4)—O]的反对称伸缩振动峰;952 cm-1处的强峰为B(3)—O 的对称伸缩振动峰;640 cm-1处的强峰可归属为三方硼镁石结构中的B6O7(OH)62-特征峰;409 cm-1处的强峰为B(4)—O的变形振动峰。综上可知,合成产物为三方硼镁石的纯物相。
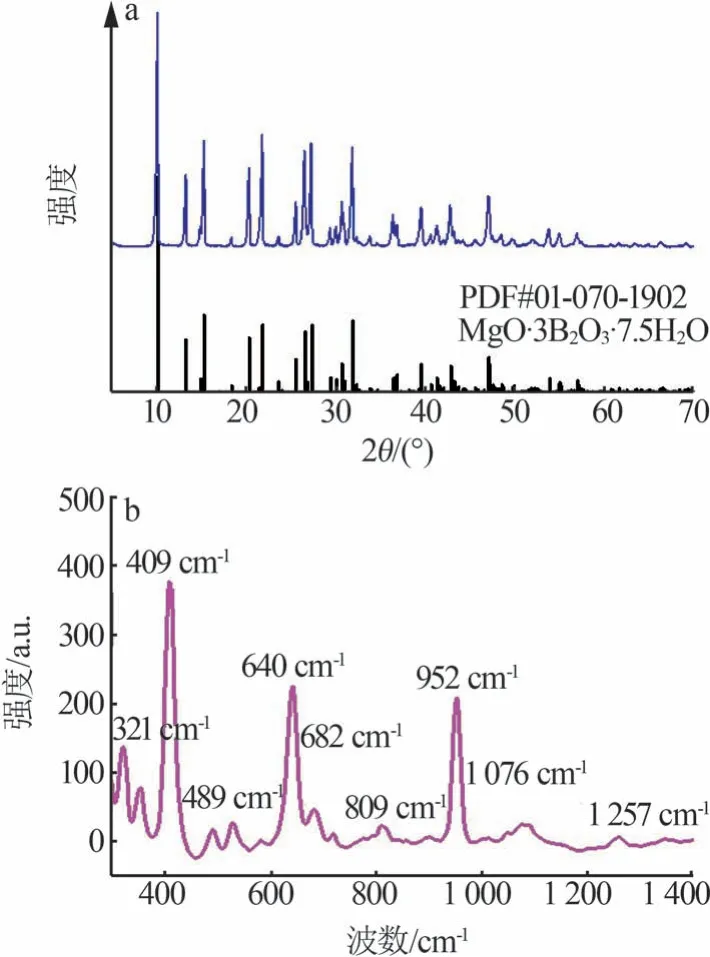
图1 25 ℃合成三方硼镁石化合物的XRD(a)和Raman(b)谱图Fig.1 XRD pattern(a)and Raman spectrum(b)of macallisterite compound synthesized at 25 ℃
对合成三方硼镁石的化学分析见表3,热分析如图2所示。由表3可知,实验分析值与理论值非常接近,表明化合物纯度较高。由图2可知,总的质量损失率为35.66%;175 ℃和200 ℃时的峰为吸热峰且失重明显,这主要是三方硼镁石失去结晶水和羟基官能团所导致;780 ℃时的峰为放热峰,是脱水后的非晶态物质转变为晶体的放热反应,与文献[16]结论相一致。
图3 为三方硼镁石的SEM 形貌图。由图3 可见,晶体表面有少量细晶,存在一定的团聚,形貌为六方片状细小晶体。

图3 三方硼镁石化合物的SEM形貌Fig.3 SEM images of macallisterite compound
2.3 三方硼镁石的结晶机理、动力学
对五硼酸钠溶液、五硼酸钠和水氯镁石混合溶液进行Raman 检测,结果如图4 所示。五硼酸钠溶液中(图4a),422、456 cm-1处为B3O(3OH)4-的弯曲振动峰,525 cm-1处为B5O(6OH)4-的特征峰,612 cm-1处归属为B3O(3OH)4-的特征峰,876 cm-1处则为B(OH)3的伸缩振动峰,由此表明五硼酸钠溶解在水中的五硼酸根[B5O(6OH)4-]可分解为B(OH)3和B3O(3OH)4-。加入水氯镁石后(图4b),除上述特征峰外,在632 cm-1处出现B6O(7OH)62-的特征峰,即为三方硼镁石化合物的阴离子结构。同时,根据溶液中B5O(6OH)4-和B3O(3O H)4-的峰强变化,可推断水氯镁石的加入可促进B3O(3OH)4-不断缩聚生成B6O(7OH)62-,从而促使B5O6(OH)4-水解生成B3O3(OH)4-,最终导致B5O(6OH)4-和B3O(3OH)4-的峰强降低,而B(OH)3分子的峰强增大。溶液中硼酸根间可能存在的化学反应如下:
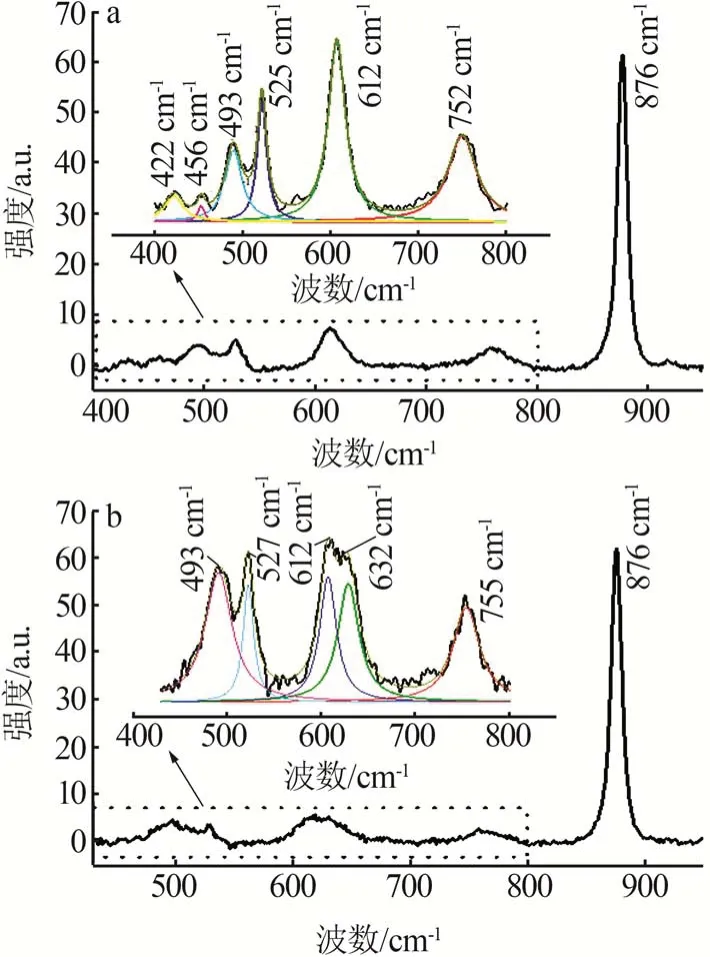
图4 五硼酸钠溶液(a)及五硼酸钠和水氯镁石溶液(b)的Raman光谱Fig.4 Raman spectra of sodium pentaborate solution(a)and its mixed solution with bischofite(b)
由反应式(1)~(5)可知,五硼酸钠和水氯镁石混合溶液中,由于B6O(7OH)62-的形成,促使反应(2)向右进行,水解生成的B(OH)3浓度比五硼酸钠纯溶液中的要高。
图5为三方硼镁石结晶过程不同时间液相中的w(B2O3)-t曲线。由图5 可知,结晶过程分为诱导期、结晶期和饱和平衡期3个阶段。诱导期较短,反应2 h 后开始结晶析盐,平衡过程比较长,60 h 后接近平衡。对不同时间取样液相进行Raman 光谱分析,结果如图6所示。
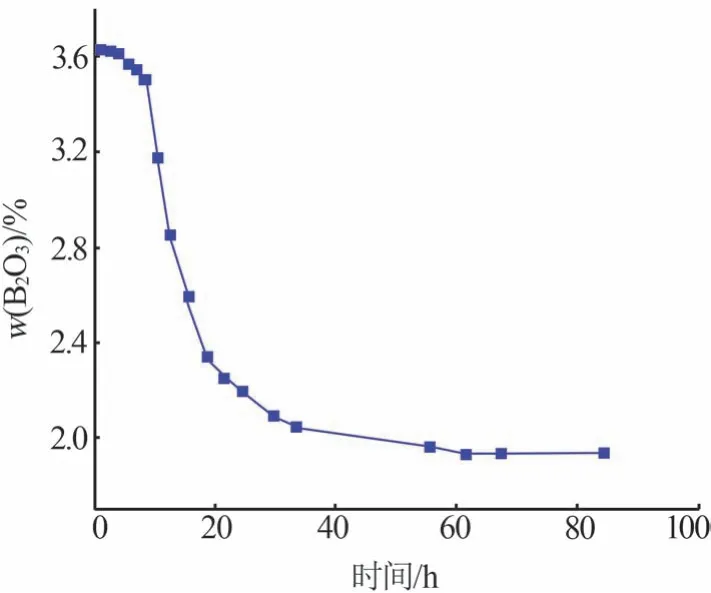
图5 25 ℃三方硼镁石结晶过程w(B2O3)-t曲线Fig.5 w(B2O3)-t curve of macallisterite compound at 25 °C
由图6可知,结晶反应前期(<12.5 h),876 cm-1处的B(OH)3谱峰强度随结晶时间的延长而增大,结晶后期(>12.5 h)峰强则逐渐降低,直至基本维持不变;而位于527 cm-1、614 cm-1和632 cm-1处的B5O6(OH)4-、B3O3(OH)4-和B6O7(OH)62-特征峰强度随结晶反应的进行不断降低。这主要是由于结晶反应前期,结晶过程经历了诱导期向结晶期的转变,此时过饱和溶液中的B6O7(OH)62-与镁离子结合生成三方硼镁石,B6O7(OH)62-浓度不断被消耗,导致过饱和度降低,B5O6(OH)4-进一步水解生成B(OH)3分子 和B3O3(OH)4-。其 中,B3O3(OH)4-缩聚生成B6O7(OH)62-,其浓度随结晶反应逐渐降低;而溶液中的B(OH)3分子在结晶反应初期的生成量大于消耗量,浓度会有所增加。随着三方硼镁石的大量析出,在进入平衡期之前,溶液中的B(OH)3可通过反应式(4)生成B3O3(OH)4-,共同参与补给三方硼镁石结晶消耗的B6O7(OH)62-,B(OH)3分子浓度逐渐下降,直至进入平衡期。但在整个结晶过程中,B(OH)3分子的Raman 峰强度变化并不是很明显,表明溶液中硼酸浓度变化不大。由此,可推断溶液中五硼酸钠与水氯镁石合成三方硼镁石的结晶机理为反应式(1)~(7):
根据晶体生长扩散理论,结晶过程经历了界面扩散和表面反应两个步骤,晶体生长主要受控于最慢的一步,通常受表面反应过程控制,分为多核控制晶体表面生长(MA 模型)、单核控制晶体表面生长(MB 模型)和线性控制晶体表面生长(MC 模型)[25-26]。化学反应动力学方程如下:
式中:令p=1、2、3 或4 中的任一整数,由此可得到MA-1(MB-1 或MC-1)、MA-2(MB-2 或MC-2)、MA-3(MB-3或MC-3)和MA-4(MB-4或MC-4)4种方程;k为结晶速率常数;t为反应时间;c为不同时刻的浓度;c∞为溶液中溶质的热力学平衡浓度。
采用MTALAB 软件,对w(B2O3)-t实验数据进行动力学拟合,以Runge-Kutta 为核心算法解微分方程,最后得到拟合优度R2和残差平方和S,计算公式如下:
式中,ycal为实验拟合值;yaver为实验平均值;yi为t时刻实验值。
对数据拟合计算发现,MB和MC模型对本实验结晶过程不具有相关性,MA模型拟合结果如表4所示,拟合曲线见图7。由表4可知,MA-1模型的拟合优度R2最大为0.986 7,残差平方和S数值最小,拟合优度较好,表明三方硼镁石的结晶机制为多核控制晶体表面生长,动力学方程如下:
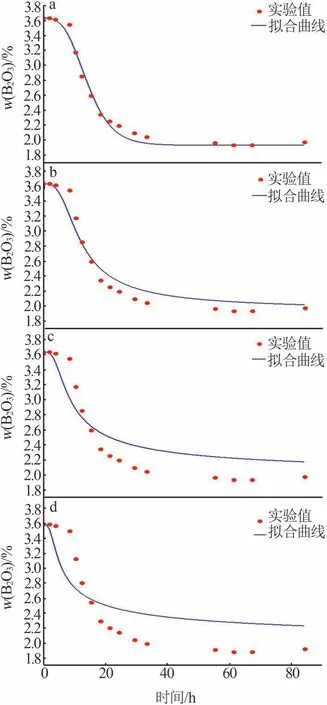
图7 25 ℃三方硼镁石结晶过程MA模型拟合曲线Fig.7 Fitting curves of MA model for macallisteritecompound at 25 ℃

表4 25 °C三方硼镁石结晶动力学MA模型拟合结果Table 4 Fitting results of MA model for macallisterite compound 25 ℃
3 结论
以盐湖副产水氯镁石、五硼酸钠溶液为原料,开展了水热法合成三方硼镁石的实验研究,通过对温度、原料及其物质的量比等条件的优化,制备得到了纯物质三方硼镁石;同时,采用动力学方法和Raman光谱技术对其结晶机理及动力学进行了研究。主要得出以下结论。
1)以氯化镁饱和老卤或水氯镁石为原料均可合成三方硼镁石。实验优化条件为:温度为25 ℃或室温;五硼酸钠和氯化镁物质的量比为1∶8。优化条件下所得三方硼镁石的合成时间短、纯度高。
2)液相Raman 光谱表明,五硼酸钠固体溶解在水中的B5O6(OH)4-可水解生成B(OH)3分子和B3O(3OH)4-;水氯镁石的加入促进B3O(3OH)4-缩聚反应生成B6O(7OH)62-,即三方硼镁石化合物的阴离子结构,对应溶液则为三方硼镁石的过饱和溶液,有利于三方硼镁石的结晶析出。
3)25 ℃时三方硼镁石的晶体生长机制为多核表面反应控制,结晶动力学方程为-dc/dt=0.141 3(c0-c)2/(3c-1.93),符合MA-1型。
本研究探究了一种快速合成三方硼镁石的方法,合成工艺简单、原料成本低,可为三方硼镁石的规模化生产提供借鉴,同时对盐湖镁资源的综合利用也具有一定的指导意义。

