布地格福联合乙酰半胱氨酸治疗老年慢性阻塞性肺疾病急性加重期临床观察*
代海云,耿立惠
(江苏省宿迁市第一人民医院,江苏 宿迁 223800)
慢性阻塞性肺疾病(COPD)为呼吸系统常见疾病,其发病机制与肺部接触雾霾、粉尘等有害物质密切相关[1]。发病特征为进行性发展的持续气流受限,病程多迁延,气候、过敏、感染等因素均可导致急性发作,临床主要表现为咳痰、咳嗽、肺功能下降等。当患者长期处于急性加重期时,会诱发心力衰竭,且由于老年患者多合并高血压等基础疾病,身体机能减退,代谢减慢,代偿能力低,耐受差,受外部刺激侵袭时难以维持自身稳态,进而导致COPD 急性加重期(AECOPD)临床症状加重,可引起呼吸衰竭、肺性脑病等严重并发症[2]。目前,临床通常采用药物治疗AECOPD。乙酰半胱氨酸作为临床常用祛痰药,具有较强的溶解黏液、抗炎、保护细胞、消除自由基等作用[3]。布地格福主要成分有布地奈德、格隆溴铵、富马酸福莫特罗,可快速缓解呼吸困难症状,纠正低氧状态,临床广泛用于肺部疾病的治疗,但较少用于老年AECOPD 患者[4]。为此,本研究中探讨了布地格福联合乙酰半胱氨酸治疗老年AECOPD 的临床疗效。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:符合《慢性阻塞性肺疾病急性加重(AECOPD)诊治中国专家共识(2014 年修订版)》中AECOPD 的诊断标准[5];年龄不低于60岁;认知、精神正常。本研究方案经医院医学伦理委员会审批(批件号为sq2019-01007),患者签署知情同意书。
排除标准:对本研究中所用药物过敏;存在肝、肾等脏器功能障碍;近期进行手术或有外伤;伴随支气管扩张、肺部肿瘤等其他肺部疾病;近期使用过激素。
病例选择与分组:选取我院2019年1月至2021年6月收治的老年AECOPD 患者100例,按随机数字表法分为观察组和对照组,各50 例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。详见表1。
1.2 方法
两组患者均予持续抗感染、吸氧(氧流量1~2 L/min)、排痰、水电解质平衡、抗炎等对症治疗。对照组患者予吸入用乙酰半胱氨酸溶液(ZAMBON S.p.A,进口药品注册证号国药准字HJ20150548,规格为每支0.3 g∶3 mL),经UN100 型雾化器(深圳尼罗河生物科技有限公司)雾化吸入,每天1~2 次,每次3 mL。观察组患者在对照组治疗基础上加用布地格福吸入气雾剂(AstraZeneca AB,进口药品注册证号H20190063,规格为每瓶120揿,每揿含布地奈德160 μg、格隆铵7.2 μg 和富马酸福莫特罗4.8 μg),每天2 次,每次2 吸。两组患者均连续治疗2周。
1.3 观察指标与疗效判定标准
观察指标:1)临床症状缓解时间。记录咳嗽、咳痰、喘息、肺部哮鸣音等临床症状缓解时间。2)肺功能。利用Master Screen 型肺功能仪(伟亚安医疗器械有限公司)检测患者治疗前后用力肺活量(FVC)、第1 秒用力呼气容积(FEV1)、最大自主通气量(MVV),计算FEV1/FVC。3)呼吸困难程度及生活质量评分。采用改良英国医学研究委员会呼吸困难量表(mMRC)[6]评估呼吸困难程度,按严重程度分为0,1,2,3,4 级,分别计0,1,2,3,4 分,分值越高,呼吸困难程度越重;采用圣乔治呼吸问卷(SGRQ)[7]评估生活质量,由肺部症状、活动能力、疾病影响组成,总分100 分,分值越高,生活质量越差。4)炎性因子水平。抽取患者治疗前后空腹静脉血各4 mL,离心(转速为3 000 r/ min)10 min,分离血清,利用贝克曼AU5800 型全自动生化分析仪(贝克曼库尔特商贸<中国>有限公司),以酶联免疫吸附试验测定肿瘤坏死因子-α(TNF-α)、白细胞介素6(IL-6)水平,以放射免疫法测定C 反应蛋白(CRP)水平。5)安全性。统计患者治疗期间恶心干呕、颜面潮红、头痛、血压升高、咽喉部不适等不良反应发生情况。
疗效判定[8]:显效,临床症状、体征改善至急性加重前状态;有效,临床症状、体征有所改善;无效,临床症状、体征均无改善。总有效=显效+有效。
1.4 统计学处理
采用SPSS 22.0 统计学软件分析。计量资料以±s表示,组间比较行独立样本t检验;计数资料以率(%)表示,行χ2检验。P<0.05为差异有统计学意义。
2 结果
结果见表2至表7。

表2 两组患者临床疗效比较[例(%),n=50]Tab.2 Comparison of clinical efficacy between the two groups[case(%),n = 50]
表3 两组患者临床症状缓解时间比较(±s,d,n=50)Tab.3 Comparison of relief time of clinical symptoms between the two groups(±s,d,n = 50)

表3 两组患者临床症状缓解时间比较(±s,d,n=50)Tab.3 Comparison of relief time of clinical symptoms between the two groups(±s,d,n = 50)
肺部哮鸣音7.12±2.02 8.87±2.31 4.033 0.000组别观察组对照组t值P值咳嗽4.86±1.15 6.78±2.01 5.863 0.000咳痰4.42±1.21 6.29±1.85 5.982 0.000喘息4.29±1.32 5.81±1.86 4.712 0.000
表4 两组患者肺功能指标比较(±s,n=50)Tab.4 Comparison of lung function indicators between the two groups(±s,n = 50)

表4 两组患者肺功能指标比较(±s,n=50)Tab.4 Comparison of lung function indicators between the two groups(±s,n = 50)
注:与本组治疗前比较,aP < 0.05。表5和表6同。Note:Compared with those before treatment,aP < 0.05(for Tab.4 - 6).
组别观察组对照组t值P值FVC(L)治疗前2.56±0.36 2.57±0.32 0.147 0.884治疗后78.46±11.65a 70.12±11.24a 3.643 0.000治疗后3.23±0.56a 2.98±0.12a 4.198 0.000 FEV1/FVC(%)治疗前51.23±5.16 51.26±5.12 0.029 0.977治疗后67.45±7.45a 59.34±7.26a 5.513 0.000 FEV1(L/min)治疗前1.32±0.35 1.33±0.34 0.145 0.885治疗后3.12±0.26a 2.56±0.16a 12.971 0.000 MVV(L/min)治疗前63.74±12.56 63.71±12.64 0.012 0.991
表5 两组患者呼吸困难程度和生活质量评分比较(±s,分,n=50)Tab.5 Comparison of mMRC and SGRQ scores between the two groups(±s,point,n = 50)

表5 两组患者呼吸困难程度和生活质量评分比较(±s,分,n=50)Tab.5 Comparison of mMRC and SGRQ scores between the two groups(±s,point,n = 50)
组别观察组对照组t值P值mMRC评分治疗前3.12±0.56 3.11±0.57 0.088 0.930治疗后33.13±5.02a 39.46±6.13a 5.649 0.000治疗后0.58±0.12a 0.89±0.21a 9.063 0.000 SGRQ评分治疗前64.21±18.32 63.23±18.31 0.268 0.790
表6 两组患者炎性因子水平比较(±s,n=50)Tab.6 Comparison of inflammatory factor levels between the two groups(±s,n = 50)

表6 两组患者炎性因子水平比较(±s,n=50)Tab.6 Comparison of inflammatory factor levels between the two groups(±s,n = 50)
组别TNF-α(ng/mL)治疗前2.56±0.59 2.57±0.56 0.087 0.931治疗后5.46±1.21a 8.45±1.23a 12.254 0.000 IL-6(ng/L)治疗前0.89±0.26 0.88±0.24 0.800 0.842治疗后1.23±0.24a 1.81±0.54a 6.940 0.000观察组对照组t值P值治疗后0.41±0.05a 0.65±0.11a 14.044 0.000 CRP(mg/L)治疗前11.46±2.36 11.48±2.34 0.043 0.966
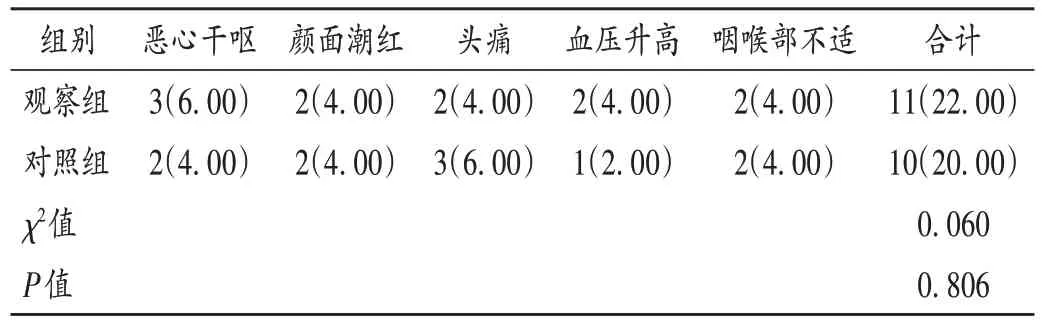
表7 两组患者不良反应发生情况比较[例(%),n=50]Tab.7 Comparison of the incidence of adverse reactions between the two groups[case(%),n = 50]
3 讨论
AECOPD 临床主要表现为咳嗽、咳痰、呼吸困难加重,合并感染时可导致发热,进而引起炎性因子水平升高,使肺功下降。老年患者由于身体机能、肺功能、免疫力及耐受力下降,患AECOPD 的风险更高,且极易并发心肌缺血、肺部感染等疾病[9]。乙酰半胱氨酸具有较强的黏液溶解作用,可降低痰液的黏滞性,使痰液易咳出[10]。布地格福作为一种三联吸入创新药物,具有起效快、安全性高等优点[11]。故本研究中观察布地格福联合乙酰半胱氨酸治疗老年AECOPD的临床疗效。
雾化吸入乙酰半胱氨酸可稀释痰液并促进排出;抑制氧化应激反应,减少肺功能损伤,进而防止气道上皮重构与增厚;显著降低患者气道内细菌的黏附力,阻碍细菌生长与繁殖,进而增强抗感染能力[12]。布地格福吸入气雾剂含布地奈德、格隆溴铵、富马酸福莫特罗。其中,布地奈德属糖皮质激素,主要通过抑制炎性致敏介质、炎性因子等物质生成来缓解炎性反应;格隆溴铵具备高耐受、长效等优点,可较好地抑制支气管平滑肌扩张;富马酸福莫特罗为长效β2受体激动剂,可较好地舒张支气管平滑肌,解除气道痉挛症状,进而改善临床症状[13]。三药联用,能更好地改善患者的临床症状和肺功能,进一步降低发病风险,从而改善生活质量。本研究结果显示,与对照组比较,观察组临床总有效率显著升高,临床症状缓解时间显著缩短,肺功能指标显著升高,mMRC 和SGRQ 评分均显著降低,表明布地格福联合乙酰半胱氨酸治疗老年AECOPD 的临床疗效良好,可有效改善患者的临床症状、肺功能和呼吸困难程度,提高生活质量,与文献[14-15]的研究结论相符。
既往研究证实,老年人呼吸道疾病及慢性炎性反应持续时间较长,可加重肺部损伤,阻碍肺组织修复和再生[16]。炎性反应为老年AECOPD 患者发病的重要因素,通常是由于患者体内炎性因子释放大量炎性介质,并诱导气道细胞化生与黏液高分泌,进而引发肺功能损伤。分析原因,病毒入侵机体时,CRP 水平会显著升高,常用于COPD 的判定。本研究结果显示,与对照组比较,观察组患者治疗后的TNF - α,IL - 6,CRP 水平均显著降低,表明布地格福联合乙酰半胱氨酸治疗老年AECOPD可减轻炎性反应。乙酰半胱氨酸溶液通过抑制患者体内核因子κB和TNF-α活性,进而减少IL-6和CRP 的生成,最终减轻炎性反应;布地格福吸入气雾剂中的格隆溴铵作为一种抗胆碱能药物,主要通过与AECOPD患者支气管胆碱能受体相结合,并抑制乙酰胆碱合成与释放,进而促使支气管扩张,减轻气道炎性反应。两组患者不良反应发生率相当,表明药物联用方案安全性良好,与文献[17-18]的研究结论相符。
综上所述,布地格福联合乙酰半胱氨酸治疗老年AECOPD 的临床疗效良好,可有效改善患者的临床症状、体征及肺功能,提高生活质量,降低炎性因子水平,且安全性良好。

