无特殊前处理条件下清洁水中低浓度氨氮测定方法的比对
周敬峰,朱红霞,王 婷,姜 丽,金淑聪,胡佳欣
1.广西壮族自治区海洋环境监测中心站,北部湾海洋生态环境广西野外科学观测研究站,广西 北海 536000
2.中国环境监测总站,国家环境保护环境监测质量控制重点实验室,北京 100012
3.宝鸡市环境监测中心站,陕西 宝鸡 721000
4.福建省环境监测中心站,福建 福州 350000
5.新疆维吾尔自治区昌吉生态环境监测站,新疆 昌吉 831100
氨氮是控制水体含氮有机物污染和保护水生生态系统的重要指标[1],目前环境水质氨氮减排工作持续开展,部分水体中氨氮质量浓度逐渐降低,尤其是水质较好的饮用水源水等清洁水样,实际监测时常出现方法间不可比的现象,现行分析方法哪些更适用于低浓度氨氮的测定成为广大环境监测工作者关心的问题。
水中氨氮的测定方法主要有纳氏试剂分光光度法[2-3]、水杨酸分光光度法、流动注射或连续流动-水杨酸分光光度法、气相分子吸收法、离子色谱法和蒸馏-中和滴定法等[4]。 纳氏试剂分光光度法操作便捷,分析时间短,但易受pH、色度、浊度、硬度、氯离子和硫化物等干扰,标准方法[2]中提到对于清洁水可以直接取样后测定,无需特殊的前处理,但缺少对清洁水样的明确定义,直接取样常出现假阳性的结果;水杨酸分光光度法灵敏度较高,但所用试剂保存时间短、稳定性差,且方法显色时间长,同时在此原理上开发出来的流动注射法和连续流动法在管路更换、分析操作及环境条件上都有较高要求;气相分子吸收法操作简便、测试快捷、抗干扰能力强、技术先进[5],其主要的干扰为硫化物等还原性物质;离子色谱法测定氨氮所用流动相为酸性,该条件下氨氮以铵根形式存在[6],灵敏度高,主要干扰为保留时间接近的钠离子;蒸馏-中和滴定法灵敏度低,主要用于生活污水和工业污水中较高浓度氨氮样品的测定。
故本文选取广泛应用的纳氏试剂分光光度法、气相分子吸收法和离子色谱法3 种方法,选用地表水质量标准氨氮I 类水限值0.15 mg/L 附近浓度的清洁水样,在无特殊前处理的条件下,开展低浓度氨氮测定的比对实验,探寻有各类干扰存在时测定低浓度氨氮准确且便捷的定量方法。
1 实验部分
1.1 主要仪器和试剂
仪器:紫外可见分光光度计(岛津UV-2550),气相分子吸收光谱仪(北裕GMA390),离子色谱仪(Thermo ICS-5000+)。
试剂:四水合酒石酸钾钠(AR,国药),纳氏试剂(坛墨质检),盐酸(GR,日本岸田),无水乙醇(95%,国药),氢氧化钠(AR,沪试),溴酸钾(99.5%,百灵威),溴化钾(AR,国药),甲烷磺酸(99%,百灵威),测试用水为无氨水,玻璃器皿用稀盐酸浸泡洗净。
500 mg/L 氨氮标准溶液(批号GSB 07-3164-2014 102218),500 度色度标准溶液(批号GSB 07-1966-2005 104311),100 mg/L 硫化物标准溶液(批号GSB 07-2733-2005 104419),1 000 mg/L钙离子标准溶液(批号215035120),100 mg/L 镁离子标准溶液(批号214025129-01),100 mg/L 钠离子标准溶液(批号214055121),均购于生态环境部环境发展中心环境标准样品研究所。
1.2 实验条件
紫外可见分光光度计:波长420 nm,石英比色皿2 cm。
气相分子吸收光谱仪:输入氮气压力为0.30 MPa,灯电流1 A,工作波长213.9 nm,泵速(样品50 r/m in,试剂40 r/m in,氧化剂30 r/min),峰高定量。
离子色谱仪:IonPac CS12 阳离子分离柱(4 mm×250 mm),IonPac CG12 阳离子保护柱(4 mm×50 mm),CERS-500(4 mm)阳离子抑制器,电导检测器,柱温30 ℃,淋洗液为20 mmol/L甲磺酸,流速1.0 m L/min,抑制电流59 mA,峰面积定量。
实验过程中样品测定均做平行双样,最终结果取均值。
2 结果与讨论
2.1 无前处理条件下方法检出限的差异
纳氏试剂分光光度法测定水中氨氮时,去除干扰的主要方式有酸性条件下加热、预蒸馏和絮凝沉淀等。 其中,酸性条件下煮沸加热和预蒸馏的方法去干扰能力最强,基本可消除色度、浊度、硬度、氯离子和硫化物等物质的影响,但这2 种方法对实验室环境条件、设备的精度和气密性以及分析人员的操作要求都较高,特别是低浓度氨氮样品分析对硬件要求尤为苛刻;絮凝沉淀可消除部分色度、浊度和硬度的干扰,但需要严格控制水样的酸碱度,在低浓度氨氮测定时尤其要注意并调整处理后水样的pH。 故首先参照《环境监测分析方法标准制订技术导则》[7]附录A 测试并计算未经前处理条件下3 种方法对水中氨氮的检出限。
由表1 可以看出,在3 种方法中纳氏试剂分光光度法样品取用量最大, 检出限最高(0.02 mg/L);气相分子吸收法取样量介于两者之间,检出限(0.006 mg/L)略高于离子色谱法;离子色谱法相较其他2 种方法,取样量最小,检出限最低(25 μL 时为0.005 mg/L,50 μL 时为0.003 mg/L)。 在《地下水质量标准》[8]中,Ⅰ类地下水对氨氮的质量浓度限值要求为0.02 mg/L,故从方法检出限分析,当清洁水中氨氮质量浓度低于0.02 mg/L 时,离子色谱法是最佳选择。

表1 3 种方法检出限Table 1 Detection limit of three methods
2.2 pH 影响
魏小玲等[9-10]研究了水样预处理的碱度控制对纳氏试剂比色分析的影响,发现pH 的影响较大;韩润平等[11]研究发现,显色后样品溶液的pH>12.59 时分析结果准确。 pH 过低,直接分析时会消耗纳氏试剂中的OH-,导致反应不完全;pH 过高则会反应生成沉淀(NH2Hg2IO),导致结果偏高[12]。 当采集的氨氮样品无法现场分析时,需要及时固定(调节pH<2),鉴于水样间pH 的差异,现场采样人员也不易精准添加固定剂H2SO4,常出现固定后样品pH 远小于2 的情况,导致实验室分析时回调困难[13]。
为研究pH 对分析的影响,以直接测定方式比较了3 种方法在pH 略低于2(pH=1.90)和远小于2(pH=1.10)2 种酸性条件下对不同质量浓度氨氮标准溶液的测定结果。 从图1 可知,在2种酸性条件下,气相分子吸收法和离子色谱法的回收率为88.6%~111%,而纳氏试剂分光光度法的回收率差异较大。 当样品pH=1.10 时,纳氏试剂分光光度法的氨氮测试结果偏差严重,低浓度氨氮标准溶液(0.10 mg/L 和0.20 mg/L)的回收率仅为2.7%~7.5%,即使达到该方法测定上限(2.0 mg/L),回收率也仅为83.6%,经核查此时显色溶液pH 为11.77,低于12.59;当样品pH 为1.90 时, 纳氏试剂分光光度法的回收率在101%~103%正常范围,此时显色溶液的pH 为12.82,满足pH>12.59 的显色条件。

图1 pH 对3 种方法测定结果的影响Fig.1 Effect of pH on the determination results of three methods
可见,在直接进样条件下,过低的pH 对纳氏试剂分光光度法影响较大,对于此类样品,建议选择其他2 种方法。
2.3 色度影响
水样颜色对分光光度法测定氨氮有一定影响[14]。 通过絮凝沉淀和预蒸馏等水样前处理可有效去除色度影响,但实验步骤和工作量会随之增加,操作过程中也极易造成低浓度氨氮的损失,王屹[15]研究发现,蒸馏法处理低浓度氨氮样品时准确度较难控制,常导致结果偏低。
为避免前处理带来的影响,比较了直接取样方式下氨氮标准溶液(0.15 mg/L)在不同色度条件下的测定结果。 如图2 所示,纳氏试剂分光光度法受色度影响,测定回收率随色度增加逐渐上升,当样品色度大于10 度时,回收率迅速上升,最高达173%。 其他2 种方法测定氨氮的回收率随色度变化波动较小,在87.6% ~104%正常范围内,故当水样色度高于10 度时用这2 种方法效果更佳。

图2 色度对3 种方法测定结果的影响Fig.2 Effect of chromaticity on the determination results of three methods
2.4 浊度影响
水样本底有浊度时,悬浮物会干扰光的散射,造成吸光度增大[16]。 为避免该影响,使用分光光度法测定氨氮时需进行浊度补偿或絮凝蒸馏。
为提高实验效率,比较了直接测定方式下氨氮标准溶液(0.15 mg/L)在不同浊度影响时的测定结果。 从表2 可知,浊度对分光光度法测定氨氮的影响很大,回收率随浊度增加而迅速增大,在浊度仅为6.5 NTU 时,测定回收率便高达157%。气相分子吸收光谱仪管路较粗,直接测定有浊度水样时回收率为92.7%~102%,离子色谱法进样前水样需经0.45 μm 滤膜过滤,回收率为102%~114%。 因此,对于有浊度的水样,选用纳氏试剂分光光度法时必须进行前处理,也可过滤后用离子色谱法测定或气相分子吸收法直接测定。
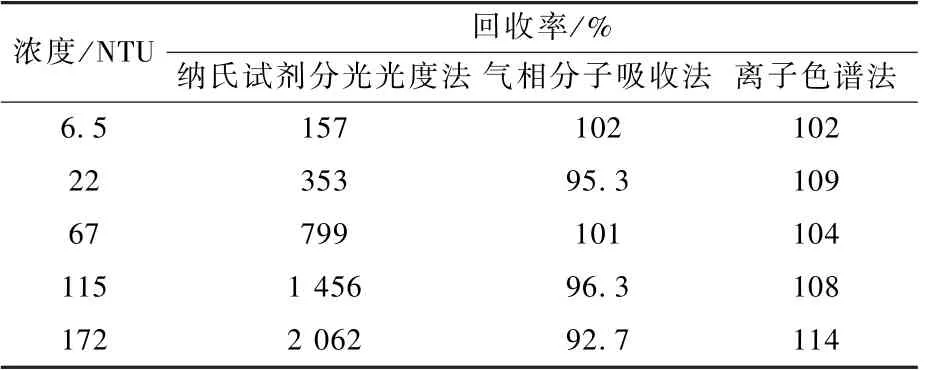
表2 浊度对3 种方法测定结果的影响Table 2 Effect of turbidity on the determination results of three methods
2.5 钙镁离子的影响
纳氏试剂分光光度法测定氨氮时,通过添加酒石酸钾钠可以掩蔽钙镁离子,但肖翔群等[17]研究发现,酒石酸钾钠的品质对钙镁离子的掩蔽效果差异很大。 原晖[18]发现当钙镁离子质量浓度过高,超过所加入酒石酸钾钠的络合能力时,会导致大量生成的络合物因饱和而析出,且在碱性条件下也容易生成氢氧化钙和氢氧化镁沉淀,进而影响吸光度。
为明确钙镁离子对3 种方法的干扰情况,研究了纳氏试剂分光光度法(不加掩蔽剂时)与其他2 种方法在不同质量浓度钙镁离子影响时氨氮标准溶液(0.15 mg/L)的测定结果。 如图3 所示,过高质量浓度的2 种离子对纳氏试剂分光光度法的测定均有影响,随钙离子质量浓度增加,光度法的回收率呈线性上升, 当钙离子大于40 mg/L 时,回收率高达137%;当镁离子质量浓度超过1.6 mg/L 时对测定结果影响更为明显,回收率随镁离子质量浓度增大而迅速上升,最高达182%。 气相分子吸收法和离子色谱法在不同质量浓度的钙离子存在时氨氮的回收率为89.2%~110%,不同质量浓度的镁离子存在时回收率为86.7%~103%。

图3 钙镁离子对3 种方法测定结果的影响Fig.3 Effect of calcium and magnesium ions on the determination results of three methods
可见,掩蔽剂在纳氏试剂分光光度法测定氨氮时有至关重要的作用,若水中钙镁离子含量较高造成标准加入量的掩蔽剂失效时,可以考虑采用其他2 种测定方法。
2.6 氯离子和钠离子影响
入海河口的样品盐含量较高,一般认为盐含量过高主要是由水体中钠离子、钙离子、镁离子和氯离子引起的[19]。
为避开蒸馏等繁琐的水样前处理步骤,应用3种方法比较了同浓度氨氮标准溶液(0.15 mg/L)在不同浓度氯离子和钠离子溶液中的影响。 如图4 所示,纳氏试剂分光光度法在氯离子质量浓度低于2 000 mg/L 时,测定结果无明显变化,回收率为102%~113%,当氯离子质量浓度大于2 000 mg/L时,测定结果出现严重偏离,呈先升高后降低趋势,回收率最高达209%;气相分子吸收法在较高质量浓度的氯离子影响下,回收率仍可维持在96.9%~98.5%,说明氯离子对该方法无显著影响。

图4 氯离子对纳氏试剂分光光度法和气相分子吸收法测定结果的影响Fig.4 Effect of chloride ion on the determination results of Nessler's reagent spectrophotom etry and gas-phase molecular absorption spectrometry
氯离子虽不影响阳离子体系离子色谱法测定氨氮,但实际水体中氯离子与钠离子常常是共存的。 常见阳离子色谱柱对钠离子和铵离子的保留时间相近[20-21],低浓度铵离子在钠离子大量存在时难以准确定量,故比较在3 种淋洗液浓度条件下不同钠铵比(钠离子质量浓度与铵离子质量浓度的比值)对水中氨氮测定的影响。
如图5 所示,在3 种淋洗液浓度条件下,测定回收率均随着钠铵比增加而逐渐上升,其中20 mmol/L 的淋洗条件在钠铵比大于6.7 后测定结果偏差增大。 从图6 色谱图也可以看出,钠铵比增大,铵离子的色谱峰逐渐变形,尤其是淋洗液浓度为15 mmol/L 和20 mmol/L 时,铵离子的色谱峰与钠离子色谱峰接近重叠,基线抬高,无法准确定量。

图5 钠离子对离子色谱法测定结果的影响Fig.5 Effect of sodium ions on the determination results of ion chrom atography
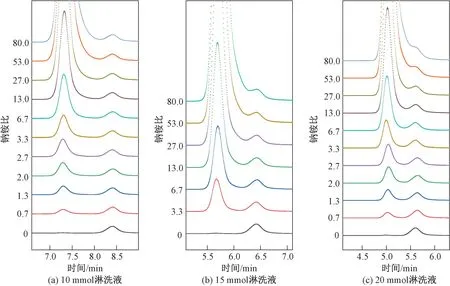
图6 3 种淋洗液浓度条件下不同钠铵比的离子色谱图Fig.6 Ion chromatograms of three eluents with different
因此,不考虑复杂的前处理,纳氏试剂分光光度法测定氨氮在氯离子浓度大于2 000 mg/L 时影响较大,离子色谱法测定氨氮时则需要关注钠离子浓度并及时调整淋洗条件,当氯离子和钠离子浓度过高时可以选择气相分子吸收法进行测定。
2.7 硫化物影响
硫化物对分光光度法和气相分子吸收法测定氨氮均有一定影响。 李念等[22]的研究表明,直接蒸馏法对硫化物的去除效果不佳,不仅需先加入硫酸进行预处理而使过程繁琐,而且还引入pH的干扰。
为避免前处理带来的干扰,比较了直接测定方式下样品在不同浓度硫化物影响时氨氮标准溶液(0.15 mg/L)的测定结果。 如图7 所示,纳氏试剂分光光度法测定结果随硫化物浓度增高呈上升趋势,硫化物含量越高影响越大,回收率最高达172%,这主要是由于硫化物和纳氏试剂反应生成黄色物质,在波长420 nm 处也有较强的吸收[23];气相分子吸收法的测定结果随硫化物浓度增高呈下降趋势,回收率从73.6%降至0,这是由于硫化物会消耗溴酸盐氧化剂,影响氧化效率;离子色谱法在硫化物影响下,回收率为94.1%~108%。因此,水样中硫化物偏高时,离子色谱法更有优势。

图7 硫化物对3 种方法测定结果的影响Fig.7 Effect of sulfide on the determination results of three methods
2.8 实际样品测定
采集北海市某地表水饮用水水源地7 个地表水样品和某地下水饮用水水源地2 个地下水样品,目测为清洁水,相关水质参数如表3 所示,纳氏试剂分光光度法测定时选用预蒸馏和直接测定2 种方式,气相分子吸收法采用直接进样,离子色谱法采用过0.45 μm 滤膜后直接进样。
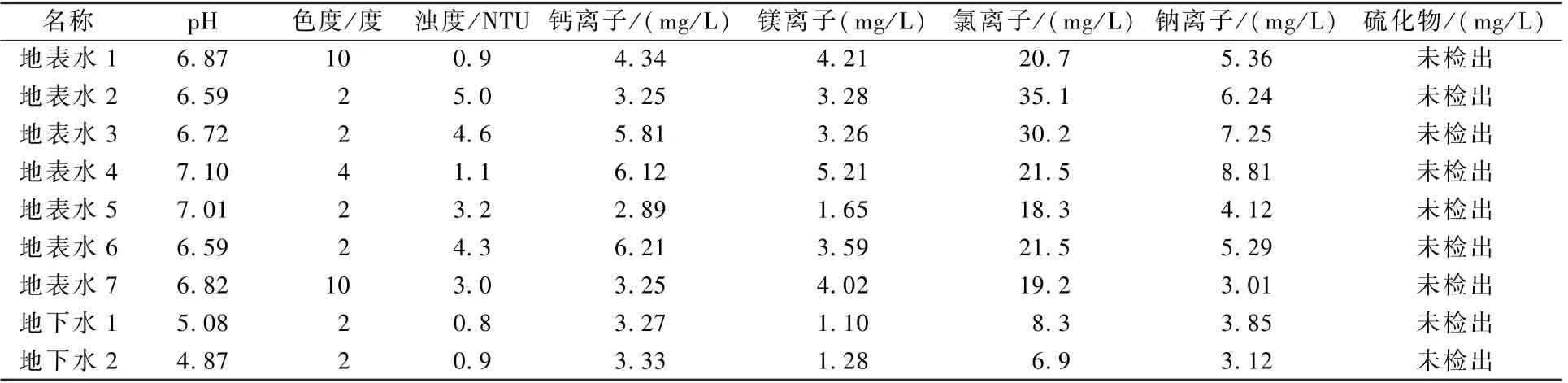
表3 实际样品水质参数Table 3 Water quality parameters of actual samples
对7 种地表水样品进行平行双样测定,均值见表4。 参照《环境监测分析方法标准制订技术导则》(HJ 168—2020)[7]附录B 要求进行测试结果比对,经蒸馏前处理的纳氏试剂分光光度法分别与直接测定的纳氏试剂分光光度法、气相分子吸收法和离子色谱法进行t 检验。 纳氏试剂分光光度法直接分析和预蒸馏分析的比对结果t =10.816>2.447(n=7,置信度为95%),说明在该浓度水平下测定结果有显著差异,直接法测定结果偏高;经预蒸馏的纳氏试剂分光光度法,与气相分子吸收法(t=1.266 <2.447)和离子色谱法直接分析(t=1.236 <2.447)的测定结果均无显著差异。 如表4 所示,由于测定的样品(地下水2)实际浓度已低于纳氏试剂分光光度法测定下限,其测定结果并不能准确定量,故在测试标准[2]规定的清洁水中低浓度氨氮时,2 种仪器方法在灵敏度、准确度和便捷性上更具优势,同时,在考虑应用纳氏试剂分光光度法时还需慎重选择直接测定的方式,前处理也要严格控制条件。

表4 实际样品测定结果Table 4 Determination results of actual samples
3 结论
1)在提高试剂纯度及保证仪器最佳状态下,离子色谱法相较其他2 种方法进样量最小,检出限最低(25 μL 时为0.005 mg/L,50 μL 时为0.003 mg/L)。 测试条件优化后离子色谱法可以对I 类地下水实现准确测定,当清洁水中氨氮质量浓度低于0.02 mg/L 时,离子色谱法是最佳选择。
2)清洁水中氨氮含量较低不适宜做样品前处理时,要根据实际水样的干扰状况选择适宜的分析方法。 纳氏试剂分光光度法分析低浓度氨氮时,需要格外关注水样中的影响因素,如pH、色度、浊度、硬度、硫化物及氯离子都会使纳氏试剂分光光度法产生干扰,pH 低于1 或略高于1、色度大于10 度、Ca2+质量浓度大于20 mg/L、Mg2+质量浓度大于1.6 mg/L、Cl-质量浓度大于2 000 mg/L、硫化物质量浓度大于0.06 mg/L 和有一定浊度的清洁水不宜直接取样测定;选择气相分子吸收法测定时,特别需要关注水样中是否存在硫化物,该物质对测定产生负干扰,此时可以选择离子色谱法进行氨氮测定;采用离子色谱法测定氨氮时,需要关注水样中Na+质量浓度,该离子容易干扰测定,此时可以选择气相分子吸收法和纳氏试剂分光光度法。
3)使用纳氏试剂分光光度法测定存在干扰的清洁水中氨氮时,需进行预蒸馏前处理才能保证3 种方法测定结果无显著差异。

