FEC 对不同混盐电解液体系的影响
张丽娟,何劲作,辛 娟,闫 啸
(青海民族大学化学化工学院,青海 西宁 810007)
目前,低温下锂离子电池的能量输出大大降低,不能满足市场的要求。 为了拓宽锂离子电池的应用温度范围,开发电解液成为研究热点。
作为电解液改性的一个热点,添加剂的种类多、效果明显,且用量小。 广泛使用的成膜添加剂,可促进电极/电解液界面膜的生长,即可形成离子导电性高的界面膜,也可抑制较差的膜的生长。 L.X.Liao 等[1]发现,添加剂氟代碳酸乙烯酯(FEC)的加入,有利于降低界面阻抗,使电池低温性能得到提高。 S.Tan 等[2]探究1 mol/L 二氟草酸硼酸锂(LiODFB)-异唑(IZ)/FEC(体积比10 ∶1)在低温-20 ℃下的性能,发现FEC 作为添加剂,在石墨负极表面可形成稳定的固体电解质相界面(SEI)膜。 辛娟等[3]探究了1 mol/L LiODFB/LiBF4混合锂盐在低温下对LiCoO2正极材料的匹配性。
在此基础上,本文作者采用FEC 作为成膜添加剂,考察对不同混合锂盐基电解液电池低温性能的影响。
1 实验
1.1 试剂与原料
碳酸乙烯酯(EC,东莞产,AR)、碳酸丙烯酯(PC,东莞产,AR)、碳酸甲乙酯(EMC,东莞产,AR)、碳酸二甲酯(DMC,东莞产,AR)、乙酸乙酯(EA,东莞产,AR)、FEC(东莞产,AR)、四氟硼酸锂(LiBF4,东莞产,AR)、LiODFB(东莞产,AR)、N-甲基吡咯烷酮(NMP,河南产,AR)、铝箔(广州产,电池级,16 μm 厚)、乙炔黑(Timcal 公司,电池级)、聚偏氟乙烯(PVDF,Arkema 公司,电池级)、钴酸锂(LiCoO2,天津产,电池级)、金属锂片(深圳产,99.9%)和Celgard 2400 膜(美国产)。
1.2 实验仪器
CT2001A 型电池测试系统(武汉产);MSK-110 型手动液压封口机(深圳产);MSK-T10 型扣式电池切片机(深圳产);JK-GYJ-100B 型实验型辊压机(深圳产);JK-TMJ-200 型台式实验涂布机(深圳产);IviumStath 型电化学工作站(荷兰产);MSK-SFM-3 型震动球磨仪(深圳产);SU8010F 型扫描电子显微镜(日本产);Escalab 250Xi+型X 射线光电子能谱(XPS)仪(上海产)。
1.3 电解液的配制
实验在手套箱[w(H2O)<10-5%、w(O2)<10-5%]中进行;将有机溶剂PC、EC、EMC、EA 按体积比1 ∶1 ∶1 ∶2分别加入聚四氟乙烯瓶中,配成混合溶剂,将锂盐LiBF4和LiODFB 按物质的量比1 ∶1溶解于上述溶液中,与纯LiBF4和纯LiODFB溶解到相同溶剂中作为对比。 添加质量分数为0、1%、3%和5%的成膜添加剂FEC,配制成实验所需电解液。 配置后封口,静置24 h 后,即可使用。
实验所用电解液体系见表1。

表1 实验所用电解液体系Table 1 Electrolyte system used in the experiment
1.4 LiCoO2 正极片的制备及扣式电池的组装
将正极材料LiCoO2、乙炔黑和黏结剂PVDF 按质量比8 ∶1 ∶1在玛瑙球磨罐中混合,再加入6 ml NMP,以1 500 r/min的转速球磨(球料比1.0 ∶1.1)10 min,得到均匀浆料,涂覆在铝箔上,在120 ℃下真空(-0.08 MPa)干燥12 h,自然冷却,辊压机上辊压,用切片机切成12 mm 圆片,电子天平称重后,装袋。 按照正极壳、正极片、电解液、隔膜、锂片、垫片、弹片和负极壳的顺序,组装CR2025 型扣式LiCoO2/Li 半电池。电池静置12 h 后,进行电化学性能测试。
1.5 测试方法
循环伏安(CV)测试的扫描速率为0.1 mV/s,扫描电压为2.7~4.2 V。
利用电池测试系统对恒流充放电、循环和倍率性能进行测试,电压为2.7 ~4.2 V,测定电池在0.2C、0.5C、1.0C、2.0C和5.0C等不同电流倍率下的放电比容量。
电池组装后静置24 h,用电化学工作站对电池进行电化学阻抗谱(EIS)测试,频率为105~10-1Hz、扰动电压为5 mV。
在手套箱内,将循环后的电池拆卸后,用溶剂DMC 冲洗多次,干燥后,进行SEM 测试和电极表面膜成分分析。
2 结果与讨论
2.1 添加剂FEC 用量的选取
将不同含量FEC 加入0.5 mol/L LiBF4+0.5 mol/L Li-ODFB 基电解液中,组装电池进行电化学测试,结果见图1。

图1 不同FEC 添加量LiBF4/LiODFB 体系电池的倍率性能和循环性能Fig.1 Rate capability and cycle performance of LiBF4/LiODFB system batteries with different FEC additions
从图1(a)可知,在1.0C低倍率下,FEC 为0 时,放电比容量最低;在2.0C倍率下,当FEC 为5%时,放电比容量最低;FEC 为1%和3%时,二者的放电比容量始终相差不大。从图1(b)可知,5%FEC 电解液组装电池循环100 次后,容量保持率最高,原因是较多的FEC 参与成膜,改善Li 沉积的形态,降低正极电解质界面(CEI)膜的阻抗[4]。 从图1(b)可知,不同电解质体系的首次比容量在未加入FEC 时最低,是由于LiODFB 参与了界面膜的形成,且膜层较厚,消耗的Li+较多,导致首次比容量降低,FEC 的加入提高了首次比容量。当FEC 含量为1%和5%时,比容量和循环稳定性差别不大;当FEC 含量为3%时,放电比容量和循环稳定性最好,可同时兼顾循环性能和倍率性能的只有3%FEC 电解质。
2.2 LiCoO2/Li 半电池的常温电化学性能
不同电解液体系LiCoO2/Li 半电池的首次充放电曲线见图2。

图2 不同电解液体系电池的首次充放电曲线Fig.2 Initial charge-discharge curves of batteries with different electrolyte systems
从图2 可知,在常温条件下,不同的电解液体系组装的LiCoO2/Li 电池的充电、放电特性差别较大。 在不同的电解液体系中,首次充放电比容量均低于理论值(140 mAh/g),主要是由于在充放电(嵌脱锂)期间,LiCoO2的结构发生不可逆的转变,且会在电极上形成一层界面膜,Li+被消耗掉,导致容量不可恢复。 LiBF4电解质的电导率较低,成膜性能较差,因此,在成膜时,Li+的损耗较大,放电比容量及效率都较低。 随着放电电压的增加,电池的比容量也随之增加。 加入LiODFB 后,锂离子电池的比容量明显提高。 由此可知,添加FEC 后,电池的充放电能力和效率得到改善。
不同电解液体系LiCoO2/Li 半电池的CV 曲线见图3。
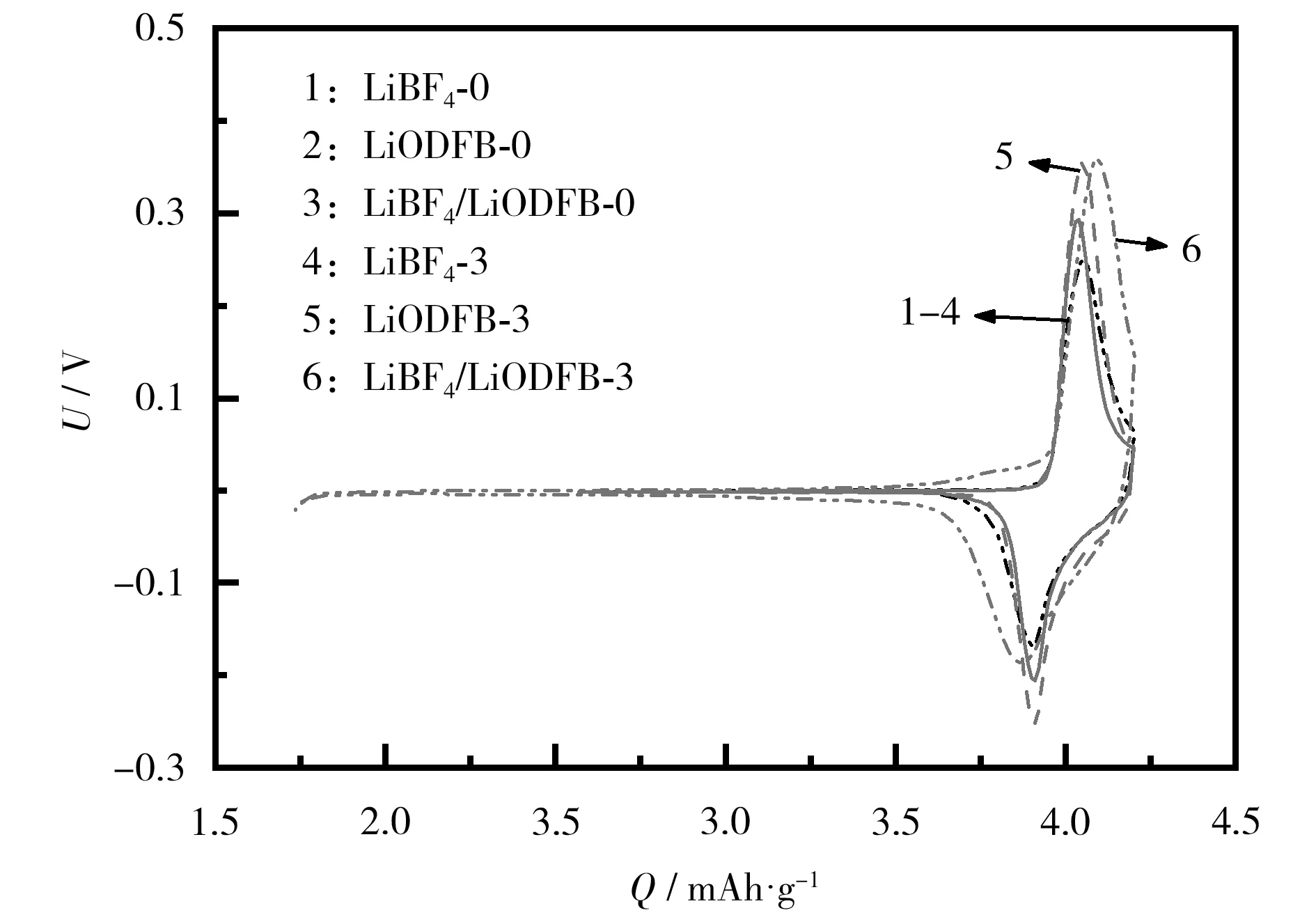
图3 LiCoO2/Li 电池在不同电解液中的CV 曲线Fig.3 CV curves of LiCoO2/Li battery in different electrolytes
从图3 可知,CV 曲线上均有一对氧化还原峰。 电解液体系锂盐中的LiODFB,优先在电极表面成膜,导致膜阻抗增大;其余体系中溶剂EC 会参与成膜,导致含量减少,锂盐溶解度降低,Li+的迁移速率降低,使电池不可逆程度及极化加剧。 氧化电位低的FEC 的加入,优先在正极表面成膜,抑制了LiODFB 和EC 参与成膜。 这表明,FEC 有利于减缓电池不可逆程度及极化的加剧,与倍率和循环性能的结果一致。
不同电解液体系LiCoO2/Li 半电池在常温下的循环性能见图4。

图4 常温下不同电解液体系电池的循环性能Fig.4 Cycle performance of batteries with different electrolyte systems at room temperature
从图4 可知,纯LiBF4和LiODFB 基电解液体系(1、2、4和5 号)在常温下循环后,容量衰减较明显,可能是由于循环次数的增加,电解液在电极表面发生了分解。 纯LiODFB 基电解液容量保持率仅约70%,是由于LiODFB 在循环过程中形成较厚的界面膜,导致离子转移阻抗增加,加剧了电池极化。 混盐体系(3 号和6 号)的循环稳定性要高于纯锂盐的。电解液体系中加入FEC 后,首次放电比容量增大,是由于FEC 成膜,不可逆损失减少,循环100 次,稳定性有所提高。
不同电解液体系LiCoO2/Li 半电池的倍率性能见图5。
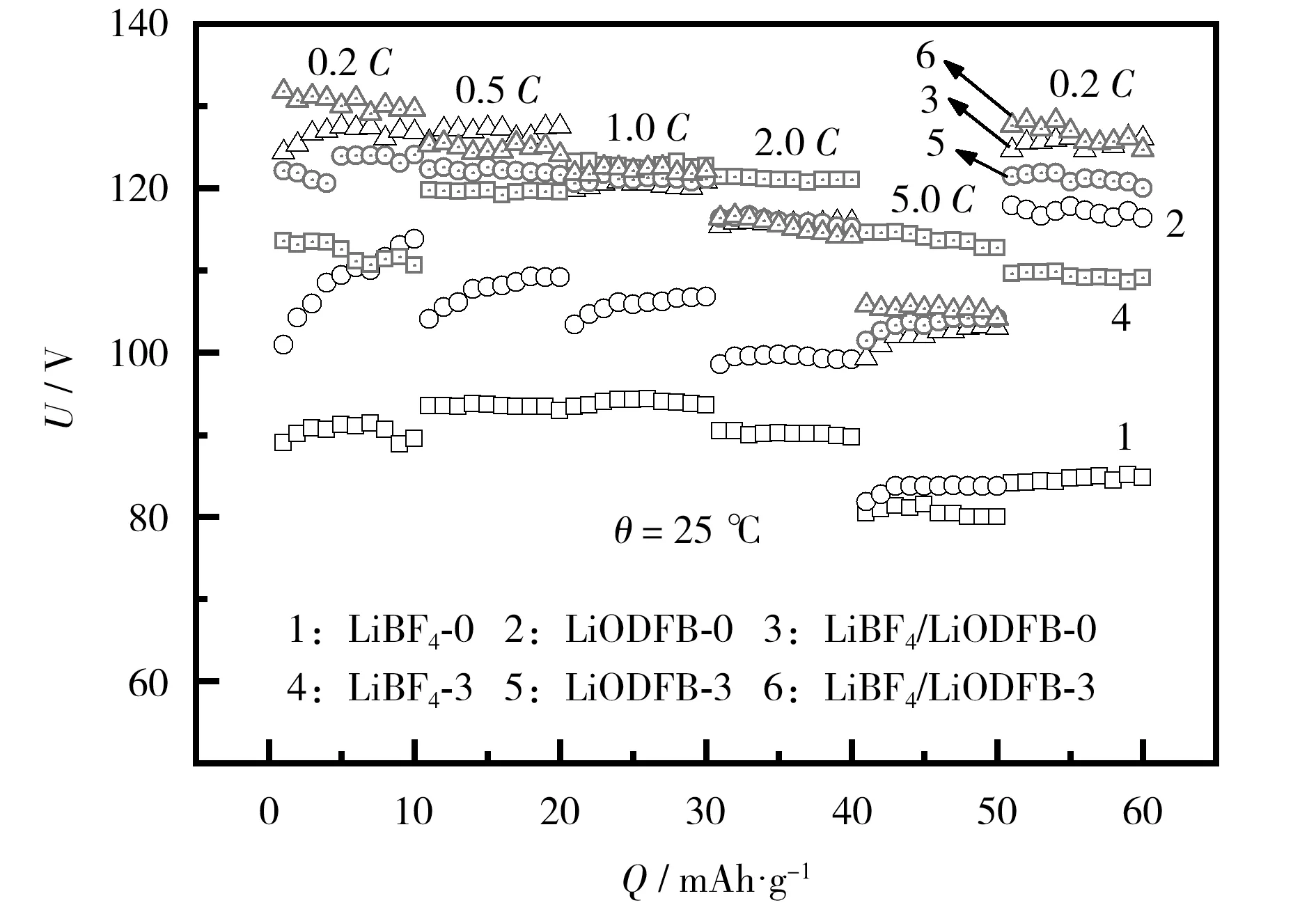
图5 不同电解液体系电池的倍率性能Fig.5 Rate capability of batteries with different electrolyte systems
从图5 可知,LiBF4/LiODFB 体系,无论从初始容量,还是在高倍率5.0C下的放电比容量,总体高于LiBF4、LiODFB。加入3% FEC 后,在0.2C倍率下,每个体系的起始放电比容量均高于未加入FEC 的。 电池在充放电过程中会消耗活性Li+,导致首次库仑效率较低。 FEC 会在正极表面优先成膜,减缓活性Li+的损失,并缓解电解液与电极的进一步接触,因此放电比容量有所提高。
2.3 -20 ℃下FEC 对电池电化学性能的影响
-20℃下不同电解液体系电池的循环性能见图6。

图6 -20 ℃下不同电解液体系电池的循环性能Fig.6 Cycle performance of batteries with different electrolyte systems at -20 ℃
从图6 可知,在-20 ℃下,将3% FEC 加入电解液体系中,放电比容量和循环稳定性有所提高。 使用LiBF4/LiODFB-3电解液电池循环50 次的放电比容量为113.5 mAh/g,容量保持率为96.34%,均高于未添加FEC 电解液的电池。 这可能是由于FEC 优先于电解液锂盐或溶剂,在正极表面成膜,缓解电解液与电极接触的进一步接触,提高了电池的性能。
-20 ℃下,添加3%FEC 的不同电解液体系组装电池循环50 次的阻抗测试结果见图7。
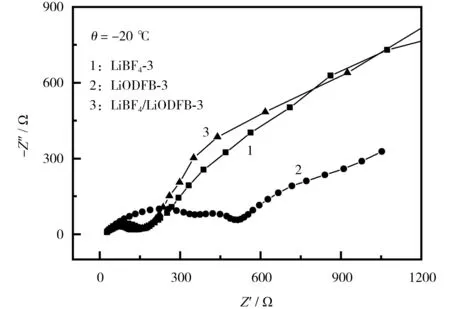
图7 不同电池-20 ℃下循环50 次后的阻抗Fig.7 Impedance of different batteries after 50 cycles at -20 ℃
从图7 可知,-20 ℃下,使用LiODFB-3(5 号)电解液的电池阻抗最大,使用LiBF4-3(4 号)电解液的阻抗次之,使用LiBF4/LiODFB-3(6 号)电解液的阻抗最小,可能是由于过量LiODFB 和添加剂协同形成的CEI 膜过于致密,也较厚,而混合锂盐LiBF4/LiODFB 因LiBF4自身的成膜性不好,借助FEC 和LiODFB 成膜性,可弥补缺点,形成相对良好的CEI膜,有利于提高电池的低温性能,与低温循环结果一致。
2.4 -20 ℃下循环后电池极片的SEM 和XPS 测试
-20 ℃下,不同电解液体系电池循环50 次后,电极的SEM 图见图8。
从图8 可知,使用LiODFB-3 电解液的电池,电极表面的CEI 膜相对致密,也较厚。 使用LiBF4-3 电解液的电池,电极表面的CEI 膜相对更蓬松。 相比其他体系,使用LiBF4/Li-ODFB-3 体系,电极表面的CEI 膜要相对稳定、致密且薄。 这3 种体系电极表面CEI 膜情况的不同,可能是由于添加剂FEC 的加入,会优先于电解液在电极表面成膜,而电解液本身也会发生分解,其中LiBF4基电解液会形成不稳定的CEI膜,而LiODFB 的加入,将形成更稳定且致密的CEI 膜,提高电池的低温性能。 当电解液为LiODFB 基时,过量的LiODFB和添加剂FEC 协同成膜,导致膜层过于致密、稳定,反而不利于电池低温性能。 SEM 分析结果与低温循环的一致。
在-20 ℃下,不同电解液体系电池循环50 次,电极的XPS 测试结果见图9。

图9 不同电解液体系电池电极的XPSFig.9 X-ray photoelectron spectroscopy(XPS) of electrodes of battery in different electrolyte systems
从图9 可知,O 1s 在532.2 eV 位置出现C==O 键、F 1s在685.1 eV 和688.9 eV 附近出现—CF2和LiF,B 1s 在192 eV 位置附近出现B—O 键。 这说明,在电池循环过程中,电极表面形成了一层CEI 膜,对比不含FEC 的XPS 可知,含有LiODFB 电解液体系中,电极表面膜中有机物ROCO3Li 峰的强度更小,说明LiODFB 的加入抑制了电解液的持续分解。对比6 个体系的O 1s、F 1s 和B 1s 峰的强度可知,体系LiBF4/LiODFB-3 的C ==O、—CF2、LiF 和B—O 的强度都是最低的,形成了具有高LiF 和低B—O 的稳定CEI 膜,说明FEC 的加入优先成膜,可缓解电解液体系的分解,提高电池性能。
3 结论
本文作者向0.5 mol/L LiBF4+0.5 mol/L LiODFB/EC+PC+EMC+EA(体积比1 ∶1 ∶1 ∶2)体系电解液引入添加剂FEC,并与1.0 mol/L LiBF4基电解液和1.0 mol/L LiODFB 基电解液进行对比。
通过倍率和充放电测试,确定FEC 的最佳加入量为3%(质量分数);由CV 曲线可知,FEC 优先在正极成膜,降低电池极化程度;由循环性能测试可知,FEC 的加入,可提高电池的放电比容量和循环稳定性。 在-20 ℃下,3% FEC 的加入,可以提高电池的放电比容量和循环稳定性,使用0.5 mol/L LiBF4+0.5 mol/L LiODFB 电解液电池第50 次循环的放电比容量为113.5 mAh/g,容量保持率为96.34%,均高于未添加FEC 电解液的电池。

