信迪利单抗联合新辅助化疗在局部晚期食管癌治疗中的疗效分析
李春霖,刘 迪,甘绍印,朱德奇,李 宾,王永连
食管癌作为我国临床上常见的恶性肿瘤之一,其发病率和死亡率均较高。外科手术切除是食管癌治疗的主要方法之一,但是因为早期食管癌患者多无明显的临床症状,多数患者出现进食不畅、胸背部疼痛等相关症状就诊时,疾病往往已经发展至局部晚期,单纯手术切除的效果以及预后均较差[1]。因此,局部晚期食管癌患者在临床治疗过程中多需进行术前新辅助治疗,在食管肿瘤或肿大的淋巴结缩小后,再通过复查胸部增强CT等影像学进一步评估,以争取获得更好的手术机会[2]。术前新辅助化疗不仅可以缩小食管瘤体及周围肿大的淋巴结,还可以杀灭一些可能存在的微小转移灶,从而降低食管肿瘤的临床TNM分期,此时再进行手术可以提高手术的R0切除率以及患者的远期生存率[3]。但是有一小部分食管癌患者对化疗药物的敏感性较差,单纯进行新辅助化疗缩瘤降期的效果并不明显,从而影响了手术的治疗效果以及患者的远期生存率[4]。
近年来,随着我国医疗卫生科技水平的不断发展,肿瘤的治疗方法也越来越多,其中免疫治疗作为一种新出现的抗肿瘤治疗方法,在肿瘤治疗中取得了良好的效果[5],其相关药物的价格也较刚上市时大幅度下降,而且部分已纳入医保报销范围。因此,在临床上的使用也是越来越普及。程序性死亡受体1(programmed cell death receptor 1,PD-1)抑制剂是用于肿瘤免疫治疗的常见药物,目前已经在食管癌的治疗中得到了广泛的临床应用且有确切的治疗效果,诸多食管癌晚期患者已从中获益。白蛋白结合型紫杉醇和奈达铂作为紫杉醇类的代表和第二代铂类化疗药物也已经广泛用于临床,两种化疗药物联合作为一线治疗方案用于晚期食管癌的治疗中取得了良好的效果[6]。信迪利单抗是我国国产的PD-1抑制剂,现已临床获批用于霍奇金淋巴瘤、非小细胞肺癌、食管癌等多项肿瘤治疗,其通过阻断相关配体的结合,激活体内T细胞功能,增强对肿瘤细胞的杀伤效果,从而产生肿瘤免疫应答[7]。本研究观察信迪利单抗联合白蛋白结合型紫杉醇+奈达铂与单独使用白蛋白结合型紫杉醇+奈达铂在局部晚期食管癌患者术前新辅助治疗中的效果,总结报道如下。
1 资料与方法
1.1 一般资料经医院医学伦理委员会批准同意,回顾性分析2019年1月至2021年12月在新乡医学院第一附属医院胸外科病区予以新辅助治疗2周期后经影像学评估后可手术切除并行胸腹腔镜联合下食管癌根治术治疗的局部晚期食管癌患者的临床资料,共计82例。病例纳入条件:①经病理确诊,且结合相关影像学检查被评估为局部晚期的食管癌患者;②未接受过相关抗肿瘤治疗;③心肺功能基本正常,ECOG评分0~1;④临床充分告知,签署相关知情同意书。排除标准:①患有严重心肺功能障碍;②不能耐受静脉化疗;③合并其他严重疾病,包括需要治疗的不稳定心脏病,重大神经系统或其他相关精神疾病。依据治疗方法不同将入组患者分为A组(40例)和B组(42例)。A组患者男性27例,女性13例;年龄54~75(65.3±5.84)岁;体质量指数(BMI)17.5~26.7(21.7±2.06) kg·m-2;鳞癌35例,非鳞癌5例;ⅢA期25例,ⅢB期15例。B组患者男性28例,女性14例;年龄53~76(65.5±6.11)岁;BMI为17.7~26(22.15±1.88) kg·m-2;鳞癌36例,非鳞癌6例;ⅢA期27例,ⅢB期15例。两组患者性别、年龄、BMI、病理分型、TNM对比无统计学差异(P>0.05),见表1。
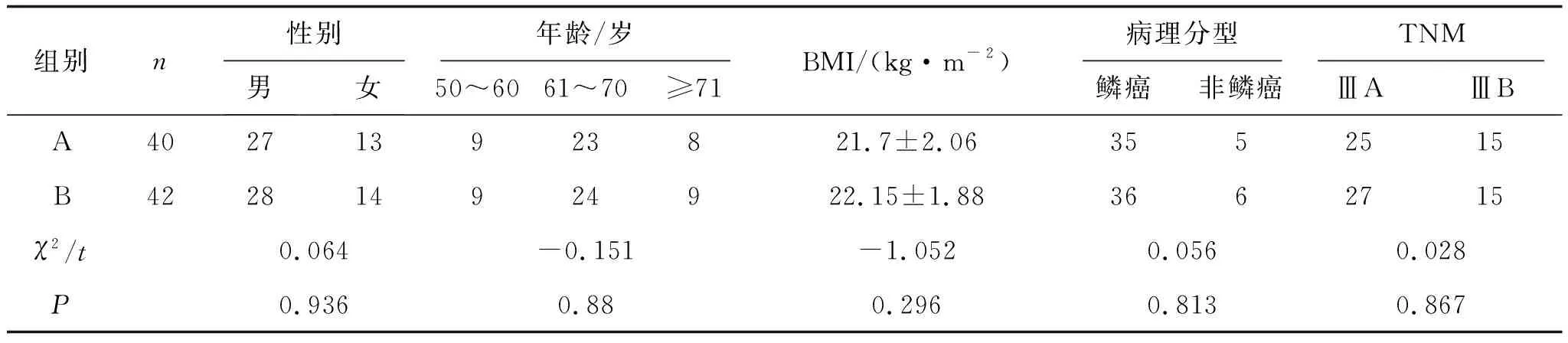
表1 两组患者一般资料对比
1.2 治疗方法A组患者接受信迪利单抗(苏州信达生物制药有限公司,国药准字S20180016,规格:10 mL∶100 mg),每次200 mg+白蛋白结合型紫杉醇(齐鲁制药有限公司,国药准字 H20193309,规格:100 mg)260 mg·m-2+奈达铂(南京先声东元制药有限公司,国药准字H20030884,规格:10 mg)80 mg·m-2静脉输注,每21 d为1个治疗周期。B组患者不用信迪利单抗免疫治疗,化疗用药方案与A组患者相同。两组患者均进行新辅助治疗2个周期,在治疗过程中未见严重的不良反应发生,所有患者均按标准剂量进行治疗,在新辅助治疗结束后4周予以相关术前检查评估后行胸腹腔镜联合三切口食管癌根治术。
1.3 观察指标①对比观察两组患者的化疗不良反应发生率,参照常见不良事件评价标准(commonterminology criteria for adverse events,CTCAE)4.0版[8]评估,包括Ⅰ~Ⅳ级。本研究主要观察指标为胃肠道反应、骨髓抑制、肝肾功异常、高血压、甲状腺功能减退。②近期临床疗效:参照实体瘤疗效评价标准1.1[9]评估两组患者在新辅助治疗2周期后的临床疗效,主要包括完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD),以及客观缓解率(objective response rate,ORR)=(CR+PR)/总例数×100%,疾病控制率(disease control rate,DCR)=(CR+PR+SD)/总例数×100%。③围手术期指标:手术时间、术中出血量、术后胸引量、住院时间、R0切除率以及术后吻合口瘘的发生率。④术后病理反应评估:根据两组患者术后的病理报告,将残留活性肿瘤细胞≥50%定义为无反应者,残留的活性肿瘤细胞≤10%定义为主要病理缓解(major pathologic response, MPR),没有残留肿瘤的定义为病理完全缓解(pathologic complete response, pCR)。
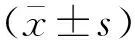
2 结果
2.1 患者化疗不良反应发生率在新辅助治疗期间,两组患者的化疗相关不良反应主要有骨髓抑制、胃肠道反应、肝肾功异常、高血压、甲状腺功能减退等,通过两组数据的比较,经χ2检验,各项数据指标差异均无统计学意义(P>0.05),见表2。

表2 两组患者新辅助治疗期间化疗不良反应比较 例 (%)
2.2 近期临床疗效两组患者在经过两个周期的新辅助治疗后均有有效的可测量靶病灶,通过影像学总体评估发现两组患者CR、PR、SD、PD的百分比分别为10%、60%、20%、10%和2.38%、33.33%、35.71%、28.57%,根据以上数据进一步统计两组患者的ORR和DCR,通过对比结果两项指标均有统计学差异(P值分别为0.004和0.034,均<0.05),见表3。

表3 两组患者近期临床疗效评估 例 (%)
2.3 围手术期指标通过对比两组患者围手术期间在手术时间、术中出血量、术后胸引量、住院时间的相关数据,经t检验,各项数据指标差异无统计学意义(均P>0.05),见表4;两组患者在术后吻合口瘘和R0切除率比较,经χ2检验,差异无统计学意义(均P>0.05),见表5。
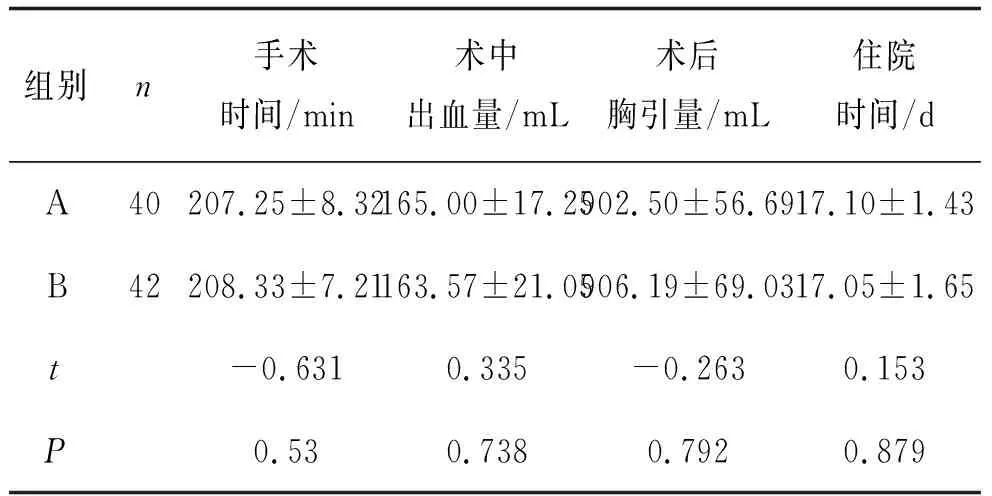
表4 两组患者围手术期指标
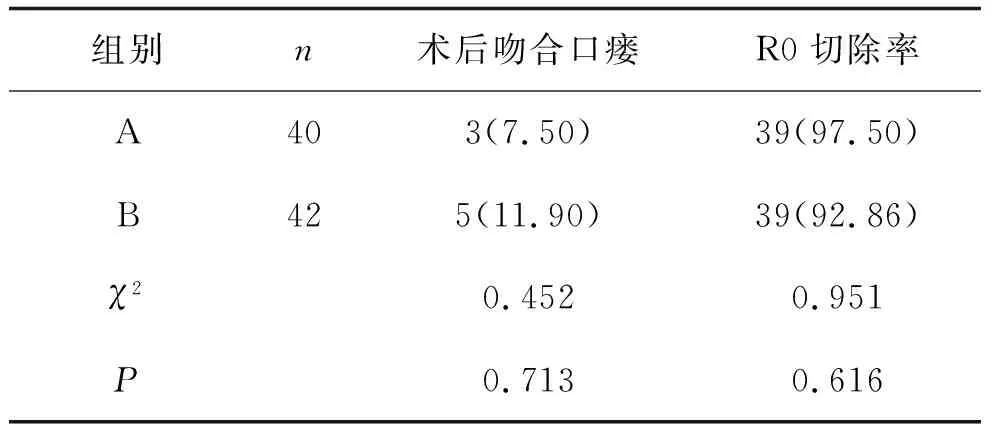
表5 两组患者吻合口瘘发生率和R0切除率 例(%)
2.4 术后病理反应评估两组患者的术后病理反应评估对比,经χ2检验,两组患者MPR A组优于B组,差异有统计学意义(P<0.05),两组在pCR及无反应方面差异无统计学意义(均P>0.05),见表6。
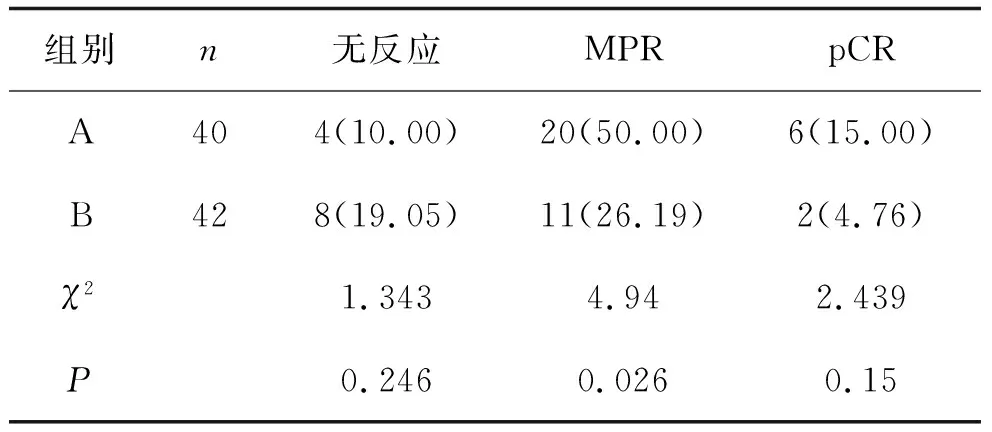
表6 两组患者术后病理反应评估 例 (%)
3 讨论
我国是世界食管癌高发地区之一,而我院所处之豫北太行山地区又为我国食管癌的高发地区[10]。食管癌的发病与个人的饮食习惯、周围的生活环境以及遗传等有关,发病早期较为隐匿,患者多无明显的进食哽噎、胸痛等症状,而且多数食管癌患者的经济水平欠佳,体检意识较差,加上胃镜检查亦未纳入常规的体检项目等多种原因,因此当多数食管癌患者有明显临床症状再行就诊检查时肿瘤已外侵明显,或者出现周围淋巴结转移,与周围组织关系密切,病情已发展为中晚期,部分病人甚至因此丧失了手术治疗的机会,此时进行单纯的手术切除风险较大,而且治疗效果欠佳,预后较差,术后发生局部复发或转移的风险均较高[11],因此针对可切除局部晚期的食管癌患者应采用以手术为主的综合治疗方式,经过多年的临床经验总结,术前进行新辅助治疗缩瘤降期后再联合外科根治手术已成为局部晚期食管癌的主要治疗模式。
在诸多的新辅助化疗的药物选择中,紫杉醇类药物具有广谱的抗肿瘤作用,可以抑制细胞的有丝分裂,加速肿瘤细胞的凋亡[12],白蛋白结合型紫杉醇作为新一代紫杉醇类药物,通过将紫杉醇和白蛋白结合制成新型的化疗药物,不仅克服了紫杉醇不溶于水的难题,降低了紫杉醇的毒性,还增加了紫杉醇对癌细胞的杀伤能力,提高生物利用度,而且用药前不需要进行抗过敏预处理,减少了不良反应的发生,已用于多种肿瘤的临床治疗并取得了良好的效果。奈达铂作为第二代铂类药物的代表,患者化疗应用后恶心、呕吐等一系列消化道反应没有顺铂强烈,而且肾毒性较小,通过抑制肿瘤细胞DNA的复制,从而产生抗肿瘤的活性,来发挥抗癌效果,对多种实体瘤都有效,已广泛应用于食管癌的临床治疗中。白蛋白结合型紫杉醇联合奈达铂两者联合使用可以使食管肿瘤及肿大淋巴结缩小,进而降低食管肿瘤术前临床诊断的TNM分期,提高手术的R0切除率,减少因肿瘤较大侵及周围脏器而带来的相关手术风险,改善术后生存率,已成为近年来局部晚期食管癌术前新辅助化疗的一线方案。但是仍然有一部分局部晚期食管癌的患者对化疗药物反应不敏感,新辅助化疗后复查胸部CT发现肿瘤缩小不明显,治疗效果不佳,患者治疗获益不明显,局部晚期食管癌的新辅助化疗发展自此遇到了一定的瓶颈。
近年来随着免疫治疗相关药物在临床上的广泛应用,中晚期恶性肿瘤的治疗从放化疗等传统治疗方法逐渐进入了免疫治疗时代,而且已经取得了良好的临床效果,KEYNOTE-590、ORIENT-15、 CheckMate -648等多种临床研究已先后证实PD-1抑制剂联合化疗,相比单纯化疗可以有效延长食管癌患者的无进展生存时间(progression free survival,PFS)和总生存时间(overall survival,OS),并显著降低死亡风险[13-15]。信迪利单抗是我国自主研发的PD-1抑制剂,有研究报道信迪利单抗用于治疗复发或转移性晚期食管癌患者能够有效地延长患者 PFS 和 OS[16],而且经过信迪利单抗联合含铂类药物的三重化疗安全可行,不会延迟手术时间,在潜在可切除的食管鳞癌患者中有20%的病理学完全缓解(pathologic complete response,pCR)[17],有报道表明,免疫治疗联合新辅助化疗可以产生一加一大于二的协同作用[18],因此信迪利单抗联合新辅助化疗应用与局部晚期食管癌的治疗中,不仅可以延长患者的远期生存,而且安全可行[19],为局部晚期食管癌的治疗打开了一扇新的门户。
本研究将PD-1抑制剂信迪利单抗与传统化疗药物白蛋白结合型紫杉醇、奈达铂联合用于经影像学评估为局部晚期食管癌患者的术前新辅助治疗,通过对比白蛋白结合型紫杉醇+奈达铂的新辅助化疗是否联合信迪利单抗的免疫治疗,结果显示,在患者新辅助治疗期间,患者的胃肠道反应、骨髓抑制、肝肾功能异常、高血压、甲状腺功能减退等化疗不良反应发生率两组患者无明显的统计学差异(均P>0.05),且已发生的不良反应多为Ⅰ~Ⅱ级,临床上安全可控,患者均可耐受,提示在局部晚期食管癌患者术前的新辅助治疗中信迪利单抗免疫治疗联合白蛋白结合型紫杉醇与奈达铂新辅助化疗安全可行,未增加明显化疗不良反应。对入组患者经两周期的新辅助治疗后通过影像学评估,发现两组患者在客观缓解率、疾病控制率A组均高于B组,差异有统计学意义(P<0.05),提示在局部晚期食管癌患者的术前新辅助治疗中使用信迪利单抗联合白蛋白结合型紫杉醇及奈达铂的治疗方案优于单纯的白蛋白结合型紫杉醇及奈达铂的化疗,可以使患者的治疗获益。
本研究发现,对局部晚期食管癌患者应用信迪利单抗免疫治疗联合白蛋白结合型紫杉醇及奈达铂的新辅助化疗的治疗方案,在围手术期间并没有增加患者相关的手术风险以及住院时间,两组患者在手术时间、术中出血量、术后胸引量、住院时间以及术后吻合口瘘的发生率、手术R0切除率等各方面比较无统计学差异(均P>0.05)。经过对比两组患者的术后病理报告,发现加用信迪利单抗进行免疫治疗患者组的MPR高于单纯新辅助化疗组(P<0.05),提示信迪利单抗联合白蛋白紫杉醇及奈达铂在局部晚期食管癌新辅助治疗中缩瘤降期效果良好,临床治疗效果优于单纯的新辅助化疗,但两组患者术后病理评估的无反应相对比无统计学差异(P>0.05),提示仍有少部分病人对新辅助治疗不敏感,在以后的工作中可以将此部分病人进行更深入的研究,以提高新辅助治疗的效果,另外加用信迪利单抗免疫治疗患者术后病理的pCR比例虽然较单纯化疗组高,但仍无统计学差异(P>0.05),考虑为本次研究的总体样本量较少所致。
本研究表明,经过使用信迪利单抗免疫治疗联合白蛋白紫杉醇及奈达铂的新辅助治疗,对局部晚期食管癌患者的临床治疗效果明显,而且患者耐受性良好,未增加明显的化疗不良反应,可以使患者治疗临床获益。但是由于本研究的样本量有限,随访时间较短,而且未进一步统计入组患者的远期预后以及总生存时间,因此在未来的工作中将进一步展开此方面的临床研究,统计相关数据,为评估该方案远期疗效和安全性提供相关依据。
综上所述,在局部晚期可手术切除食管癌患者的新辅助治疗中,信迪利单抗联合白蛋白结合型紫杉醇及奈达铂的免疫治疗联合化疗优于单纯的白蛋白结合型紫杉醇及奈达铂的化疗,没有增加明显的化疗不良反应,而且患者的耐受性良好,提高了客观缓解率和疾病控制率,改善了手术治疗的效果,达到了治疗降期的临床目的,可以在临床治疗中进一步推广使用。

