氨三乙酸配位辅助原位合成Ni@B-HZSM-5对苯和甲醇烷基化反应的影响
蔡 润,代小平,王 琦,冯 博,曹轶华,霍 猛,黄星亮
(中国石油大学(北京) 化学工程与环境学院 重质油国家重点实验室,北京 102249)
苯和甲醇烷基化反应能充分利用产能过剩的苯和廉价的甲醇解决中国对二甲苯产能不足的问题[1]。工业上甲苯歧化反应生成对二甲苯,但也产生相同量的苯[2]。而将苯和甲醇发生烷基化反应加入到二甲苯生产体系中,可消耗甲苯歧化产生的苯,并生成大量的甲苯、二甲苯和少量C9芳烃。其中对二甲苯可从混合二甲苯中分离出来,典型的分离手段包括吸附分离和深冷分离[3-4],但乙苯动力学半径与对二甲苯接近、乙苯凝点低的物化特性导致这两种分离方式效率降低。因此,在生产过程中需要脱除乙苯,但无论是脱乙基反应,还是乙苯异构反应,均导致二甲苯流失[5],故降低产物中乙苯含量至关重要。苯和甲醇烷基化反应的催化剂通常为分子筛,如Beta[6]、MCM-22[7]、Y[8]和ZSM-5[9]分子筛,其中ZSM-5分子筛具有适宜的微孔孔径和丰富的弱酸位,更适合苯和甲醇烷基化反应[10],但以ZSM-5分子筛为催化剂的产物中乙苯含量高,甚至在C8产物中摩尔分数高达40%以上[11],其主要来源于苯和乙烯烷基化反应,而乙烯则由甲醇制烯烃(MTO)反应生成[12-13]。为了改善催化剂性能特别是降低产物中乙苯含量,对ZSM-5分子筛改性成为一种重要的手段,如通过降低B酸与L酸比例抑制催化剂的MTO反应[12]、降低分子筛酸强度以提高稳定性[14-16]、引入加氢能力强的金属将乙烯加氢生成乙烷以降低乙苯含量[17]等。
近年来,通过原位合成将元素引入分子筛的方法受到了研究者的广泛关注[18-20],如直接将硼酸加入初始凝胶中,进而降低分子筛酸强度,提高催化剂选择性[19]。然而有些金属在碱性条件下容易形成难溶的氢氧化物,较难进入分子筛的体相中,往往采用后负载方法引入分子筛;而酸性条件下分子筛晶化时间长,颗粒尺寸大,若以F-为金属矿化剂,具有污染程度大和安全性低的缺点[21]。利用配位作用使金属在碱性条件下形成可溶性配合物可用于合成分子筛,如Yang等[22]以乙二胺四乙酸(EDTA)络合铁离子合成了Silicalite-1分子筛,Fe在分子筛体相中均匀分布,呈单原子状态。相对EDTA,氨三乙酸(NTA)更价廉易得,且该物质可被微生物降解,对环境友好。基于此,笔者利用NTA3-对Ni2+的配位作用,在碱性条件下合成了Ni高分散的B改性ZSM-5分子筛,采用XRD、SEM、TEM、N2吸附-脱附、XRF、Py-IR、NH3-TPD和H2-TPR等对催化剂进行了表征,考察了H3BO3、Ni2+和NTA3-添加对Ni@B-HZSM-5催化剂苯和甲醇烷基化反应性能和稳定性的影响。
1 实验部分
1.1 试剂
氢氧化钠(NaOH),AR,福晨(天津)化学试剂有限公司产品;去离子水,自制;硼酸(H3BO3,AR),偏铝酸钠(NaAlO2,AR),乙酸镍四水合物(Ni(Ac)2·4H2O,AR),均为国药集团化学试剂有限公司产品;氨三乙酸三钠一水合物(Na3NTA·H2O,质量分数99.8%),广州穗欣化工有限公司产品;碱性硅溶胶(质量分数30%,pH=8~10),河南信宜化工有限公司产品;四丙基氢氧化铵(TPAOH,质量分数25%水溶液),北京华威锐科化工有限公司产品;晶种(H-ZSM-5分子筛,n(SiO2)∶n(Al2O3)=276),南京黄马公司产品。除特殊标注外,其余试剂均为分析纯,未经任何处理。
1.2 催化剂制备
(1)xNi@Ba-HZSM-5的制备:以4%Ni@B2-HZSM-5为例,将15 mL水、1120 mg Ni(Ac)2·4H2O、3.095 g Na3NTA·H2O、92.72 mg H3BO3、22.5 g碱性硅溶胶依次加入烧杯中,搅拌10 min得蓝色混合液A。将10 mL水、210 mg NaOH、61.5 mg NaAlO2、6 mL TPAOH溶液、180 mg晶种依次加入烧杯中,搅拌10 min,得混合液B。将A与B混合后搅拌20 min,于70 ℃静置2 h。将混合物投入聚四氟乙烯反应釜密闭,170 ℃晶化36 h。初始凝胶摩尔比为n(SiO2)∶n(Al2O3)∶n(B2O3)∶n(NiO)∶n(TPA+)∶n(OH-)∶n(H2O)∶n(Seed)∶n(NTA3-)=300∶1∶a∶b∶20∶30∶6000∶8∶(2y+3)。其中:a=2;b为3、6、9、12,b对应的Ni摩尔分数(x)为1%、2%、3%、4%(占比SiO2投料)。冷却产物经转速7000 r/min离心10 min后水洗,重复3次,将得到的固体120 ℃烘干,550 ℃焙烧6 h除去模板剂,再以1.0 mol/L的氯化铵溶液于70 ℃离子交换5次后,于120 ℃烘干,550 ℃焙烧6 h得Ni@B-HZSM-5。
(2)HZSM-5与xNi/HZSM-5的制备:HZSM-5的制备与xNi@Ba-HZSM-5相似,除了溶液A不含Ni(Ac)2·4H2O、Na3NTA·H2O和H3BO3,以及仅添加150 mg NaOH。对获得的HZSM-5采用浸渍法制备xNi/HZSM-5,步骤为:将配制好的Ni(Ac)2·4H2O均匀滴加在分子筛上,静置6 h后120 ℃烘干,于500 ℃焙烧6 h获得xNi/HZSM-5,x为摩尔分数1%、2%、3%、4%。
(3)Ba-HZSM-5的制备:Ba-HZSM-5的制备与xNi@Ba-HZSM-5相似,除了溶液A不添加Ni(Ac)2·4H2O,a为2、4,记为B2-HZSM-5或B4-HZSM-5。
1.3 催化剂表征
采用德国蔡司公司Gemini SEM 300型电子显微镜(SEM)和Tecnai G2 F20 场发射透射电子显微镜(TEM)对催化剂形貌进行分析。物相分析在德国D8 Advance型X射线衍射仪上进行。采用TriStar II 3020自动气体吸附仪分析样品比表面积和孔结构。以Panalytical Axios X射线荧光光谱仪(XRF)分析样品元素种类和含量。以Micromeritics公司的Auto Chem Ⅱ 2920型全自动化学吸附仪对样品进行氨气程序升温脱附(NH3-TPD)和氢气程序升温还原(H2-TPR)分析表征。样品的酸量和酸种类采用吡啶红外光谱仪(Thermo Fisher Nicolet IS10)分析。
1.4 催化剂性能评价
将上述粉末催化剂压片后筛分20~40目颗粒,在固定床反应器进行反应性能评价。将2 g催化剂装填至反应管恒温区,以石英棉固定,两端装填10~20目石英砂;在温度460 ℃、压力0.4 MPa、载气H2(LHSV(H2)=3600 h-1)下对催化剂预处理1 h后,苯和甲醇的混合物(n(C6H6)∶n(CH3OH)=1.2∶1)与载气H2混合预热后进入催化剂床层反应,产物用冰水浴冷却。气相产物经气包收集,采用安捷伦7890B色谱离线分析,面积归一化计算得体积分数;液体产物采用鲁南瑞虹化工仪器有限公司SP-6890色谱以氢离子火焰检测器离线分析,色谱柱为DB-wax填料柱,面积归一化计算样品摩尔选择性。苯转化率(XB,%)、甲苯选择性(ST,%)、C8选择性(SC8,%)、C9及以上物质选择性(SC9+,%)、C8产物中乙苯摩尔分数(xEB in C8)的计算方法分别如式(1)~式(5)。
(1)
(2)
(3)
(4)
(5)
式中:nB、nT、nC8、nC9+、nEB分别为各对应物质(苯、甲苯、C8、C9+、乙苯)色谱结果计算的物质的量,mol。
2 结果与讨论
2.1 催化剂的表征结果
图1(a)为HZSM-5、4%Ni/HZSM-5、B2-HZSM-5和4%Ni@B2-HZSM-5的XRD谱图。由图1(a)可知,在22.5°~25.0°均出现了较强的衍射峰,对应MFI拓扑结构,且无其他杂晶,表明合成的是纯相ZSM-5分子筛,与HZSM-5相比,引入Ni、B后对样品的晶相和结晶度没有明显影响。同时,4%Ni@B2-HZSM-5中未发现NiO和含硼物质的衍射峰,表明NiO与含硼物质在分子筛上以无定型形式存在或呈现高分散的状态。图1(b)~(c)为4%Ni@B2-HZSM-5的SEM照片,由图1(b)~(c)可以看出,分子筛棱角减少,表面粗糙,体相之外出现了少量海绵状物质。采用元素能谱扫描(EDS,图1(d)~(h))发现,B、Ni在分子筛表面分布均匀,从断口可看出分子筛体相内含Ni,但海绵状物质上Ni含量较高,分子筛表面Al含量比投料量高而B含量较少,这与其他研究结果相似[23]。
表1为不同催化剂样品的XRF元素分析。由表1可知,Ni、B前驱体投料对分子筛实际硅/铝摩尔比影响不大,而4%Ni@B2-HZSM-5的NiO含量高于投料比例,这是因为更多的硅物种被溶解在母液中。EDS表面元素分析与XRF体相元素分析的Ni含量接近,表明Ni在分子筛体相呈现均匀分布,这主要归因于氨三乙酸与Ni2+在碱性条件下形成了可溶性Ni-NTA配合物,进而阻止了Ni(OH)2沉淀的形成,使得Ni可均匀地引入分子筛体相内。

图1 不同催化剂样品XRD谱图、4%Ni@B2-HZSM-5的SEM照片、摩尔分数及元素分布图Fig.1 XRD patterns of different catalyst products,SEM images,molar fraction and element distribution diagram of 4%Ni@B2-HZSM-5(a)XRD patterns;(b)—(c)SEM images of 4%Ni@B2-HZSM-5;(d)—(h)Element mapping and molar ratio of 4%Ni@B2-HZSM-5

表1 不同催化剂样品的物质摩尔比Table 1 Molar ratio of substances in different catalysts
图2为4%Ni@B2-HZSM-5的TEM照片及EDS元素分布。由图2(a)~(b)可以看到,海绵状物质上有较短且稀疏的晶格条纹,晶格间距为0.216 nm,与NiO(012)晶面接近(PDF#47-1049)[24]。图2(d)~(g)的EDS结果表明,分子筛表层元素分布均匀,但海绵状物质含大量的Si物种,Al和Ni含量比分子筛外表面含量高。已有研究表明,以TPA+为有机模板合成的ZSM-5分子筛体相外部含铝量高,分子筛形成初期,基本单元互相组合形成分子筛的富铝外壳,随后富硅物种填充分子筛外壳,晶体逐渐变成实心[25-26],海绵状物质铝含量比分子筛晶体表面高,其应先于富铝外壳形成,否则铝被外壳消耗,可能是老化前搅拌不均匀导致,因此,海绵状物质为NiO分散的无定形硅铝酸盐。
图3(a)~(b)为各催化剂N2吸附-脱附等温线和孔分布图。可以看出,所考察催化剂均属于Ⅰ和Ⅳ混合型,在p/p0为0.4~0.9之间有滞后环,表明分子筛既有微孔结构也有介孔结构。不同催化剂的BET比表面积和孔体积见表2所示。由表2可知,改性后催化剂比表面积特别是介孔比表面积降低,微孔体积增加,说明原位合成负载和浸渍法负载都会导致催化剂介孔孔道堵塞,且硼有增加分子筛催化剂微孔孔道的能力。图3(c)和表3为催化剂的NH3程序升温脱附曲线和酸性质。可以看出,B的加入未明显影响分子筛NH3脱附峰最高点在397 ℃的强酸强度与酸量,仅大量增加了脱附峰在191 ℃的弱酸量。当B2-HZSM-5中硼含量较低时,硼与铝之间的相互作用较弱,催化剂酸强度未发生明显改变;而当硼含量升高时,携带—OH的硼覆盖了分子筛孔内的Al物种,强酸强度和强酸量降低。浸渍Ni后,4%Ni/HZSM-5催化剂的酸量增大,酸强度加强,说明分子筛外表面聚集的NiO易产生较强的L酸;而4%Ni@B2-HZSM-5的弱酸强度降低,弱酸量略减少,Ni在分子筛内分布较均匀。图3(d)为4%Ni/HZSM-5和4%Ni@B2-HZSM-5的H2程序升温还原图。由图3(d)可知:4%Ni/HZSM-5的H2还原峰对应温度均低于500 ℃,表明浸渍法负载的Ni易被氢气还原;而原位合成的4%Ni@B2-HZSM-5分子筛的H2还原峰分为低温峰(350 ℃)和高温峰(700 ℃),高于500 ℃的还原峰表明Ni与分子筛之间的相互作用较强[27]。低温还原峰对应外表面海绵状物质中少量镍的还原,而高温峰对应分子筛晶体内的镍的还原,从二者的面积可以看出,大部分镍进入分子筛的晶体中。

图2 4%Ni@B2-HZSM-5的TEM照片、元素分布及元素所占摩尔分数Fig.2 TEM images,element distribution and molar fraction of elements of 4%Ni@B2-HZSM-5(a)—(b)TEM images;(c)—(g)Element distribution from TEM-mapping on 4%Ni@B2-HZSM-5
图4和表4分别为各催化剂的Py-IR谱图及依据谱图计算的不同酸种类的酸量。由图4和表4可知:H-ZSM-5与B2-HZSM-5的B酸量明显高于L酸量;硼的加入并未明显影响分子筛的酸种类,仅大量增加了弱B酸,这与NH3-TPD表征结果相似。而当加入Ni后,在1612、1410 cm-1处出现新的吸收峰,吡啶与L酸吸附的吸收峰偏离了1455 cm-1处,硼产生的B酸被NiO携带的L酸代替。

图3 各催化剂BET表面积、孔性质及化学吸附还原图Fig.3 BET surface area,pore properties and chemical adsorption reduction diagram of catalysts(a)N2 adsorption-desorption isotherm;(b)Pore distribution;(c)NH3-TPD profile;(d)H2-TPR profile

图4 不同分子筛催化剂Py-IR谱图Fig.4 Py-IR spectra of different zeolite catalysts
2.2 不同催化剂催化苯与甲醇烷基化反应性能
图5为不同Ni负载量原位合成和浸渍法合成催化剂在2~10 h-1质量空速下对应的苯转化率和C8产物中乙苯选择性。由图5(a)苯转化率可以看出,浸渍Ni的分子筛对应苯转化率均比HZSM-5低2%~7%,但随质量空速的提高,苯转化率降低不明显。而图5(b)中除HZSM-5催化剂乙苯含量随质量空速提高有所降低外,其他催化剂上C8产物中乙苯含量均随质量空速提高有升高趋势。Ni负载量较低时,在较高空速下乙苯含量升高明显,表明催化剂加氢能力不足。图5(c)为原位合成分子筛对应的苯转化率,可以看出,在2~10 h-1质量空速下Ni原位合成的催化剂对应苯转化率均高于40%,且4%Ni@B2-HZSM-5催化剂对应苯转化率达到48%以上。图5(d)为各Ni原位合成分子筛对应乙苯含量,可以看出,在Ni原位合成分子筛催化剂作用下,乙苯随质量空速增加上升趋势较弱,C8中乙苯摩尔分数均低于15%,特别是4%Ni@B2-HZSM-5在空速为2 h-1时低于5%。这主要归因于B为催化剂提供了丰富的弱酸且Ni提供的加氢能力适宜。

表2 不同分子筛催化剂的BET比表面积和孔体积Table 2 BET specific surface area and pore volume of different zeolite catalysts

表3 不同分子筛催化剂的酸性质Table 3 Acid properties of different zeolite catalysts

表4 不同分子筛催化剂的酸量Table 4 Acid amount of different zeolite catalysts
表5为HZSM-5及B、Ni改性分子筛催化苯与甲醇烷基化反应后液体产物与气体产物分布。由表5液体反应产物分布可知,相对于HZSM-5分子筛的苯转化率47.2%,B2-HZSM-5的苯转化率提高至49.3%,但4%Ni/HZSM-5的苯转化率降低至40.0%,4%Ni@B2-HZSM-5分子筛的苯转化率未出现大幅降低的现象,仅略低于HZSM-5,可达46.4%。对于甲苯的选择性则是4%Ni/HZSM-5最高,为64.9%,4%Ni@B2-HZSM-5次之,B2-HZSM-5则低至50.6%。而C8芳烃选择性与甲苯选择性规律相反,B2-HZSM-5的C8芳烃选择性最高,为41.0%,而4%Ni/HZSM-5最低。该反应中苯首先与甲醇生成甲苯,甲苯再甲基化生成C8芳烃中的二甲苯,催化产物苯转化率高且C8芳烃选择性高而甲苯选择性低表明催化剂有较好的活性,因硼为分子筛提供丰富的弱酸,B2-HZSM-5的活性最高,而浸渍Ni会极大降低催化剂的活性。在需要反应程度更深的C9+芳烃选择性中,B2-HZSM-5却比HZSM-5的9.9%低,这说明B2-HZSM-5丰富的弱酸适宜地调节了烷基化的反应深度,4%Ni/HZSM-5与4%Ni@B2-HZSM-5的C9+芳烃选择性相差不大。然而在C8芳烃乙苯摩尔分数中,B2-HZSM-5却仅比HZSM-5的38.5%略低,为35.2%。这说明仅增加弱酸很难降低C8产物乙苯选择性。4%Ni/HZSM-5与4%Ni@B2-HZSM-5的C8产物中乙苯选择性远低于前两者,分别为2.3%和6.1%,表明Ni的加氢作用可明显降低C8产物中乙苯选择性。在C9+芳烃产物中,乙基甲苯、正丙基苯和异丙基苯由乙烯、丙烯参与反应生成,而偏三甲苯和均四甲苯是由苯与甲醇甲基化生成,HZSM-5与B2-HZSM-5前三者占比较高,而4%Ni/HZSM-5与4%Ni@B2-HZSM-5的偏三甲苯、均四甲苯选择性较高。这说明Ni改性的分子筛芳烃与烯烃烷基化的反应被抑制,其原因为烯烃在氢气氛围下被Ni催化加氢饱和从而失去烷基化能力,因4%Ni@B2-HZSM-5偏三甲苯、均四甲苯选择性低于4%Ni/HZSM-5,结合其乙苯选择性略高,说明4%Ni@B2-HZSM-5中Ni的加氢能力适中。本研究也在表6中列出了以上4种样品催化苯与甲醇烷基化的气体产物:HZSM-5与B2-HZSM-5的甲烷体积分数均低于10%,而Ni改性分子筛催化气体产物中甲烷含量比其他样品的高得多,4%Ni/HZSM-5 甚至达94.4%。HZSM-5的气体产物含大量乙烯与丙烯,分别占总体积的49.2%与33.9%,几乎无乙烷与丙烷,这些烯烃会与芳烃烷基化反应生成乙苯、乙基甲苯、正丙基苯和异丙基苯。B2-HZSM-5的气体产物中乙烯与丙烯占比下降,4%Ni@B2-HZSM-5与4%Ni/HZSM-5的烯烃占比都更低,其中4%Ni@B2-HZSM-5的略高,也体现了原位合成分子筛加氢能力的适中。B2-HZSM-5的气体产物中C4+含量较高,可能是因为烷基化反应速率较快,消耗大量的低碳烯烃。4%Ni/HZSM-5的气体产物中烃类物质摩尔分数为4%,计算得到的含碳量约占进料甲醇含碳量摩尔分数的40%,这意味着浪费了大量甲醇;而4%Ni@B2-HZSM-5的气体产物中烃类物质摩尔分数为1.25%。不同Ni负载方式对甲醇利用率有较大差别。研究认为,乙苯含量降低主要是因为乙烯被加氢生成乙烷,无法与苯进行烷基化反应[28]。依此推测本实验中4%Ni/HZSM-5与4%Ni@B2-HZSM-5的气体产物中乙烷含量应与HZSM-5产物乙烯相近,然而二者气体产物中甲烷含量却较高。MTO反应机理认为,芳烃循环和烯烃循环分别主要产生乙烯和丙烯[13],其形成的碳正离子非常稳定,二者很难在本实验条件下再加氢裂化形成甲烷;且密度泛函理论(DFT)计算表明[29],ZSM-5分子筛应用于苯和甲醇烷基化反应时,较难产生甲烷。因此,甲烷很可能是甲醇被Ni吸附后直接加氢形成。4%Ni/HZSM-5催化剂中Ni在HZSM-5表面分布,可推测甲醇在进入分子筛微孔前被消耗,孔内甲醇浓度降低,不仅使苯转化率降低,苯的烷基化程度也降低;而对于4%Ni@B2-HZSM-5,分子筛外表面Ni含量降低,其外表面对甲醇的加氢能力降低,孔内参与烷基化的甲醇浓度更高,并且有丰富的弱酸提高催化剂活性以及部分L酸降低了烯烃生成速率,因此苯转化率更高,烷基化程度更深,乙苯选择性低且有更佳的甲醇利用率。
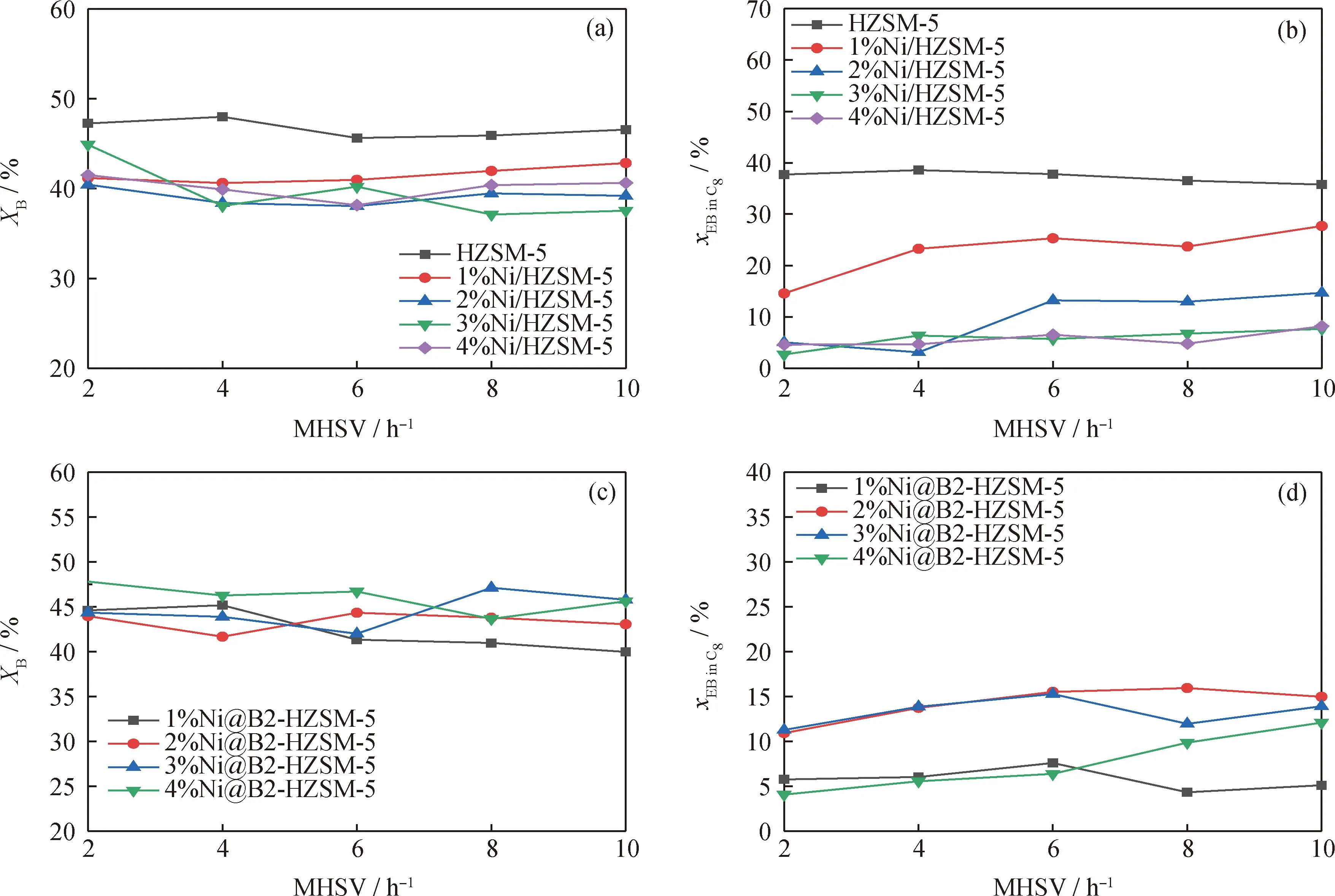
图5 质量空速2~10 h-1下浸渍法和原位合成法制备的不同Ni负载量分子筛催化苯与甲醇烷基化反应性能Fig.5 Reactivity of zeolite catalysts with different Ni loading capacities prepared by impregnation and in-situ synthesis methods under the mass hourly space velocity of 2—10 h-1 for alkylation of benzene with methanol(a)Benzene conversion (XB)of HZSM-5 catalyst with different Ni impregnation amounts;(b)Ethylbenzene molar fraction in C8 aromatics (xEB in C8)of HZSM-5 catalyst with different Ni impregnation amounts;(c)Benzene conversion of HZSM-5 catalyst for in-situ synthesis with different Ni additions;(d)Ethylbenzene molar fraction in C8 aromatics of HZSM-5 catalyst for in-situ synthesis with different Ni additions Reaction conditions: p=0.4 MPa;T=460 ℃;V(H2)/m(Liquid)=1800 mL/g;LHSV(H2)=3600 h-1
综上所述,4%Ni@B2-HZSM-5催化剂在实验范围内具有最佳的苯转化率、液相产物中高的甲苯和C8选择性、低的乙苯选择性,因此可对4%Ni@B2-HZSM-5进一步考察稳定性,并与HZSM-5、B-HZSM-5、4%Ni/HZSM-5稳定性对比。

表5 不同分子筛催化剂上苯与甲醇烷基化反应的性能及液体产物分布Table 5 Properties and liquid product distribution in alkylation of benzene with methanol on different zeolite catalysts

表6 不同分子筛催化剂上苯与甲醇烷基化反应的气体产物分布Table 6 Gas product distribution in alkylation of benzene with methanol on different zeolite catalysts x/%
2.3 催化剂催化苯与甲醇烷基化反应稳定性评价
苯和甲醇烷基化催化剂的稳定性是一个重要参数,通常使用加速失活的方式提高稳定性实验效率[30]。图6为各分子筛催化剂催化苯和甲醇烷基化反应稳定性实验中的苯转化率以及各产物的选择性。图6(a)~(e)为质量空速20 h-1的加速失活实验结果,与表5中质量空速为2 h-1的苯转化率对比可知,质量空速提高至20 h-1时各催化剂的苯转化率有所降低。随反应时间增加,HZSM-5和4%Ni/HZSM-5活性明显降低,在反应时间60 h内苯转化率均快速降低至15%以下,失活严重;B2-HZSM-5稳定性和苯转化率较HZSM-5有一定提升;而B4-HZSM-5苯转化率明显降低至30%以下,这是因为硼添加量过高的催化剂酸强度低且强、酸弱酸比例失调。4%Ni@B2-HZSM-5对应的苯转化率可在反应时间70 h内保持在35%以上。其他研究指出,在460 ℃,对二甲苯、间二甲苯、邻二甲苯的热力学平衡摩尔比为23∶56∶21[31]。以4%Ni/HZSM-5为催化剂时,对二甲苯占二甲苯的摩尔分数在反应前8 h已达到51%,且越来越高,而对二甲苯的动力学半径较小,在分子筛孔径降低时产物中该物质摩尔分数会提高,表明4%Ni/HZSM-5中分子筛微孔孔道被堵塞,而4%Ni@B2-HZSM-5的原位合成方法对分子筛微孔堵塞程度不高。更进一步,Ni/HZSM-5对加氢能力的提升仅限于分子筛体相外,而甲醇经双循环机理生成积炭前驱体烯烃发生在分子筛体相微孔孔道内,虽然从孔内扩散出的烯烃被加氢饱和,但在孔内其仍然快速生成积炭,Ni对反应稳定性提升有限;4%Ni@B2-HZSM-5中Ni分布在分子筛体相内,烯烃生成后被体相内Ni吸附加氢,减缓了积炭生成速率,稳定性大大提升。由图6(e)可以看出,随反应时间延长,4%Ni@B2-HZSM-5对应C8芳烃中乙苯摩尔分数有下降趋势,但4%Ni/HZSM-5对应的乙苯含量有上升趋势,表明4%Ni/HZSM-5的加氢活性降低。图6(f)显示,当进料质量空速为2 h-1时,4%Ni@B2-HZSM-5具有优异的稳定性,对应苯转化率不断提高,在168 h提高至48.4%,但乙苯摩尔分数也持续升高至19.5%,其性能愈来愈接近B2-HZSM-5,这表明催化剂中Ni的加氢能力也在逐渐降低。

图6 各分子筛催化剂催化苯和甲醇烷基化反应稳定性实验的苯转化率(XB)以及各产物的选择性(S)Fig.6 Benzene conversion (XB)and selectivity (S)of each product in the stability experiment of different zeolite catalysts for alkylation of benzene with methanol(a)—(e)Stability of different catalysts under MHSV=20 h-1,p=0.4 MPa,T=460 ℃,LHSV(H2)=3600 h-1;(f)Alkylation stability of 4%Ni@B2-HZSM-5 at MHSV=2 h-1
3 结 论
(1)利用NTA3-与Ni2+的配位作用在碱性条件下原位合成了Ni@B2-HZSM-5分子筛催化剂,结果表明,Ni@B2-HZSM-5分子筛外表面变粗糙,分子筛的MFI结构和结晶度无明显改变,Ni和B分布较均匀,B元素的加入使分子筛的弱B酸量增加,酸强度微弱降低,而Ni的加入会使分子筛产生L酸,Ni@B2-HZSM-5中Ni与分子筛的相互作用强导致还原性有所降低。
(2)Ni/HZSM-5外表面的Ni的强加氢能力使H2与甲醇反应形成大量烷烃,C8芳烃产物中乙苯含量降低,但苯转化率大幅降低;而Ni@B-HZSM-5由于Ni分布较均匀加氢能力适中,添加B和Ni使催化剂具有丰富的弱酸和一定量的L酸。在H2压力0.4 MPa、温度460 ℃和质量空速2 h-1条件下,4%Ni@B2-HZSM-5催化苯和甲醇烷基化反应的苯转化率可达46.4%,稳定运行168 h后乙苯在C8芳烃中摩尔分数仍低于20%,表现出较好的稳定性。

