持续气道正压通气与氨溴索联合治疗新生儿呼吸窘迫综合征的疗效探讨*
邓 波,任亚方
1.方城县妇幼保健院新生儿科,河南 南阳 473200;2.南阳市中心医院新生儿科,河南 南阳 473200
新生儿呼吸窘迫综合征,又称新生儿肺透明膜病,是婴幼儿常发的呼吸道疾病之一,且多发于早产儿群体,胎龄越小,发病率越高,多因肺泡表面生成活性物质过少,使肺泡产生进行性危险所致。在分娩后4~12 h,患儿就会出现发绀、呻吟和进行性呼吸困难等症状,情况严重者甚至会发生呼吸衰竭和呼吸困难,可引发脑损伤,危及患儿生命健康[1]。因此,积极地展开抢救治疗尤为重要。
临床治疗新生儿呼吸窘迫综合征,常采用气管插管和机械通气配合肺表面活性物质来改善患儿呼吸困难的症状,但前者操作较为复杂,且属于介入性创伤操作,容易引发肺气漏和肺部感染等并发症;后者价格昂贵,对一般家庭造成一点的经济压力。故而本研究选择采用持续气道正压通气配合氨溴索展开联合治疗,前者操作简单,并发症发生率低,可有效调节氧浓度,给予充分的呼吸支持;后者可刺激肺泡II型上皮细胞内细胞器发育,加速分泌与合成肺泡表面活性物质,联合使用两药,可有效改善患者的临床症状,促进病情康复,预后结局较好[2]。现将研究结果报告如下。
1 对象与方法
1.1 研究对象
回顾性分析2019 年1 月—2022 年1 月方城县妇幼保健院收治的80 例新生儿呼吸窘迫综合征患者,随机分为两组,每组各40 例。观察组:男22 例,女18 例;胎龄27~36 周,平均胎龄(33.64±3.68)周;出生体质量(1.40~2.65)kg,平均体质量(1.73±0.46)kg。对照组:男21例,女19 例;胎龄27~36 周,平均胎龄(33.64±3.68)周;出生体质量(1.44~2.32) kg,平均体质量(1.73±0.46)kg。本研究经院伦理委员会批准通过,两组患者基线数据具有可比性(P>0.05)。
纳入标准:家属知情同意,愿意参与研究;符合《2019 版欧洲新生儿呼吸窘迫综合征防治指南》[3]对新生儿呼吸窘迫综合征的诊断标准,有导致肺泡表面活性物质匮乏、急性发病、呼吸窘迫、氧合指数低于200 mmHg(1 mmHg=0.133 kPa)、肺动脉楔压低于18 mmHg,X 线检查显示特异性表现。
排除标准:合并凝血功能障碍,合并心房颤动、严重心动过速等影响P 波改变的情况,合并严重感染,合并神经功能障碍。
1.2 方法
所有患儿均给予保温、生命体征监护、呼吸道管理、抗感染、纠正水电解质失衡等对症支持治疗,保证液体和营养供应,稳定患儿内环境,改善机体微循环和营养状况。对照组:给予持续气道正压通气治疗:采取INFANT FLOW SYSTEM 型呼吸机治疗,选择符合患儿的鼻塞,参数设置:呼气末正压保持在4~8 cmH2O,流速维持在6~10 L/min,吸氧浓度保持在25%~40%,临床医师可根据血气分析结果和患儿个体病情,合理地调整呼吸机参数。吸氧浓度小于30%,并且保持正常的血气水平,观察患儿反应,若未发生呼吸窘迫或窒息现象,可撤离呼吸机。观察组:在对照组的基础上加用氨溴索治疗,用量用法:每6 h 给药1 次,1 次注射7.5 mg/kg,在呼吸道症状缓解后减少剂量,坚持治疗3~5 d。
1.3 观察指标
比较两组患儿临床效果(显效:发绀、呻吟和进行性呼吸困难等临床症状消失,有效:临床症状得到显著改善,无效:临床症状无变化)、血气水平[包括动脉氧分压(PaO2)、动脉二氧化碳分压(PACO2)、氧合指标(OI)]、肺功能指标[采取德国格莱特Geratherm 肺功能仪检测吸气分数(IC/TLC)、第1 秒最大呼气容积(FEV1)1 秒率(FEV1/FVC)]、治疗情况(呼吸机使用时间、用氧时间、呼吸暂停次数、住院时长)、RC 评分[采用COPD 呼吸困难评分(MRC)评价患者的主观呼吸困难情况,0 级:除了剧烈活动以外,无明显呼吸困难;1 级:仅在爬坡或平地快走的时候伴有气短出现;2 级:在平地行走的时候比同龄人慢或每走100 m 就需要停下呼吸;4级患者出现穿脱衣服时气短,或伴有明显的呼吸困难无法离开房间,0 级为1 分,1~2 级为1 分,3 级为2 分,4 级为3 分,分数越低说明呼吸困难症状越轻。BRMS 评分躁狂评分,PSQI 睡眠评分分数越高相关情况越差]、并发症(呼吸机相关性肺炎、口咽部不适、肺气漏)。
1.5 统计学方法
采用SPSS 21.0 软件进行统计分析。计量资料以均数±标准差(±s)表示,组间比较采用t 检验。计数资料以例数和百分比(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者疗效情况
治疗后,观察组(95.00%)治疗有效率显著高于对照组(77.50%),差异有统计学意义(χ2=5.165,P<0.05)。
2.2 两组患儿治疗前后血气水平情况
治疗后,观察组患儿的PaO2和OI 显著高于对照组,PaCO2显著低于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组患儿治疗前后血气水平情况(±s) mmHg
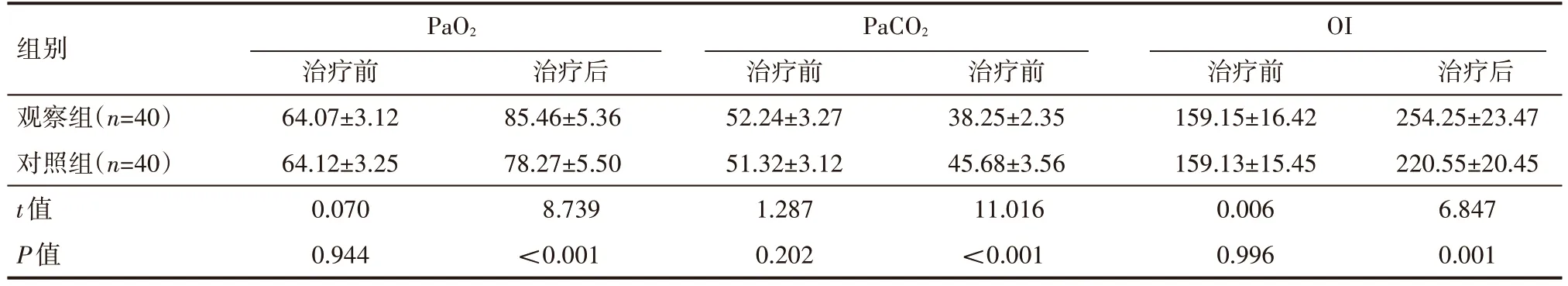
表1 两组患儿治疗前后血气水平情况(±s) mmHg
组别PaO2 PaCO2观察组(n=40)对照组(n=40)t值P值治疗前64.07±3.12 64.12±3.25 0.070 0.944治疗后85.46±5.36 78.27±5.50 8.739<0.001治疗前52.24±3.27 51.32±3.12 1.287 0.202治疗前38.25±2.35 45.68±3.56 11.016<0.001 OI治疗前159.15±16.42 159.13±15.45 0.006 0.996治疗后254.25±23.47 220.55±20.45 6.847 0.001
2.3 两组患儿各项治疗情况
治疗后,观察组呼吸机使用时间、用氧时间、呼吸暂停次数和住院时间均少于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患儿各项治疗情况(±s)

表2 两组患儿各项治疗情况(±s)
组别观察组(n=40)对照组(n=40)t值P值呼吸机使用时间(h)94.85±30.35 125.00±50.22 3.287 0.002用氧时间(h)75.04±29.39 103.59±48.48 3.185 0.002呼吸暂停次数(次)4.04±1.09 8.58±2.49 10.564<0.001住院时长(d)12.49±5.68 21.35±6.80 6.324<0.001
2.4 两组患者治疗前后肺功能水平情况
治疗后,观察组的IC/TLC、FEV1、FEV1/FVC 高于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组患者治疗前后肺功能水平情况(±s) %
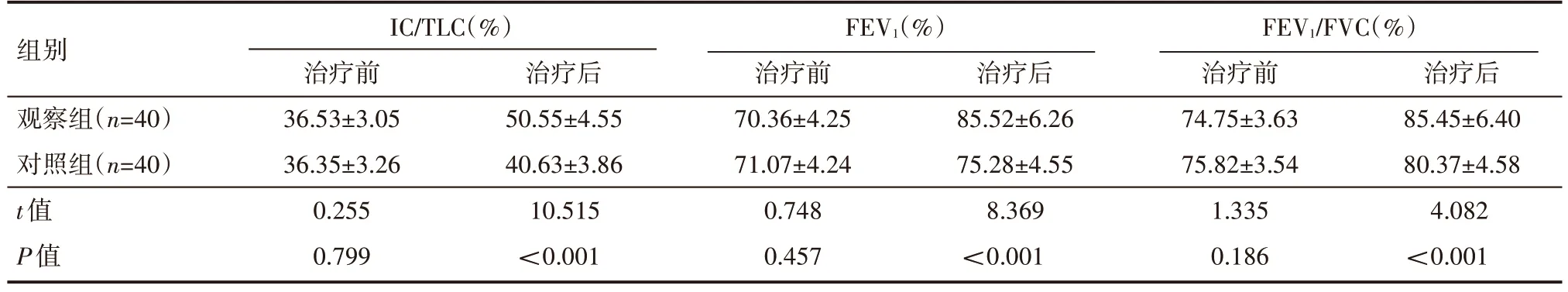
表3 两组患者治疗前后肺功能水平情况(±s) %
组别观察组(n=40)对照组(n=40)t值P值IC/TLC(%)治疗前36.53±3.05 36.35±3.26 0.255 0.799治疗后50.55±4.55 40.63±3.86 10.515<0.001 FEV1(%)治疗前70.36±4.25 71.07±4.24 0.748 0.457治疗后85.52±6.26 75.28±4.55 8.369<0.001 FEV1/FVC(%)治疗前74.75±3.63 75.82±3.54 1.335 0.186治疗后85.45±6.40 80.37±4.58 4.082<0.001
2.5 两组患者治疗前后康复评分情况
治疗后,观察组的MRC 评分、BRMS 评分和PSQI 评分低于对照组,差异有统计学意义(P<0.05),见表4。
表4 两组患者治疗前后康复评分情况(±s) 分
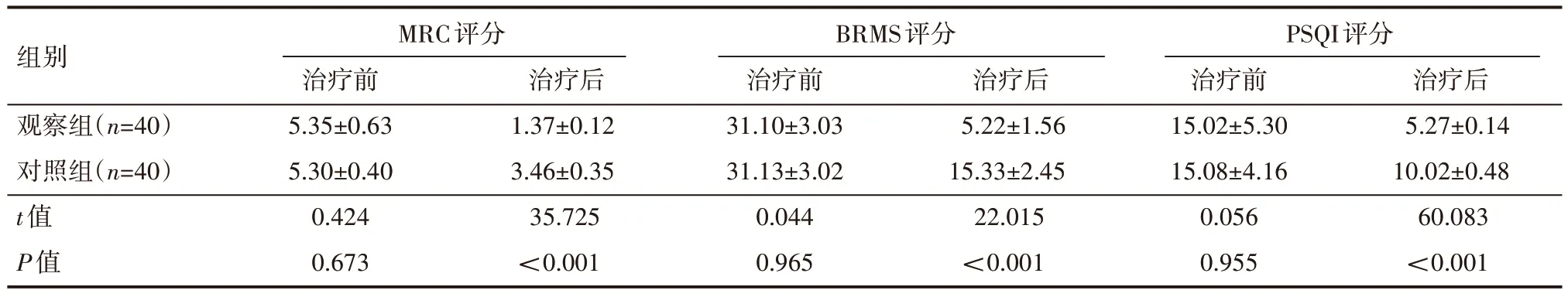
表4 两组患者治疗前后康复评分情况(±s) 分
组别观察组(n=40)对照组(n=40)t值P值MRC评分治疗前5.35±0.63 5.30±0.40 0.424 0.673治疗后1.37±0.12 3.46±0.35 35.725<0.001 BRMS评分治疗前31.10±3.03 31.13±3.02 0.044 0.965治疗后5.22±1.56 15.33±2.45 22.015<0.001 PSQI评分治疗前15.02±5.30 15.08±4.16 0.056 0.955治疗后5.27±0.14 10.02±0.48 60.083<0.001
2.6 两组患者并发症发生情况
干预后,观察组(2.50%)并发症发生率低于对照组(17.50%),差异有统计学意义(χ2=5.000,P<0.05)。
3 讨论
新生儿呼吸窘迫综合征是临床常发的儿科疾病之一,病理机制复杂多变,剖宫产、母体糖尿病、围产期窒息和早产等均是诱发此病的独立危险因子。多因肺泡表面活性物质匮乏,导致呼气时肺泡塌陷,使得抑制功能残气量增高,诱发进行性肺不张,情况严重者可继发呼吸衰竭等严重症状[4]。通常来说,新生儿呼吸窘迫症患儿在出生后的4~12 h,就会伴有典型的临床表现,如吸气性三凹征、发绀和进行性呼吸困难,如未及时发现给予有效干预,病情还会进一步加重。有研究[5]显示,新生儿呼吸窘迫综合征的病理学机制与患儿体内肺表面活性物质过少存在密切关系。新生儿呼吸窘迫综合征是新生儿和早产儿病死的危重因素。因此,积极采取治疗干预尤为关键。
由于新生儿呼吸窘迫症患儿的呼吸中枢发育不成熟,导致自主呼吸浅表和不规则,呼吸肌容易发生疲劳,从而引发频繁的呼吸暂停。这种呼吸暂停具体指的是早产儿呼吸停止时间大于20 s,足月儿呼吸停止时间大于15 s,又或者呼吸停止时间不超过15~20 s,普遍伴有肌肉张力下降、皮肤苍白或青紫,心跳缓慢等症状[6]。临床调查[7]报告显示,国内的新生儿呼吸暂停发病率普遍较高,约23%,其中低出生体重患儿的发病率,高达90%;情况严重的还会反复发作心动过缓和低氧血症,如果处理不及时,很有可能引发脑白质软化和脑缺氧缺血性损害。故而,临床治疗本病时,通常给予无创通气治疗帮助患儿维持正常呼吸,再配合各类抗炎、抗感染和纠正水电解质失衡等对症支持疗法,普遍可获得一定的治疗效果,但由于本病的病理机制在于肺泡表面活性物质匮乏,因此,仍需加用相关治疗药物,若单独开展无创通气疗法难以获得全面良好的效果[8]。
本研究结果表明,持续气道正压通气治疗帮助本病患儿在呼气末维持肺泡正压,预防肺泡塌陷,拓展肺泡面积,维持功能残气量,减少肺内分流,改善血流和通气比例,提高肺顺应性,改善氧合功能,减少吸氧量,增加肺表面释放活性物质,预防视网膜发生病变和支气管肺发育不良[13]。氨溴索是一种新型黏液溶解剂,可激活呼吸道黏膜浆液腺和肺泡II型上皮细胞内细胞器,使其快速分泌和合成肺泡表面活性物质,高特异性作用于肺组织,以此促进肺成熟,预防肺泡萎缩[14]。氨溴索可以激活活性蛋白基因的表达,加速合成表面活性蛋白,迅速增加内源性肺表面活性物质,减轻肺表面张力,加大肺通气量,提高肺顺应性和潮气量。联合上述两药,可迅速改善患儿的氧合指数,缩短氧疗时间和住院时间,减少因缺血、缺氧引发的肺损伤,维护机体细胞膜,改善呼吸困难症状,促进患者快速康复。
综上所述,以持续气道正压通气联合氨溴索治疗新生儿呼吸窘迫症患者,可有效减轻其临床症状,调控血气水平,缩短治疗时间,改善肺功能水平,促进患者康复,不良并发症少,安全有效。

