新型环糊精衍生物HPn-SBEm-β-CD动物血管给药的生物效应评价
王晖,陈乘,周成梁,余书勤
(南京师范大学生命科学学院,江苏省医药超分子材料及应用重点实验室,江苏南京 210046)
环糊精(cyclodextrin,CD)系淀粉经环糊精葡聚糖转位酶酶解环合后得到的由6~15个葡萄糖分子连接而成的环状低聚糖天然产物[1-3],常见的有 α -、β -和γ-CD,使用最为广泛的是β-CD。但由于其溶解度小、溶血作用强、非肠道给药不仅刺激性强还具有明显的肾毒性,因此,只适合口服而不能用于非肠道给药[4]。为了克服天然β-CD环糊精的缺点,一系列β-CD环糊精衍生物被合成。作为药用辅料,环糊精衍生物(CDD)具有增加药物的溶解度及稳定性、提高药物的生物利用度、控制药物的释放速率等优点,应用越来越广泛,其中2个重要的衍生物分别是羟丙基-β-环糊精(HP-β-CD)和磺丁基醚-β-环糊精(SBE-β-CD)[5],二者均具有水溶性好、肾毒性低、溶血作用小及局部刺激性轻微等特点。
本实验室新合成的环糊精衍生物HPn-SBEm-β-CD是以羟丙基和磺丁基混合取代的环糊精衍生物,研究人员期望其在理化性质、性能和安全性方面均优于HP-β-CD和SBE-β-CD。已有实验证明,其溶解性好,包合药物能力较强,有极好的应用前景,但安全性值得关注。本实验主要研究HPn-SBEm-β-CD经血管给药后对红细胞的毒性和对动物的神经精神系统、心血管和呼吸系统的影响。
1 材料与方法
1. 1 材料
1.1.1 实验动物 (1)昆明种小鼠,体重18~22 g,雌雄各半,由东南大学医学院实验动物中心提供,饲养温度22~26℃,小鼠饲养3 d后使用。(2)Beagle犬由苏州西山中科实验动物有限公司提供。(3)健康新西兰大白兔由东南大学医学院实验动物中心提供,体重约2.0 kg。实验前对所有动物称重并观察进食量、一般行为表现以确认受试动物健康。
1.1.2 药物与试剂 不同取代度的 HPn-SBEm-β-CD由江苏省医药超分子材料与应用重点实验室合成;盐酸氯丙嗪注射液(北京永康制药厂);β-CD、SBE7-β-CD(TCI,日本);HP-β -CD、M-β -CD(南京德宝生化器材有限公司);戊巴比妥钠(上海化学试剂公司分装),戊二醛溶液(Sigma,美国),其余试剂均为国产分析纯。
1.1.3 仪器 低温离心机(Centrifuge 5417R型,德国Eppendorf),扫描电子显微镜(JSM-5610LV型,日本电子公司),离心沉淀机(LDZ5-2型,北京医用离心机厂),可见紫外分光光度计(UV-2450,日本岛津),恒温水浴锅(常州国华电器有限公司),六光道SYS-I型小鼠自发活动测定仪(自制),RM-6000型多导生理记录仪(日本光电);WDT-204型自动平衡记录仪(上海大华仪表厂)。
1. 2 方法
1.2.1 HPn-SBEm-β-CD 的溶血试验[6]取新鲜兔血10 ml置于洁净三角瓶中,玻璃棒搅拌10 min去除纤维,加入约20倍生理盐水置于离心机中,以1500 r·min-1离心3 min,除去上清液,如此反复洗涤直到上清液澄清为止。将制备的红细胞以生理盐水配制成5%(V/V)悬浮液。
由于 β-CD溶解度差,故浓度梯度设为1、6、12 mmol·L-1,而11 种不同取代度的 HPn-SBEm-β -CD、HP-β -CD、SBE7-β -CD 浓度梯度设为1、6、12、25、35 mmol·L-1,红细胞与各种环糊精在37℃下振摇作用 30 min,冷却,以 2 500 r·min-1离心 5 min,取上清液于λ=543 nm处测定紫外吸收值,溶血百分率的计算公式如下:溶血百分率=(A受试物-A阴性对照)/A阳性对照×100%
1.2.2 扫描电镜观察HPn-SBEm-β-CD对红细胞形态的影响 观察方法参照文献[7]。红细胞悬液制备方法同溶血试验。本实验选取HP3-SBE2-β-CD作为受试物,M-β-CD为对照。将配好的两种环糊精溶液与红细胞悬液以1∶1混合,使其终浓度都分别为10、5和2.5 mmol·L-1,然后37 ℃ 水浴。1 h后将各管中的液体以1 500 r·min-1离心 5 min,弃上清,PBS 洗两遍。各管中分别加入适量的2.5%戊二醛溶液,于4℃ 固定12 h以上。PBS洗两遍,将红细胞重悬到适当浓度进行细胞涂片,之后进行30%、50%、60%、70%、80%、90%、100%乙醇梯度脱水,每步10 min。样品片剪为大小合适的小片,黏附于载物台上镀金,扫描电镜观察。
1.2.3 HPn-SBEm-β-CD 对小鼠神经精神系统的影响[8-9](1)对小鼠一般行为的影响。取小鼠40只,随机分为4组,即HP4-SBE3-β-CD 3个剂量组(80、160、320 mg·kg-1)和对照组;观察各给药组在静脉注射给药后小鼠的行为表现、姿势、步态、被毛、饮食、大小便、眼、黏膜、瞳孔等变化。(2)对小鼠自主活动次数的影响。取健康小鼠,预选5 min内活动次数在220~320之间的共50只,随机分为5组,即空白对照组、阳性对照组(氯丙嗪 2 mg·kg-1)、HP4-SBE3-β -CD 3 个剂量组(80、160、320 mg·kg-1)。静脉注射给药,用六光道自发活动仪分别记录给药后即刻、30、60、120及180 min的小鼠5 min内的自主活动次数。
1.2.4 HPn-SBEm-β-CD 对麻醉犬呼吸系统及心血管系统的影响[9]取Beagle犬24只,随机分为4组,即空白对照组和HP4-SBE3-β-CD 3个剂量组(40、80、160 mg·kg-1)。以戊巴比妥钠 40 mg·kg-1腹腔注射麻醉后,背位固定,右颈总动脉插管连接TP-101型压力换能器记录收缩压(SAP)舒张压(DAP)及平均动脉压(MAP);针形电极刺入皮下记录Ⅱ导联心电图(ECG);气管插管连接呼吸换能器,记录呼吸频率及幅度。术后稳定20 min,用多导生理记录仪记录上述各项指标,作为给药前基础值。然后静脉注射给药后30、60、120及180 min时记录上述各项指标,观察呼吸频率、幅度及心电、心率和血压的变化。
1. 3 统计学处理
2 结 果
2. 1 HPn-SBEm-β -CD 的溶血试验
本实验以 β-CD 、HP-β-CD 、SBE7-β-CD 为对照,进行溶血试验。结果表明:在测试浓度下,所有化合物的溶血性均远远小于β-CD;多数化合物的溶血性小于对照品 HP-β-CD;化合物HP2-SBE3-β-CD、HP1-SBE4-β-CD、HP3-SBE6-β-CD 等的溶血性小于SBE7-β -CD;少量化合物在浓度 >25 mmol·L-1时溶血性大于HP-β-CD。见图1~3。
2. 2 红细胞形态变化
扫描电镜结果显示,5 mmol·L-1和10 mmol·L-1的HP3-SBE2-β -CD 对红细胞形态无影响,2.5 mmol·L-1的M-β-CD使红细胞形状发生了改变,而且细胞浓度降低,而5 mmol·L-1的M-β-CD完全破坏了细胞膜的完整性,几乎看不到正常的红细胞形态。见图4。

图1 HP-β-CD、HP1-SBE4-β-CD、HP2-SBE3-β-CD、HP3-SBE6-β-CD、SBE7-β-CD溶血性试验结果Fig 1 Hemolytic activity results of HP-β -CD,HP1-SBE4-β -CD,HP2-SBE3-β -CD,HP3-SBE6-β -CD,SBE7-β -CD

图2 β-CD、HP-β-CD、HP5-SBE3-β-CD、HP4-SBE2-β-CD、HP4-SBE3-β-CD、HP2-SBE2-β-CD溶血性试验结果Fig 2 Hemolytic activity results of β -CD,HP-β -CD,HP5-SBE3-β -CD,HP4-SBE2-β -CD,HP4-SBE3-β -CD,HP2-SBE2-β -CD
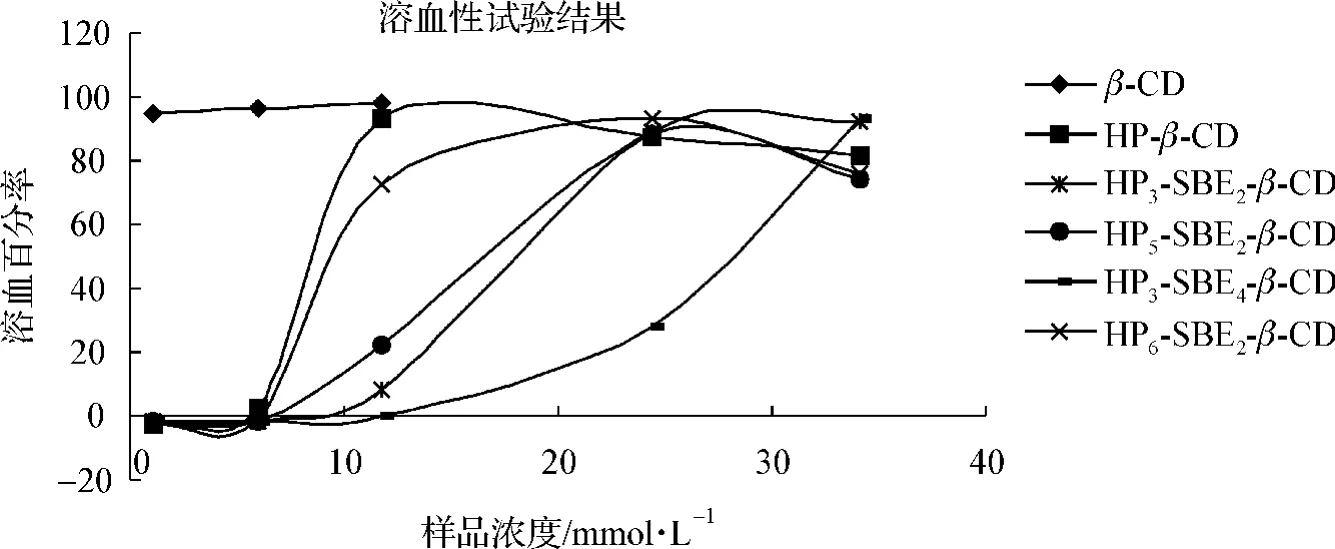
图3 β-CD、HP-β-CD、HP3-SBE2-β-CD、HP5-SBE2-β-CD、HP3-SBE4-β-CD、HP6-SBE2-β-CD溶血性试验结果Fig 3 Hemolytic activity results of β -CD,HP-β -CD,HP3-SBE2-β -CD,HP5-SBE2-β -CD,HP3-SBE4-β -CD,HP6-SBE2-β -CD

图4 扫描电镜观察各种环糊精作用下兔血红细胞的形态Fig 4 Effects of different CD on morphological changes of RBC by SEM
2. 3 HP4-SBE3-β-CD对小鼠神经精神系统的影响
2.3.1 对小鼠一般行为的影响 小鼠分别静脉注射80、160 及 320 mg·kg-1HP4-SBE3-β -CD 后,其行为表现、活动姿势、被毛、饮食、大小便、黏膜、瞳孔均未见异常,与对照组比较差异无统计学意义(P>0.05),表明HP4-SBE3-β-CD对小鼠一般行为无明显影响。
2.3.2 对小鼠自发活动次数的影响 小鼠分别静脉注射 80、160 及320 mg·kg-1HP4-SBE3-β -CD 后,其自发活动次数各时间点与对照组比较差异无统计学意义(P >0.05),给予氯丙嗪(2 mg·kg-1)的小鼠自发活动次数与对照组比较,差异有统计学意义(P<0.05),表明HP4-SBE3-β-CD对小鼠自发活动无明显影响。见表1。
表1 HP4-SBE3-β-CD对小鼠自发活动的影响Tab 1 Effects of HP4-SBE3-β-CD on spontaneous action of mouse次·(5 min)-1

表1 HP4-SBE3-β-CD对小鼠自发活动的影响Tab 1 Effects of HP4-SBE3-β-CD on spontaneous action of mouse次·(5 min)-1
与对照组比较,a P >0.05,b P >0.05
组 别 n用药后不同时间自发活动10 316±46 277±46 225±55 187±24 170±36 HP4-SBE3-β -CD 组80 mg·kg-1 10 319±50 246±79a 225±38a 179±20a 166±45a 160 mg·kg-1 10 289±43 227±70a 207±63a 181±40a 150±48a 320 mg·kg-1 10 296±43 248±59a 206±56a 193±41a 146±53a氯丙嗪组 10 302±75 57±40b 16±20b 22±19b 25±28 30 min 60 min 120 min 180 min对照组用药前自发活动b
2. 4 HP4-SBE3-β-CD对麻醉犬呼吸及心血管系统的影响
2.4.1 对呼吸系统的影响 分别静脉注射40、80、160 mg·kg-1的 HP4-SBE3-β -CD 后,各时间点麻醉犬的呼吸频率、幅度与对照组比较差异无统计学意义(P>0.05),用药后与用药前比较差异也无统计学意义(P>0.05),表明 HP4-SBE3-β-CD 对麻醉犬呼吸系统无明显影响。见表2。
表2 HP4-SBE3-β-CD对麻醉犬呼吸的影响(n=6)Tab 2 Effects of HP4-SBE3-β -CD on the respiratory system of anesthetical dogs(n=6,)

表2 HP4-SBE3-β-CD对麻醉犬呼吸的影响(n=6)Tab 2 Effects of HP4-SBE3-β -CD on the respiratory system of anesthetical dogs(n=6,)
与对照组比较,a P >0.05;与用药前比较,b P >0.05
组 别 用药前呼吸频率/次·min-1 用药后不同时间呼吸频率/次·min-1 30 min 60 min 120 min 180 min对照组 17.8 ±5.60 16.7 ±6.09 18.3 ±5.85 19.5 ±5.92 20.0 ±5.25 HP4-SBE3-β -CD 组40 mg·kg-1 19.5 ±3.67 20.5 ±5.17ab 20.7 ±3.72ab 19.3 ±4.23ab 20.0 ±5.25ab 80 mg·kg-1 18.5 ±6.41 20.3 ±5.50ab 19.7 ±6.05ab 19.8 ±6.99ab 21.3 ±7.94ab 160 mg·kg-1 18.0 ±4.24 19.0 ±3.46ab 19.7 ±2.73ab 20.8 ±3.81ab 20.3 ±2.94ab组 别 用药前呼吸幅度/mm 用药后不同时间呼吸幅度/mm 30 min 60 min 120 min 180 min对照组 14.2 ±1.33 14.8 ±0.76 13.5 ±0.84 13.2 ±1.47 14.0 ±1.09 HP4-SBE3-β -CD 组40 mg·kg-1 13.3 ±1.50 14.8 ±1.83ab 14.8 ±2.04ab 14.3 ±1.21ab 14.7 ±2.06ab 80 mg·kg-1 13.54 ±1.76 14.5 ±1.76ab 14.3 ±1.86ab 14.8 ±1.16ab 15.0 ±1.90ab 160 mg·kg-1 13.5 ±2.73 14.2 ±2.32ab 13.8 ±1.94ab 14.0 ±1.90ab 14.2 ±2.14ab
2.4.2 对心血管系统的影响 分别静脉注射给予40、80、160 mg·kg-1HP4-SBE3-β -CD 后,各时间点麻醉犬的心电、心率和血压与对照组比较差异无统计学意义(P>0.05),用药后与用药前比较差异也无统计学意义(P>0.05),表明 HP4-SBE3-β-CD 对麻醉犬心血管系统无明显影响。见表3~5。
表3 HP4-SBE3-β-CD对麻醉犬心电图的影响(n=6,x±s)Tab 3 Effects of HP4-SBE3-β -CD on ECG of anesthetical dogs(n=6,)
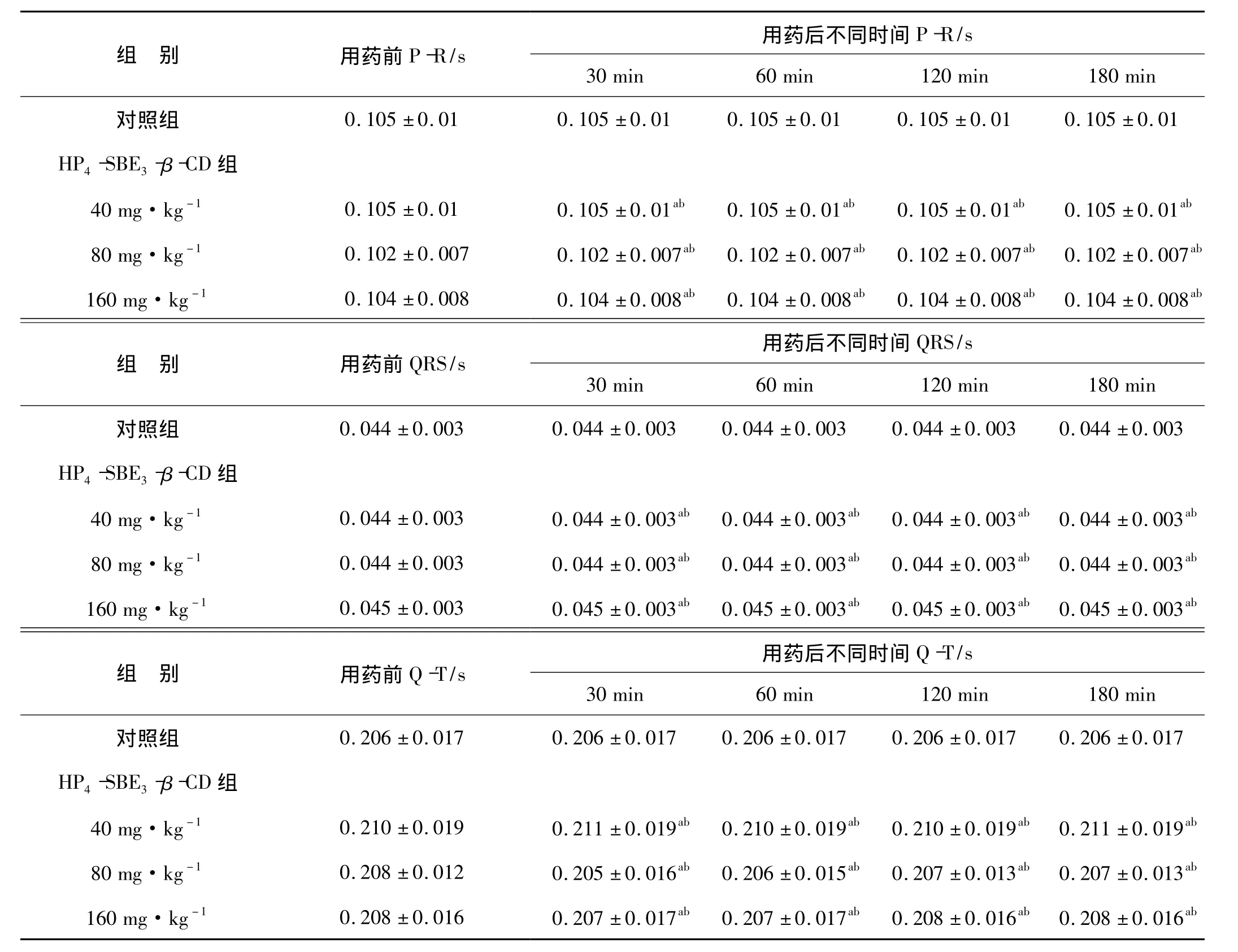
表3 HP4-SBE3-β-CD对麻醉犬心电图的影响(n=6,x±s)Tab 3 Effects of HP4-SBE3-β -CD on ECG of anesthetical dogs(n=6,)
与对照组比较,a P >0.05;与用药前比较,b P >0.05
组 别 用药前P-R/s 用药后不同时间P-R/s 30 min 60 min 120 min 180 min对照组 0.105 ±0.01 0.105 ±0.01 0.105 ±0.01 0.105 ±0.01 0.105 ±0.01 HP4-SBE3-β -CD 组40 mg·kg-1 0.105 ±0.01 0.105 ±0.01ab 0.105 ±0.01ab 0.105 ±0.01ab 0.105 ±0.01ab 80 mg·kg-1 0.102 ±0.007 0.102 ±0.007ab 0.102 ±0.007ab 0.102 ±0.007ab 0.102 ±0.007ab 160 mg·kg-1 0.104 ±0.008 0.104 ±0.008ab 0.104 ±0.008ab 0.104 ±0.008ab 0.104 ±0.008ab组 别 用药前QRS/s 用药后不同时间QRS/s 30 min 60 min 120 min 180 min对照组 0.044 ±0.003 0.044 ±0.003 0.044 ±0.003 0.044 ±0.003 0.044 ±0.003 HP4-SBE3-β -CD 组40 mg·kg-1 0.044 ±0.003 0.044 ±0.003ab 0.044 ±0.003ab 0.044 ±0.003ab 0.044 ±0.003ab 80 mg·kg-1 0.044 ±0.003 0.044 ±0.003ab 0.044 ±0.003ab 0.044 ±0.003ab 0.044 ±0.003ab 160 mg·kg-1 0.045 ±0.003 0.045 ±0.003ab 0.045 ±0.003ab 0.045 ±0.003ab 0.045 ±0.003ab组 别 用药前Q-T/s 用药后不同时间Q-T/s 30 min 60 min 120 min 180 min对照组 0.206 ±0.017 0.206 ±0.017 0.206 ±0.017 0.206 ±0.017 0.206 ±0.017 HP4-SBE3-β -CD 组40 mg·kg-1 0.210 ±0.019 0.211 ±0.019ab 0.210 ±0.019ab 0.210 ±0.019ab 0.211 ±0.019ab 80 mg·kg-1 0.208 ±0.012 0.205 ±0.016ab 0.206 ±0.015ab 0.207 ±0.013ab 0.207 ±0.013ab 160 mg·kg-1 0.208 ±0.016 0.207 ±0.017ab 0.207 ±0.017ab 0.208 ±0.016ab 0.208 ±0.016ab
表4 HP4-SBE3-β-CD对麻醉犬心率的影响(n=6,)Tab 4 Effects of HP4-SBE3-β -CD on heart rate of anesthetical dogs(n=6,x±s) 次·min-1

表4 HP4-SBE3-β-CD对麻醉犬心率的影响(n=6,)Tab 4 Effects of HP4-SBE3-β -CD on heart rate of anesthetical dogs(n=6,x±s) 次·min-1
与对照组比较,a P >0.05;与用药前比较,b P >0.05
用药后不同时间心率组.2 190.0 ±18.8 HP4-SBE3-β -CD 组40 mg·kg-1 188.8 ±18.2 188.2 ±19.2ab 189.3 ±22.6ab 188.5 ±23.2ab 190.0 ±19.1ab 80 mg·kg-1 187.5 ±18.5 194.5 ±18.9ab 198.3 ±18.9ab 195.8 ±18.8ab 197.8 ±18.7ab 160 mg·kg-1 185.3 ±22.1 187.3 ±23.8ab 188.5 ±21.4ab 190.7 ±19.2ab 188.8 ±18.0 30 min 60 min 120 min 180 min对照组 187.3 ±10.6 185.72 ±14.9 191.3 ±20.2 192.7 ±18别用药前心率ab
表5 HP4-SBE3-β-CD对麻醉犬血压的影响(n=6,x±s)Tab 5 Effects of HP4-SBE3-β -CD on blood pressure of anesthetical dogs(n=6,) mmHg

表5 HP4-SBE3-β-CD对麻醉犬血压的影响(n=6,x±s)Tab 5 Effects of HP4-SBE3-β -CD on blood pressure of anesthetical dogs(n=6,) mmHg
与对照组比较,a P >0.05;与用药前比较,b P >0.05注:1 mmHg=0.133 kPa
用药后不同时间收缩压30 min 60 min 120 min 180 min对照组 145.5 ±15.6 144.0 ±13.8 144.7 ±18.2 144.0 ±19.2 144.0 ±18.3 HP4-SBE3-β -CD 组40 mg·kg-1 148.3 ±15.0 147.5 ±15.8ab 145.8 ±16.3ab 147.2 ±18.6ab 147.7 ±20.2ab 80 mg·kg-1 144.7 ±15.5 148.0 ±15.5ab 150.3 ±15.9ab 149.7 ±14.9ab 148.7 ±13.4ab 160 mg·kg-1 146.0 ±14.8 144.3 ±17.2ab 148.0 ±13.3ab 149.5 ±13.2ab 149.3 ±12.8ab组 别 用药前舒张压 用药后不同时间舒张压30 min 60 min 120 min 180 min对照组 104.8 ±10.6 102.5 ±11.7 103.7 ±13.0 101.8 ±14.4 102.5 ±14.1 HP4-SBE3-β -CD 组40 mg·kg-1 104.0 ±9.4 103.3 ±11.1ab 101.8 ±12.7ab 101.8 ±11.8ab 100.2 ±15.1ab 80 mg·kg-1 103.0 ±10.6 103.3 ±10.6ab 105.5 ±12.2ab 104.7 ±9.4ab 104.7 ±10.2ab 160 mg·kg-1 101.5 ±9.3 99.3 ±11.7ab 100.0 ±9.0ab 103.7 ±9.8ab 102.3 ±10.4ab组 别 用药前收缩压用药后不同时间平均动脉压30 min 60 min 120 min 180 min对照组 121.3 ±12.7 117.8 ±11.3 119.5 ±16.4 118.2 ±17.4 119.2 ±17.2 HP4-SBE3-β -CD 组40 mg·kg-1 120.5 ±11.5 120.3 ±12.6ab 119.0 ±14.1ab 119.2 ±15.0ab 115.3 ±14.5ab 80 mg·kg-1 119.2 ±11.2 120.5 ±12.7ab 122.2 ±13.6ab 120.7 ±12.3ab 121.3 ±11.4ab 160 mg·kg-1 119.0 ±11.8 116.2 ±12.8ab 117.8 ±11.1ab 119.2 ±11.3ab 119.7 ±11.4ab组 别 用药前平均动脉压
3 讨 论
环糊精作为药用辅料应用越来越广泛,非肠道应用其安全性是首要考虑的因素。目前研究比较多的是HP-β-CD和 SBE-β-CD,两者的安全性比其他 CDD要可靠。
很多报道[10-14]认为,环糊精特别是甲基化环糊精的毒性来自于其能溶解细胞膜上磷脂、胆固醇等分子,引起细胞膜成分耗竭,以致细胞死亡,而且溶血程度与溶解胆固醇程度相一致[15]。HPn-SBEm-β-CD引入了羟丙基和磺丁基两种基团,二者是能够有效降低母体环糊精溶血作用的亲水性基团,本研究结果显示,各种取代物的溶血性都低于β-CD,也低于常用的药物赋形剂 HP-β -CD,部分取代物(HP2-SBE3-β -CD、HP1-SBE4-β -CD、HP3-SBE6-β -CD)溶血性低于 SBE7-β -CD。结果表明溶血性与羟丙基和磺丁基取代度直接相关:当磺丁基的取代度≤2时表现出较大的溶血性;当磺丁基的取代度≥2.5时,溶血性显著降低;当总取代度为4~7,其中磺丁基取代度为3~3.5时溶血性最低。同时扫描电镜结果显示,HP3-SBE2-β-CD对红细胞形态影响明显低于M-β-CD,说明HPn-SBEm-β-CD耗竭细胞膜成分的能力弱,对细胞膜毒性小。
本研究结果表明,HPn-SBEm-β-CD对受试动物呼吸系统和心血管系统无影响,显示样品无活性。本实验的HPn-SBEm-β-CD具有适度的平均分子质量,如总取代度=5且溶血作用显著低于HP5-β-CD的HP1-SBE4-β -CD、HP2-SBE3-β -CD 和 HP3-SBE2-β -CD的平均分子量范围为1 571~1 730,远低于SBE7-β-CD的2 089~2 264平均分子量。这对控制制剂中赋形剂使用量有重要而实际的意义。综上所述,本实验的HPn-SBEm-β-CD毒性低,具有极好的应用前景。
[1]SEZJTLI J.Introduction and general overview of cyclodextrin chemistry[J].Chem Rev,1998,98(5):1743-1753.
[2]MARTIN E M.Cyclodextrins and their uses:a review[J].Pocess Biochemisrty,2004,39(9):1033-1046.
[3]ALBERS E,MULLER B W.Cyclodextrin derivatives in pharmaceutics[J].Crit Rev Ther Durg Carrier Syst,1995,12(4):311-337.
[4]谢伯泰,杨国武,谢薇梅.羟丙基-β-环糊精特性及其在医药领域中的应用与安全性[J].国外医药:合成药、生化药、制剂分册,2002,23(5):302-306.
[5]潘雪梅,房德敏.羟丙基-β-环糊精和磺丁基醚-β-环糊精应用进展[J].天津药学,2005,17(5):59-61.
[6]国家药品监督管理局.中药注射剂研究的技术要求,中药新药研究的技术要求[S].1999.
[7]LISANTI M P,TANG Z,SCHERER P E,et al.Caveolae purification and glycosylphosphatidylinositol-linked protein sorting in polarized epithelia[J].Methods Enzymo,1995,250(1):655-668.
[8]徐叔云.药理实验方法学[M].2版.北京:人民卫生出版社,1991:641.
[9]卫生部药政司.新药(西药)临床前研究指导原则汇编1993,42.
[10]FAUVELLE F,DEBOUZY J C,CROUZY S,et al.Mechanism of α -cyclodextrin-induced hemolysis.1.The two-step extraction of phosphatidylinositol from the membrane[J].Pharm Sci,1997,86(8):935-943.
[11]GNIADECKI R.Depletion of membrane cholesterol causes ligand-independent activation of fas and apoptosis[J].Biochem Biophys Res Commun,2004,320(1):165-169.
[12]IRIE T,OTAGIRI M,SUNADA M,et al.Cyclodextrin-induced hemolysis and shape changes of human erythrocytes in vitro[J].Pharmacobiodyn,1982,5(9):741-744.
[13]MOTOYAMA K,TOYODOME H,ONODERA R,et al.Involvement of lipid rafts of rabbit red blood cells in morphological changes induced by methylated β -cyclodextrins[J].Biol Pharm Bull,2009,32(4):700-705.
[14]OHTANI Y,IRIE T,UEKAMA K,et al.Differential effects of α -,β -and γ -cyclodextrins on human erythrocytes[J].Eur J Biochem,1989,186(1-2):17-22.
[15]IRIE T,UEKAMA K.Pharmaceutical applications of cyclodextrins Ⅲ.Toxicological issues and safety evaluation[J].Pharm Sci,1997,86(2):147-162.

