高纯度2-羟基对苯二甲酸的合成新技术
金宁人,谢品赞,张建庭,孙 刚,胡燕红,赵德明
(1浙江工业大学化学工程与材料学院,浙江 杭州 310032;2鼎龙化工集团公司,浙江 杭州 310005)
研究开发
高纯度2-羟基对苯二甲酸的合成新技术
金宁人1,谢品赞1,张建庭1,孙 刚1,胡燕红2,赵德明1
(1浙江工业大学化学工程与材料学院,浙江 杭州 310032;2鼎龙化工集团公司,浙江 杭州 310005)
系统地研究了以间羟基苯甲酸(HBA)为原料、经改进的Koble-Schmitt法常压合成2-羟基对苯二甲酸(HTA)的新工艺及其精制方法,并与2-溴对苯二甲酸(BTA)催化水解法制备HTA技术进行了比较。结果表明:以HBA为原料,甲酸钾为溶剂,在碳酸钾存在下,反应温度为230~240 ℃时,CO2常压羧化反应6 h制得纯度约90%的HTA粗品,采用二次酸碱精制法可使HTA质量达聚合级单体的水平(纯度>99.5%,金属离子<50 mg/kg),总收率56%以上。产品经FT-IR和MS表征确认。该技术具有常压反应、操作方便、产品质量优异、经济性良好及易于产业化等优点,能为进一步合成羟基改性的新型高性能材料及新单体提供原料。
2-羟基对苯二甲酸;甲酸钾;改进的Koble-Schmitt法;常压羧化;间羟基苯甲酸
2-羟基对苯二甲酸(HTA)作为BB型聚合单体可应用于高性能纤维材料——聚对亚苯基苯并二唑(PBX)的改性,利用其羟基产生的氢键和表面极性,改进材料的轴向抗压和复合黏结性能[1]。基于浙江工业大学研究团队关于AB型聚合单体的研究[2-3],发现HTA在实现有序聚合物用AB型新单体制备等方面有潜在的应用前景,如羟基改性的聚对亚苯基苯并二口恶唑(PBO)和聚对苯二甲酰对苯二胺(PPTA)等,合成路线设计见式(1)和式(2)。此外,HTA作为重要有机中间体,在医药和功能材料等方面也具有一定应用价值[4]。相比于大宗产品对苯二甲酸(TPA),HTA的制备国内外大都处于实验室规模研究,至今仍没见工业化生产和商品报道,因此对于HTA的合成及其有价值的产业化路线研究具有非常重要的意义。
HTA的制备有半合成法和化学合成法,其中半合成法仅由 Ruppen等[5]首先采用对苯二甲酸生物野生型菌株制备得到 1,2-二羟基-3,5-二烯-1,4-环己二甲酸,然后再用化学法即在稀硫酸中加热脱去 1位羟基生成HTA,属生物与化学合成的结合,见式(3)。而化学合成法制备HTA国外研究较多,国内鲜见报道,涉及的方法有:采用氨基对苯二甲酸二甲酯皂化水解、重氮后再酸性水解法[6-7];2-羟基对二甲苯先羟基保护后氧化再脱保护的甲基氧化法[8-9];对苯二甲酸二甲酯的酯基和羟基苯腈的氰基水解法[10];溴代对苯二甲酸(BTA)催化水解法[11];(三氟甲基)羟基苯甲酸CO2的高压羧化法[12];间羟基苯甲酸(HBA)在SiO2存在下的CO2高压羧化法[13]。有关上述各种方法的优缺点分析详见文献[4]。
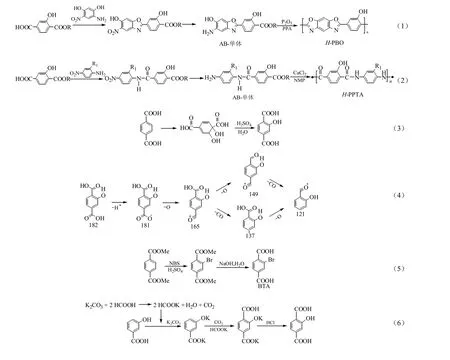
本文在文献 [4]基础上,选择其中的BTA催化水解路线(1)和HBA的CO2羧化法路线(2)进行 HTA合成的研究(图 1),旨在寻找生产条件许可且经济的HTA生产工艺,从而达到实用及产业化之目的,尤其是常压羧化反应新技术。

图1 2-羟基对苯二甲酸HTA的主要合成路线
1 实验部分
1.1 试剂和药品
3-羟基苯甲酸(HBA),99%的工业品;溴代对苯二甲酸(BTA,自制品)、甲酸(85%)、铜粉、K2CO3、NaOH、NaHCO3、盐酸、NaHSO3、氨水(25%)及活性炭等,均为化学纯或分析纯。
1.2 仪器
IR用FTIR Nicolet-6700型红外光谱仪(美国Thermo公司)KBr压片测定;DECAX-60000LCQ Deca XP 液相色谱-离子阱质谱仪(美国Thermo公司);S2型原子吸收分光光度计(美国热电)测定HTA中金属离子含量;WRS-1A 型数显熔点仪;P-230型液相色谱仪(大连依利特)用于测定产品HTA及原料的HPLC纯度。
1.3 实验过程
1.3.1 2-溴对苯二甲酸催化水解法
100 mL四口烧瓶中,依次加入纯度为95.6%的自制BTA 0.89 g(3.6 mmol)、0.87 g NaOH(21.8 mmol)、0.10 g铜粉(1.6 mmol)和16.6 mL水,搅拌、加热升温至100 ℃回流反应11.5 h(TLC控制反应时间),待反应液冷却后滤去铜粉,滤液在搅拌下滴加10%盐酸酸析,抽滤、水洗、干燥得0.42 g水解物,HPLC纯度96.65%,收率63.27%。熔点314~322 ℃(文献值315~319 ℃[11]),FTIR结果见图2(a)。
1.3.2 间羟基苯甲酸CO2羧化法
(1)羧化溶剂HCOOK制备 500 mL四口烧瓶中加入140.3 g K2CO3(1.015 mol)和70 mL H2O搅拌均匀,滴加110.0 g HCOOH(85%,2.03 mol),加毕升温至回流搅拌反应1 h,减压蒸馏脱水至釜温200 ℃以上,冷却后即为甲酸钾(熔点 167~170℃)。
(2)CO2羧化法合成 HTA 将以上制得的HCOOK升温至180 ℃以上,在有效搅拌下,一次性加入80.0 g HBA(0.579 mol),通CO2,并于180~190 ℃分批缓慢(0.5~1.0 h)加入 96.0 g K2CO3(0.695 mol),加毕升温至230 ℃,在CO2存在下搅拌反应6 h,待冷却至60 ℃,缓慢加入到0.1% NaHSO3热水溶液500 mL中,搅拌至全溶后滴加浓盐酸调节pH值至中性,加入活性炭脱色过滤,滤液用浓盐酸调pH=1~2,经过滤、水洗、干燥得101.6 g粗产物HTA,粗品收率96.3%。
(3)HTA的精制 将所得粗品HTA 加入7.5倍水(质量比),搅拌下用浓氨水中和至中性,待完全溶解后,加入活性炭脱色吸附过滤,滤液用浓盐酸调pH=1~2,冷却后过滤,滤饼再用300 mL 10%盐酸打浆洗涤,过滤水洗后得到折干70 g 的HTA一次精制品(HPLC纯度96.8%,K+376 mg/kg),总收率 66.4%;再经同样方法二次精制,110 ℃干燥后得到HTA的聚合级单体62.1 g(HPLC纯度99.7%,金属离子K+21 mg/kg、Na+8 mg/kg),熔点314~317 ℃,以HBA计总收率58.9%。FTIR结果见图2(b),质谱MS详见图4。
2 结果与讨论
2.1 物质的定性
2.1.1 羟基对苯二甲酸的鉴定和分析
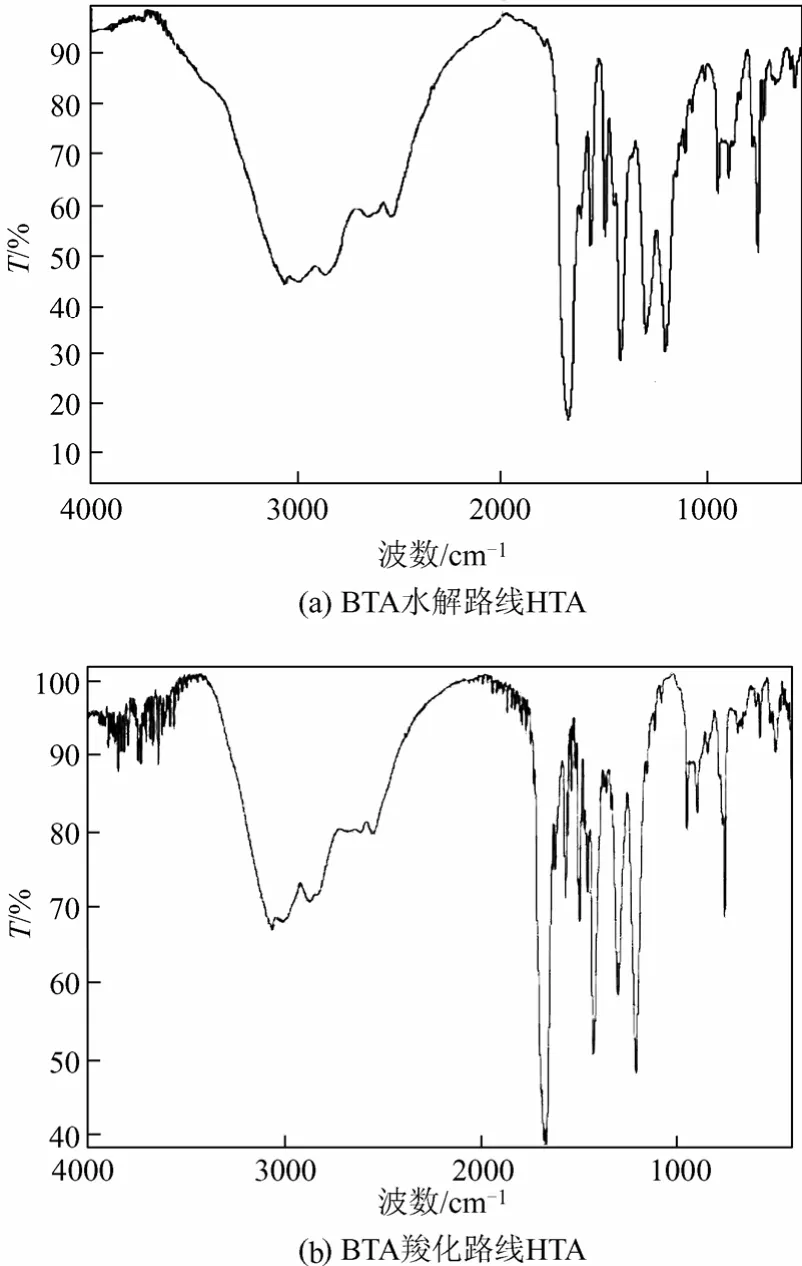
图2 2-羟基对苯二甲酸HTA的红外图谱
(1)红外IR剖析及定性 HTA无标准红外可参照,本研究由不同原料BTA和HBA分别水解和羧化路线制备的产物其红外吸收相同[见图 2(a)和图2(b)],首先说明产物是同一物质。选择图1(a)对产物进行 IR归属剖析可知:①羟基已形成,在2500~3100 cm-1出现一个宽而散的吸收峰,是由羧酸形成分子间氢键使羟基伸缩振动吸收峰向低频方向移动所致,而1207 cm-1为C—O伸缩振动和酚O—H弯曲振动耦合,由此可见BTA水解路线的溴被羟基亲核取代已完全;②1678 cm-1处出现羧羰基的伸缩振动吸收峰也是向低频方向移动的结果,且属于二缔合体;因此结合文献[14]邻位羟基酸大部分以二聚体形式存在的推断,BTA水解路线的产物以二分子 HTA氢键缔合体的形式存在(图3),当然HBA羧化路线产物也以二缔合体存在,且与HTA的分子结构相符。
(2)质谱MS剖析及定性 首先由HBA羧化路线合成 HTA的质谱图(图 4)数据[M+]的m/z180.9879推断其相对分子质量为181.9958,与HTA相对分子质量的理论值182.1324误差为-0.075%,故相对分子质量完全相符;同样对BTA水解路线合成的 HTA粗品在精制后进行质谱分析,测得的数据[M+]m/z181.0(质谱图略)与图4的数据[M+]m/z180.9879相一致而属同一种物质,再次证明图2(a)和图2(b)红外分析为同一物质HTA的正确性。其次由图4离子碎片峰数据又完全符合式(4)所推断的碎片离子峰形成的机理,亦可证实。
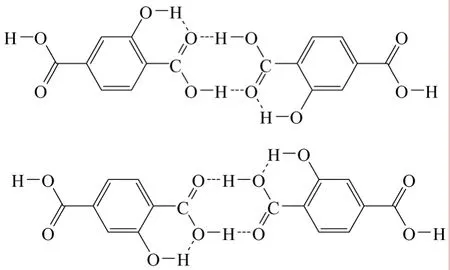
图3 二缔合体形式的HTA
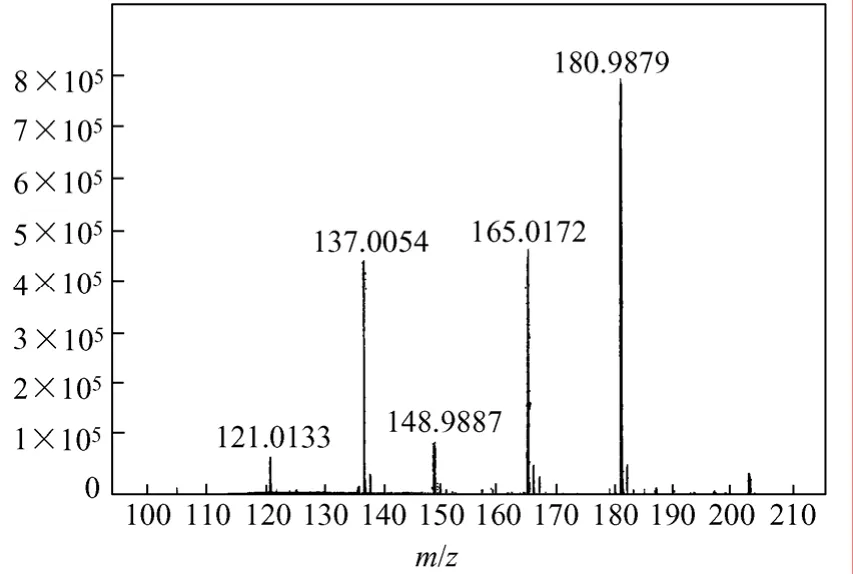
图4 HBA羧化路线HTA质谱图
这样,由质谱及其裂解碎片均进一步确证产物为羟基对苯二甲酸(HTA)。可见,本文研究的HBA常压羧化法制备HTA的合成新工艺是有效的,可进一步发展成更经济实用的合成新技术。
2.2 HTA合成技术分析及比较
2.2.1 2-溴对苯二甲酸催化水解法探索及分析
BTA催化水解合成HTA技术借鉴唯一的早期文献[11],针对BTA钠盐在碱性溶液中铜粉催化下水解反应3天制备HTA的低产能状况。本研究对其工艺进行部分改进,在n(BTA)∶n(NaOH)∶n(Cu)=1∶6∶0.43时进行BTA的羟基取代反应,仅需11.5 h就可制得纯度为97.65%、熔点314~322℃的HTA产品,但收率仅为63.27%。
虽然本文探索的 BTA催化水解技术其反应时间已比文献大大缩短,但由于其所用原料BTA价格高,再加上BTA原料分子在产品分子中的原子利用率理论值仅为67.8%,使此路线制备的HTA十分昂贵;即使采用式(5)对苯二甲酸二酯NBS溴化[15]后水解法自行制备和合成,又由于实际收率太低(粗品也只有42.1%),使 BTA生产成本已远高于HBA的价格而缺乏实用价值。可见,BTA催化水解制 HTA的经济性差可能是至今尚无产业化的主要障碍,不宜作为产业化研究的路线及进一步研发的选择。应重点对HBA羧化路线进行深入的工艺研究。
2.2.2 间羟基苯甲酸CO2羧化法
对比BTA催化水解法,HBA羧化法合成HTA的明显优势在于原料HBA分子在产品HTA中的原子利用率理论值高达100%,其价格又比BTA低得多,且操作简单、收率高等。文献[13]涉及的HBA羧化法是在高温高压下操作,因此,关键是如何将高压的操作降至常压或低压以及探讨如何使得产品达聚合级质量标准的精制技术。
(1)常压下羧化工艺初探 依据Koble-Schmitt法的CO2羧化机理,原料HBA必须先生成酚钾盐后才能进入羧化反应[见式(6)],要生成酚钾盐的条件是:所用碱K2CO3与HBA的摩尔比需大于或等于1.0。为此需对羧化工艺进行探索,在HBA投料为25.0 g(0.181 mol),对K2CO3用量和高温溶剂甲酸钾用量的摩尔比n(K2CO3)∶n(HCOOK)∶n(HBA)以及高温常压CO2羧化进行初步试验,制得HPLC纯度85%~90%的HTA,结果见表1。
由表1看出, 以甲酸钾为高温溶剂CO2羧化完全可在常压下进行;在n(K2CO3)∶n(HBA)= (1.0~1.5)∶1,n(HCOOK)∶n(HBA)=(3~5)∶1的体系中通入CO2常压230~260 ℃反应1~3 h,即可方便制得收率65%以上纯度为85%~90%的HTA粗品(实验编号 2~4);而实验编号 1的收率明显降低是受羧化温度低于 190 ℃影响所致。这比HBA在烃类溶剂中3.0~5.5 MPa的CO2高压羧化法[13]具有更安全、设备常规、无需SiO2助催化且更易产业化等优点。较好工艺条件为:n(K2CO3)∶n(HBA)=1.2∶1,n(HCOOK)∶n(HBA)=3.5∶1,羧化温度230~240 ℃,反应时间3.5 h。相应的粗品收率高达92.6%(实验编号3);相应的条件下做了5批重复实验,粗品平均收率为90.2%(平均纯度为87.8%),精制后的总收率50%以上(纯度为99.5%以上)。
HTA是在HCOOK为溶剂K2CO3存在下制备的,因此导致粗产品中含有大量的钾离子(5000~15000 mg/kg),其次还由于CO2和原料仅在表面反应,反应液黏稠及HBA在甲酸钾溶剂中溶解性差、颗粒内部反应不完全及高温反应副产物多等不利因素所致。可见,要达到HTA作为单体使用的聚合级指标(纯度>99%,金属离子<50 mg/kg)要求,必须研究HTA有效的精制技术。
(2)HTA的精制提纯技术及应用 采用酸碱精制方法,对两种不同的精制工艺,即直接酸析洗涤法[精制工艺(1)]和单钾盐重结晶法[精制工艺(2)]对表1实验3制得的HTA粗品进行精制提纯的比较实验,结果见表2。
由表2数据可见:工艺(1)精制1次所得产品HTA的纯度只有97.2%,要达聚合级纯度还必须进行第2次精制才能达到99.5%及以上。虽然精制总收率仅58.2%,产品损失大,但它对迅速降低K+含量效果非常显著,每次精制均可降低金属离子20~40倍[见精制工艺(1)中精制次数为 1和 2的数据]。这是由于使用氨水中和没有引入外加的金属离子所致,此外盐酸洗涤更有助于洗去溶于盐酸的有机杂质。
而选用工艺(2)对HTA粗品进行精制,其精制收率高达81%以上,纯度已完全满足聚合级要求,但产品中的钾离子仍高达数千上万(10 000 mg/kg),对降低离子含量基本无效。主要是精制过程加入额外的金属K离子及其HCl中的H+置换K+不完全、水洗不到HTA晶体颗粒内部等因素所致。但是单钾盐重结晶法对提高纯度是十分有效的,一次精制即可将纯度提高至99.6%。
可见两种精制工艺各有优缺点,关于精制方法的选择还与HTA的用途有关:若HTA用于高聚物的合成,以采用精制工艺(1)的直接酸析洗涤技术,并对HTA粗品进行二次精制,使其纯度和K+含量均达到大于 99.5%和小于 50 mg/kg聚合级指标要求;若HTA用于有机合成,作为制备AB型单体的中间体[式(1)、式(2)],则以纯度和收率为主(K+含量可不考虑),显然应选择提纯效果好收率高的单钾盐重结晶法精制工艺(2)且只需精制1次其纯度就可达99.5%以上。

表1 K2CO3、高温溶剂及羧化条件初探

表2 HTA精制方法试验及比较
(3)适于产业化的羧化工艺确定及建议 为确定合适的羧化工艺并应用于产业化,选择扩大投料量3.2倍的80.0 g HBA、96.0g K2CO3和110.0g HCOOH与 140.3 g K2CO3制得的 HCOOK,即n(K2CO3)∶n(HCOOK)∶n(HBA)=1.2∶3.5∶1.0,反应温度 230~240 ℃,在强化搅拌下对羧化反应时间进行单因子的实验,并用精制工艺(1)连续对羧化粗品进行精制2次操作,结果见表3。
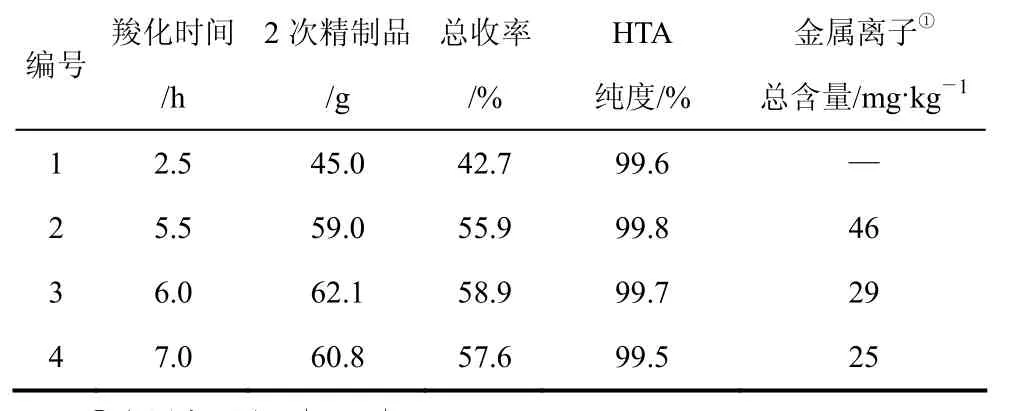
表3 CO2羧化反应时间的影响
由表3可见,在强化搅拌效果后延长其羧化时间至5.5~7.0 h、连续精制2次后均可达到99.5%以上纯度和金属离子小于50 mg/kg的聚合级HTA,总收率56%~59%,并以6.0 h为佳。时间过长导致收率略下降(对比实验编号3和编号4),可能由于高温产生的副反应增加所致,但影响不大(也可归于实验误差的范围);而时间过短收率低(实验编号 1)则反应不完全,主要是羧化反应仅发生在与CO2接触的HBA二钾盐表面之不利所致。
由于HBA价廉易得且其分子利用率高,经表3中实验2~4合成聚合级HBA总收率56%的核算,CO2羧化法的经济性良好,具有产业化发展前景。加上研究的HCOOK溶剂代替文献[13]烃类溶剂进行降低压力至常压的CO2羧化新技术,操作更安全,唯一不足就是反应过程存在明显的放大效应。为此,从产业化角度考虑使用研发的新技术,必须解决工业羧化反应器的搅拌及其釜内的结构设计,以增加反应物的表面与CO2气体的接触,并减少反应中结块现象、缩短羧化时间。建议最好是经过中试或干冰(固体CO2)取代气体CO2的改进研究后实施产业化,而 230~240 ℃反应温度的反应器加热形式可在远红外加热或导热油加热中选择。
3 结 论
成功开发了以间羟基苯甲酸为原料,二氧化碳常压羧化合成羟基对苯二甲酸的新工艺及其精制方法,产品经IR和MS等表征定性确认,其质量达聚合级水平、总收率56%以上。该工艺具有避开高压、操作方便、经济性良好及易于产业化等特色,明显好于2-溴对苯二甲酸催化水解法技术,为进一步合成羟基改性的新型高性能材料及其新单体等研究提供技术及原料基础。
(1)以甲酸与碳酸钾反应脱水至 200 ℃以上制得甲酸钾高温溶剂,然后在碳酸钾存在下 HBA于 230~240 ℃,经改进的 Koble-Schmitt法进行CO2常压羧化、反应6 h制得HTA粗品,纯度88%~91%,具有溶剂制备简便、反应常压进行且易控制等优点。
(2)采用氨水溶解、活性炭吸附脱色、滤液直接酸析稀盐酸洗涤的精制技术,对HTA粗品进行连续二次精制,使HTA纯度达99.5%以上、K+和Na+含量<50 mg/kg聚合级指标要求,二次精制总收率 58%以上,直接用于高聚物合成;而采用 HTA单钾盐重结晶后盐酸酸化的精制技术,精制一次就可达99.5%以上的高纯度,但HTA中的金属离子难以去除,由于精制收率高,用于有机合成及AB型单体的制备有效。
[1]Tang Y H,Tsai M H,Wu C C,et al. Electronic properties of heterocyclic aromatic hydroxyl rigid-rod polymers[J].Polymer,2004,45:459-465.
[2]金宁人,胡晓锋,赵德明,等. 4-(5-氨基-6-羟基-2-苯并口恶唑基) 苯甲酸的合成[J]. 化工进展,2009,28(2):316-319,333.
[3]金宁人,张建庭,赵德明,等. 4-(5-氨基-6-羟基-2-苯并口恶唑基) 苯甲酸盐的合成、性能及应用[J]. 化工学报,2008,59(10):2680-2686.
[4]张建庭,赵德明,金宁人,等. 多羟基对苯二甲酸类化合物的合成与应用研究进展[J]. 应用化学,2010,27(11):1241-1251.
[5]Ruppen M E,Hagedorn S. 1,2-Dihydroxy-3,5-cyclohexadiene-1,4-dicarboxylic acid and a method for its preparation;preparation of 2-hydroxy-1,4-benzenedicarboxylic acid: US, 5068414[P]. 1991-11-26.
[6]Guadarrama P,Fomina L,Fomine S. Solid-supported synthesis of hyperbranched polymer withβ,β-diethynylstyryl units[J].Polymer International,2001,50(1):76-83.
[7]Bolton O,Kim J. Design principles to tune the optical properties of 1,3,4-oxadiazole-containing molecules[J].Journal of Materials Chemistry,2007,17(19):1981-1988.
[8]查代军,陈义旺,谌烈,等. 含空间位阻侧链取代炔烃的合成及其催化聚合[J]. 催化学报,2007,28(8):737-742.
[9]Hahn S W,Yun Y K,et al. Thermotropic hyperbranched polyesters prepared from 2-[(10-(4-hydroxy-phenoxy)decyl)oxy]terephthalic acid and 2-[(10-((4'-hydroxy-1,1'-biphenyl-4-yl)oxy)decyl)oxy]terephthalic acid[J].Macromolecules,1998,31(19):6417-6425.
[10]Wessely I F,Grossa M. Reactions of vanillin and isovanillin o-quinol acetates[J].Monatshefte Fuer Chemie,1966,97(2):570-578.
[11]Miura Y,Torres E,Panetta C A,et al. Electroactive organic materials. Preparation and properties of 2-(2'-hydroxyethoxy)-7,7,8,8-tetracyano-p-quinodimethane[J].Journal of Organic Chemistry,1988,53(2):439-440.
[12]Hauptschein M,Nodiff E A,Saggiomo A J. Trifluoromethyl derivatives of hydroxybenzoic acids and related compounds[J].Journal of the American Chemical Society,1954,76:1051-1054.
[13]Henkel,Cie G H. Hydroxyterephthalic acid: GB,1109828[P]. 1968-04-18.
[14]谢晶曦. 红外光谱在有机化学和药物化学中的应用[M]. 北京:科学出版社,1987:200,291.
[15]Suzuki H,Nomura M. Production of dialkyl 2-bromo-and/or 2,5-dibromoterephthalate:JP,11279123[P]. 1999-10-12.
Synthesis of high-purity 2-hydroxyterephthalic acid
JIN Ningren1,XIE Pinzan1,ZHANG Jianting1,SUN Gang1,HU Yanhong2,ZHAO Deming1
(1College of Chemical Engineering and Materials Science,Zhejiang University of Technology,Hangzhou 310032,Zhejiang,China;2Dragon Chemicals Group Company,Hangzhou 310005,Zhejiang,China)
2-hydroxyterephthalic acid(HTA)was synthesized by modified Koble-Schmitt atmospheric carboxylation method. and refined. The new synthesis method was compared with 2-bromoterephthalic acid(BTA)catalytic hydrolysis. The results showed that crude product HTA with purity of 90% was prepared from HBA by CO2atmospheric carboxylation for 6 h at 230—240 ℃ in the presence of K2CO3and potassium formate solvent,and purified through two times acid-alkali refining to obtain polymerization-grade HTA with high-purity of 99.5 % and metal ions of below 50 mg/kg,total yield of above 56%(base on HBA). The prepared HTA was identified by FT-IR and MS,and the process had the advantages of atmospheric carboxylation,convenient operation,excellent product quality,good economy and easy commercialization. The prepared HTA could provide the raw material for new high-preformance materials modified with hydroxy group and new monomers.
2-hydroxyterephthalic acid(HTA);potassium formate solvent;modified Koble-Schmitt method;atmospheric carboxylation;3-hydroxybenzoic acid(HBA)
TQ 246.3
A
1000-6613(2011)08-1789-07
2011-01-19;修改稿日期2011-04-19。
江苏省科技攻关重大项目(BE 2006077)。
及联系人:金宁人(1954—),男,教授。E-mail cnhzjnrh@mail.hz.zj.cn。

