β-咔啉肟酯类化合物的合成及其抑菌活性
卢少莹, 张耀谋
(华南农业大学 理学院,广东 广州 510642)
具有较好的抑菌活性或杀虫活性的化合物具有以下结构特点:(1)有一个较大的取代基(如取代苯基);(2)取代基上有不饱和键。例如,吡嘧磺隆{1-甲基-5-[(4,6-二甲氧基嘧啶)-2-氨基甲酰氨基磺酰基]-4-吡唑甲酸乙酯}具有较好的除草和杀菌活性[1,2]。β-咔啉肟酯类化合物也具有以上两种结构特点。
本文以L-色氨酸(1)和取代苯甲醛(2a,2d和2g)为原料,经Pictet-Spengle环合[3~4]、甲酯氧化脱氢、水解及酰氯化[5]等反应合成了1-取代-β-咔啉-3-酰氯(3a,3d,3g); 借鉴文献[6]方法,3a,3d和3g分别与香草醛肟(4a),对硝基苯甲醛肟(4b)及3,4,5-三甲氧基苯甲醛肟(4c)反应,合成了9个新型的β-咔啉肟酯类化合物(5a~5i, Scheme 1),其结构经1H NMR和IR表征。并测定了5a~5i对香蕉炭疽,芒果炭疽和番茄晚疫的抑菌活性。
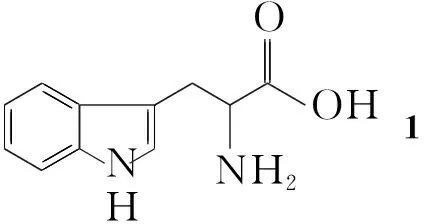


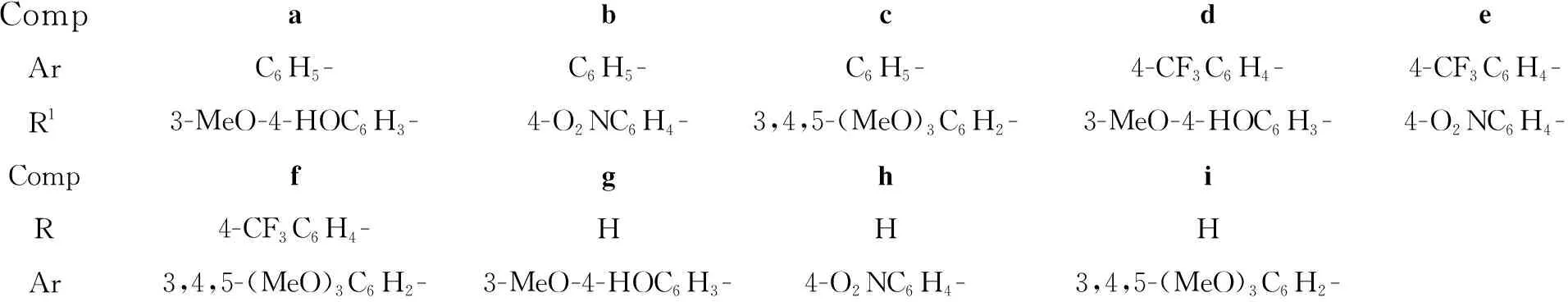
CompabcdeArC6H5-C6H5-C6H5-4-CF3C6H4-4-CF3C6H4-R13-MeO-4-HOC6H3-4-O2NC6H4-3,4,5-(MeO)3C6H2-3-MeO-4-HOC6H3-4-O2NC6H4-CompfghiR4-CF3C6H4-HHHAr3,4,5-(MeO)3C6H2-3-MeO-4-HOC6H3-4-O2NC6H4-3,4,5-(MeO)3C6H2-
Scheme1
1 实验部分
1.1 仪器与试剂
XT-4型双目显微熔点仪(温度计未经校正);Varian XL-500型核磁共振仪(DMSO-d6为溶剂,TMS为内标);ACATAR 360 FT-IR型红外光谱仪(KBr压片)。
4a(白色针状固体,产率65%),4b(淡黄色块状固体,产率62%)和4c(白色粉状固体,产率58%)[7,8]按文献方法合成;其余所用试剂均为分析纯。
1.2 合成
(1)3合成(以3a为例)[9]
在反应瓶中加入1 20.4 g(100 mmol)和冰乙酸100 mL,搅拌下加入苯甲醛(2a)10.6 g(100 mmol),回流反应2 h(TLC跟踪)。抽滤,滤饼用水洗数次后用乙醇重结晶,真空干燥得白色固体1-苯基-2,3,4,9-四氢-1H-吡啶[3,4-b]并吲哚-3-甲酸(A)24.8 g,产率80%。
在单口瓶中加入无水甲醇20 mL,冰水浴冷却,搅拌下缓慢加入二氯亚砜2 mL,搅拌20 min后撤掉冰浴。加入A 5.88 g(20 mmol),于室温反应过夜(TLC跟踪)。减压蒸除溶剂和过量SOCl2,残留物用水溶解后用饱和NaHCO3溶液调至pH 7左或。抽滤,滤饼干燥后用乙醇重结晶得白色粉状固体1-苯基-2,3,4,9-四氢-1H-吡啶[3,4-b]并吲哚-3-甲酸甲酯(B)4.21 g,产率65%。
在单口瓶中加入B 5.72 g(20 mmol)的DMF(20 ml)溶液,冰浴冷却,搅拌下分批加入KMnO41.58 g(10 mmol),反应2 h(TLC跟踪);于室温反应过夜;抽滤,滤液减压浓缩至干,残余物用乙醇重结晶得浅黄色粉状固体1-苯基-4,9-二氢-1H-吡啶[3,4-b]并吲哚-3-甲酸甲酯(C)3.56 g,产率62%。
在反应瓶中加入C 6.1 g(20 mmol)和乙醇25 mL,搅拌下加热至回流,加入饱和NaOH溶液至反应液呈碱性,反应1 h。分批滴加HCl至pH 6;冷却、过滤,滤饼干燥得灰色固体1-苯基-β-咔啉-3-甲酰氯(3a),产率65%。
用类似的方法合成淡绿色固体3d(产率58%)和灰白色固体3g(产率60%)。
(2) 5的合成(以5a)为例
在单口瓶中加入4a4.18 g(25 mmol)和二氯甲烷20 mL,冰浴冷却,搅拌下加入1~2滴PEG-600,待其溶解完全后加入新蒸三乙胺2.5 g(25 mmol);分批加入3a9.18 g(30 mmol),反应1 h;于室温反应过夜。过滤,滤液减压浓缩,残余物经硅胶柱层析[洗脱剂:V(石油醚) ∶V(乙酸乙酯)=2 ∶1]纯化得1-苯基-β-咔啉-3-甲酸-(3′-甲氧基-4′-羟基苯甲醛肟)酯(5a)。
用类似的方法合成5b~5i。
5a: 产率62%, m.p.246 ℃~248 ℃;1H NMRδ: 3.83(s, 3H, OCH3), 5.35(s, 1H, OH), 6.91~8.12(s, 12H, ArH), 7.95(s, 1H, ArH), 8.34(s, 1H, N=CH), 11.80(bs, 1H, NH); IRν: 3 427(N-H), 1 670(C=O), 1 490(C=N), 754(苯环) cm-1。
5b: 产率55%, m.p.230 ℃~232 ℃;1H NMRδ: 7.29~8.33(s, 13H, ArH), 7.88(s, 1H, ArH), 8.41(s, 1H, N=CH), 11.56(bs, 1H, NH); IRν: 3 422(N-H), 1 661(C=O), 1 491(C=N), 1 358(C-N), 754(苯环) cm-1。
5c: 产率60%, m.p.267 ℃~269 ℃;1H NMRδ: 3.83(s, 9H, OCH3), 7.14~8.22(s, 11H, ArH), 7.90(s, 1H, ArH), 8.36(s, 1H, N=CH), 11.86(bs, 1H, NH); IRν: 3 425(N-H), 1 741(C=O), 1 510(C=N), 1 389(C-N), 743(苯环) cm-1。
5d: 产率45%, m.p.234 ℃~236 ℃;1H NMRδ: 3.88(s, 3H, OCH3), 5.40(s, 1H, OH), 7.26~8.17(s, 11H, ArH), 7.88(s, 1H, ArH), 8.40(s, 1H, N=CH), 11.96(bs, 1H, NH); IRν: 3 404(N-H), 1 679(C=O), 1 454(C=N), 1 327(C-N), 737(苯环) cm-1。
5e: 产率52%, m.p.226 ℃~229 ℃;1H NMRδ: 7.12~8.35(s, 13H, ArH), 7.94(s, 1H, ArH), 8.38(s, 1H, N=CH), 11.94(bs, 1H, NH); IRν: 3 408(N-H), 1 705(C=O), 1 519(C=N), 1 329(C-N), 738(苯环) cm-1。
5f: 产率58%, m.p.246 ℃~248 ℃;1H NMRδ: 3.90(s, 9H, OCH3), 7.21~8.34(s, 11H, ArH), 7.89(s, 1H, ArH), 8.42(s, 1H, N=CH), 11.94(bs, 1H, NH); IRν: 3 488(N-H), 1 674(C=O), 1 489(C=N), 1 355(C-N), 728(苯环) cm-1。
5g: 产率42%, m.p.216 ℃~218 ℃;1H NMRδ: 3.78(s, 3H, OCH3), 5.42(s, 1H, OH), 7.26~7.94(s, 1H, ArH), 8.45(s, 7H, ArH), 9.01(s, 1H, ArH), 8.39(s, 1H, N=CH), 11.91(bs, 1H, NH); IRν: 3 398(N-H), 1 684(C=O), 1 441(C=N), 1 379(C-N), 774(苯环) cm-1; MSm/z: 446, 467, 347, 333, 319, 273, 230, 167。
5h: 产率46%, m.p.230 ℃~232 ℃;1H NMRδ: 7.24~8.85(s, 8H, ArH), 7.92(s, 1H, ArH), 8.43(s, 1H, N=CH), 9.12(s, 1H, ArH), 11.93(bs, 1H, NH); IRν: 3 407(N-H), 1 637(C=O), 1 452(C=N), 1 355(C-N), 737(苯环) cm-1。
5i: 产率52%, m.p.225 ℃~227 ℃;1H NMRδ: 3.88(s, 9H, OCH3), 7.18~8.24(s, 6H, ArH), 7.79(s, 1H, ArH), 9.08(s, 1H, ArH), 8.32(s, 1H, N=CH), 11.91(bs, 1H, NH); IRν: 3 399(N-H), 1 655(C=O), 1 443(C=N), 1 403(C-N), 747(苯环) cm-1。
1.3 抑菌活性
采用生长速率法[10,11]测定5对香蕉炭疽、芒果炭疽和番茄晚疫的抑菌活性。

表1 5的抑菌活性*Table 1 Antibacterial activities of 5
*c(5)=100 mg·L-1
将5配成浓度为10 g·mL-1的DMSO溶液,吸取0.5 mL于49.5 mL的PDA培养基(40 ℃~50 ℃)中,充分摇匀得c(5)=100 mg·L-1。分别倒入3个直径为9 cm的灭菌后的培养皿中,每个浓度设3次重复。吸取0.5 mL DMSO于49.5 mL PDA培养基为空白对照。沿培养的新鲜病原菌菌落边缘3 cm~4 cm处打取直径为0.4 cm的菌饼,反向移接到平板中央,置于27 ℃培养箱中培养4 d。用十字交叉法测量菌落直径D(表1)。从表1可见,在c(5)=100 mg·L-1时,5g和5h的抑菌效果最佳,显示出一定的抑菌活性,可以作为候选化合物做进一步的研究。
2 结论
合成了9个新型的β-咔啉肟酯类化合物(5a~5i)。初步生物活性测试结果表明,5g对香蕉炭疽的抑制率达57.58%,说明β-咔啉肟酯类化合物具有一定的抑菌活性,为进一步的研究新型的杀菌剂提供参考。
[1] Obata Toklo. Pyrazole oxime derivative and insect-killing-mite-killing-bacterium killing agent[P].JP 3 240 755,1991.
[2] 史大斌,欧阳贵平,刘静姿,等.N-取代磺酰基吡唑肟酯衍生物的合成及其生物活性研究[J].遵义医学院学报,2008,18(2):23-25.
[3] Brian E L. Synthesis ofβ-carboline.A review[J].Org Prep Proced Int,1996,28(1):1-46.
[4] 肖森,董菁,胡键,等. L-色氨酸甲酯氢溴酸盐与醛的高立体选择性Pictet-Spengler反应合成手性1,3-二取代-1,2,3,4-四氢-β-咔啉[J].合成化学,2009,17(6):687-691.
[5] 董肖椿,闻韧,肖春望,等. 1-吲哚基取代-β-咔啉生物碱及其衍生物的合成和初步抗肿瘤活性[J].药学学报,2004,39(4):259-262.
[6] 崔平,刘新华,智丽萍,等. 新型5-芳基-吡唑肟酯化合物的合成与杀菌活性[J].应用化学,2008:25-27.
[7] 杨丽敏,华水波,刘钊杰. 含氯羧酸吡唑醛肟酯化合物的合成及生物活性[J].应用化学,2005,22(8):54-57.
[8] T Obata, M Takaishi, H Hideo,etal. Triplet state stude ofβ-carbolines[P].JP 3 240 775,1997.
[9] 刘长令. 新农药开发文集[M].北京:化学工业出版社,2002.
[10] 李树生,张素华. 杀菌剂筛选方法的研究[J].农药,1997,36(9):20-22.
[11] 孔凡彬,高扬帆,陈锡岭,等. 新型杀虫剂活性研究[J].广西农业科学,2006,37(2)148.

