通便玉蓉丸的长期毒性实验*
周永学 吴永丰 王 斌 陕西中医学院(咸阳712046)
便秘是消化道疾病中最常见的病证之一,全世界大约有5%~25%的人口受到本病的困扰。其中60岁以上的老年人约占18%~23%,如果仅把排便困难作为本病的主诉来评定,发病率将超过50%[1~3],随着我国人口老龄化加剧,老年便秘人群比重正在不断加大。通便玉蓉丸由肉苁蓉、当归、芒硝、黄芩组成,具有温肾益精,润肠通便的功效,临床可用于治疗肾虚之习惯性便秘,尤其是老年肾虚便秘。其组方不含蒽醌类药物,避免了蒽醌成分的毒副作用[4]。
本实验旨在通过观察连续重复给大鼠灌服通便玉蓉丸浸膏粉3、6个月所产生的毒性反应的症状、严重程度、靶器官及其恢复、发展情况,评价药物的长期毒性反应,为临床研究提供参考依据。
1 实验材料 1.1 动物 SD大鼠180只,清洁级,体重60g~90g,雌雄各半,由第四军医大学实验动物中心提供,合格证号:SCXK(军)2007-007。
1.2 药品 通便玉蓉丸由陕西中医学院药物研究所提供,批号100101。为黑褐色干燥粉末,每g浸膏粉相当于生药1.997g,与临床用通便玉蓉丸同;实验前用蒸馏水配成70%、35%(g浸膏粉/100mL)通便玉蓉丸浸膏粉混悬液,置4℃冰箱保存备用,用时置于水浴锅36℃~39℃加热搅匀。
1.3 仪器及试剂 全自动生物组织脱水机,TP1020型,德国;生物组织包埋机,EG1150型,德国;生物组织切片机,HM315型,德国;光学显微镜,DmLS2型,德国;生物组织烘片机,HI1220型,德国;生物组织摊片机,TP-1型,天津航利达;病理图文处理系统,BI-2000,四川成都;电子天平,赛多利斯科学仪器(北京)有限公司;MINDRAY 血常规自动分析仪,RA7C-3368,迈瑞生物医疗电子股份有限公司;生化自动分析仪,BS-300,北京普利生仪器有限公司;高性能血凝仪,C2000-A,北京普利生仪器有限公司;CORNLEY 电解质分析仪,CAFT-500;网织红细胞染色液,J115,温州市康泰生物科技有限公司;瑞姬氏复合染液,JK10,温州市康泰生物科技有限公司。
2 实验方法[5~6]2.1 分组及给药 SD大鼠适应性饲养1周,按体重随机分为高剂量组(42g/kg·d-1)、中剂量组(21g/kg·d-1)、低剂量组(10.5g/kg·d-1)和对照组,每组45只,受试药物按60kg成人每日服用30g等效换算,分别等效于成人量的42、21、10.5倍,给药体积均为1.5mL/100g,对照组给予等体积蒸馏水,连续给药6个月,每周给药6d。
2.2 检测方法 每天进行一般观察,每周记录一次体重,摄食摄水量。给药3个月和6个月,每次每组1/3大鼠麻醉(10%水合氯醛),颈动脉取血检测血液学、血液生化学、主要脏器湿重并计算脏器系数,镜检脏器及组织病理变化。其余SD大鼠停药,常规饲养4周后处死,检测内容及方法同前。
2.3 检测内容 2.3.1 一般情况观察 观察动物外观体征、行为活动、呼吸、腺体分泌、粪便性状,摄食量、摄水量、体重以及死亡情况和中毒反应。
2.3.2 对大鼠体重、摄食量和摄水量的影响 每周称取一次体重并测取摄食量、摄水量各一次,记录后统计。
2.3.3 血液学的检测项目[7]包括白细胞数(WBC)、血红蛋白(HGB)、红细胞数(RBC)、红细胞比容(HCT)、红细胞平均容积(MCV)、红细胞平均血红蛋白(MCH)、红细胞平均血红蛋白浓度(MCHC)、红细胞分布宽度变异系数(RDW-CV)、红细胞体积分布宽度标准差(RDW-SD)、血小板计数(PLT)、血小板分布宽度(PDW)、血小板积压(PCT)、以及平均血小板体积(MPV);活化部分凝血酶时间(APTT)、凝血酶原时间(PT)、凝血酶时间(TT);推片计数网织红细胞(RC)和白细胞分类。
2.3.4 血液生化学的检测项目 血清丙氨酸氨基转移酶(ALT)、谷草转氨酶(AST)、谷草/谷丙(AST/ALT)、碱性磷酸酶ALP总胆红素TBIL总蛋白TP白蛋白ALB球蛋白(GLB)、白蛋白/球蛋白(ALB/GLB)、总胆固醇(T-CHO)、甘油三酯(TG)、尿素氮(BUN)、肌酐(Cr)、血糖(GLU)、钾离子(K+)、钠离子(Na+)、氯离子(Cl-)、钙离子(Ca2+)。
2.3.5 计算脏器系数 精密称量肝、心、脾、肺、肾、脑、肾上腺、胸腺、子宫、卵巢、睾丸、附睾,计算脏器系数(脏器系数=脏器重量g/体重g×100)。
2.4 病理组织学检查 肝、心、脾、肺、肾、胸腺、甲状腺、颌下腺、肾上腺、食管、气管、胰腺、胃、小肠、大肠、肠系膜淋巴结、脊髓(颈、胸、腰)、膀胱、卵巢、子宫、阴道、脑(大脑、小脑、脑干)、垂体、睾丸、附睾、前列腺、坐骨神经、胸骨(骨、骨髓)、主动脉等。将上述脏器和组织取材修剪后放入10%福尔马林液中固定,常规取材、脱水、浸蜡、包埋、切片、HE染色,光镜下进行病理学检查。
3 结 果 3.1 对一般情况的影响 给药7d后高剂量组SD大鼠部分有肛门不洁现象,中、低剂量组较少。给药4周后,黑稀药便有所减少,多呈尚能成形的黑润便,给药组肛门多有不洁,以高剂量组为剧;各给药组的鼠盒内大便数量明显较对照组多。停药后,大便恢复正常。除此之外在实验过程中各组大鼠行为、自主活动、摄水、摄食以及尿液等均未见异常,口、眼、耳、鼻未见异常分泌物。
3.2 对大鼠体重的影响 高剂量组雄性大鼠1周、2周、3周、5周、19周、26周与对照组比较差异有显著性意义(P<0.05或P<0.01),高剂量组雄性大鼠体重均数普遍低于对照组,在恢复期(27-30周)高剂量组雄性大鼠体重均数高于对照组;高剂量组雌性大鼠体重1周、2周与对照组比较差异有显著意义(P<0.05或P<0.01);之后无差异。结果见表1。
表1 通便玉蓉丸给药对大鼠体重的影响(g,±s)

表1 通便玉蓉丸给药对大鼠体重的影响(g,±s)
注:各给药组与对照组比较△P<0.05 ▲P<0.01;下表同。
性别 时间对照组低剂量组中剂量组高剂量组雄性 0周111.59±10.66 112.14±10.49 114.17±10.63 114.87±9.02 1周171.82±14.27 174.82±11.93▲173.48±12.76▲159.74±14.62▲2周234.55±16.23 236.86±11.37▲236.61±14.29▲220.00±12.12▲3周298.32±19.77 301.73±13.93▲293.13±18.55△280.32±13.91▲4周338.91±22.51 357.86±27.15▲345.73±25.44△327.55±22.17 5周387.64±28.39 391.41±25.96△386.86±25.58 369.82±27.48△6周378.50±28.26 402.95±31.22▲△394.09±28.27 380.24±29.18 19周584.33±40.45 578.13±65.89 575.07±54.57 546.29±55.04△26周623.93±60.58 623.20±71.71 615.43±53.69 572.62±66.45△27周595.14±35.68 631.71±72.84 634.14±26.66△621.83±62.77 28周593.86±36.10 632.71±69.39 653.57±33.71▲624.50±60.02 29周600.29±40.02 646.57±75.41 658.00±42.15△636.67±74.24 30周609.14±54.38 665.57±79.78 652.43±54.52 649.83±89.69雌性 0周112.74±9.57 112.96±8.81 111.86±7.83 113.05±8.30 1周160.09±11.16 160.26±9.72△154.77±9.72 151.32±13.93△2周195.26±13.34 193.78±11.63▲191.14±11.32△182.09±16.82▲3周216.30±14.38 216.17±14.07 215.64±12.57 212.50±11.39 6周247.04±17.47 254.57±17.10 255.55±18.13 253.59±17.76 9周279.39±20.76 286.09±17.06 278.90±19.90 286.82±18.78 12周295.26±26.00 302.70±21.03 297.05±26.03 302.55±21.12 16周315.00±23.78 308.53±24.11 311.14±16.90 316.73±23.36
3.3 对大鼠摄食量的影响 在通便玉蓉丸长期毒性实验初期各组摄食量增长明显,在中后期在一定水平基本呈S型变化;其中大剂量组摄食量线平均水平低于其它三线,说明大剂量组摄食量略低于其它组别,但差别不明显,在后期基本一致。见图1。
3.4 对大鼠摄水量的影响 在通便玉蓉丸长期毒性实验初期各组大鼠摄水量均呈增长趋势,中后期在一定水平呈不规则S形分布,在不同时期,各摄水量线基本一致。见图2。

图1 通便玉蓉丸长期毒性实验对各组大鼠摄食量的影响

图2 通便玉蓉丸长期毒性实验对各组大鼠摄水量的影响
3.5 通便玉蓉丸对大鼠血液学指标的影响 给药3、6个月后血液学与对照组比较具有统计学差异(P<0.05或P<0.01)指标中,高剂量组在3个月给药结束后TT呈剂量-效关系,但6个月给药结束后未见差异,不能说明是持续灌服通便玉蓉丸造成的。其余PLT、PCT、HCT、MCHC均未见量-效关系和时-效关系,停药4周后血液学指标在各组之间均未见统计学差异,说明通便玉蓉丸对大鼠血液学指标的影响具有可逆性且无延迟反应。结果见表2。
表2 通便玉蓉丸对血液学指标的影响(±s)
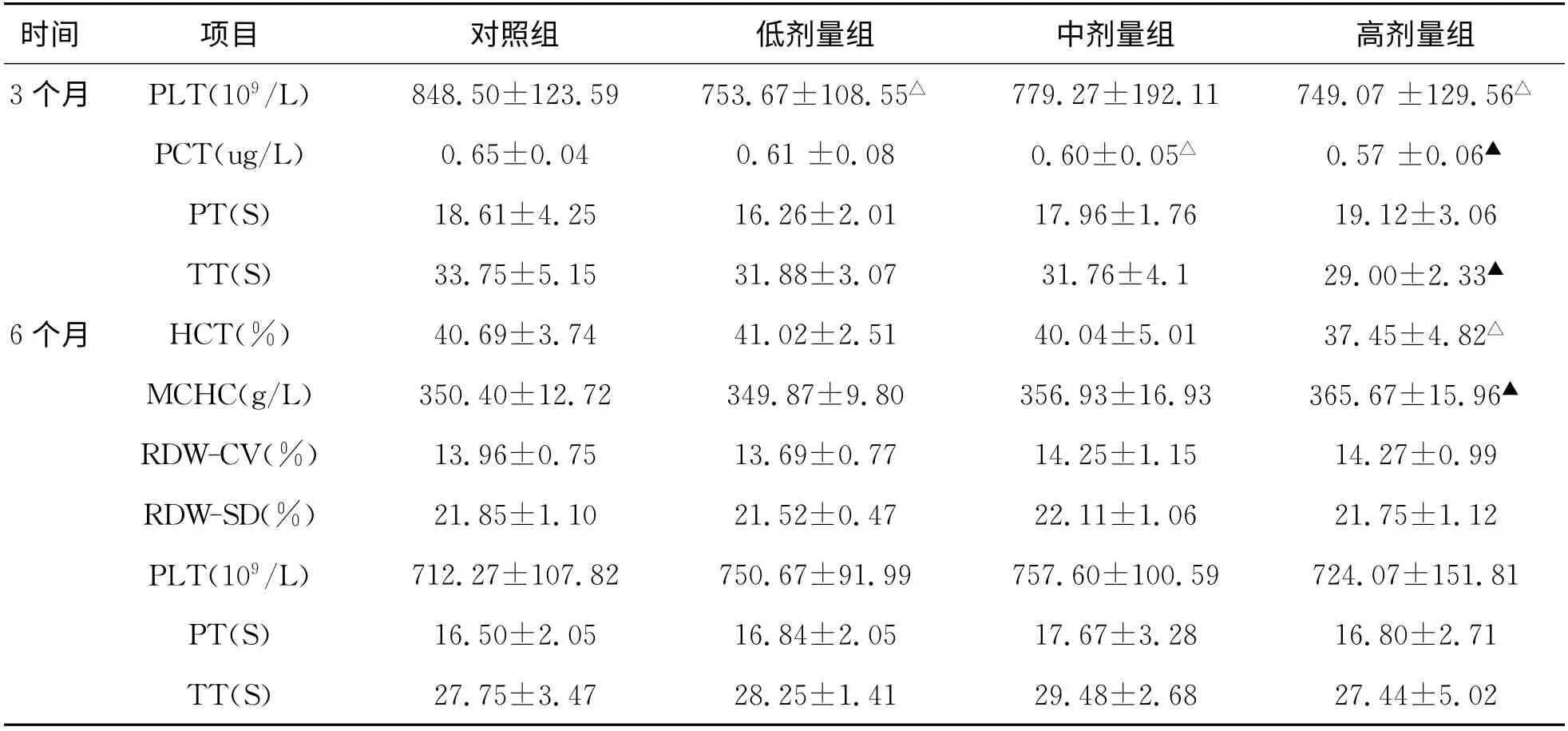
表2 通便玉蓉丸对血液学指标的影响(±s)
时间项目对照组低剂量组中剂量组高剂量组3个月PLT(109/L)848.50±123.59 753.67±108.55△779.27±192.11 749.07±129.56△PCT(ug/L)0.65±0.04 0.61±0.08 0.60±0.05△0.57±0.06▲PT(S)18.61±4.25 16.26±2.01 17.96±1.76 19.12±3.06 TT(S)33.75±5.15 31.88±3.07 31.76±4.1 29.00±2.33▲6个月HCT(%)40.69±3.74 41.02±2.51 40.04±5.01 37.45±4.82△MCHC(g/L)350.40±12.72 349.87±9.80 356.93±16.93 365.67±15.96▲RDW-CV(%)13.96±0.75 13.69±0.77 14.25±1.15 14.27±0.99 RDW-SD(%)21.85±1.10 21.52±0.47 22.11±1.06 21.75±1.12 PLT(109/L)712.27±107.82 750.67±91.99 757.60±100.59 724.07±151.81 PT(S)16.50±2.05 16.84±2.05 17.67±3.28 16.80±2.71 TT(S)27.75±3.47 28.25±1.41 29.48±2.68 27.44±5.0 2
3.6 通便玉蓉丸对大鼠血液生化学指标的影响 给药3、6个月后血液生化学与对照组比较具有统计学差异(P<0.05或P<0.01)的指标中,TG在高剂量组给药3个月结束后降低并呈现量-效关系,并且在6个月给药结束后中、高剂量组也有统计学差异性降低,故推测通便玉蓉丸对高剂量组TG有降低作用,临床意义重大;6个月给药结束后高剂量组GLB增高并呈现剂量-效应关系,应与高剂量组1d灌胃两次而使食管损害大于其它给药组引起相关的炎症和感染有关;其余与对照组比较具有统计学差异的指标均未呈现量-效关系,而低剂量组在给药6个月后AST、ALT、Cr均明显低于对照组,说明通便玉蓉丸在该剂量下有保护肝肾的作用;停药4周后血液生化学指标在各组之间均未见统计学差异,说明通便玉蓉丸对大鼠血液生化学指标的影响具有可逆性且无延迟反应。结果见表3。
表3 通便玉蓉丸给药对血液生化学指标的影响±s

表3 通便玉蓉丸给药对血液生化学指标的影响±s
时间项目对照组低剂量组中剂量组高剂量组3个月ALT(u/L)54.14±13.24 52.60±15.24 47.20±14.07 53.93±11.85 AST(u/L)170.21±48.68 188.20±46.33 177.67±66.15 173.64±33.28 TG(mmol/L)1.13±0.47 0.95±0.32 0.87±0.27 0.77±0.28△Cr(μmol/L)77.13±12.66 80.08±12.49 76.89±12.06 75.44±10.22 6个月GLB(g/L)27.80±2.37 28.80±2.01 29.00±3.16 30.27±2.69△ALB/GLB 1.31±0.07 1.28±0.07 1.25±0.08 1.23±0.09△ALT(u/L)40.67±12.25 32.60±7.26△40.40±15.87 38.73±13.84 AST(u/L)131.33±40.96 96.60±22.76▲125.13±54.57 124.27±41.77 TG(mmol/L)1.21±0.39 1.20±0.31 0.81±0.24▲0.84±0.24▲Cr(μmol/L)81.07±6.94 70.40±7.85▲73.86±7.37△77.66±8.94
3.7 通便玉蓉丸对大鼠脏器系数的影响 6个月给药结束后中、高剂量组的肝、肾脏器系数和高剂量组脾脏器系数与对照组比较具有统计学差异(P<0.05或P<0.01),并呈现剂量-效应关系,分析与通便玉蓉丸对高剂量组雄性大鼠体重的抑制作用有关,当体重随着药物剂量增加而减小且各组脏器湿重无差异时,脏器系数会出现增大的假象(结合病理组织学检查无病理变化的结果)。停药4周后各组大鼠脏器系数均无异常。结果见表4。
表4 通便玉蓉丸给药6个月对大鼠脏器系数的影响(±s)

表4 通便玉蓉丸给药6个月对大鼠脏器系数的影响(±s)
脏器对照组低剂量组中剂量组高剂量组肝2.339±0.177 2.465±0.207 2.595±0.347△2.872±0.362▲0.166±0.024 0.170±0.031 0.186±0.042 0.201±0.058△肾0.578±0.087 0.616±0.082 0.660±0.100△0.682±0.090脾▲
3.8 病理组织学检查 各时期高剂量组与对照组中有1/15只或2/15只大鼠的肺皆有肺泡间隔增厚、肺泡有局灶性炎细胞浸润和小肠绒毛有局灶性变性,其余主要脏器及组织系统尸解和病理组织学检查,未见明显异常病理改变。
4 讨 论 通便玉蓉丸各剂量组长期灌胃后,大鼠未出现生命体征及血液学、血液生化学指标的明显改变,对大鼠的主要脏器湿重及脏器系数无明显变化,主要脏器和组织无病理改变;其通过停药4周的观察和各项指标的检测,得出通便玉蓉丸对大鼠各指标的影响具有可逆性且无延迟反应。病理报告分析各时期高剂量组与对照组中有1/15只或2/15只大鼠的肺和小肠有相同的病理改变,分别为成年大鼠自发性症状和固定不及时而出现自溶现象有关,两者皆非药物特异性毒性反应。其余主要脏器及组织系统尸解和病理组织学检查,未见明显异常病理改变。即通便玉蓉丸6个月病理学检查,未发现明显毒性靶器官。
以上结果提示,通便玉蓉丸在42g/kg·d-1高剂量(等效于临床成人量的42倍)下无毒副作用,实验大鼠连续服用6个月安全,停药4周各指标具有可逆性且无延迟反应,可以为临床实验提供参考依据。
[1] 郭晓峰,柯美云,潘国宗.北京地区成年人慢性便秘流行病学调查及其相关因素分析[J].基础医学与临床,2001,21:18-20.
[2] Ronald B,Stewart MS,Mary T Moore,etal.Correlates of constipation in an ambulatory elderly population[J].The Am Gus,1992,87(7):859.
[3] 魏艳静,卞红磊,赵 发.便秘的国内流行病学研究进展[J].疾病控制杂志,2004,8(5):449-451.
[4] 马春玉.蒽醌类泻药与大肠黑变病临床研究[J].中国社区医师.医学专业,2011,3(13):7.
[5] 《中药、天然药物长期毒性研究技术指导原则》课题研究组.中药、天然药物长期毒性研究技术指导原则[S].2005:1-16.
[6] 秦 川.实验动物学[M].北京:人民卫生出版社,2010,:245.
[7] (美)谢恩C.加德(Shayne C.Gad).药物安全性评价(Drug Safety Evaluation)[M].北京:化学工业出版社,2006:208-212.

