微波辐射β分子筛负载固体超强酸催化制备2-(2-1H-苯并咪唑基)-苯酚
沈喜海,由鑫钰,王亚楠,秦兆文
(河北科技师范学院,河北 秦皇岛,066600)

1 实验部分
1.1 主要仪器与试剂
WX-4000-微波快速消解系统(上海屹尧分析仪器有限公司); UV-2401型紫外可见分光光度计(日本岛津公司); FTIR-8900红外光谱仪(日本岛津公司);WRS-AB数字熔点仪(上海精密科学仪器有限公司)。水杨酸、邻苯二胺、硫酸铁、浓硫酸、1,4-二氧六环、β分子筛等均为分析纯。
1.2 实验步骤
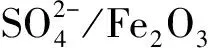

1.2.32-(2-1H-苯并咪唑基)-苯酚的合成 取邻苯二胺(1.14 g)与水杨酸(1.38 g),加入一定质量的已制备好的催化剂和5 mL的1,4-二氧六环,调节微波合成仪的功率,反应一定时间,趁热过滤除去催化剂,冷却,反应液经减压蒸馏脱除溶剂得红色固体粗产物,粗产物用去离子水反复洗涤3次,干燥,用无水乙醇重结晶,活性炭脱色,得针状结晶。
1.3 表征方法
1.3.1红外光谱表征 采用KBr压片法、用傅立叶红外光谱仪分析2-(2-1H-苯并咪唑基)-苯酚的官能团结构。
1.3.2紫外光谱测定 将2-(2-1H-苯并咪唑基)-苯酚溶解于无水乙醇中,用紫外分光光度计测试其紫外吸收光谱。分析其共振结构。
1.3.3熔点测定 采用毛细管法,样品装入封口毛细管中,用数字熔点仪测定其熔点。
2 结果与讨论
2.1 水杨酸与邻苯二胺的摩尔比对产物产率的影响
在水杨酸6.90 g(0.05 mol),催化剂 0.10 g,1,4-二氧六环15 mL,调节微波辐射功率为500 W,反应5 min的条件下,考察物料摩尔比对产物产率的影响。结果表明,在2-(2-1H-苯并咪唑基)-苯酚的合成反应中,水杨酸与邻苯二胺的最佳摩尔比是1.0∶1.1(表1)。
2.2 微波辐射功率对产物产率的影响
在邻苯二胺5.70 g(0.055 mol),水杨酸6.90 g(0.05 mol),催化剂 0.10 g,1,4-二氧六环15 mL条件下,调节微波辐射功率,反应5 min的条件下,考察微波辐射功率对产物产率的影响。结果表明,在2-(2-1H-苯并咪唑基)-苯酚的合成反应中,最佳微波辐射功率为500 W(表1)。
2.3 微波辐射时间对产物产率的影响
在邻苯二胺5.70 g(0.055 mol),水杨酸6.90 g(0.05 mol),催化剂 0.10 g,1,4-二氧六环15 mL条件下,调节微波辐射功率500 W,考察微波辐射时间对产物产率的影响,结果表明,在2-(2-1H-苯并咪唑基)-苯酚的合成反应中,最佳微波辐射时间为5 min(表1)。
2.4 催化剂用量对产物产率的影响
在水杨酸6.90 g(0.05 mol),邻苯二胺5.70 g(0.055 mol),1,4-二氧六环15 mL。调节微波辐射功率为500 W,反应5 min的条件下,考察催化剂用量对产物产率的影响。结果表明,最佳催化剂量为0.10 g(表1)。

表1 反应条件对对反应产率的影响
由以上实验可知:当n(水杨酸)∶n(邻苯二胺)=1.0∶1.1(水杨酸6.90 g,邻苯二胺5.70 g),固体超强酸相对用量0.10 g,微波辐射功率500 W,微波辐射时间5 min,产率最高达87.8%。
2.5 催化剂的重复使用效果
反应后分离出的催化剂,按制备催化剂的条件,重新活化再生,进行循环使用 ,产率略有下降但下降缓慢(表2),说明催化剂重复使用效果较好 。

表2 催化剂的重复使用效果
2.6 分子筛和固体超强酸单独使用的催化效果

2.7 2-(2-1H-苯并咪唑基)-苯酚的表征
2.7.1晶体外观 2-(2-1H-苯并咪唑基)-苯酚为针状晶体(图1)。
2.7.2红外光谱分析 分析产物的红外光谱,可知3 694.25 cm-1为酚羟基-OH的伸缩振动吸收峰,3 429.20 cm-1为-NH-的伸缩振动吸收峰,3 137.97 cm-1为苯环上C-H的伸缩振动吸收峰,1 598.88 cm-1及其左右2个吸收峰为苯环骨架振动吸收峰,1 458.54,1 384.80 cm-1为咪唑环骨架振动吸收峰,1 54.36,1 121.73 cm-1分别为C-N和C-O的弯曲振动吸收峰,787.68,757.97 cm-1为苯环邻二取代C-H面外振动吸收峰(图2)。红外光谱数据可以得出产物含有2-(2-1H-苯并咪唑基)-苯酚的官能团。
2.7.3紫外吸收图谱分析 分析产物的紫外吸收图谱(图3),可知212.5 nm处为—C=N键π→π*跃迁吸收峰, 在235 nm处有一酚羟基苯环的n→π* 跃迁吸收峰,296 nm处为苯环的π→π*震动吸收峰(图3)。这些数据可以确定咪唑环、苯环和带有酚羟基苯环的存在。结合FTIR数据可以确定产物为2-(2-1H-苯并咪唑基)-苯酚。
2.7.4熔点测定 利用数字熔点仪测定产物的熔点,熔点为156~159 ℃,与文献值相符,可以确定产物为2-(2-1H-苯并咪唑基)-苯酚。

图1 产物晶体外观 图2 产品的红外光谱图
2.7.5XRD分析 2-(2-1H-苯并咪唑基)-苯酚在2θ为5.7,15.7,18.2时有强吸收峰, 2θ为6.1,16.2,22.0,24.0,27.0时有较强吸收峰(图4)。
3 结 论

图3 产品的紫外光谱图 图4 产品的XRD谱图
[1] 刘雅茹,冯雪松.2-巯基-5-甲氧基-1H-苯并咪唑的合成[J].广东药学院学报,2006,22(1):39-40.
[2] Bag S K,Chakraborty S B,Chavdhuri S R.Anticorrosion film of benzimidazole on brass in ammonia[J].J Indian Chem Soc,1996,73:113-118.
[3] 戴桂元,刘德龙,王苏惠,等.新型吡啶类苯并咪唑衍生物的合成[J].有机化学,2004,24(3):315-318.
[4] 李焱,马会强,王玉炉.苯并咪唑衍生物合成与应用研究进展[J].有机化学,2008,28(2):210-217.
[5] 李莹莹,周永花,郭玉芳,等.苯并咪唑衍生物的合成改进[J].有机化学,2006,26(8):1 097-1 099.
[7] 赵立芳,何柱生,马玉英.负载型固体超强酸催化合成富马酸二甲酯[J].宝鸡文理学院学报:自然科学版,2002,22(2):138-140.
[8] 郑社教.固体酸催化剂的研究与进展[J].甘肃化工,2001(3):107-109,114.
[10] 刘鸿,温明.微波辐射磷钨杂多酸催化合成 2-(2-1H-苯并咪唑基)苯酚[J].化学工程师,2009(8): 16-17,24.


- 河北科技师范学院学报的其它文章
- 双光子协同光化学周环反应的选择规则

