优质壳聚糖/壳寡糖的制备工艺及水溶性壳寡糖Fe(Ⅲ)配合物的合成
杨俊玲,赵福龙,夏 军,张晓波,王 璇
(天津工业大学环境与化学工程学院,天津 300387)
优质壳聚糖/壳寡糖的制备工艺及水溶性壳寡糖Fe(Ⅲ)配合物的合成
杨俊玲,赵福龙,夏 军,张晓波,王 璇
(天津工业大学环境与化学工程学院,天津 300387)
以皮皮虾壳作基本原料,分别采用稀盐酸、稀碱溶液浸泡,除去虾壳中的钙质等无机质和蛋白等有机成分,以浓碱脱除甲壳素上的乙酰基,制得壳聚糖.再以其为原料,采用H2O2氧化降解法得到水溶性壳寡糖.将所制水溶性壳寡糖加入到氯化铁溶液中,设定各项条件,使二者进行配位反应.经系列实验证实,得出制备高脱乙酰度壳聚糖最适宜条件为:温度85℃,时间9 h,NaOH质量分数45%,料液比1∶300.所得产品脱乙酰度为89.6%,收率(壳聚糖/甲壳素)为73.1%,其他各项指标也均为优良级.制备水溶性壳寡糖最适宜条件为:温度65℃,时间6 h,醋酸质量分数4.0%,H2O2质量分数4.0%,产品平均粘均分子质量为2.9 ku,外观为淡黄色粉末,溶解性能优良.通过对FT-IR和UV谱图的分析,证实了水溶性壳寡糖Fe(Ⅲ)配合物的生成.
高脱乙酰度壳聚糖;水溶性壳寡糖;水溶性壳寡糖Fe(Ⅲ)配合物
壳聚糖(chitosan,简称CTS)是地球上最丰富的天然高分子化合物之一,其在很多领域都展现出较高的应用前景[1].经研究证实,高脱乙酰度壳聚糖(HD-chitosan)在降解、结晶、活细胞和酶的固定化、制作反渗透膜和超滤膜等中具有更优的理化性质[2].因此,高脱乙酰度壳聚糖更具研究意义和应用价值.但壳聚糖的分子质量大,仅溶于少数酸性体系,这限制了其应用前景[3].而其降解产物壳寡糖(COS)的聚合度一般在2~10之间,其水溶性好、易被机体吸收利用,具有抑菌、抗肿瘤等生物活性,在医药、食品、农业、环保等领域[4-6]具有广阔的应用前景,日益受到专家学者以及厂商们的关注[7].由于壳聚糖良好的生物相容性,对其化学改性亦种类繁多[8].其中,与金属形成配合物是重要一项.因其对过渡金属具有良好的配位作用,使壳聚糖基金属配合物材料产生许多优良性能[9-11].目前,以壳聚糖金属铁配合物的研究居多,而以水溶性壳寡糖为基质,络合具有功能特性的过渡金属铁(Ⅲ)的报道鲜有见到.为此,本文通过研究壳聚糖/壳寡糖的制备工艺,获得优质壳聚糖/壳寡糖产品,然后选用更具活性的水溶性壳寡糖作为基质络合过渡金属Fe(Ⅲ),再以FT-IR和UV来表征水溶性壳寡糖Fe(Ⅲ)配合物的结构特征.
1 实验部分
1.1 原材料与仪器
原材料:皮皮虾壳,市售;过氧化氢,天津大沽精细化工有限公司生产;氢氧化钠(工业级),济南永茂化工有限公司生产;盐酸、醋酸、氢氧化钠、氯化铁、邻菲罗琳等试剂,均为分析纯,市售.
仪器:DF-101S-B型集热式恒温加热磁力搅拌器,山东鄄城华鲁电热仪器有限公司生产;紫外分光光度计(UV),北京瑞利分析仪器有限公司生产;370DTGS型红外光谱仪,美国Thermo公司生产;FA1004型电子天平,上海瞬宇恒平科学仪器有限公司生产;SHZ-3型循环水式真空泵,上海康华生化仪器制造有限公司生产;电热真空干燥箱,天津市中环实验电炉有限公司生产;HK-1D型恒温水浴槽,南京大学应用物理研究所生产;SX2-4-10型箱式电阻炉,山东省龙口市先科仪器有限公司生产;乌氏粘度计,内径0.5 mm,淄博现代科学仪器有限公司生产.
1.2 壳聚糖的制备
首先将称取的皮皮虾壳清洗干净,用稀盐酸浸泡除去钙质等无机盐,水洗至中性,加入稀氢氧化钠(工业级)溶液中搅拌脱除蛋白和酯类,然后与浓氢氧化钠(工业级)溶液反应脱除乙酰基,过滤水洗至中性后,烘干即得壳聚糖.其间,分别以温度、时间、氢氧化钠浓度、料液比为单因素变量,以壳聚糖产品的脱乙酰度为标准,探讨壳聚糖的制备工艺条件.按文献[12-13]的方法对壳聚糖脱乙酰度进行测定.
1.3 壳寡糖的制备
准确称取所制壳聚糖产品(采取优化条件下产品:脱乙酰度为89.6%;粘均分子质量为8.8×106),并溶入一定质量分数的乙酸中,待完全溶解后,设定温度,缓慢加入双氧水,恒温搅拌水浴中降解,调节至中性后蒸馏浓缩,用3倍体积的无水乙醇进行醇沉,静置过夜.真空干燥后即得水溶性壳寡糖产品.其间,分别以温度、双氧水浓度、醋酸浓度、时间为单因素变量,以寡糖产品的分子质量为标准,研究壳寡糖的制备工艺条件.
1.4 壳寡糖相对分子质量的测定
精确称取自制壳寡糖样品,将其溶入0.1 mol/L的乙酸-0.2 mol/L氯化钠缓冲溶液中,待样品溶解后,用乌氏粘度计于(25±0.01)℃下恒温测量样品粘度,以文献[14-15]所提方法计算其相对分子质量.
1.5 壳寡糖Fe(Ⅲ)配合物的合成
准确称取壳寡糖产品(为优化条件下所制),将其加入到一定浓度的氯化铁溶液中,以0.1 mol/L盐酸调节pH至1.8左右,然后置于45℃恒温水浴锅中络合反应6 h.反应结束后,调节至中性,有沉淀析出,抽滤,分别以蒸馏水、乙醇-丙酮混合液淋洗.55℃下真空干燥后,即得橙黄色壳寡糖Fe(Ⅲ)配合物.
1.6 红外光谱表征
采用KBr压片法对壳寡糖Fe(Ⅲ)配合物进行红外表征.
1.7 紫外吸收光谱表征
以1.0%醋酸为空白试剂,于190~450 nm波长范围内测定壳寡糖Fe(Ⅲ)配合物的紫外吸收光谱.
2 结果与分析
2.1 壳聚糖的制备工艺
为研究各因素对脱乙酰反应的影响,分别进行了反应温度、反应时间、料液比(g∶mL)、NaOH质量分数4个单因素条件实验,结果如图1至图4所示.

图1 温度对脱乙酰反应的影响Fig.1 Effect of temperature on deacelation reaction
由图1可知,温度对脱乙酰反应的影响较大,温度在60~70℃之间时,脱乙酰度增加明显,但其值较低,其应用效果有限;当温度增大至85~90℃时,可看出脱乙酰度显著增大,其值能达90%以上.因此,从效能角度考虑,温度选择在85℃左右为宜.由图2可知,增大反应时间有利于提高壳聚糖的脱乙酰度,其影响效应比较接近于线性规律,当时间增加至9 h时,其脱乙酰度接近80%,足可以展现其应用性质.因此,时间选择在9 h为宜.由图3可知,随着NaOH浓度的增大,壳聚糖脱乙酰度的增大呈现前缓、中快、后慢的变化趋势.当NaOH质量分数增大至45%时,其脱乙酰度就已在85%以上,NaOH质量分数大于45%时,其影响效果逐渐变小.由图4可知,料液比对脱乙酰反应的影响基本类似于NaOH质量分数的影响,同样呈现出前缓、中快、后慢的增大趋势.当料液比达到1∶300时,壳聚糖的脱乙酰度就已增大至80%以上,随着料液比的继续增大,脱乙酰度的增大并不显著.因此,对以上2个因素下的成本、效果等角度综合分析,可得出:NaOH质量分数选在45%为宜,料液比选在1∶300为宜.从皮皮虾壳至各阶段产品的收率如表1所示.

图2 时间对脱乙酰反应的影响Fig.2 Effect of time on deacelation reaction
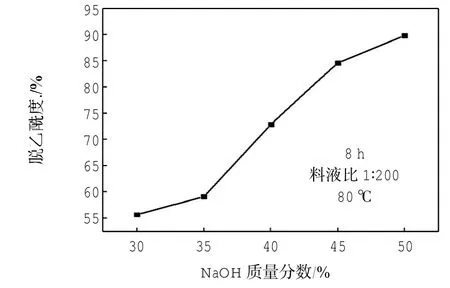
图3 NaOH质量分数对脱乙酰反应的影响Fig.3 Effect of mass fraction of Sodium hydroxide on deacelation reaction
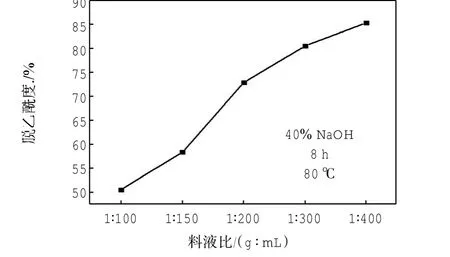
图4 料液比对脱乙酰反应的影响Fig.4 Eeffect of ratio of material to solvent on deacelation reaction

表1 从皮皮虾壳至各阶段产品的收率Tab.1 Yield of products from mantisshrimp shell to each stage
为验证上述反应条件的适宜性,进行了3次脱乙酰反应实验,结果如表2所示.

表2 优化条件下所制壳聚糖的质量指标分析Tab.2 Quality analysis of chitosan prepared under optimized conditions
从表2中看出,3次实验所得壳聚糖产品的脱乙酰度平均值为89.6%,收率(壳聚糖/甲壳素)平均值为73.1%,其他各项指标也均为优良级.故可将制备优质高脱乙酰度壳聚糖的最适宜条件定为:温度85℃,时间9 h,NaOH质量分数45%,料液比1∶300.
2.2 水溶性壳寡糖的制备工艺
为研究各因素对H2O2降解反应的影响,分别进行了反应温度、反应时间、乙酸质量分数、H2O2质量分数4个单因素条件实验,结果如图5至图8所示.
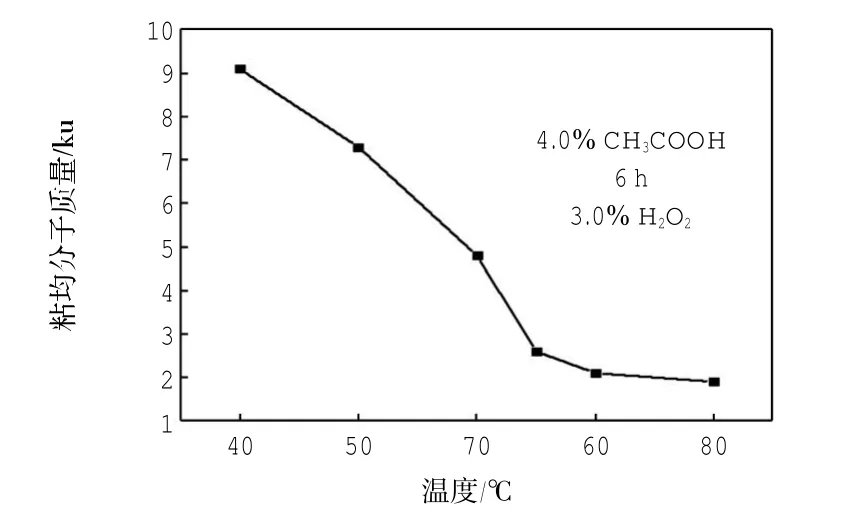
图5 温度对降解反应的影响Fig.5 Effect of temperature on degradation reaction
由图5可见,温度对降解反应的影响很显著,当温度为40~65℃时,粘均分子质量呈现快速减小趋势,之后趋势变得缓和,可得出温度是影响降解程度的主要因素之一.结合表3分析,温度变大,虽有利于增大降解程度,但产品颜色加深(可能其他副反应增多),不利于得到优质降解产品,故温度不宜过高;由图6可见,随着降解时间的延长,降解产品的相对分子质量呈现均匀下降趋势,至6 h时,该趋势变得缓和,即再增大降解时间,其影响效果亦有限.由图7可见,醋酸质量分数对降解反应的影响不大,随着醋酸浓度的增大,产品的分子质量先减小后增大,当醋酸质量分数至4.0%时,达到最低.由图8可见,随着双氧水质量分数增大,降解产品的相对分子质量先快速减小后缓慢增大,质量分数至4.0%时达到最低值,说明双氧水浓度并非越大越有利于氧化降解.从产品成本、成色品质、效能等角度考虑,再结合以上分析结果,得出制备水溶性壳寡糖的H2O2氧化降解的适宜条件:温度65℃,时间6 h,醋酸质量分数4.0%,H2O2质量分数4.0%.
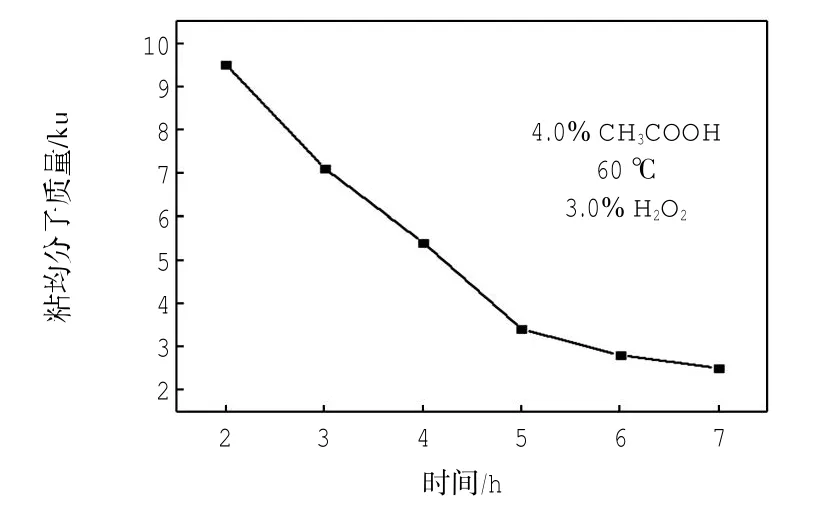
图6 时间对降解反应的影响Fig.6 Effect of time on degradation reaction
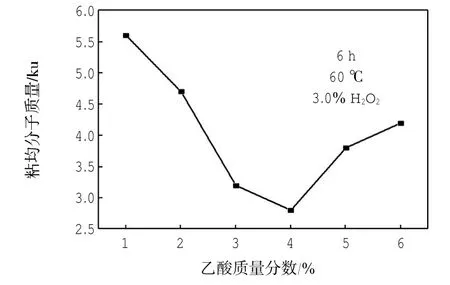
图7 乙酸质量分数对降解的影响Fig.7 Effect of mass fraction of acetic acid on degradation reaction
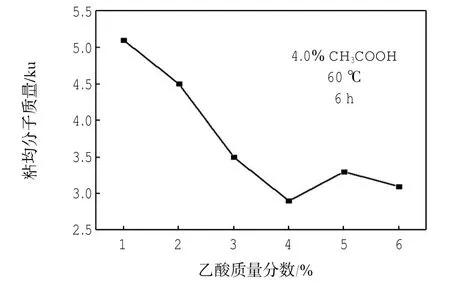
图8 双氧水质量分数对降解的影响Fig.8 Effect of mass fraction of hydrogen peroxide on degradation reaction

表3 不同温度下制备的壳寡糖成色分析Tab.3 Fineness determination of chitooligosaccharide prepared at different temperatures
为验证上述反应条件的适宜性,进行了3次H2O2降解实验.结果为:产品的相对分子质量平均值为2.9 ku,外观品质为淡黄色粉末,其溶解性能见表4.可看出:降解产品具有良好的溶解性能.验证结果证明,可将温度65℃,时间6 h,醋酸4.0%,H2O24.0%定为H2O2氧化降解壳聚糖的最适宜条件.
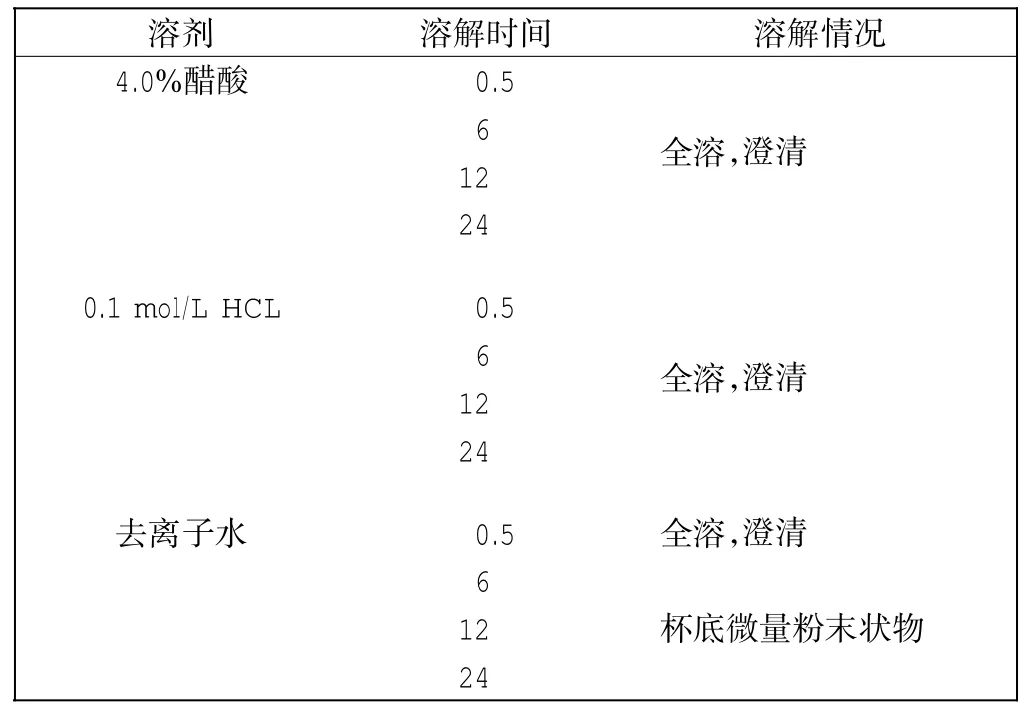
表4 优化条件下所制壳寡糖在不同溶剂中的溶解性能检验Tab.4 Solubility property of chitooligosaccharide prepared under optimized conditions with different solvent systems
2.3 壳寡糖Fe(Ⅲ)配合物的红外分析
图9所示为壳寡糖与壳寡糖Fe3+配合物的红外谱图.
从图9中对比可知:位于3 440 cm-1处氨基和羟基的N-H、O-H伸缩振动峰红移至3 412 cm-1处且峰形变得尖锐,说明了-NH2、-OH可能参与了与Fe3+的配位反应,位于1 634 cm-1处的N-H伸缩振动峰移至1 637 cm-1处,位于1 600 cm-1处的-NH2变形振动峰移至1 617 cm-1处,这进一步说明了-NH2与Fe3+发生了配位;位于1 155 cm-1处的仲羟基C-O伸缩振动峰与1 091 cm-1处的伯羟基C-O伸缩振动峰分别移至1 212 cm-1、1 133 cm-1处,同样表征了-OH参与了配位.
2.4 壳寡糖Fe(Ⅲ)配合物的紫外分析
图10为壳寡糖与壳寡糖Fe3+配合物的紫外谱图.
由图10可见,壳寡糖在波长范围内几乎没有吸收,而其Fe(Ⅲ)配合物在230 nm处有最大吸收峰,而且其峰形宽而强,其原因可能是配合物中的N、O孤对电子产生了n→σ*跃迁,致使光谱发生变化.由此可知,Fe3+确实与壳寡糖产生了配位反应.
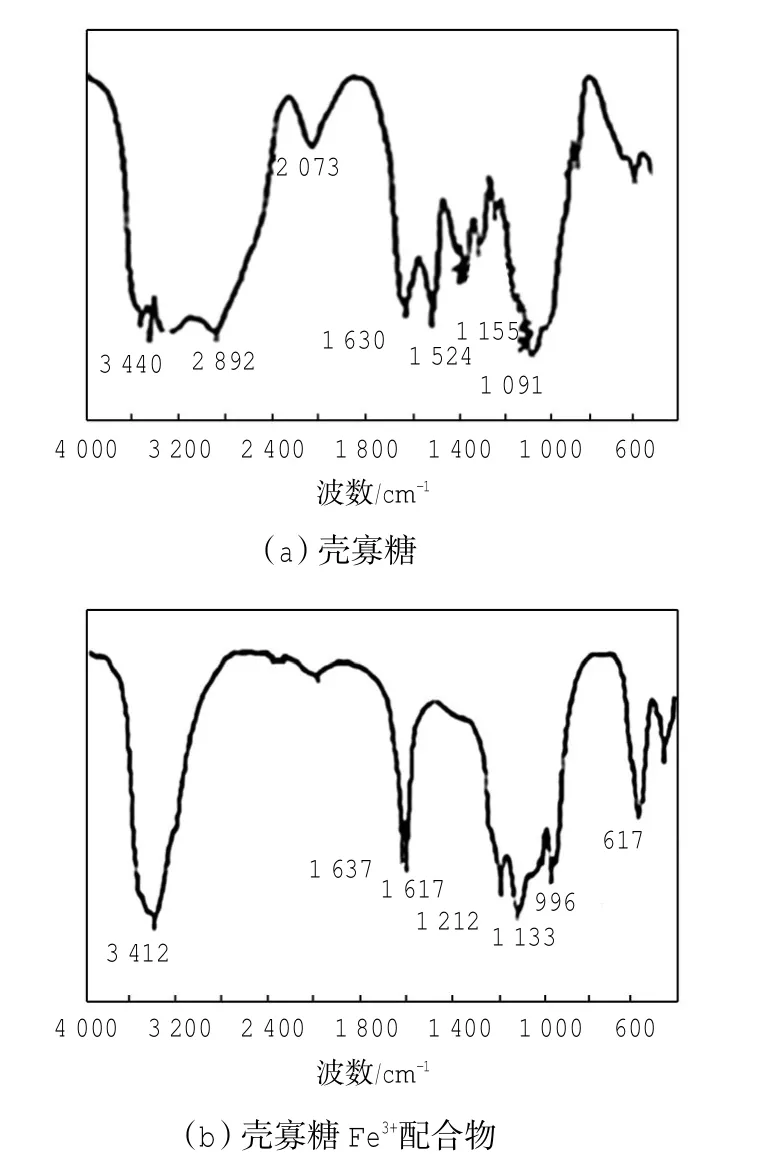
图9 壳寡糖与壳寡糖Fe3+配合物的红外谱图Fig.9 FT-IR spectrum of oligosaccharide and oligosaccharide-Fe3+complex
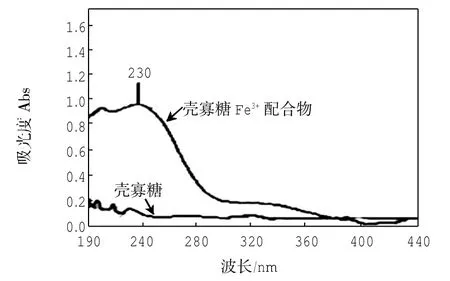
图10 壳寡糖与壳寡糖Fe3+配合物的紫外谱图Fig.10 UV spectrum of oligosaccharide and oligosaccharide-Fe3+complex
3 结论
(1)通过对高脱乙酰度壳聚糖和水溶性壳寡糖的工艺条件研究,优化了二者的制备工艺,得出前者最适宜条件为:温度85℃,时间9 h,NaOH质量分数45%,料液比1∶300.此条件下所得产品脱乙酰度为89.6%,收率(壳聚糖/甲壳素)为73.1%,其他各项指标也均为优良级.后者最适宜条件:温度65℃,时间6 h,醋酸质量分数4.0%,H2O2质量分数4.0%,产品平均粘均分子量为2.9 ku,外观为淡黄色粉末,溶解性能优良.
(2)对配合物的FT-IR和UV谱图分析表明:壳寡糖分子链上的-NH2与-OH确实与Fe3+发生了配位,证实了水溶性壳寡糖Fe(Ⅲ)配合物的生成.
(3)本文系统全面地介绍了优质壳聚糖与水溶性壳寡糖的制备工艺.同时,对水溶性壳寡糖与Fe(Ⅲ)的配位性质进行了初步研究,合成了水溶性壳寡糖Fe(Ⅲ)配合物.可将本文作为高分子材料和金属有机材料研究的有效参考.
[1]张文博,陈盛.甲壳素/壳聚糖的提取及应用研究新进展[J].福建师范大学福清分校学报,2008,2(1):18-25.
[2]蒋挺大.壳聚糖[M].北京:化学工业出版社,2007.
[3]季者,蒋霞云,李小倩,等.盐酸法降解壳聚糖制备特定聚合度壳寡糖的研究[J].上海海洋大学学报,2013,22(4):635-640.
[4]WANG Yu-Chi,KAO Shu-Huei,HSIEH Hsyue-Jen.A chemical surface modification of chitosan by glycoconjugates to enhancethecell-biomaterialinteraction[J].Biomacromolecules,2003(4):224-231.
[5]BALAN Vera,VERESTIUC Liliana.Strategies to improve chitosan hemocompatibility:A review[J].European Polymer Journal,2014(53):171-188.
[6] LIU shing-hwa,CHANG yu-han,CHING meng-tsan.Chitosan reduces gluconeogenesis and increases glucose uptake in skeletal muscle in streptozotocin-induced diabetic Rats[J]. Food Chem,2010(58):5795-5800.
[7]郑必胜,周萌.壳聚糖氧化降解制备壳寡糖的研究[J].现代食品科技,2012,28(8):960-965.
[8]杨俊玲.甲壳素和壳聚糖的化学改性研究[J].天津工业大学学报,2001,20(5):79-82.
[9]郎惠云,张秀军.不同分子量的壳聚糖亚铁配合物的合成及其对尿素的吸附性能[J].食品科学,2005,26(3):31-34.
[10]姜炜,李凤生.磁性-Fe2O3/壳聚糖复合微球的制备及性能[J].南京理工大学学报,2006,30(6):770-773.
[11]王孝平,姜皓然.壳聚糖与羧甲基壳聚糖对铁离子的络合性能研究[J].化学与生物工程,2009,26(3):30-33.
[12]蒋元勋,李海鹰,杨文智,等.壳聚糖脱乙酰度测定方法的总结与比较[J].应用化工,2011,40(10):1837-1840.
[13]王伟,薄淑琴,秦汶.不同脱乙酸度壳聚糖mrak-houwink方程的订定[J].中国科学,1990,11(11):1127-1131.
[14]陈鲁生,周武,姜云生.壳聚糖粘均分子量的测定[J].化学通报,1996(4):7-9.
[15]王亚珍,林雨露,吴天奎.粘度法测高聚物相对分子量实验成败探讨[J].江汉大学学报:自然科学版,2004,32(4):59-62.
Preparation process of quality CTS/soluble COS and synthesis of soluble COS-Fe(Ⅲ)complex
YANG Jun-ling,ZHAO Fu-long,XIA Jun,ZHANG Xiao-bo,WANG Xuan
(School of Environmental and Chemical Engineering,Tianjin Polytechnic University,Tianjin 300387,China)
HD-chitosan was produced with basic material-mantis shrimp shell which was removed inorganic salt with chlorhydric acid,proteins with dilute alkali solution,then dislodged acetyl group with concentrated alkaline solution.Next,the above-mentioned HD-chitosan was degraded with H2O2for producing soluble COS.With adjusted conditions,the soluble COS was added to ferric chloride solution for complexing.It was confirmed by series of experiments that the optimized conditions of preparing HD-chitosan was 45%NaOH,the ratio of material to solvent(g/ml)1∶300,and at constant temperature 85℃for 9 h.The yield of HD-chitosan to chitin was 73.1% with other excellent quality index.The optimized conditions of preparing soluble oligosaccharide was 4.0%acetic acid,4.0%H2O2and at constant temperature 65℃for 6 h.The viscosity average molecular weigh of products was 2.9 ku.In addition,it was also observed that the products of oligosaccharide was desirable faint yellow powder and had fine solubility.According to analysis of FT-IR and UV spectrum,the formation of soluble COS-Fe(Ⅲ)complex was certified.
HD-chitosan;soluble COS;soluble COS-Fe(Ⅲ)complex
TQ314.1
A
1671-024X(2014)05-0039-05
2014-05-20
国家自然科学基金项目(21101113)
杨俊玲(1957—),女,教授,硕士生导师.E-mail:yangjunling@tjpu.edu.cn

