胰激肽原酶治疗糖尿病肾病疗效的系统评价
陈晓正,陈曦,何健敏
(韶关市铁路医院内二科,广东韶关512023)
·循证医学·
胰激肽原酶治疗糖尿病肾病疗效的系统评价
陈晓正,陈曦,何健敏
(韶关市铁路医院内二科,广东韶关512023)
目的评价胰激肽原酶治疗糖尿病肾病的疗效。方法通过检索近二十年PubMed、Science Direct、EBSCO Host、EMbase、The Cochrane Library、中国学术期刊全文数据库、万方数据库、维普中文科技期刊全文数据库,对纳入研究的方法学进行评价。研究者对纳入文献的质量进行严格评价和资料提取,使用Review manager 5.0软件对符合质量标准的RCTs行系统评价。结果12个RCT共纳入762例患者,其中治疗组389例,对照组373例,系统评价结果显示,相比于血管紧张素Ⅱ受体拮抗剂、血管紧张素转化酶抑制剂、前列地尔,采用胰激肽原酶治疗糖尿病肾病,更能显著降低尿白蛋白排泄率,从而缓解糖尿病肾病的病理进程。结论胰激肽原酶可显著提升治疗糖尿病肾病的疗效,值得推广。
胰激肽原酶;糖尿病肾病;尿白蛋白排泄率
糖尿病肾病(Diabetic nephropathy,DN)是糖尿病最常见的微血管并发症之一,DN可累及肾小球、肾血管直至肾间质,所致肾脏损害呈进行性加重[1],若不积极处理将迅速引发慢性肾功能衰竭,是糖尿病患者死亡的主要原因。据2008年的调查结果显示,在20岁以上的成人中糖尿病的患病率为9.7%[2]。因此有效控制DN的发病和进展是当前内分泌医师所面临的重要课题。目前DN的治疗以控制血糖、血压为基础,缓解肾脏损伤,保护残余肾功能,延缓肾脏病变进程。但目前尚未见特效治疗方式能逆转DN所引起的肾功能损害[3]。DN主要病理改变特征为肾小球基底膜增厚、系膜细胞增生、肾小球毛细血管硬化等微血管病变,从而引起肾小球微循环障碍[4],因此激肽系统和肾素-血管紧张素-醛固酮系统(Renin-angiotensin-aldosterone system,RAAS)在DN病理进程中具有重要作用。胰激肽原酶(Kininogenase)通过激活激肽系统,扩张肾小球动脉壁和毛细血管,可显著改善微循环[5],使肾脏毛细血管功能得以恢复,从而抑制系膜细胞增殖、基底膜的增厚,延缓DN的进展。随着该药逐渐应用于临床,产生一系列相关研究,对其具体疗效产生了一定争论,且缺少循证医学依据。
系统评价作为循证医学的最高级别依据,能够有效整合多项相似研究成果,达到增大样本总量、降低随机误差、避免假阴性或假阳性结果的成效[6],从而进一步精确主要效应结果,对于临床工作具有重要指导意义。本文将参照Cochrane体系,对胰激肽原酶应用于DN的疗效进行系统评价,以期进一步明确其具体差异性。
1 资料与方法
1.1 文献检索系统评价作为对文献的二次评价,其检索不够全面则可造成数据偏倚、语种偏倚、查找偏倚等结果[7]。本研究经由两名研究员进行文献检索、评估、筛选、资料提取,然后交叉核对,如有分歧则协商解决,若难以达成一致,则与第三方商讨决定。为提高检索覆盖率,对于局部篇幅不全面的文献辅以手工检索、请求原文传递、文本追溯等方式。检索策略:①检索英文数据库:PubMed、Science Direct、EBSCO Host、EMbase、The Cochrane Library;中文数据库:中国学术期刊全文数据库(CNKI)、万方数据库(CECDB)、维普中文科技期刊全文数据库(CQVIP);②检索年限:1993年01月01日至2013年01月01日;③检索关键词:英文为“Diabetic nephropathy”、“Kininogenase”;中文为“胰激肽原酶”、“胰激肽原酶”;以“Randomized quasi-randomized controlled trials”或“随机分组对照试验”缩小检索范围;所有关键词之间以“And”或“和”连接;④检索对象限定为“Adult”或“成年”。
1.2 文献纳入标准①以论著形式发表,治疗DN的随机分组对照临床试验(RCT);②治疗组使用胰激肽原酶,对照组为血管紧张素Ⅱ受体拮抗剂(AngiotensinⅡreceptor antagonist,ARB)、血管紧张素转化酶抑制剂(Angiotensin converting enzyme inhibitors,ACEI)、前列地尔;③对DN的诊断标准相同[8];④治疗组和对照组的样本量明确;⑤论文明确注明了发表的时间、地点;⑥论文的研究类型、研究方法、研究人群均相同。
1.3 文献排除标准①排除“综述”、“述评”、“非随机分组的对照研究”、“会议报道”、“短篇病例报道”等论文;②根据改良版Jadad量表,排除低质量文献(Jadad≤2);③排除仅有摘要而无全文、内含信息量过少的文献;④排除未明确注明发表地点、作者单位、研究方向的文献;⑤排除未明确交代随访及疗程时间的文献;⑥排除治疗组病例数偏低(n≤10)的报道;⑦排除涵盖以下患者的研究报道:终末期肾衰竭、急性肾损伤、糖尿病以外其他原因所致慢性肾损伤、合并严重肝脏疾患、合并严重凝血功能障碍、恶性肿瘤。
1.4 质量评定根据Cochrane Handbook for Systematic Reviews评价手册推荐的方法学质量评价标准[9]对纳入RCTs的质量进行评估,具体内容包括:①采用何种随机分配方法,方法是否得当;②是否采用盲法,对哪些患者实施了盲法;③是否进行分配隐藏;④是否存在数据缺失及失访,是否采用意向性分析(ITT)原则处理;⑤结论数据的完整性及检验数据的稳健性;⑥结局指标的基线情况是否可比;⑦是否选择性报告研究结果。若完全满足上述7项标准,说明该RCT存在偏倚的风险较小,评为A级;满足3~6项上述标准说明发生偏倚的风险为中度,评为B级;满足质量标准低于2项说明发生偏倚的风险较高,评为C级。
1.5 资料提取筛选、核实所有RCTs后提取下述指标:①文献题目、第一作者、发表年限等基本资料;②研究设计、方法学质量指标;③研究对象的基线情况;④失访人数、失访处理;⑤相关干预措施、随访时限、结局指标;⑥连续性指标的均数、标准差,二分类指标的百分比。
1.6 统计学方法将数据提取后经进一步核对整理,使用Cochrane协作网提供的Review Manager 5.0软件进行系统评价。首先采用χ2检验测算各组研究的异质性,若各研究间不具有异质性(P>0.10,I2<50%),则采用PetoMantel-Haenszel固定效应模型;若异质性显著(P≤0.10,I2≥50%),则采用Dersimonian-Laird随机效应模型去除异质性,并探寻异质性原因。若P<0.10且无法判断异质性来源导致无法合并,则采用描述性分析,必要时行亚组分析,乃至于最终放弃系统评价。采用相对危险度(RR)及其95%可信区间(95%CI)表示二分类资料;采用权重均数差值(WMD)及其95%CI表示单位相同的连续变量资料;采用标准化均数差值(SMD)及其95%CI表示单位不同的连续变量资料。根据整合后的结果绘制森林图,以显示各项研究结论及其特征。以二分类资料RR对数值(LogRR)为横坐标,以RR对数值标准误的倒数1/SE(LogRR)为纵坐标绘制漏斗图,使用Stata 11.0软件的Egger线性回归模型检验漏斗图的散点分布是否对称,从而评估结果是否存在偏倚。再采用失效安全数进一步验证是否存在发表偏倚,并对结果进行稳定性分析。
2 结果
2.1 纳入研究的流程依照上述检索策略,本文初检得到相关文献179篇,其中137篇外文文献,42篇中文文献;按照文献纳入、排除标准剔除其来源及质量低劣、创新性欠缺的文献,纳入112篇文献;再经由阅读摘要初步筛除描述性研究及病例对照设计纳入37篇文献;最后通过阅读全文以全面评价RCTs质量,再度筛除其中非随机对照、欠缺明确对照组的文献,最终纳入12篇文献作为本次系统评价的RCT[10-21],其中外文文献10篇、中文文献2篇。文献检索与筛选纳入流程见图1,RCTs明细情况详见表1。

图1 文献检索与筛选纳入流程
2.2 纳入研究的基本特征经由方法学质量评价,本次纳入12篇RCT,有6篇[10-11,13-14,17,19]提及ITT分析,有4篇[12,15,17-18]详细描述了分配隐匿、随机分组的方法和过程,结局评价指标存在一定变异性。但整体可信度尚可(依从性、基线相似性较好),研究方法基本相似,治疗组和对照组之间基线可比(P>0.05),方法学质量为中等,文献最终质量评分均为B级,具体评价指标和结果见表2。再根据Cochrane协助网推荐的偏倚风险评估法则衡量所纳入的RCT,可见12篇文献均存在不同程度的偏倚,详见图2、图3。
2.3 纳入研究的基本内容纳入12篇RCT中治疗组与对照组的患者在年龄、既往史、收缩压等方面差异无统计学意义。均就两组患者经治疗后尿白蛋白排泄率(Urinary albumin excretion rates,UAER)进行了比较:①6篇RCT[10-12,15,17,20]以ARB为对照组;②3篇RCT[14,16,21]以ACEI为对照组;③3篇RCT[13,18-19]以前列地尔为对照组。
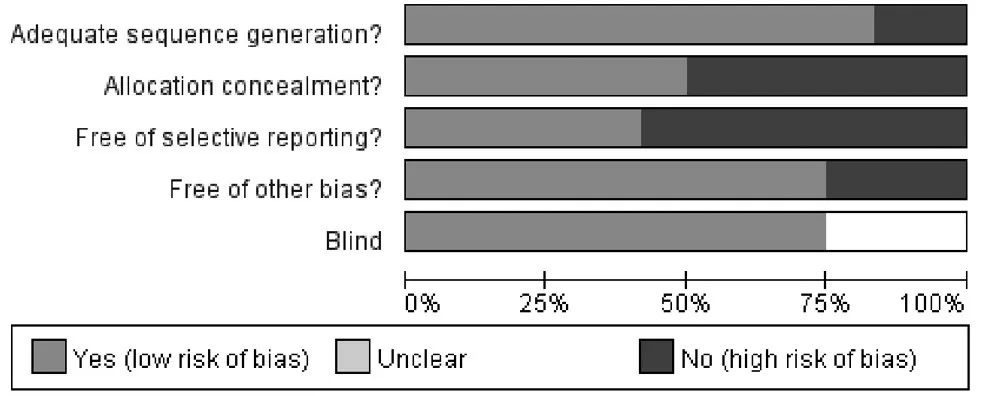
图2 12篇RCT的研究偏倚风险百分图
表1 纳入研究的一般情况

表1 纳入研究的一般情况

表2 纳入研究的质量评价

图3 12篇RCT的研究偏倚风险总结图
2.3.1 胰激肽原酶与ARB的疗效比较6篇RCT[10-12,15,17,20]对两组患者经治疗后UAER含量进行了报道。系统评价显示,纳入的研究不存在异质性(P=0.94,I2=0%),遂使用固定效应模型进行系统评价,合并效应值RR为-16.98,95%CI∈(-32.60,-1.37),结果显示两组患者差异具有统计学意义,即相比ARB治疗,使用胰激肽原酶可显著降低DN患者UAER含量,从而缓解症状、延缓病情进展。对其漏斗图分析结果显示:除一点外,其余各点基本呈倒置漏斗状分布,表明发表偏倚较小,进一步说明本次系统评价受发表偏倚的影响较小,结论可靠,见图4、图5。

图4 森林图[P=0.94、I2=0%、RR=-16.98、95%CI∈(-32.60,-1.37)]
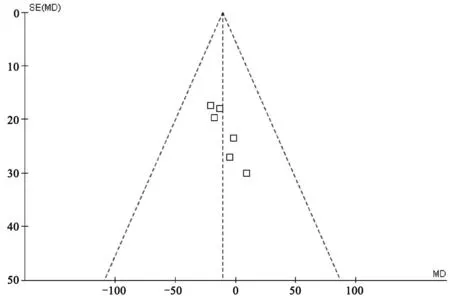
图5 漏斗图
根据公式N=K[(Z2-1.6452)]/1.645 2计算本研究的失效安全数,P取0.05水平,其中K表示需要合并的研究个数,Z表示合并效应统计检验的Z值,其结果为4.33。表明尚需要4篇以上的阴性研究结果加入才能逆转本次研究的结果,进一步说明了本次研究存在发表偏倚的可能性尚可,对研究结果的影响较小。再将合并研究的随机效应模型及固定效应模型互换,并未发现不同效应模型的结果发生逆转,表明本次系统评价结果稳定性良好。
2.3.2 胰激肽原酶与ACEI的疗效比较3篇RCT[14,16,21]对两组患者经治疗后UAER含量进行了报道。系统评价显示,纳入的研究不存在异质性(P= 0.16,I2=46%),遂使用固定效应模型进行系统评价,合并效应值RR为-44.99,95%CI∈(-70.00,-19.98),结果显示两组患者的差异具有统计意义,即相比ACEI治疗,使用胰激肽原酶可显著降低DN患者UAER含量,从而缓解症状、延缓病情进展。对其漏斗图分析结果显示:各点基本呈倒置漏斗状分布,表明发表偏倚较小,进一步说明本次系统评价受发表偏倚的影响较小,结论可靠,见图6、图7。

图6 森林图[P=0.16、I2=46%、RR=-44.99、95%CI∈(-70.00,-19.98)]

图7 漏斗图
根据公式N=K[(Z2-1.6452)]/1.6452计算本研究的失效安全数,P取0.05水平,其中K表示需要合并的研究个数,Z表示合并效应统计检验的Z值,其结果为6.97。表明需要近7篇阴性研究结果加入才能逆转本次研究的结果,进一步说明了本次研究存在发表偏倚的可能性尚可,对研究结果的影响较小。再将合并研究的随机效应模型及固定效应模型互换,并未发现不同效应模型的结果发生逆转,表明本次系统评价结果稳定性良好。
2.3.3 胰激肽原酶与前列地尔的疗效比较3篇RCT[13,18-19]对两组患者经治疗后UAER含量进行了报道。系统评价显示,纳入的研究不存在异质性(P= 0.74,I2=0%),遂使用固定效应模型进行系统评价,合并效应值RR为-16.97,95%CI∈(-34.45,0.51),结果显示两组患者的差异具有统计意义,即相比前列地尔治疗,使用胰激肽原酶可显著降低DN患者UAER含量,从而缓解症状、延缓病情进展。对其漏斗图分析结果显示:各点基本呈倒置漏斗状分布,表明发表偏倚较小,进一步说明本次系统评价受发表偏倚的影响较小,结论可靠,见图8、图9。

图8 森林图[P=0.74、I2=0%、RR=-16.97、95%CI∈(-34.45,0.51)]
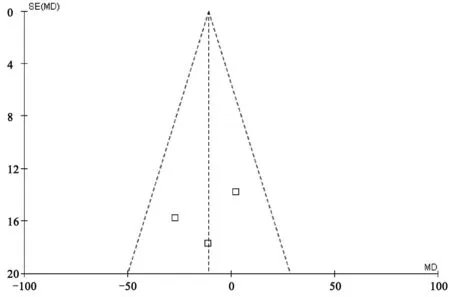
图9 漏斗图
根据公式N=K[(Z2-1.6452)]/1.645 2计算本研究的失效安全数,P取0.05水平,其中K表示需要合并的研究个数,Z表示合并效应统计检验的Z值,其结果为2.69。表明需要至少2篇阴性研究结果加入才能逆转本次研究的结果,进一步说明了本次研究存在发表偏倚的可能性尚可,对研究结果的影响较小。再将合并研究的随机效应模型及固定效应模型互换,并未发现不同效应模型的结果发生逆转,表明本次系统评价结果稳定性良好。
2.3.4 纳入研究中发生不良反应的报道2篇RCT[13,17]报道患者出现肝功能损伤:其中Lei等[13]为3例(治疗组1例+对照组2例)、Późniak等[17]为5例患者(治疗组3例+对照组2例);Vío等[19]报道治疗组3例患者出现乏力、头昏症状,对照组1例患者并发腰骶部疼痛;Yu等[20]报道治疗组1例患者出现牙龈出血、1例患者引起顽固性高磷血症伴甲状旁腺素异常,具体机理有待进一步探讨。
3 讨论
胰激肽原酶是从猪胰腺组织中提取具有舒张血管作用的循环系统酶,在体内作用于激肽原释放出激肽,从而产生相应药理作用:①舒张微小动脉和毛细血管,改善微循环[22];②激活磷酸脂酶A2,促使肾髓质分泌前列腺素E2[22],抑制氧化应激[14],增加血流量;③促进前列环素(PGI2)分泌,抑制血栓素(TXA2)生成,避免血小板过度聚集[23],降低血黏度,预防血栓形成,避免加重肾脏微循环损害。
本研究通过综合既往文献对胰激肽原酶治疗DN的疗效做了进一步分析,基于本文纳入的12篇RCT,其结果为:①采用胰激肽原酶治疗DN,较ARB可显著降低患者UAER含量;②采用胰激肽原酶治疗DN,较ACEI可显著降低患者UAER含量;③采用胰激肽原酶治疗DN,较前列地尔可显著降低患者UAER含量。分析其原因可能为:①胰激肽原酶通过扩张肾脏出球小动脉改善局部循环血流[15],降低出入球小动脉之间的压力差,缓解肾小球内压[19],从而显著降低肾小球基底膜通透性[17],减缓肾小球的损害;②胰激肽原酶通过降低TXA2/PGI2比例,从而阻断TXA2-血栓形成-TXA2的恶性循环链条,纠正肾脏的微循环失衡[21]。
基于本文纳入的12篇RCT,其局限性为:①根据改良版Jadad量表,1篇纳入的RCT[21]质量相对欠佳,6篇RCT[10-11,13-14,17,19]提及ITT分析,4篇RCT[12,15,17-18]详细描述了分配隐匿。由于本研究疗程长、涉及长期随访,难以做到患者及干预者的双盲,故纳入RCT均为评价者单盲。综合上述因素,系统评价结果可能存在少许选择&测量偏移;②纳入研究的样本量相对较少,12篇RCT共纳入762例患者,故代表性相对较差,致系统评价结果的推广受到限制;③未进行费用-效益分析;④纳入RCT缺少对DN患者远期预后进行长期随访;⑤纳入RCT并未就胰激肽原酶与其他药物联合治疗DN的疗效做深入分析,而通过本次研究证实,胰激肽原酶与ARB类药物联用具有良好的互补性,其联用与单药的疗效对比需要在今后研究中进一步完善。
系统评价能克服单个RCT研究样本量偏小、结果变异大等缺陷,在资料一致性的前提下,通过综合同类研究,应用循证医学对大量单项研究结果进行统计分析,评价其合并效应量,使结果更客观,从而得出全面、量化的理论依据。但系统评价并非真正意义的疗效试验性研究,不能取代大规模、多中心的随机分组对照试验,只是对现有RCTs的系统整合、定量分析的结果,随着新的研究证据出现,其结论必然不断加以更新。再者,限于作者自身循证医学水平有限,文献检索及筛选的全面精确性尚有所欠缺,故而在后续研究中应继续追踪国内外相关的临床研究,严格遵守循证医学的理论,使研究结果更加客观可靠,以期进一步指导临床。
综上所述,受纳入RCTs所限,本次系统评价结论尚需更多高质量研究以进一步充分验证其预后,但胰激肽原酶治疗DN的疗效显著,得到充分肯定,值得广泛推广。
[1]Zuccollo A,Navarro M,Catanzaro O.The diabetic nephropathy and the development of hypertension in rats[J].Int J Exp Diabetes Res, 2001l,2(3):195-199.
[2]中华医学会糖尿病学分会.中国2型糖尿病防治指南(2010年版) [J].中国糖尿病杂志,2012,20(1):s1-s37.
[3]Yuan G,Deng J,Wang T,et al.Tissue kallikrein reverses insulin resistance and attenuates nephropathy in diabetic rats by activation of phosphatidylinositol3-kinase/proteinkinaseBandadenosine 5'-monophosphate-activated protein kinase signaling pathways[J]. Endocrinology,2007,148(5):2016-2026.
[4]刘婧承,李竞.厄贝沙坦联合前列地尔治疗糖尿病肾病的Meta分析[J].临床内科杂志,2012,29(9):622-623.
[5]石琳琳,张秀英,刘波,等.胰激肽原酶治疗早期糖尿病肾病和临床糖尿病肾病的疗效比较[J].吉林大学学报,2005,31(6): 935-936.
[6]赵耐青.临床医学研究设计和数据分析[M].上海:复旦大学出社, 2005:275-291.
[7]薛茜,张茜.浅谈META分析常见的偏倚[M].循证医学, 2006,6(2):105-108.
[8]Mogensen CE.Management of eariy nephropathy in diabetic patients[J].Annu Rev Med,1995,10(46):79-80.
[9]Higgins JPT,Green S.Cochrane Handbook for Systematic Reviews of Interventions version 5.0.2[M].The Cochrane Collaboration, 2009:201-203.
[10]Bodin S,Chollet C,Goncalves-Mendes N,et al.Kallikrein protects against microalbuminuria in experimental type I diabetes[J].Kidney Int,2009,76(4):395-403.
[11]Jaffa AA,Durazo-Arvizu R,Zheng D,et al.Plasma prekallikrein:a risk marker for hypertension and nephropathy in type 1 diabetes[J]. Diabetes,2003,52(5):1215-1221.
[12]Kayashima Y,Smithies O,Kakoki M.The kallikrein-kinin system and oxidative stress[J].Curr Opin Nephrol Hypertens,2012,21(1): 92-96.
[13]Lei L,Mao Y,Meng D,et al.Diabetic nephropathy is associated with prostate-specific antigen levels in type 2 diabetes mellitus[J]. Cancer Causes Control,2012,23(11):1875-1879.
[14]廖渝,尹南,陈心怡,等.胰激肽原酶与依那普利联合治疗临床糖尿病肾病疗效分析[J].湘南学院学报,2009,11(3):41-42.
[15]Manto A,Cotroneo P,Porcelli G,et al.Urinary kallikrein excretion in type 1(insulin-dependent)diabetes mellitus[J].Diabetologia, 1993,36(5):423-427.
[16]Pérez-Blanco FJ,Manzanares-Olivares L,Domínguez-Vicent JR,et al.Urinary kallikrein excretion in early diabetic nephropathy[J]. Clin Nephrol,1997,47(1):64-65.
[17]Późniak J.Regulation of natriuresis in diabetic nephropathy[J].Ann Acad Med Stetin,2000,46(10):241-252.
[18]Tang SC,Leung JC,Lai KN.The kallikrein-kinin system[J].Contrib Nephrol,2011,10(170):145-155.
[19]Vío CP,Jeanneret VA.Local induction of angiotensin-converting enzyme in the kidney as a mechanism of progressive renal diseases [J].Kidney Int Suppl,2003,10(86):57-63.
[20]Yu H,Bowden DW,Spray BJ,et al.Identification of human plasma kallikrein gene polymorphisms and evaluation of their role in end-stage renal disease[J].Hypertension,1998,31(4):906-911.
[21]赵伟河,田永红,王守林,等.胰激肽原酶与依那普利治疗糖尿病肾病的对照研究[J].中国医师进修杂志.2006,29(18):9-11.
[22]Allard J,Buléon M,Cellier E,et al.ACE inhibitor reduces growth factor receptor expression and signaling but also albuminuria through B2-kinin glomerular receptor activation in diabetic rats [J].Am J Physiol Renal Physiol,2007,293(4):1083-1092.
[23]Pérez Blanco FJ,Cuesta López MJ,Fernández García C,et al.Renal kallikrein in diabetic nephropathy[J].Rev Clin Esp,1991,188 (3):123-126.
Clinical efficacy of Kininogenase in the treatment of diabetic nephropathy:a systematic evaluation.
CHEN Xiao-zheng,CHEN Xi,HE Jian-min.Department of Internal Medicine,Shaoguan Railway Hospital,Shaoguan 512023, Guangdong,CHINA
ObjectiveTo evaluate the clinical efficacy of Kininogenase in the treatment of diabetic nephropathy.MethodsThe methodology were evaluated based on references in the recent 20 years from PubMed,Science Direct,EBSCO Host,EMBASE,The Cochrane Library,CNKI,CECDB CQVIP.The researchers performed rigorous evaluation on the quality of the included studies and extracted data.The Review Manager 5.0 Software was used to evaluate the qualified randomized controlled trials(RCTs).ResultsTwelve RCTs were included,involving 762 patients(389 cases of the treatment group and 373 cases of the control group).Compared to angiotensinⅡreceptor antagonist(ARB),angiotensin converting enzyme inhibitors(ACEI),alprostadil,kininogenase can significantly reduce the urinary albumin excretion rate in the treatment of diabetic nephropathy,thus alleviating the pathological process of diabetic nephropathy.ConclusionKininogenase has significant curative effect in the treatment of diabetic nephropathy and is worthy of promotion.
Kininogenase;Diabetic nephropathy;Urinary albumin excretion rate
R587.2
A
1003—6350(2014)01—0119—07
10.3969/j.issn.1003-6350.2014.01.0047
2013-06-02)
陈晓正。E-mail:gdsgcxz@163.com

