GN化疗方案治疗晚期非小细胞肺癌疗效观察
沈维敏(上海市华东医院,上海200040)
GN化疗方案治疗晚期非小细胞肺癌疗效观察
沈维敏
(上海市华东医院,上海200040)
摘要:目的观察吉西他滨、长春瑞滨联合( GN方案)治疗晚期非小细胞肺癌( NSCLC)的疗效,以及对血清肿瘤标志物癌胚抗原( CEA)、糖类抗原125( CA125)、细胞角蛋白片段19( Cyfra21-1)的影响。方法将68例晚期NSCLC患者随机分为观察组33例和对照组35例,分别采用GN方案和紫杉醇+顺铂化疗; 2个疗程后观察疗效,记录不良反应发生情况,治疗前及治疗后半年检测血清CEA、CA125、Cyfra21-1。结果观察组有效率为57.58%、疾病控制率为84.85%,对照组分别为34.29%、74.28%,P均<0.01;两组不良反应比较,P均>0.05;治疗后半年,两组血清CEA、CA125、Cyfra21-1水平较治疗前显著下降,观察组均低于对照组,P均<0.05。结论GN方案治疗晚期NSCLC可提高疗效、降低血清肿瘤标志物水平,且不增加不良反应的发生。
关键词:非小细胞肺癌;吉西他滨;长春瑞滨;癌胚抗原;糖类抗原125;细胞角蛋白片段19
目前,对于晚期或已有远处转移的非小细胞肺癌( NSCLC)多采用化疗,以顺铂为主的联合化疗是标准治疗方案[1~4],但其疗效有降低趋势。2010年6月~2013年6月,我们采用吉西他滨、长春瑞滨联合( GN方案)治疗晚期NSCLC患者33例,观察其疗效及对血清肿瘤标志物癌胚抗原( CEA)、糖类抗原125( CA125)、细胞角蛋白片段19( Cyfra21-1)的影响。现报告如下。
1 资料与方法
1.1临床资料选择上海市华东医院收治的晚期NSCLC患者68例,均经病理或细胞学检查确诊,排除合并其他严重疾病患者,预期生存期大于半年。其中,男33例、女35例,年龄43~76 ( 63.4±4.9)岁;鳞癌38例,腺癌30例。将患者随机分为观察组33例和对照组35例,两组临床资料具有可比性。
1.2方法
1.2.1治疗方法观察组行GN方案化疗,吉西他滨1 000 mg/m2静脉滴注30 min,第1、8天;长春瑞滨25 mg/m2静脉推注,21 d重复1次。对照组予紫杉醇175 mg/m2溶于生理盐水250 mL静脉滴注,用药结束30 min后静脉滴注顺铂75 mg/m22 h,第1 ~3天,21 d为1个周期。两组均于2个疗程后观察临床疗效。
1.2.2评价标准疗效评价参考WHO实体瘤疗效评价标准,分为完全缓解( CR)、部分缓解( PR)、无变化( SD)与进展( PD)。其中,有效率( RR) = ( CR + PR)/总例数×100%,疾病控制率( DCR) = ( CR + PR + SD)/总例数×100%。不良反应应按WHO抗癌药物急性和亚急性毒性反应分度标准进行评价,分为0~Ⅳ级。
1.2.3血清肿瘤标志物检测方法于治疗前、治疗完成后半年采集空腹静脉血5 mL,2 500 r/min离心20 min,取血清-20℃保存。采用全自动化学发光免疫分析仪及其配套试剂盒(罗氏公司)检测血清CEA、CA125、Cyfra21-1,判断标准采用试剂盒推荐标准。
1.2.4统计学方法采用SPSS15.0统计软件。计量资料以珋x±s表示,采用t检验;计数资料以率表示,采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1两组疗效比较观察组CR 9例、PR 10例、SD 9例、PD 5例,对照组分别为4、8、14、9例。观察组RR为57.58%、DCR为84.85%,对照组分别为34.29%、74.28%,两组RR、DCR相比差异有统计学意义(χ2= 8.125,P =0.05;χ2=11.564,P<0.01)。
2.2两组不良反应比较观察组血小板减少Ⅲ~Ⅳ度10例、中性粒细胞减少Ⅲ~Ⅳ度7例、贫血Ⅲ~Ⅳ度3例,对照组分别为12、6、4例,P均>0.05。观察组出现轻度蛋白尿8例、轻度肝损伤1例,对照组分别为7、2例,P均>0.05。两组未发生因治疗产生的相关死亡。
2.3两组治疗前后血清CEA、CA125、Cyfra21-1比较见表1。
表1 两组治疗前后血清CEA、CA125、Cyfra21-1比较(±s)
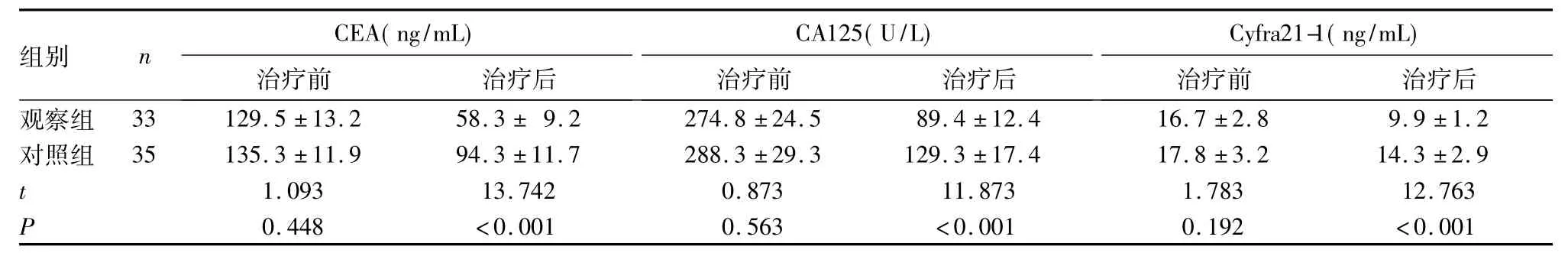
表1 两组治疗前后血清CEA、CA125、Cyfra21-1比较(±s)
组别 n CEA( ng/mL)治疗前 治疗后CA125( U/L)治疗前 治疗后Cyfra21-1( ng/mL)治疗前 治疗后观察组 33 129.5±13.2 58.3±9.2 274.8±24.5 89.4±12.416.7±2.8 9.9±1.2对照组 35 135.3±11.9 94.3±11.7 288.3±29.3 129.3±17.4 17.8±3.2 14.3±2.9 t 1.093 13.742 0.873 11.873 1.783 12.763 P 0.448 <0.001 0.563 <0.001 0.192 <0.001
3 讨论
研究发现,晚期NSCLC不论采用何种治疗方案,均存在一定的不足[5]。NSCLC是一种在分子生物学上个体差异极大的疾病,因此开展个体化化疗将成为一种趋势[6~8]。研究发现,切除修复交叉互补基因1在抗肿瘤的治疗中非常重要,其高表达能增加肿瘤对铂类抗肿瘤药物的耐药性[9],这也是临床铂类药物使用一段时间后药效明显降低的原因。然而,吉西他滨可增加肿瘤细胞对其他药物的敏感性,并具有抑制DNA合成的效果;同时,长春瑞滨可与微管蛋白结合,使细胞在有丝分裂过程中微管形成障碍[10~13]。本研究结果显示,吉西他滨、长春瑞滨联合应用,可达到良好的化疗效果。
肿瘤标志物水平的监测用于肿瘤诊断与疗效判定,已得到大多数学者的公认。CEA是存在于癌组织和胚胎组织中的一种高分子糖蛋白,在肺癌中阳性表达率约50%,与肿瘤转移和复发相关。CA125是糖蛋白复合物,在NSCLC中阳性率可达40%,对预测化疗的敏感性和疗效有重要意义。CYFRA21-1可作为肺磷癌首选肿瘤标志物,在晚期小细胞肺癌患者血清中显著升高,在判断肺癌疗效中具有重要意义[14]。本研究发现,治疗后半年,观察组血清CEA、CA125、Cyfra21-1显著低于对照组。由此可见,GN方案治疗NSCLC相比传统的铂类药物组合具有优势。
参考文献:
[1]Barlesi F,Chouaid C,Crequit J,et al.A randomized trial comparing adjuvant chemotherapy with gemcitabine plus cisplatin with docetaxel plus cisplatin in patients with completely resected nonsmall-cell lung cancer with quality of life as the primary objective [J].Interact Cardiovasc Thorac Surg,2015,20( 6) : 783-790.
[2]Moro-Sibilot D,Smit E,de Castro Carpeno J,et al.Outcomes and resource use of non-small cell lung cancer ( NSCLC) patients treated with first-line platinum-based chemotherapy across Europe: FRAME prospective observational study[J].Lung Cancer,2015,88( 2) : 215-222.
[3]Kotsakis A,Kentepozidis N,Emmanouilidis CH,et al.Sequential administration of vinorelbine plus cisplatin and bevacizumab followed by docetaxel plus gemcitabine and bevacizumab compared to docetaxel plus cisplatin and bevacizumab regimen as first-line therapy for advanced or metastatic non-squamous non-small cell lung cancer: A multicenter randomized phaseⅡtrial of the Hellenic Oncology Research Group ( HORG)[J].Lung Cancer,2015,88( 1) :57-62.
[4]Pilkington G,Boland A,Brown T,et al.A systematic review of the clinical effectiveness of first-line chemotherapy for adult patients with locally advanced or metastatic non-small cell lung cancer [J].Thorax,2015,70( 4) : 359-367.
[5]Moldvay J,Rokszin G,Abonyi-Tóth Z,et al.Lung cancer drug therapy in Hungary 3-year experience[J].Oncol Targets Ther,2015,( 8) : 1031-1038.
[6]Dingemans AM,Bootsma G,van Baardwijk A,et al.A phase I study of concurrent individualized,isotoxic accelerated radiotherapy and cisplatin-vinorelbine-cetuximab in patients with stageⅢnon-small-cell lung cancer[J].J Thorac Oncol,2014,9( 5) :710-716.
[7]Zustovich F,Ferro A,Lombardi G,et al.Bevacizumab-based therapy for patients with brain metastases from non-small-cell lung cancer: preliminary results[J].Chemotherapy,2015,60( 5) :294-299.
[8]Zhong W,Yang X,Yan H,et al.PhaseⅡstudy of biomarkerguided neoadjuvant treatment strategy forⅢA-N2 non-small cell lung cancer based on epidermal growth factor receptor mutation status[J].J Hematol Oncol,2015,8( 1) : 54.
[9]Deng Q,Yang H,Lin Y,et al.Prognostic value of ERCC1 mRNA expression in non-small cell lung cancer,breast cancer,and gastric cancer in patients from Southern China[J].Int J Clin Exp Pathol,2014,7( 12) : 8312-8321.
[10]Subhani S,Jayaraman A,Jamil K.Homology modelling and molecular docking of MDR1 with chemotherapeutic agents in non-small cell lung cancer[J].Biomed Pharmacother,2015,( 71) :37-45.
[11]Geater SL,Xu CR,Zhou C,et al.Symptom and quality of life improvement in lux-lung 6: an open-label phaseⅢstudy of afatinib versus cisplatin/gemcitabine in asian patients with egfr mutationpositive advanced non-small-cell lung cancer[J].J Thorac Oncol,2015,10( 6) : 883-889.
[12]Bondarenko IM,Ingrosso A,Bycott P,et al.PhaseⅡstudy of axitinib with doublet chemotherapy in patients with advanced squamous nonsmall-cell lung cancer[J].BMC Cancer,2015,15( 1) :339.
[13]Go SI,Lee WS,Lee GW,et al.Gemcitabine plus vinorelbine as the second-line treatment and beyond in elderly patients with platinum-pretreated advanced non-small cell lung cancer[J].Chemotherapy,2014,60( 4) : 267-273.
[14]Ji Z,Bi N,Wang J,et al.Risk factors for brain metastases in locally advanced non-small cell lung cancer with definitive chest radiation[J].Int J Radiat Oncol Biol Phys,2014,89( 2) : 330-337.
收稿日期:( 2015-01-12)
文章编号:1002-266X( 2015) 30-0043-02
文献标志码:B
中图分类号:R734.2
doi:10.3969/j.issn.1002-266X.2015.30.017

