别嘌醇及非布司他治疗中国痛风患者的成本效果
焦 洋,方卫纲,曾学军
(中国医学科学院 北京协和医学院 北京协和医院普通内科, 北京 100730)
ChinJAllergyClinImmunol,2016,10(4):334- 339
血尿酸代谢异常引起高尿酸血症,而当尿酸盐结晶沉积到关节内引起急性炎症反应则进展为痛风。痛风急性发作可导致非常剧烈的疼痛,而长期慢性炎症则进一步导致关节畸形、破坏和功能丧失。近年随着中国大陆地区经济快速发展,人群生活方式的明显改变,中国高尿酸血症和痛风的发病率和患病率均显著增加,根据最新统计分析结果,高尿酸血症患者已占总人口13.3%,痛风患者约占总人口1.1%[1]。别嘌醇和非布司他是两种黄嘌呤氧化酶(xanthine oxidase,XO)抑制剂类的降尿酸药物,分别于1966年及2009年开始被美国食品药品监督管理局(Food and Drug Administration,FDA)批准用于降尿酸治疗,也是目前国际上降尿酸治疗最主要的用药。虽然在临床研究中非布司他与别嘌醇相比起效更快,治疗达标比例及药物不良反应基本相当,但药品价格却明显高于别嘌醇[2- 6]。尽管2012年美国风湿免疫医师协会的痛风诊治指南推荐两种药物均为一线治疗选择,但该指南是基于RAND-UCLA共识法制定,并未充分考虑降尿酸治疗的成本或成本效果。而这一点对于筛选符合中国国情、具备最佳成本效益的降尿酸治疗方案却是非常重要的。到目前为止,基于中国人群的降尿酸治疗方案中,两种临床药物的常用剂量与国外有一定差异,而基于国内医疗卫生系统及人群流行病学调查结果的相关经济成本花费及临床效果方面的数据尚存在空白。本研究通过建立合理的卫生经济学分析模型,结合已发表的流行病学数据进行比较和评估,从而获取相对可靠的成本效果分析结果,为我国拟定和实施最优化降尿酸治疗策略提供证据支持。
资料和方法
研究对象
模型研究对象为中国大陆地区成年患者,临床确诊为慢性痛风,血尿酸水平>476 μmol/L,无明显肝肾功能损害,对别嘌醇及非布司他无过敏。根据目前国内常用临床方案,比较以下三种治疗策略:(1)首选别嘌醇 300 mg、1次/d治疗;6个月后评估如果未达标(血尿酸水平<360 μmol/L)则改为非布司他 40 mg、1次/d治疗;6个月后再次评估如果仍未达标则加量至非布司他 80 mg、1次/d治疗;(2)首选非布司他 40 mg、1次/d治疗;6个月后评估如果仍未达标则加量至非布司他 80 mg、1次/d治疗;(3)不治疗。
模型及代入参数设定
研究选取医疗健康服务提供者角度,因此仅纳入直接医疗成本。通过决策树模型(图1)对上述基于别嘌醇或非布司他为首选药物的降尿酸治疗成本效果进行分析。每次用药方案的治疗观察期为6个月。治疗成本效果观察时间跨度2年。治疗成功达标(血尿酸水平降低至<360 μmol/L)患者被认为将维持当前治疗。而在6个月观察周期内未达标患者将调整治疗方案,如无进一步治疗方案可调整则设定患者将放弃治疗。直接医疗成本包括:降尿酸药物成本、急性发作期用药成本、专科医师诊视成本以及肝肾功能、尿酸等检查成本等。痛风急性发作被认为平均需要1次急诊医师就诊及1次专科医师门诊就诊,降尿酸治疗每次开始新方案治疗的2周末、3个月末和6个月末至少需要各1次专科医师门诊就诊及抽血评估(服用别嘌醇患者评估肝肾功能、尿酸和血常规;服用非布司他患者评估肝功能和尿酸)。服药2周末出现肝功能异常患者平均需要1次复查和2次专科医师门诊就诊。由于国内患者临床接受度与欧美国家患者的差异,虽然开始降尿酸治疗可引起早期急性痛风发作频率增高,但目前国内降尿酸治疗未应用至少8周以上的预防性治疗,因此未将预防性治疗费用加入到模型计算当中[7]。模型主要收益为节省的质量调整生命年(quality-adjusted life year,QALY)。所有成本均以2015年人民币值计算。采用3倍人均国内生产总值(gross domestic product,GDP)为支付意愿阈值,根据中国国家统计局公布数据,2015年人均GDP为5.2万元,故本研究支付意愿阈值为15.6万元/QALY。结果显示为增量成本效果比,即为增加成本/增加临床收益。模型运算的基准分析数据主要采纳中国大陆地区完成并发表的多中心、随机、双盲临床药物试验结果[5,8]。各药物临床治疗效率数据及并发症发病率的变化范围区间部分由其他已发表相关文献中归纳总结获得(表1)。
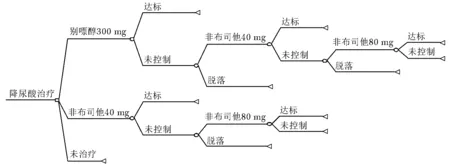
图1决策树模型示意图
Fig1Sketch map of decision tree model
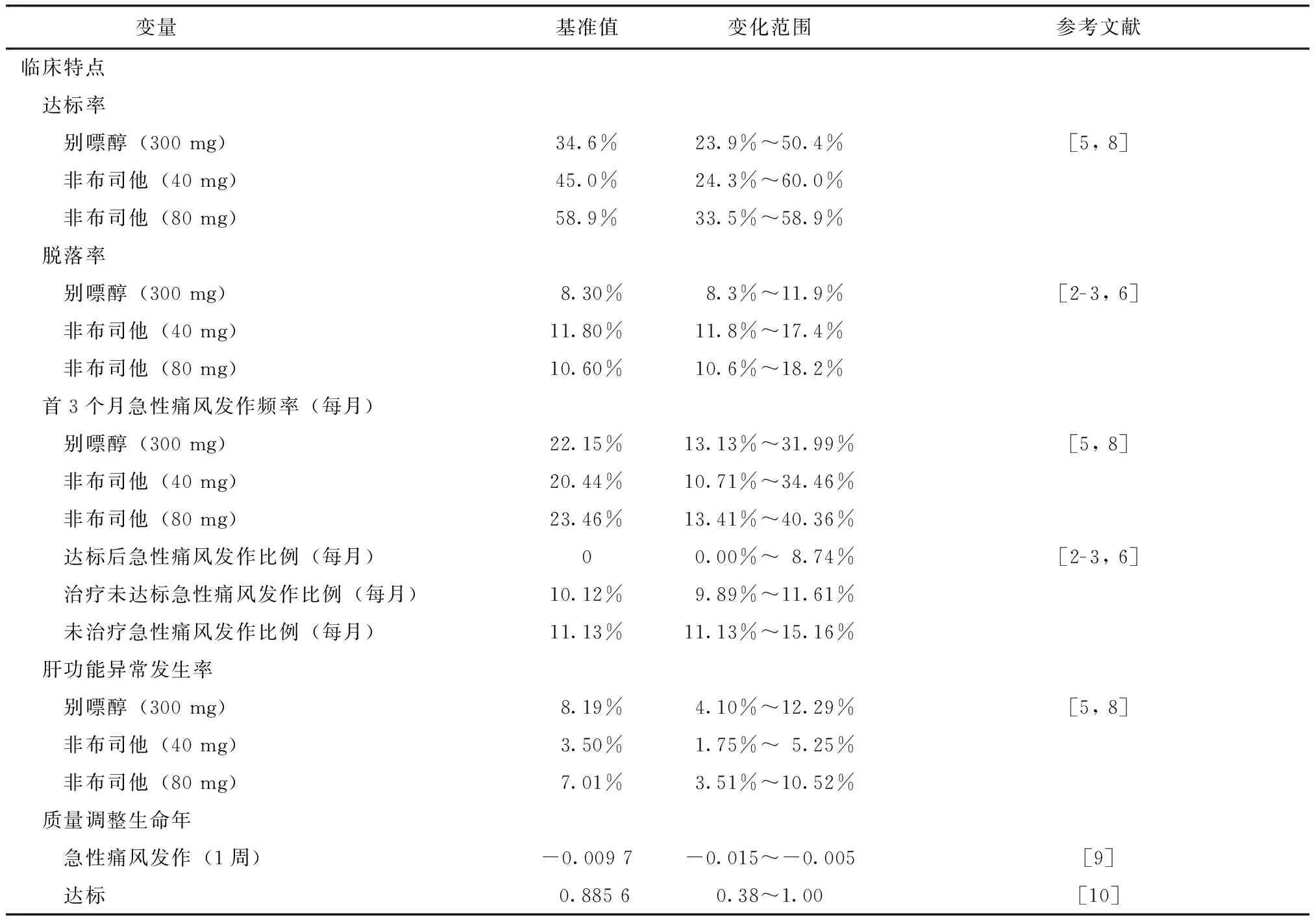
表1 决策树模型参数:基准值和变化范围Table 1 Decision tree model parameters: reference value and range of variation
续表1

变量基准值变化范围参考文献 未达标0.72670.35~0.75 未治疗0.61380.33~0.75成本 降尿酸治疗药费(6个月) 医疗服务成本基准值主要参考中国大陆地区医疗服务价格及专家意见 别嘌醇(300mg)148元74 ~ 222 元 非布司他(40mg)5040元2520 ~7560 元 非布司他(80mg)10080元5040 ~15120 元 急性发作治疗药费85元42.5~127.5元 专科医师诊疗5元2.5~7.5元 急诊医师诊疗5元2.5~7.5元 肝功能40元20 ~60 元 肾功能11元5.5~16.5元 尿酸5元2.5~7.5元 全血细胞分析20元10 ~30 元
敏感性分析
敏感性分析应用Tornado分析方法用于评估模型中所有设定参数的不确定性会对最终结果的影响。基准值如有95%置信区间数据,将应用置信区间数据;如无,则将相关参数以基准值±50%范围或基于已发表文献复习结果获得参数变化区间来代入进行敏感性分析[11](表1)。
统计学处理
模型建立与数据分析采用Treeage Pro 2016软件。治疗方案的增量成本效果比(incremental cost-effectiveness ratio,ICER)与成本效果阈值比较,若结果低于成本效果阈值则认为该方案具有成本效果。
结 果
增量成本效果比
三种不同降尿酸治疗策略的成本、效果及增量成本效果比结果显示:对于无明显肝肾功能损害、对别嘌醇及非布司他无过敏或不耐受的成人痛风患者,应用别嘌醇作为一线治疗药物,如不能达标再转为应用非布司他治疗的方案为优选方案。与直接应用非布司他作为一线方案比,两者QALY获益基本相当,但前者临床花费明显低于后者(表2)。
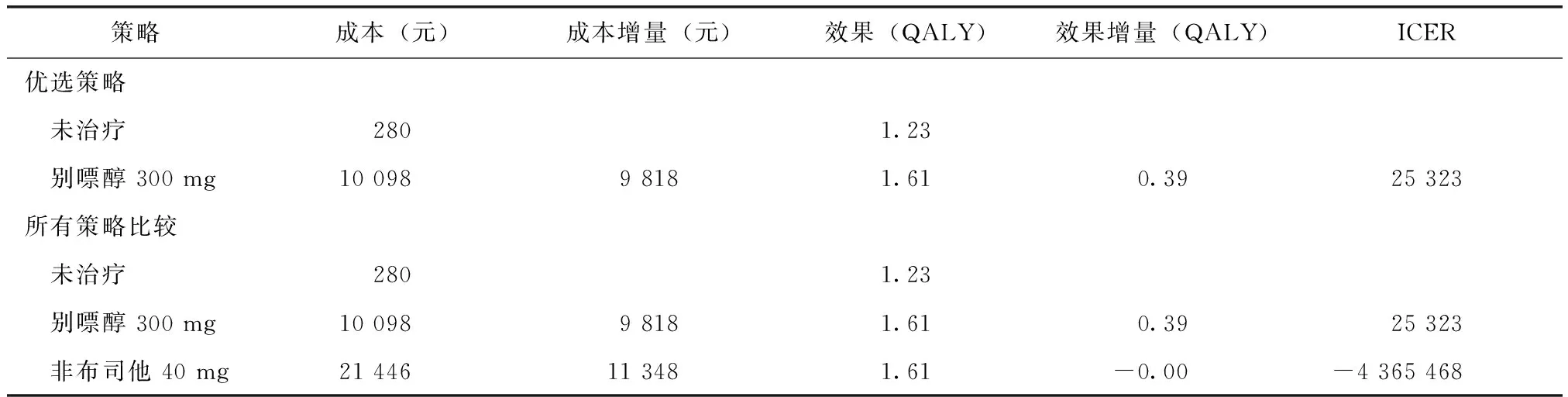
表2 降尿酸治疗策略比较结果Table 2 Comparison of therapeutic strategies for lowering uric acid
QALY:质量调整生命年; ICER:增量成本效果比
敏感性分析
敏感性分析结果表明达标治疗后、未达标以及未经治疗的QALY值,别嘌醇和非布司他治疗6个月的临床达标率,非布司他40 mg的药物价格是6个最主要的对增量成本效果结论的影响因素。
讨 论
持续的高尿酸血症是进展为痛风的主要病理生理机制。而充分达标的降尿酸治疗是有效控制痛风病情进展、改善患者生活质量的前提条件。近年随痛风发病率及患病率的显著提高,由其带来的疾病经济负担也日益受到重视。新型黄嘌呤氧化酶抑制剂药物非布司他由于疗效显著,且没有药物超敏反应等不良反应,自FDA批准后即在临床逐渐被广泛的应用,但与其优势相对应的是其费用显著高于别嘌醇治疗,两者之间价格比在中国大陆地区约为30~35倍。但目前国内尚未见相关卫生经济学评估研究报道。
2012美国风湿免疫医师协会的痛风诊治指南将别嘌醇及非布司他均推荐为一线治疗选择,但该指南的制定是基于RAND-UCLA共识法制定,并未充分考虑降尿酸治疗的成本效果。英国国家卫生与临床优化研究所(National Institute for Health and Care Excellence,NICE)最初通过决策树模型比较别嘌醇300 mg每天1次及非布司他80 mg每天1次或120 mg每天1次两种治疗策略,结果显示与别嘌醇治疗相比,应用非布司他治疗策略的增量成本效果为16 574英镑/QALY,略低于NICE推荐的单位OALY的支付阈值,被认为具有成本效果。但该研究结果被认为并未充分考虑临床治疗实际策略选择,如通常情况下在别嘌醇治疗不达标的情况下可序贯应用非布司他治疗[12]。
本研究通过决策树模型分析显示,在两年期的降尿酸治疗中,别嘌醇300 mg每天1次降尿酸治疗无法达标的情况下,改为二线非布司他40 mg或80 mg治疗可获得最佳成本效果。从卫生经济学角度,在中国大陆地区,该方案显著优于直接应用非布司他 40 mg作为一线起始治疗方案。虽然在医疗服务价格上与欧美国家存在差异,但本研究结果与欧美国家已发表的卫生经济学评估结果[10- 11,13]基本一致。而通过敏感性分析评估模型的稳定性,同样发现治疗前后以及不同尿酸控制水平下的效用值对最终增量成本效果比有最主要的影响。而急性痛风发作对成本和效用的影响,以及目前医疗成本服务价格±50%的波动均不能改变最终卫生经济学判断。
虽然近期研究表明痛风的严重程度与高尿酸状态均可增高人群的死亡率[14]。但本研究并未引入其对死亡的直接风险;且因为评估周期仅为2年,亦未引入竞争风险的评估。目前国外针对降尿酸治疗策略的卫生经济学评估多采取5年评估周期,其主要原因是获得了原EXCEL和FOCUS两个随机临床试验的长期、开放性延续试验的数据[3,15]以及CONFIRMS随机临床试验数据的支持[16]。而目前国内缺乏长期疗效及安全性临床观察数据,同时也由于国内患者非布司他用药常用剂量与高加索人群有明显差别,因此暂时缺乏有效数据支持更为复杂的模型及更为长期的卫生经济学评估。
[1]Liu R, Han C, Wu D, et al. Prevalence of hyperuricemia and gout in mainland china from 2000 to 2014: a systematic review and meta-analysis[J]. Biomed Res Int, 2015, 2015: 762820.
[2]Becker MA, Schumacher HR Jr, Wortmann RL, et al. Febuxostat compared with allopurinol in patients with hyperuricemia and gout[J]. N Engl J Med, 2005, 353: 2450- 2461.
[3]Becker MA, Schumacher HR, MacDonald PA, et al. Clinical efficacy and safety of successful longterm urate lowering with febuxostat or allopurinol in subjects with gout[J]. J Rheumatol, 2009, 36: 1273- 1282.
[4]Faruque LI, Ehteshami-Afshar A, Wiebe N, et al. A systematic review and meta-analysis on the safety and efficacy of febuxostat versus allopurinol in chronic gout[J]. Semin Arthritis Rheum, 2013, 43: 367- 375.
[5]Huang X, Du H, Gu J, et al. An allopurinol-controlled, multicenter, randomized, double-blind, parallel between-group, comparative study of febuxostat in Chinese patients with gout and hyperuricemia[J]. Int J Rheum Dis, 2014, 17: 679- 686.
[6]Schumacher HR Jr, Becker MA, Wortmann RL, et al. Effects of febuxostat versus allopurinol and placebo in reducing serum urate in subjects with hyperuricemia and gout: a 28-week, phase III, randomized, double-blind, parallel-group trial[J]. Arthritis Rheum, 2008, 59: 1540- 1548.
[7]Zhang W, Doherty M, Bardin T, et al. EULAR evidence based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT)[J]. Ann Rheum Dis, 2006, 65: 1312- 1324.
[8]Xu S, Liu X, Ming J, et al. A phase 3, multicenter, randomized, allopurinol-controlled study assessing the safety and efficacy of oral febuxostat in Chinese gout patients with hyperuricemia[J]. Int J Rheum Dis, 2015, 18: 669- 678.
[9]Khanna PP, Nuki G, Bardin T, et al. Tophi and frequent gout flares are associated with impairments to quality of life, productivity, and increased healthcare resource use: Results from a cross-sectional survey[J]. Health Qual Life Outcomes, 2012, 10: 117.
[10] Beard SM, von Scheele BG, Nuki G, et al. Cost-effectiveness of febuxostat in chronic gout[J]. Eur J Health Econ, 2014, 15: 453- 463.
[11] Jutkowitz E, Choi HK, Pizzi LT, et al. Cost-effectiveness of allopurinol and febuxostat for the management of gout[J]. Ann Intern Med, 2014, 161: 617- 626.
[12] Stevenson M, Pandor A. Febuxostat for the management of hyperuricaemia in patients with gout: a NICE single technology appraisal[J]. Pharmacoeconomics, 2011, 29: 133- 140.
[13] Perez-Ruiz F, Díaz-Torné C, Carcedo D. Cost-effectiveness analysis of febuxostat in patients with gout in Spain[J]. J Med Econ, 2016, 19: 604- 610.
[14] Perez-Ruiz F, Martínez-Indart L, Carmona L, et al. Tophaceous gout and high level of hyperuricaemia are both associated with increased risk of mortality in patients with gout[J]. Ann Rheum Dis, 2014, 73: 177- 182.
[15] Schumacher HR Jr, Becker MA, Lloyd E, et al. Febuxostat in the treatment of gout: 5-yr findings of the FOCUS efficacy and safety study[J]. Rheumatology (Oxford), 2009, 48: 188- 194.
[16] Becker MA, Schumacher HR, Espinoza LR, et al. The urate-lowering efficacy and safety of febuxostat in the treatment of the hyperuricemia of gout: the CONFIRMS trial[J]. Arthritis Res Ther, 2010, 12: R63.