气相色谱-质谱法测定地下水中多氯萘
黎 宁,张红庆,饶 竹*,许丹丹,谷子欣
(1.国家地质实验测试中心,北京 100037;2.中国地质大学 材料与化学学院,湖北 武汉 430074;3.中国矿业大学 地球科学与测绘工程学院,北京 100083)
气相色谱-质谱法测定地下水中多氯萘
黎 宁1,2,张红庆1,饶 竹1*,许丹丹3,谷子欣2
(1.国家地质实验测试中心,北京 100037;2.中国地质大学 材料与化学学院,湖北 武汉 430074;3.中国矿业大学 地球科学与测绘工程学院,北京 100083)
建立了地下水中1-氯萘、2-氯萘、1,4-二氯萘、1,2,3,4-四氯萘、1,3,5,7-四氯萘、1,2,3,5,7-五氯萘、1,2,3,5,6,7-六氯萘、1,2,3,4,5,6,7-七氯萘和八氯萘9种多氯萘(PCNs)的气相色谱-质谱(GC-MS)分析方法。对比研究了液液萃取(LLE)和固相萃取(SPE)萃取地下水中PCNs的提取效率,优选二氯甲烷-液液萃取为PCNs检测的前处理方法。在优化条件下,9种PCNs的线性范围为5~100 μg/L,各组分的相关系数(r)大于0.995,方法检出限(S/N=3)为4.21~7.41 ng/L,地下水的平均加标回收率为70.7%~112%,相对标准偏差(RSD,n=5)均小于9.9%。该方法已用于地下水样中多氯萘的检测。
多氯萘(PCNs);气相色谱-质谱联用(GC-MS);液液萃取(LLE);地下水
多氯萘(Polychlorinated naphthalenes,PCNs)作为近年出现的一类新型有机污染物而倍受关注。多氯萘是指萘环上氢原子被氯原子所取代后形成的一类化合物总称[1]。因其具有PCDD/Fs类似的毒性、生物富集性、持久性和远距离迁移性[2-4]而被欧盟纳入“关于持久性有机污染物的斯德哥尔摩公约”中优先控制的有机污染物(POPs)。PCNs的蒸汽压介于1.3×10-4~2.1 Pa(25 ℃)之间,具有半挥发性,可在全球范围内传输[5-6]。同时PCNs具有较高的亲脂性,能与芳香烃受体结合或激活特定的酶来改变细胞的生物化学性质,从而产生毒性效应,并易通过食物链积累危害人体健康[7]。PCNs曾被广泛用于电容器、变压器介质、润滑油添加剂等。近年来在空气、土壤、地表水、沉积物等介质中均已检出[8-11]。然而,对地下水中PCNs的分析研究却鲜见报道。目前中国地下水污染形势异常严峻,但是地下水中有机污染物的分析方法缺乏,特别是新型有机污染物检测。因此,亟待建立地下水中多氯萘的分析方法。
目前,水中半挥发性有机物的提取方法主要有液液萃取法[12-14]、固相萃取法[15-16]。固相萃取所需溶剂少、绿色环保,但萃取率低、不稳定;液液萃取是经典的样品提取方法,经济、结果稳定、回收率高,有利于地下水中痕量污染物的富集。多氯萘的检测方法主要有气相色谱法[17]、液相色谱法[18]、气相色谱-高分辨质谱联用法[19]和液相色谱-质谱联用[20]等方法。气相色谱法检测可能存在假阳性,气相色谱-高分辨质谱联用法仪器昂贵、难以普及;PCNs具有较高的亲脂性,因此液相色谱及液相色谱-质谱应用较少。本文选取广泛使用而且定性较准确的气相色谱-质谱联用仪建立地下水中9种PCNs的分析方法,为批量地下水中PCNs污染的调查、评价提供了技术支撑。
1 实验部分
1.1 仪器与试剂
GCMS-QP2010气相色谱-质谱仪、AOC-20i自动进样器(日本岛津有限公司);Milli-Q超纯水系统(美国Millipore 公司);LABOROTA-4003型旋转蒸发仪(德国Heidolph公司);DB-5MS气相色谱柱(30 m×0.25 mm×0.25 μm,美国Agilent公司);1 L分液漏斗,带聚四氟乙烯活塞(北京欣维尔玻璃仪器有限公司);HLB小柱(3 cc/60 mg,吸附剂为二乙烯苯和N-乙烯基吡咯烷酮)购于美国Waters公司;1 L棕色细颈螺旋口预清洗样品瓶(美国热电公司)。
6种多氯萘标准混合溶液(1.0 μg/mL):1,2,3,4-四氯萘、1,3,5,7-四氯萘、1,2,3,5,7-五氯萘、1,2,3,5,6,7-六氯萘、1,2,3,4,5,6,7-七氯萘、八氯萘(美国CIL公司);3种多氯萘标准溶液(10.00 μg/mL):1-氯萘、2-氯萘、1,4-二氯萘(美国Chem Service公司)。替代物标准:苊-D10,内标:苝-D12,美国AccuStandard公司;正己烷、二氯甲烷、乙酸乙酯(色谱纯,北京J & K百灵威科技公司);氯化钠、无水硫酸钠(分析纯,北京化工厂),使用前分别于700 ℃马弗炉中烘烤4 h,冷却后置于干燥器备用;高纯氦气和氮气(纯度≥99.999%,北京诚维峰气体有限公司)。
1.2 样品前处理
量取1 L水样于1 L分液漏斗中,分别加入30.0 g NaCl和50 μL替代物标准溶液苊-D10(2.0 μg/ mL),然后加入50 mL二氯甲烷作为萃取溶剂,充分摇匀后排气,于振荡器上振摇萃取10 min,静置分层后,将有机相转移至250 mL平底烧瓶中;后两次分别加入30 mL二氯甲烷,重复上述操作,合并3次有机相。取适量的无水硫酸钠除水,旋蒸浓缩至2~3 mL;然后转移至KD浓缩瓶中,氮吹至0.5~1.0 mL,用二氯甲烷定容至1.0 mL。将定容后的样品转移至样品瓶中,加入50 μL内标物苝-D12标准溶液(2.0 μg/ mL),待测。
1.3 气相色谱条件
色谱柱:DB-5MS气相色谱柱(30 m×0.25 mm×0.25 μm,美国Agilent公司);进样口温度:270 ℃;载气:氦气(纯度≥99.999%);恒流流速:1.5 mL/min:进样量:1 μL;不分流进样;程序升温:初始温度80 ℃,保持2 min;然后以10 ℃/min升至300 ℃,保留5 min。
1.4 质谱条件
电子轰击源(EI),电离电压70 eV;离子源温度:240 ℃;GC-MS接口温度:280 ℃;溶剂延迟时间:5 min;选择离子监测(SIM)模式,9种多氯萘的保留时间、定性、定量特征离子见表1。

表1 多氯萘的保留时间及定性、定量离子Table 1 Retention times,quantitative ion and qualitative ions of PCNs
(续表1)

No.CompoundRetentiontimet/minQualitativeions(m/z)CN-521,2,3,5,7⁃Pentachloronaphthalene(1,2,3,5,7⁃五氯萘)17 530310∗,240,312CN-671,2,3,5,6,7⁃Hexahydropyrrolizinium(1,2,3,5,6,7⁃六氯萘)19 585344∗,346,348CN-731,2,3,4,5,6,7⁃Heptachloronaphthalene(1,2,3,4,5,6,7⁃七氯萘)21 755378∗,207,281CN-75Octachloronaphthalene(八氯萘)23 470414∗,207,281
*quantitative ion
1.5 地下水样品采集
2015年10月13日~15日采集苏州、杭州部分地区地下水样品。根据前期调查和地质资料布设采样点。样品采集后放入1 L细口棕色玻璃瓶,标明时间、地点等信息后放入低温(4 ℃左右)冷藏箱中保存,并尽快送实验室检测。采样技术要求详见《地下水污染地质调查评价规范》(DD 2008-01)中样品采集部分。
2 结果与讨论
2.1 液液萃取溶剂的选择
本实验对液液萃取的提取溶剂进行了考察。选择正己烷(Hex)、二氯甲烷(DCM)、二氯甲烷-正己烷(DCM-Hex,3∶1)、二氯甲烷-乙酸乙酯(DCM-EtOAC,3∶1)、正己烷-乙酸乙酯(Hex-EtOAC,3∶1)、正己烷-二氯甲烷(Hex-DCM,3∶1) 6种单一和混合溶剂按照“1.2”前处理方法萃取地下水中9种多氯萘,得到的基体加标回收率见表2。由于目标物为含氯化合物,采用二氯甲烷萃取时的回收率最好,回收率为81.6%~107%,且二氯甲烷沸点较低,易于蒸发浓缩,故选择二氯甲烷作为本方法的萃取溶剂。
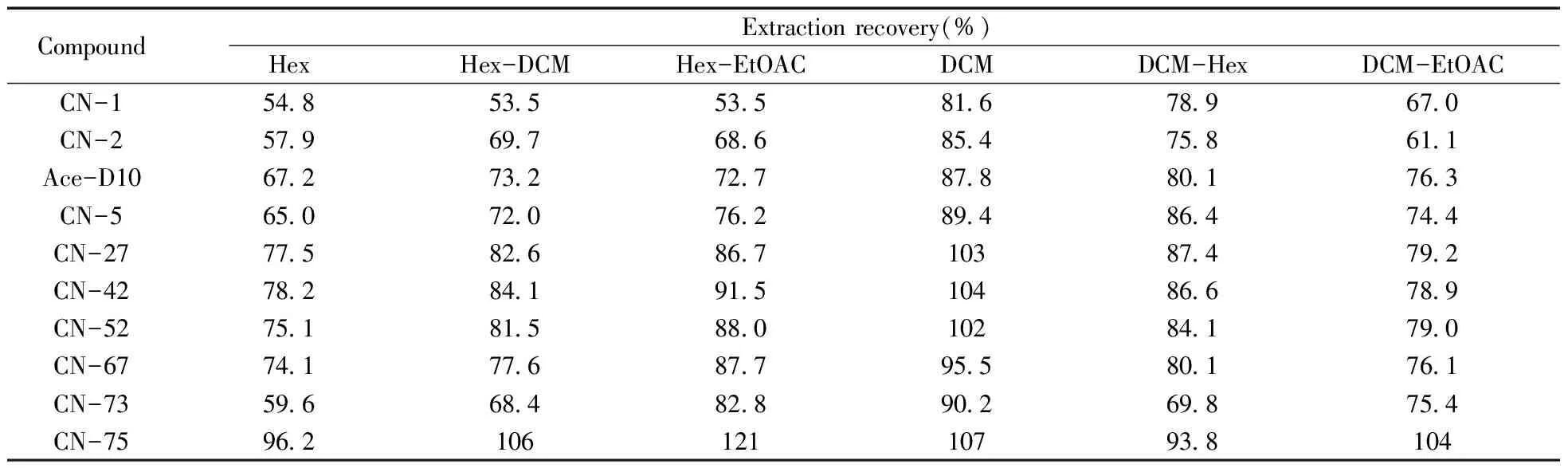
表 2 液液萃取溶剂的优化Table 2 The optimization of the extraction solvent
*spiked level:100 ng/L;Ace-D10:Acenaphthene-D12

图1 液液萃取与固相萃取的回收率对比Fig.1 Comparison of extraction recovery between LLE and SPE for 9 PCNs
2.2 液液萃取与固相萃取的对比研究
对比研究了液液萃取(LLE)和固相萃取(SPE)两种前处理方法对9种PCNs的萃取回收率。SPE使用HLB(Waters)固相萃取柱,富集方法为:5 mL甲醇活化小柱,10 mL超纯水洗涤,上样,氮气干燥,5 mL二氯甲烷淋洗,样品富集体积1 L。由于二氯甲烷为含氯溶剂,而多氯萘也为含氯有机物,按照相似相溶原则有利于多氯萘的淋洗。LLE和SPE两种前处理方法萃取目标物的回收率结果见图1。从图中看出,SPE提取地下水中9种PCNs的回收率为48.9%~101%,而LLE法的回收率为81.6%~107%,整体高于SPE提取回收率,满足《地下水污染调查评价样品分析质量控制技术要求》[21]关于地下水中半挥发性有机污染物回收率一般控制在70%~130%的要求。因此,本方法选择LLE为地下水中9种多氯萘提取的前处理分析方法。
2.3 色谱进样口温度的优化
进样口温度是色谱分析的重要条件之一。本实验对进样口温度进行了优化,结果显示,随着进样口温度从250 ℃升至270 ℃时,目标物的响应值达到最大,之后保持稳定直至290 ℃。如果进样口温度过高,会影响仪器的寿命,也不利于低沸点目标物的检测。综合考虑,实验选择进样口温度为270 ℃。
2.4 离子源温度的选择
离子源温度的高低会直接影响到离子化效率,从而影响检测灵敏度。离子源温度过低,不利于样品气化,离子化效率降低;而离子源温度过高,会影响到离子源本身寿命,同时可能导致不稳定化合物降解,影响离子化效率。本实验在220~260 ℃内对离子源温度进行了优化,实验结果显示,随着温度的升高,目标物的响应值不断增大,当离子源温度为240 ℃时,目标物响应达到最高,此后则随着温度升高而开始下降。所以,最终选择离子源温度为240 ℃。

图2 9种PCNs标准溶液(100 μg/L)的选择离子扫描总离子流图Fig.2 TIC chromatogram of 9 PCNs(100 μg/L) standard solution in SIM mode
2.5 方法的性能指标
分别配制5.0,10.0,20.0,50.0,100 μg/L 5个浓度水平的多氯萘标准溶液,加入50 μL替代物(苊-D10)和内标物(苝-D12)混合标准溶液(2.0 μg/mL),在优化条件下选择离子检测,内标法定量,得到线性方程、相关系数(见表3)。由表3可知,9种多氯萘在5~100 μg/L浓度范围内线性良好,相关系数(r)均大于0.995。在100 μg/L的浓度水平下,9种PCNs标准溶液的选择离子扫描总离子流图见图2。
为验证方法的准确性和稳定性,分别配制7个25 ng/L和5个100 ng/L浓度水平的地下水基体加标平行样品,按照优化后的实验方法,经过液液萃取、GC-MS检测,得到各目标物的加标回收率及相对标准偏差(见表3)。从表3可以看出,在不同浓度下9种多氯萘的平均加标回收率均在70.7%~112%之间,RSD均小于10%;按照美国EPA:MDLs=t(n-1,0.99)×S公式计算方法检出限,9种PCNs的方法检出限在4.21~7.41 ng/L之间,能够满足地下水中多氯萘的检测要求。

表3 方法性能指标Table 3 The performance parameters of the method
*y:peak area,x:mass concentration of PCNs(ng/L)
2.6 实际样品测定
利用建立的方法测定了苏杭地区8个地下水样品。结果表明,8个地下水样中均未检出9种PCNs。取2个地下水样品进行基质加标回收实验,9种目标物的回收率为72.4%~115%,表明该方法的分析结果准确可靠,可用于地下水实际样品中多氯萘的检测。

表4 苏杭地区地下水中多氯萘的检测结果Table 4 Analytical results of 9 PCNs in groundwater of Suzhou and Hangzhou area
3 结 论
本文建立了二氯甲烷-液液萃取/气相色谱-质谱测定地下水中9种多氯萘的分析方法;通过对比研究,得到液液萃取的回收率为81.6%~107%,优于固相萃取(48.9%~101%)的回收率,前者更适用于地下水痕量多氯萘的富集;建立的分析方法在5~100 μg/L浓度范围内线性关系良好,各组分的基体加标回收率满足地下水检测规范要求[21](70%~130%),方法检出限为4.21~7.41 ng/L,可以实现地下水中9种痕量多氯萘的测定。
[1] Guo L,Zhang B,Xiao K,Zhang Q H,Zheng M H.Sci.Bull.(郭丽,张兵,肖珂,张庆华,郑明辉.科学通报),2008,53(2):153-158.
[2] Liu Z T,Liu G R,Zheng M H,Gao L R.Sci.Sin.Chim.(刘芷彤,刘国瑞,郑明辉,高丽荣.中国科学:化学),2013,43(3):279-290.
[3] Ai L F,Li W,Wang J,Ma Y S,Chen R C,Guo C H.J.Instrum.Anal.(艾连峰,李玮,王敬,马育松,陈瑞春,郭春海.分析测试学报),2015,34(5):570-575.
[4] Zhou L,Li H R,Ma S T,Ren M,Yu Z Q,Sheng G Y,Fu J M.J.Instrum.Anal.(周林,李会茹,马盛幍,任曼,于志强,盛国英,付家谟.分析测试学报),2013,32(10):1160-1165.
[5] Mari M,Schuhmacher M,Feliubadaló J,Domingo J L.Chemosphere,2008,70(9):1637-1643.
[6] Wang X T,Jia J P,Li Y C,Sun Y Z,Wu M H,Sheng G Y,Fu J M.ActaSci.Circum.(王学彤,贾金盼,李元成,孙阳昭,吴明红,盛国英,傅家谟.环境科学学报),2011,31(12):2707-2713.
[7] Guo L,Ba T,Zheng M H.Prog.Chem.(郭丽,巴特,郑明辉.化学进展),2009,21(Z1):377-388.
[8] Wang Y,Zhang Q,Lv J,Li A,Liu H,Li G.Chemosphere,2007,68(9):1683-1691.
[9] Pan J,Yang Y L,Yang W X,Lu G H,Sachi T,Yamashita N.ActaSci.Circum.(潘静,杨永亮,杨伟贤,路国慧,谷保佐知,山下信义.环境科学学报),2011,31(4):816-823.
[10] Guo Z S,Cai S T,Zhang X L,Zhu M J,Jian C.Environ.Sci.Technol.(郭志顺,蔡素婷,张晓岭,朱明吉,蹇川.环境科学与技术),2015,38(2):115-119.
[11] Rao Z.ActaGeol.Sin.(饶竹.地质学报),2011,85(11):1948-1962.
[12] Gao R,Rao Z,Guo X C,Huang Y,Li X J.J.Instrum.Anal.(高冉,饶竹,郭晓辰,黄毅,李晓洁.分析测试学报),2014,33(5):539-544.
[13] Mahmood A,Malik R N,Li J,Zhang G.Sci.TotalEnviron.,2014,485/486(3):693-700.
[14] Wang H,Mu S,Zhang Y,Zhang B B,Hu G J.Admin.Tech.Environ.Monitor.(王荟,穆肃,章勇,张蓓蓓,胡冠九.环境监测管理与技术),2014,26(3):38-40.
[15] Li Y.Chin.J.HealthLab.Technol.(李晔.中国卫生检验杂志),2007,17(1):94-95.
[16] Li Q Z,Zhou M H,Liu Y F,Zheng J G,Zhai C P,Li D.J.Inspect.Quarant.(李全忠,周明辉,刘莹峰,郑建国,翟翠萍,李丹.检验检疫学刊),2009,19(6):28-30.
[17] Huang R,Zhang S K,Ren M Z,Ma F P,Feng G X,Du G Y,Fu J P,Qing X.Environ.Chem.(黄蓉,张素坤,任明忠,马飞攀,冯桂贤,杜国勇,付建平,青宪.环境化学),2015,34(3):529-535.
[18] Mahmood A,Malik R N,Li J,Zhang G,Jones K C.Sci.TotalEnviron.,2014,481(1):409-417.
[19] Tong L,Wu S Q,Yang J J.J.Instrum.Anal.(佟玲,吴淑琪,杨佳佳.分析测试学报),2010,29(4):398-402.
[20] Kuznetsova M V,Maslennikova I L,Karpunina T I,Nesterova L Y,Demakov V A.Can.J.Microbiol.,2013,59(9):604-610.
[21] 中国地质调查标准.地下水污染调查评价样品分析质量控制技术要求(DD2014-15).
Determination of Polychlorinated Naphthalenes(PCNs) in Groundwater by GC-MS
LI Ning1,2,ZHANG Hong-qing1,RAO Zhu1*,XU Dan-dan3,GU Zi-xin2
(1.National Research Center for Geoanalysis,Beijing 100037,China;2.Faculty of Materials science and Chemistry,China University of Geosciences,Wuhan 430074,China;3.College of Geoscience and Surveying Engineering,China University of Mining and Technology,Beijing 100083,China)
A GC-MS method was established for the determination of 9 polychlorinated naphthalenes(PCNs),including 1-chloronaphthalene,2-chloronaphthalene,1,4-dichloronaphthalene,1,2,3,4-tetrachloronaphthalene,1,3,5,7-tetrachloronaphthalene,1,2,3,5,7-pentachloronaphthalene,1,2,3,5,6,7-hexahydropyrrolizinium,1,2,3,4,5,6,7-heptachloronaphthalene and octachloronaphthalene in groundwater.Comparative study was conducted between the liquid-liquid extraction(LLE) and solid phase extraction(SPE) for extraction of 9 PCNs in groundwater,and LLE was selected as sample preparing method as it has higher extraction efficiency than SPE.The calibration curves of 9 PCNs were linear in the range of 5-100 μg/L with correlation coefficients(r) more than 0.995.The spiked recoveries for groundwater samples ranged from 70.7% to 112% with relative standard deviations(RSD,n=5) less than 9.9%,and the method detection limits(S/N=3) were in the range of 4.21-7.41 ng/L.The method was accurate and sensitive,and was successfully applied in the determination of 9 PCNs in real groundwater sample.
polychlorinated naphthalenes(PCNs);gas chromatography-mass spectrometry(GC-MS);liquid-liquid extraction(LLE);groundwater
2016-09-06;
2016-09-09
中国地质调查项目(DD20160312,1212011120283,1212010816028)
10.3969/j.issn.1004-4957.2017.02.017
O657.63;O625.23
A
1004-4957(2017)02-0252-05
*通讯作者:饶 竹,研究员,研究方向:环境有机污染分析,Tel:010-68999554,E-mail:raozhu@126.com

